基于铁基载氧体的市政污泥气化特性模拟及实验研究
2020-03-04梁文政王金玉王翠苹
王 坤, 梁文政, 颜 浩, 王金玉, 王翠苹,2
(1.青岛大学 机电工程学院,山东 青岛 266071; 2.山东科技大学 土木工程与建筑学院,山东 青岛 266590)
污泥是污水处理的副产物,中国具有庞大的污泥生产体量,但是相对于污泥生产量的快速增长,污泥处置方式的相对落后成为制约中国污泥处理行业的一大问题[1]。污泥因其高有机质和挥发分含量而具有很好的能源价值。传统的污泥处置方式[2]包括发酵堆肥、自然干化、直接填埋和焚烧等,由于其在大气污染物控制、重金属污染以及运营成本等方面的问题而限制了其实际应用和长远发展[3-4]。相比于传统处置方式,污泥气化[5]作为一种能够有效资源化利用污泥的新型处理方式广受关注。与传统的需要加气化介质(如富氧气体)的较高气化成本不同,化学链气化技术利用载氧体在两个串联的反应器(燃料反应器(FR)和空气反应器(AR))中的不断还原、氧化、再生的特性实现氧的传递,从而制取高品质的合成气[6-8]。化学链气化技术因污泥在气化过程中不与空气直接接触,能够有效避免热力型和快速型NOx的产生[9-11];通过控制载氧体与燃料的比值,可获取以CO和H2为主的合成气;载氧体的性能对合成气的制取起着至关重要的影响,其中Fe基载氧体因为价格低廉且不存在二次污染而广受欢迎[12-13]。
笔者以Aspen Plus V9.0平台为基础,结合HSC Chemistry 6.0的部分计算数据,对污泥化学链气化特性进行模拟,继而进行了部分验证实验,考察载氧体中活性氧与污泥中碳的摩尔比(n(O)/n(C))、气化温度、水蒸气与污泥质量流量比(q(V)/q(S))对燃料反应器中的气化、含硫污染物排放的影响,以及空气反应器中空气与载氧体摩尔流量比(空载比)对载氧体再生和NOx生成的影响,为系统化研究污泥的化学链气化提供理论依据。
1 基于Aspen Plus的污泥化学链气化的模拟
1.1 模型建立
在Aspen Plus中建立污泥化学链气化模型如图1 所示,该系统共由8个模块和15股工艺物流组成,主要模块包含RStoic反应器、RPlug反应器、RGibbs反应器以及Mixer混合器和SEP分离器。

图1 Aspen Plus模拟污泥化学链气化流程图Fig.1 Aspen Plus flow chart of the simulated sludge chemical chain gasificationMS—Municipal sludge; MEO-IN—Oxygen carrier feed; MEO-OUT—Oxygen carrier outflow;ME—Reduced oxygen carrier;AIR-OUT—Air outflow; S1/S2/S3—Separator 1/2/3; M1/M2—Mixer 1/2; FUEL-IN—Fuel feed; FUEL-OUT—Fuel outflow;DECOMP—Decomposition reactor; F-REACT—Fuel reactor; A-REACT—Air reactor; A-OUT—Air reaction flowout;DCOM-OUT—Decomposition reactor flowout; SYNGAS—Synthesis gas; GAS-IN—Gas in mixer
为使模型合理化,做出如下假设:
(1)各输出物流参数以及反应器条件在设定后不再随时间发生变化,反应过程稳定,给料温度选取室温25 ℃,压力0.1 MPa;
(2)物流中的灰分为惰性组分,其中所含物质不再参与以及影响热力学反应;
(3)选择铁基载氧体作为载氧体,其成分设定为纯Fe2O3;
(4)设定载氧体再生所需的空气为79%(体积分数)N2和21%(体积分数)O2所构成,忽略其他气体组分;
(5)气相成分相互之间反应速率极快,化学反应平衡在此条件上建立;
(6)设定F-REACT中气化产物为合成气的主要成分H2、CO2、CO、CH4,忽略其他碳氢化合物和焦油产生的影响;
(7)污泥化学链气化模拟选取污泥流率为1 kg/h。
1.2 燃料反应器中主要反应
(1)热解气化过程:污泥在高温下快速热解,析出大量挥发分,随后焦炭和各气相组分之间发生反应,反应方程式见式(1)~(6)。
C+H2O=CO+H2
(1)
C+O2=CO2
(2)
C+CO2=2CO
(3)
2CO+2H2=CH4+CO2
(4)
CO+H2O=CO2+H2
(5)
CH4+H2O=CO+3H2
(6)
(2)载氧体反应:污泥热解生成的气化产物与载氧体发生进一步反应,反应方程式见式(7)~(14)。
CH4+3Fe2O3=6FeO+CO+2H2O
(7)
CH4+4Fe2O3=8FeO+CO2+2H2O
(8)
CH4+9Fe2O3=6Fe3O4+CO+2H2O
(9)
CH4+12Fe2O3=8Fe3O4+CO2+2H2O
(10)
H2+Fe2O3=2FeO+H2O
(11)
H2+3Fe2O3=2Fe3O4+H2O
(12)
CO+Fe2O3=2FeO+CO2
(13)
CO+3Fe2O3=2Fe3O4+CO2
(14)
各反应的吉布斯自由能与平衡常数比较见图2。对于化学反应的吉布斯自由能,当ΔG>0时,反应不能自发进行;当ΔG=0时,反应达到平衡状态;当ΔG<0时,反应可以自发进行,且ΔG值越小,反应自发进行的可能性越大。由图2(a)可知:在所选取700~1000 ℃范围内,燃料反应器中除反应(4)外绝大部分反应ΔG均小于0,说明均可发生且可以自发进行;随着温度的升高,CH4与载氧体的反应(7)~(10)的ΔG值均有明显下降趋势,说明随温度升高,反应越发容易进行。由图2(b)可知,除反应(2)、(4)、(5)、(13)、(14)外,绝大多数反应的lnK值随着温度的升高而增加,说明反应程度随温度升高逐渐增加。

图2 燃料反应器(FR)中温度对化学反应(1)~(14)ΔG和lnK的影响Fig.2 Effects of temperatures on chemical reaction (1)-(14) ΔG and lnK in FR(a) ΔG; (b) lnK
1.3 空气反应器中主要反应
被还原的载氧体主要成分在空气中与O2进行氧化再生反应,反应式见式(15)~(16),为快速放热反应。
4FeO+O2=2Fe2O3
(15)
4Fe3O4+O2=6Fe2O3
(16)
2 污泥化学链气化实验
2.1 污泥燃料分析
模拟与实验所选污泥均为市政污泥,其工业分析和元素分析结果如表1所示。

表1 污泥的工业分析和元素分析Table 1 Proximate and ultimate analyses of sludge
2.2 实验过程
污泥化学链气化实验过程采用小型流化床实验系统,包括流化床反应器、蒸汽发生器、进气装置、温控装置、冷凝装置、旋风分离装置、烟气分析仪(英国凯恩公司产品,KANE9506),流化床反应器为高1000 mm、下部内径40 mm、上部提升段内径32 mm的耐高温306钢管,外部为电加热单元和保温材料,通过控制进入流化床的气体成分可以实现其FR-AR功能的切换。流化床具体装置示意图如图3所示。

图3 实验用鼓泡流化床系统示意图Fig.3 Diagram of experimental bubbling fluidized bed system
实验每次取污泥质量为1 g,所使用复合铁基载氧体成分Fe2O3和Al2O3的摩尔比为6∶4,CaO质量分数为5%。载氧体和污泥颗粒粒径均破碎为0.1~0.2 mm,实验中流化气体采用N2,体积流量为12 L/min,假定反应时长为15 min,其他实验工况如表2所示。

表2 污泥化学链气化实验工况Table 2 Experimental conditions of chemical looping gasification of sludge
3 模拟与实验结果的对比与分析
3.1 燃料反应器中氧/碳摩尔比(n(O)/n(C))的影响
定义氧/碳摩尔比(n(O)/n(C))为进入燃料反应器的载氧体中活性氧与所使用污泥中碳的摩尔比。
为了考虑污泥的气化程度,现定义碳转化率ηC为:
(17)
其中,qV,OUT为燃料反应器出口气体体积流量,L/min;其公式为:
qV,OUT=qV,N2/(1-φCO-φCO2-φCH4-φH2)
(18)
式中:qV,N2为进口氮气的体积流量,L/min;φCO、φCO2、φCH4、φH2分别为燃料反应器出口处CO、CO2、CH4、H2的体积分数;Vm为标准状况下气体的摩尔体积,为22.4 L/mol;nC,MS为污泥中碳的物质的量,mol;t为检测出口气体成分所持续的时间,s。
图4为模拟和实验结果中氧/碳摩尔比对产物合成气摩尔分数和碳转化率的影响,其中气化温度为900 ℃,水蒸气与污泥质量流量比(q(V)/q(S))为12。由图4(a)可见,模拟结果生成的合成气中H2比例占到35%~70%,且随着n(O)/n(C)的升高明显下降;CO则占到5%,CO2比例随着n(O)/n(C)升高从30%上升到65%。这是因为增加n(O)/n(C)值提高了载氧体的供氧量,而H2与Fe2O3的反应速率更高,使得H2不断被载氧体氧化,导致H2量不断减少。由图4(b)看到,实验所得合成气各组分的变化趋势与模拟结果大致相同。CO含量相比模拟结果较高,主要因为模拟过程中CO理论上转化为CO2,而在实验反应时间内气相组分浓度不均匀,CO无法与载氧体在短时间内充分混合,因此减少了CO的消耗。在n(O)/n(C)从2.0增加到2.5的过程中,CO2和H2组分的含量稳定上升,分析其原因为载氧体加入量的升高促进了反应(5)与反应(6)向正方向进行,水蒸气参与反应程度加深,使H2、CO2的含量得以提高。随着n(O)/n(C)的逐渐增大,气化产物被载氧体提供的晶格氧氧化程度加深,合成气对污泥气化程度的抑制作用减弱,使碳转化率有所上升。
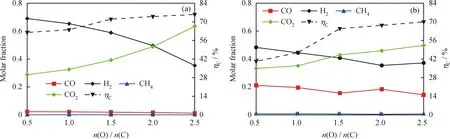
图4 模拟和实验结果中氧/碳摩尔比(n(O)/n(C))对合成气摩尔分数和碳转化率的影响Fig.4 Effects of n(O)/n(C) on molar fraction of syngas components and carbon conversion in the simulation and experimental resultsReaction conditions: T=900 ℃; q(V)/q(S)=12(a) Simulation results; (b) Experimental results
图5为氧/碳摩尔比对含硫污染物排放的影响。由图5(a)可以看出:模拟结果中,随着n(O)/n(C)的增加,H2S和羰基硫(COS)的排放量逐渐下降,而SO2的排放量不断上升。COS与H2S的排放量存在较大数量级的差距,主要是因为温度超过450 ℃时,H2可与COS发生反应,使其生成H2S;增加n(O)/n(C),载氧体的供氧量增加,H2S被Fe2O3氧化生成SO2,导致H2S被消耗,而SO2浓度增大。实验过程中无法测得COS的含量,但是根据实验测得的SO2、H2S的排放量与模拟结果趋势相同,可以推测实验中COS排放量的变化与模拟结果也应一致。
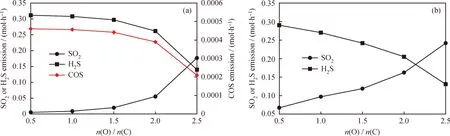
图5 模拟和实验结果中氧/碳摩尔比(n(O)/n(C))对含硫污染物排放的影响Fig.5 Effects of n(O)/n(C) on S-containing pollutant emissions in the simulation and experimental resultsReaction conditions: T=900 ℃; q(V)/q(S)=12(a) Simulation results; (b) Experimental results
由图4可知,合成气中可燃成分随着载氧体的增加而逐渐被消耗,使合成气热值降低。为保证合成气热值较高,n(O)/n(C)不宜取过大,并同时考虑污泥的碳转化率和污染的排放,也不可太小,最终选取n(O)/n(C)为1.5。
3.2 燃料反应器中气化温度的影响
温度对于污泥化学链气化的影响主要表现在影响化学反应的速率以及部分可逆反应的进行程度。当n(O)/n(C)为1.5、q(V)/q(S)=12时,模拟和实验结果中气化温度对合成气组分摩尔分数和碳转化率的影响结果如图6所示。结合图2(b),从理论上分析污泥气化过程可知,温度升高可促进甲烷重整反应(6)以及反应(1)、(3)的发生,使得CO与H2含量有所提高,并且CO与Fe2O3的反应平衡常数随着温度的升高而降低,反应受到抑制,CO2的含量进一步减少。但从图6(a)的模拟结果来看,各组分的含量受到温度的影响不大,分析原因为模拟过程不需考虑反应时间的影响,各组分之间在短时间内充分混合,组分分布均匀,达到完全反应的状态,改变温度对于各反应已充分反应的状态影响不大。由图6(b)看到,随着温度升高,污泥碳转化率逐渐增大,CO的生成量增加明显,CO2所占比例显著降低,900 ℃后增、减速率都有所放缓。图6的模拟结果与实验结果存在着一定差异,其主要原因与3.1节氧/碳摩尔比的影响类似,是由于在实验过程中气相组分分布不均匀,导致CO的消耗减少。
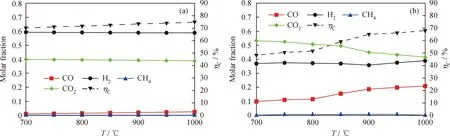
图6 模拟和实验结果中气化温度对合成气组分摩尔分数和碳转化率的影响Fig.6 Effects of temperatures on molar fraction of syngas components and carbon conversion in the simulation and experimental resultsReaction conditions: n(O)/n(C)=1.5; q(V)/q(S)=12(a) Simulation results; (b) Experimental results
气化温度对含硫污染物排放的影响如图7所示。由图7可知,在温度超过850 ℃时,无论是模拟还是实验结果,SO2排放均明显上升,H2S与SO2的排放趋势发生了相反的变化;而模拟结果中COS的排放量则在950 ℃时出现峰值,分析其原因为H2S和COS作为最终含硫污染物SO2的前驱体,高温下皆会被铁基载氧体所氧化,其主要反应方程式如式(19)~(22)所示:
H2S+9Fe2O3=6Fe3O4+SO2+H2O
(19)
H2S+3Fe3O4=9FeO+SO2+H2O
(20)
COS+9Fe2O3=6Fe3O4+SO2+CO2
(21)
COS+3Fe3O4=9FeO+SO2+CO2
(22)
通过其反应平衡常数与温度的关系(见图8)可知,反应(20)与(22)难以自发发生,而反应(19)与(21)的反应程度随着温度升高而提升,且考虑到在高温状况下COS的生成受到反应热力学平衡控制,其生成量与H2S浓度有关[14],并且在较高温度下,COS比H2S更易于与氧化铁反应,使其浓度开始减小。与n(O)/n(C)对硫污染物排放的影响同理,在改变气化温度的实验过程中并未对COS的排放量进行测试,但对比SO2与H2S的实验与模拟结果,可以推测出实验过程中COS的变化趋势与模拟结果相同。
从合成气中可燃成分CO、H2的含量(决定热值)和污染物排放以及碳转化率角度出发,气化温度不宜过低,最终选取为900~950 ℃。
3.3 燃料反应器中H2O的影响
H2O作为气化介质,其参数的改变也会对气化产物的生成产生重要的影响。模拟选取了气化温度为900 ℃、n(O)/n(C)为1.5的条件下,q(V)/q(S)对合成气摩尔分数的影响所得模拟和实验结果如图9 所示。因为水蒸气的流量难以调节到更大值,因而仅有q(V)/q(S)=12的实验数据与模拟值比较。由图9看到,实际H2生成量低于理论计算值,而CO实测值高于模拟数据,推测原因为H2与载氧体发生的副反应抑制了CO与载氧体的反应。
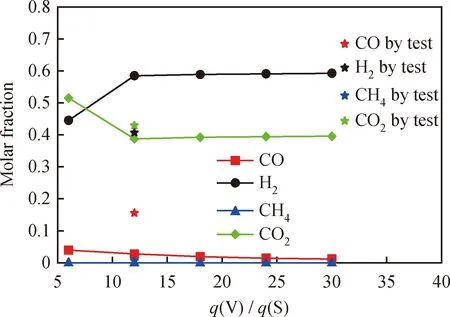
图9 模拟与实验结果中水蒸气与污泥质量流量比(q(V)/q(S))对合成气摩尔分数的影响Fig.9 Effects of q(V)/q(S) on molar fractions ofsyngas in the simulation and experimental resultsReaction conditions: T=900 ℃; n(O)/n(C)=1.5
由图9还看出,H2的摩尔分数在q(V)/q(S)从6增加到12时明显上升,继续增大水蒸气的质量流量,H2的摩尔分数基本稳定。而在q(V)/q(S)从6增加到12时,CO2的摩尔分数下降。这是因为H2产率的增加更为明显,而实际CO2的产率在缓慢提高。CO和CH4的产率则有所下降,主要是因为增加水蒸气的质量流量,使得污泥气化过程中水汽变化反应(5)得到加强,CO消耗生成H2和CO2,并促进了甲烷的重整反应(6),因此CH4的产率不断降低,水蒸气的存在加深了污泥的气化程度。
图10为模拟和实验结果中q(V)/q(S)对含硫污染物排放的影响。由图10可以看出:模拟结果中,H2S、SO2的排放量在q(V)/q(S)大于12后有着相反的变化趋势,且COS的排放量随着水蒸气质量流量的增加急剧减小;在q(V)/q(S)=12时由实验所
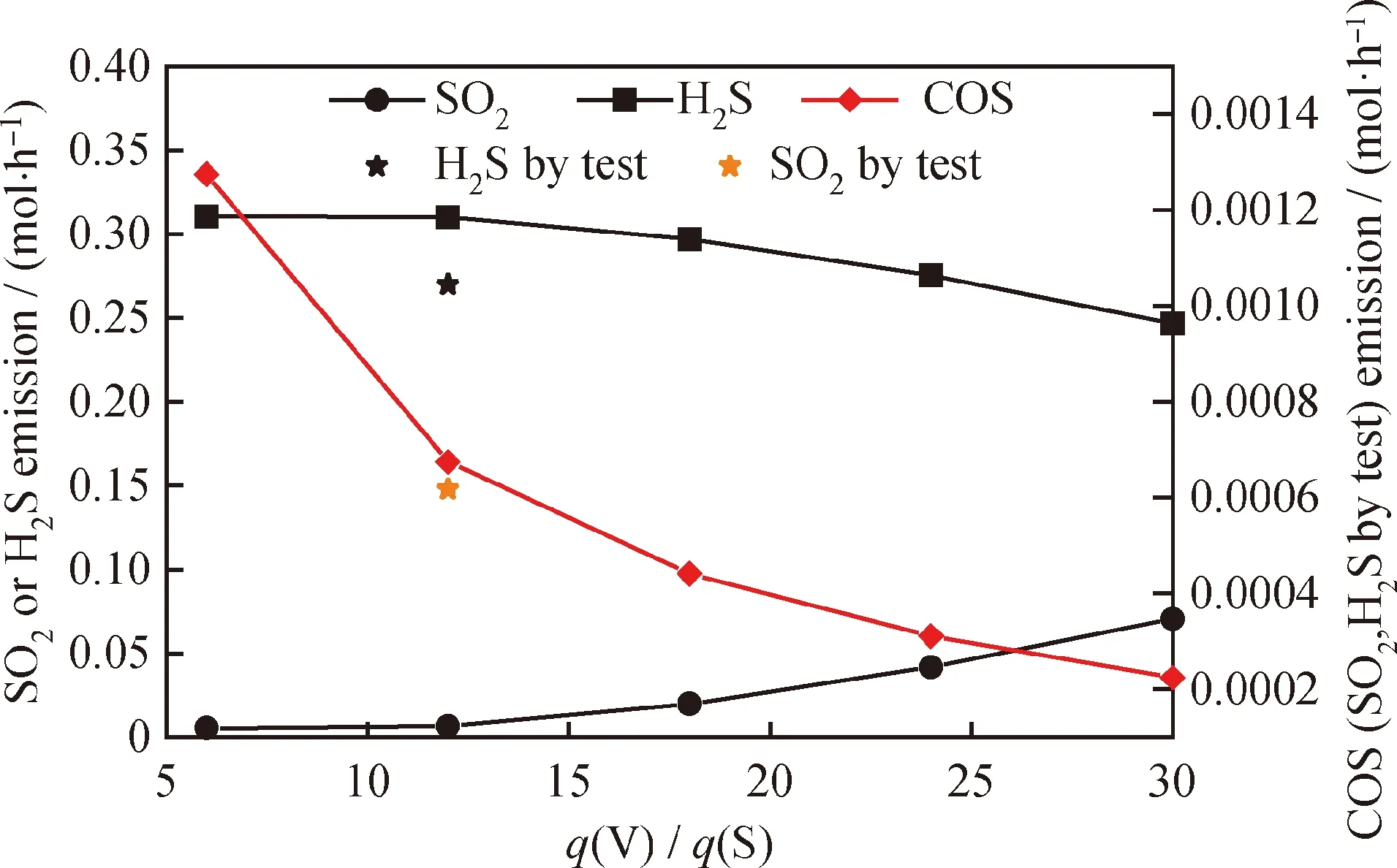
图10 模拟和实验结果中水蒸气与污泥质量流量比(q(V)/q(S))对含硫污染物排放的影响Fig.10 Effects of q(V)/q(S) on S-containing pollutantemission in the simulation and experimental resultsReaction conditions: T=900 ℃;n(O)/n(C)=1.5
测得的H2S和SO2生成量与模拟结果比较SO2的生成量较少而H2S较多。这主要因为实验过程中H2S与载氧体接触不充分,未被完全氧化为SO2。综合比较,选择q(V)/q(S)=12较为合理。
3.4 空气反应器中空载比的影响
燃料反应器中产生的还原态载氧体被送入空气反应器中氧化,完成载氧体的再生,定义空载比为空气与进入空气反应器的载氧体的摩尔流量(kmol/h)之比。
燃料反应器排出的载氧体组分主要为Fe3O4、FeO,经过空气反应器氧化再生后的产物主要为Fe2O3,以此作为进、出反应的物质进行模拟,选取空气反应器温度(Tair)为1000 ℃,空载比对载氧体再生的影响如图11所示。由图11可知,在空载比达到1.3时,载氧体基本实现了完全氧化,其氧化再生前后载氧体的具体成分变化,笔者所在课题组在此之前已进行过相关研究工作[15]。
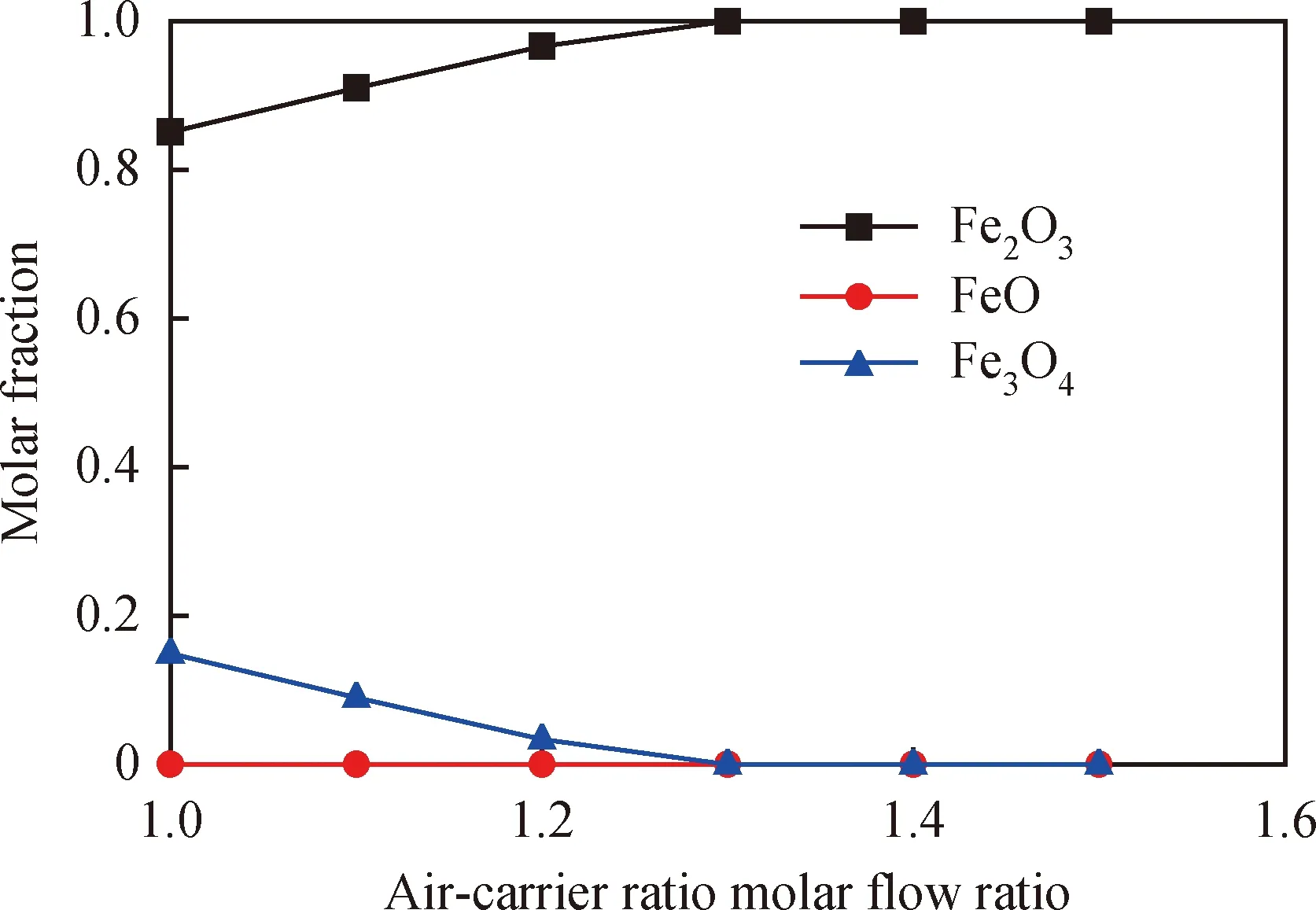
图11 模拟结果中空载比对载氧体再生的影响Fig.11 Effects of air-carrier molar flow ratio on oxygen carrier regeneration in the simulation resultsReaction condition: Tair=1000 ℃
因为空气中的N2与O2甚至载氧体中的晶格氧会生成热力型NOx,因此考察空载比对氮污染物生成的影响如图12所示。由图12可以看出,在空载比超过1.2时,NO和NO2的摩尔分数急剧增长。这是因为在空载比较低的情况下,空气中O2主要用于氧化再生载氧体并释放热量;随着空载比的增大,载氧体被完全氧化,O2与N2在高温下生成NOx,且主要为NO。
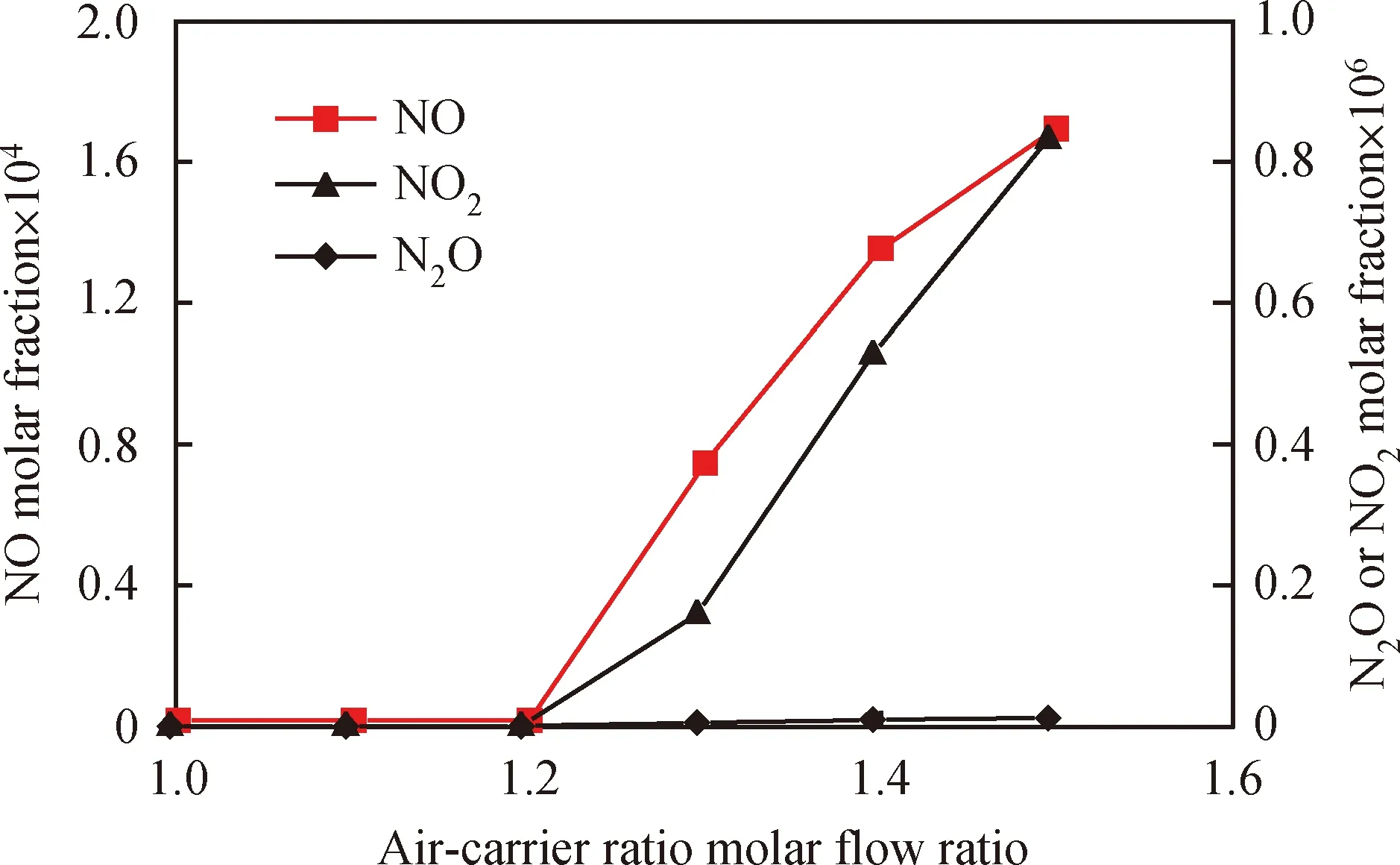
图12 模拟结果中空载比对含氮污染物生成的影响Fig.12 Effects of air-carrier molar flow ratio on N-containing pollutant generation in the simulation resultsReaction condition: Tair=1000 ℃
结合载氧体再生和污染物产生的情况,最终确定最佳空载比为1.3。反应温度越高,NOx生成量越大,空气反应器中的气化温度以满足燃料反应器中反应用热为依据(热质衡算)来确定。
4 结 论
通过Aspen Plus建立了污泥化学链气化模型,并加以实验验证,讨论了燃料反应器中载氧体中活性氧与污泥中碳的摩尔比(n(O)/n(C))、反应温度、水蒸气与污泥质量流量比(q(V)/q(S))对气化特性硫污染物排放的影响,以及空气反应器中空气与载氧体摩尔流量比(空载比)对载氧体再生和NOx生成的影响,得到主要结论如下:
(1)模拟与实验结果显示,n(O)/n(C)的增加会显著提高污泥的碳转化率,但是n(O)/n(C)过高会引起合成气热值明显下降,同时H2S、COS排放量会随着n(O)/n(C)的升高而明显下降。
(2)模拟与实验结果显示,燃料反应器中反应温度的升高会使合成气中CO、H2的摩尔分数稍有上升,同时增大污泥的碳转化率;有效减少了H2S的生成,但会使SO2的排放增多,而COS则随着温度升高呈现先上升后下降的趋势。
(3)模拟结果显示,当q(V)/q(S)从6增加到12时,H2的摩尔分数显著增大,有效提高了合成气的热值;当q(V)/q(S)大于12时无明显变化趋势。q(V)/q(S)的增加能够抑制H2S和COS的生成,但会少量增加SO2的生成。
(4)模拟结果显示,空气反应器中空载比的增加能够提高载氧体的再生程度,但是过大空载比会使多余的氧气在高温下与氮气反应产生大量NOx,且以NO为主。
