聚二乙炔囊泡的制备及其在医疗检测领域的应用
2020-02-29郝瑜佳朱光明
郝瑜佳 朱光明


摘 要 聚二乙炔(Polydiacetylene, PDA)因具有独特的光学及电子特性而受到广泛关注。两亲性共轭二乙炔(Diacetylene, DA)单体在一定条件下可以自组装成囊泡结构,紫外线辐射后,经1,4-加成聚合得到聚合物PDA囊泡。PDA在环境刺激下经历颜色和荧光变化,而PDA囊泡的类细胞膜结构使其具有很好的仿生特性,因此PDA囊泡可以用于细菌、病毒、酶等的检测以及疾病诊断和药物控释。本文介绍了PDA囊泡传感系统的制备以及固相聚合和颜色变化的机理,综述了PDA囊泡传感系统在医疗检测领域的研究和应用进展,并对PDA囊泡传感系统存在的问题和未来发展方向进行了总结和展望。
关键词 聚二乙炔; 囊泡; 自组装; 固相聚合; 医疗检测; 评述
1 引 言
共轭聚合物作为新型功能材料已被广泛研究,它们具有广泛离域的π-电子网络,内在构象的限制使其具有独特的光学和电学性质[1~4],因此常被用于设计成传感器、储能器件等[5~12]。聚二乙炔(Polydiacetylene,PDA)是其中具有代表性的化合物,它的主链高度有序,侧链可以被功能性基团修饰。PDA具有特殊的光学性质,受到外界刺激时会经历颜色和荧光的双重变化[13,14],近年来被广泛用于生物和化学传感领域。
PDA是共轭二乙炔(也称为联乙炔、二乙炔,Diacetylene, DA)单体在紫外线和γ射线等照射条件下聚合得到的,由于聚合过程不需要引发剂或催化剂[15],因此其纯度高,这对于传感、检测的应用具有重要意义。 其次,两亲性DA单体具有疏水尾和亲水端基,可以在水性溶液中自组装成囊泡[16,17]、单层或多层平面膜[18,19]、胶束[20,21]等结构,单体排列有序,有利于拓扑固相聚合过程的发生,其中自组装囊泡的制备程序相对简单,易于规模化生产,其双层球状结构具有很好的仿生特性[22],且用量容易控制,因此更适合于检测应用。聚合后的蓝色PDA囊泡呈蓝色,在受到热[23~25]、有机溶剂[26]、金属离子[24,27~34]、机械应力[35,36]、受体配体相互作用[37~40]、光[41,42]、pH[24,41]、电流[41,43]等刺激时, 会经历从蓝色到红色的颜色变化。DA单体亲水端基易于修饰,可以结合功能性基团实现特定物质的检测[44]。以上这些性质使得PDA囊泡传感器具有灵敏的双重检测能力,因此被用于各种无标记比色传感系统[31],用于检测病毒[45,46]、细菌[47,48]、蛋白质[49,50]、抗生素[11]、激素[16]、CO2 [51]、三聚氰胺[52]、唾液酸[12]、金属离子[24, 31]等或进行药物输送[53,54]。本文阐述了PDA囊泡传感器的制备方法,总结了PDA固相聚合和颜色变化机理的研究进展,介绍了近几年PDA囊泡用于医疗检测领域的一些代表性研究工作。
2 PDA囊泡传感器的制备
2.1 两亲性DA单体及其功能化
DA单体的形式为R1CCCCR2,通常由Cadiot-Chodkiewicz反应制备,即乙炔和卤代乙炔的铜催化的偶联反应[55]。DA分子的堆积排列与DA的側链或取代基密切相关[56]。通常,可用作亲水性端基设计的基团有羧酸、酰胺、脲、磺酸酯基团或其盐的取代基等,它们能够形成氢键,有利于分子的自组装和聚合,较大的侧基不利于二乙炔的聚合[15,39]。单体10,12-二十五碳二炔酸 (10,12-pentacosadiynoic acid, PCDA) 和 10,12-二十三碳二炔酸 (10,12-tricosadiynoic acid, TCDA)(图1)因其颜色响应的稳定性而受到研究者的青睐[39]。PDA囊泡可以直接对一些环境刺激做出反应,但这种传感信号较弱且不具有特异性,由于DA分子的亲水端基易修饰,可以将功能性基团引入到PDA上,赋予PDA特异性的检测能力和更显著的比色响应。
功能性基团通常是通过酰胺化反应或者酯化反应共价连接在二乙炔酸(如PCDA)单体上,然后功能化的单体直接自组装或与其它脂质混合自组装[37,45],再经过固相聚合过程得到具有特殊传感性能的PDA囊泡。改进的酰胺化反应通常是通过1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(N-(3-Dimethylaminopropyl)-N′-ethylcarbodiimide hydrochloride, EDC) 和N-羟基琥珀酰亚胺(N-hydroxysuccinimide, NHS)来活化PCDA得到PCDA的琥珀酰亚胺活性酯(PCDA-NHS),这种活性酯再与待连接基团的胺基进行酰胺化学反应, 得到功能化的PCDA[57~59]。目前, 研究人员已经成功制备了糖类功能化PDA[37]、脂质功能化PDA[60]、蛋白质功能化PDA[45]、氨基酸功能化PDA[61]和核酸功能化PDA[31]等多种用于医疗检测的PDA。
2.2 PDA囊泡
两亲性DA单体具有特殊的结构,理论上单体分子之间可能存在氢键、静电相互作用、疏水/亲水相互作用、π-π堆积、主客体相互作用、范德华力等非共价相互作用[24],这些非共价相互作用都有利于DA单体在水性溶液中自然排列(自组装)[36,62]。通过改变单体的端基和链长,可以控制所得自组装膜的结构[36,55,63~65]。自从Wegner[66]在1969年首次合成PDA以来,利用PDA自身的自组装过程将其制备成多种形式,如自组装单分子膜[67~69]、朗缪尔膜[37,60,70,71]和囊泡等。自组装单分子膜和朗缪尔膜这种平面膜结构的PDA制备程序相对复杂,且难以制造出大面积性能稳定的膜[55]。囊泡(Vesicles)也可以称为脂质体(Liposome),是PDA在医疗检测领域应用最多的一种形式。囊泡是两亲性DA单体和其它所需的脂质成分在溶液中自组装形成的具有封闭双层结构的“小球”,其内部可以包裹药物或其它活性成分[72]。囊泡结构的PDA传感器制备程序简单,且具有很好的仿生性。
在水性溶液中制备PDA囊泡需采用体积法(图2)[17]: 将两亲性DA单体和其它所需的脂质成分完全溶解在氯仿中,使其均匀分布,然后在真空中通过N2气流或者旋转蒸发除去溶剂; 向干脂质膜中加入去离子水或水性缓冲液,充分水合后, 进行聚碳酸酯膜挤出, 或在高于60℃(DA的相变温度)下进行探针超声处理,所得囊泡溶液再通过多孔膜过滤, 以除去聚集体,然后在254 nm紫外光下进行聚合反应, 得到PDA囊泡[40,44]。PDA囊泡溶液的总脂质浓度通常应控制在0.5~2 mmol/L之间,浓度过高会导致PDA的聚集或沉淀。这种体积法制得的囊泡具有多分散性, 一定程度上会影响传感器系统的质量[73]。
Kim等[73]基于流体动力学聚焦原理,通过使用微流体芯片制造了尺寸分布均匀的PDA囊泡,使用体积法制备的PDA囊泡的直径平均值和标准偏差为88和31 nm,使用微流体法制备的囊泡的平均值和标准偏差为39和12 nm,且使用微流体法制备的囊泡荧光性能有所提高。体积法的制备过程简单,微流体法制备过程相对复杂,但制得的囊泡性能较高。
纯PDA囊泡中二乙炔单体通过横向交联的聚合物链连接,限制了膜的流动性。将脂质插入PDA囊泡, 有利于改变PDA的物理性质,如大小[11]、表面电荷和脂质排列等[74], 从而增强PDA囊泡传感器的灵敏度和稳定性。实验证明,适当地掺杂二肉豆蔻酰磷脂酰胆碱(DMPC)、二肉豆蔻酰基磷脂酸(DMPA)等有利于提高囊泡的膜流动性,增强囊泡的仿生特性[74],从而增强囊泡与一些生物分子的功能性相互作用[75]。
因为可以很容易控制用量, 相对于平面膜,胶体分散体形式的PDA囊泡更易制备和规模化生产,更适于作分析试剂,但是PDA囊泡溶液中的分散体很容易聚集或从溶液中沉淀出来,而且用配体等生物功能分子对PDA囊泡进行修饰时,需要通过色谱方法从囊泡溶液中分离除去未反应的配体,否则游离的配体会与目标分子结合,会降低PDA材料的反应性[55]。将囊泡固定化可以解决上述两种问题,并且能保持PDA良好的比色性质[76,77],固定有利于提高检测灵敏度。目前常用的方法是通过自发吸附[77,78]、共价结合[46,76]以及包封作用[24]实现囊泡的固定化。自组装的PDA囊泡可以被固定在微珠[79]、纤维素膜[80,81]等固体基底上, 以及溶胶-凝胶材料[24,82]中。不同的形式适用于不同的传感应用,胶体溶液形式的PDA囊泡适用于大部分检测,而当PDA囊泡溶液发生严重的聚集或耐用性和方便性作为首要考虑因素时,固体化的PDA囊泡更适用于检测[55]。
3 固相聚合及PDA变色
3.1 固相聚合
DA的固相聚合是拓扑化学反应,该反应可以在各种紧密堆积的结构中进行[27], 如晶体[83,84]、自组装的单层或多层膜[36,37,65,67]、囊泡[11,31]、凝胶[24]、电纺纤维[54,85,86]和纳米复合材料[43,87,88]等。
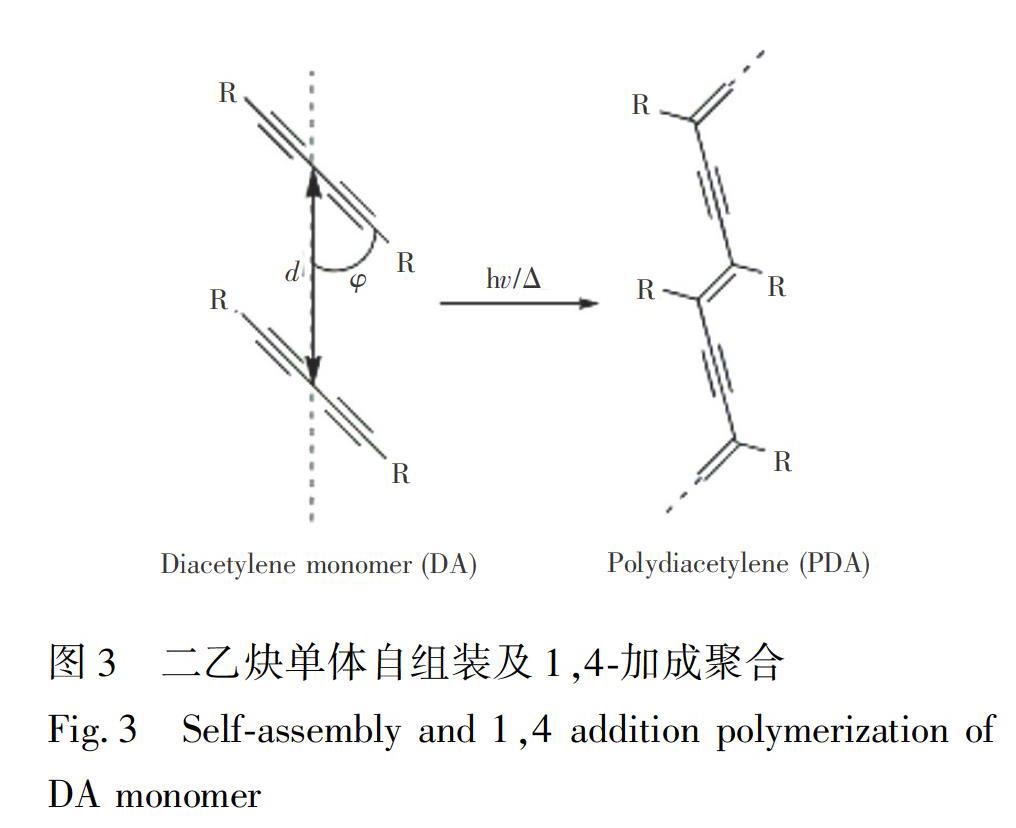
单体的紧密堆积是聚合所必需的,如图3所示,当单体的排列满足一定的结构参数, 即相邻DA分子的距离d≈0.5 nm, DA杆和填充轴之间的夹角φ≈45°时,在受到外界刺激的情况下, 如光(UV、γ射线、X射線)、热(退火)或施加应力, 1,4-加成聚合才会发生。254 nm紫外线很容易诱导聚合得到蓝色(最大吸收波长约为640 nm)的PDA囊泡[75,89,90]。
3.2 颜色变化机理
PDA在医疗检测领域的应用与比色性质密切相关。研究者从多个角度对PDA的变色机理进行了研究。 Lio等[91]揭示了PDA的热致变色行为与侧链的重排有关; Cheng等[61]认为PDA的微观结构在热致变色和pH致变色时可能通过不同的机制进行; Carpick等[36]认为PDA颜色的变化与其光吸收有关,PDA中的光吸收是通过线性π共轭聚合物主链中的π-π*吸收发生的,未聚合的薄膜在可见光区不显示吸收,呈白色。聚合后PDA通常呈现蓝色(最大吸收波长约为640 nm),受到外部刺激时PDA由蓝向红(最大吸收波长约为540 nm)的颜色转变与可见光谱吸收从低能到高能的转变有关。具体的吸收光谱和颜色转变的温度随着侧基和PDA形式的不同而变化。
蓝相和红相PDA之间的转换机制仍未被完全阐明。目前被广泛认可的一种说法是主链的吸收特性对应变非常敏感,理论计算表明,主链中碳碳键旋转几度就会显著改变π-轨道重叠,影响电子状态,导致主链吸收特性发生变化[55]。侧链在未聚合时就会通过氢键、范德华力等支配分子间排列[92~94]。在聚合过程中,由于侧链排列施加的几何限制,延伸的主链将形成应变构型,即侧链的堆积能形成一个能量障碍,阻止主链采用更松弛的形式。在光聚合后,外部环境的刺激会引起侧链结构的变化,允许主链采用更松弛的构象,主链中CC键发生旋转,破坏共轭主链的平面性 (如图4所示),导致PDA主链吸收光谱蓝移[36,55]。
3.3 亲和变色
导致PDA由蓝向红转变的外界刺激因素有很多,通常将由于发生特定目标分子识别而引起PDA颜色变化的过程称为亲和变色[19]。在医疗检测领域,各种生物分子、离子或微生物导致PDA的变色基本都属于亲和变色,这种生物化学效应产生于待检测物质和PDA 膜表面的多点相互作用破坏了膜表面结构; 待检测物质的疏水结构域插入PDA膜结构引起结构扰动[39, 95~97]。PDA的结构一旦发生扰动,有可能破坏其共轭主链的平面性,导致光吸收的变化,呈现出肉眼可见的颜色变化。
4 PDA囊泡在医疗检测领域的应用
采用PDA囊泡,目前已经实现了对病毒[45,46]、细菌[47,48]、蛋白质[49,50]、抗生素[11]、激素[16]等的检测以及疾病诊断和药物输送[37,53,54]。检测的原理为待检测物质引起PDA囊泡的结构发生扰动,破坏了PDA共轭主链的平面性,从而引起光吸收的变化。目前研究者多采用了使DA单体功能化的方法提高单体和待检测物质之间的结合能力,从而增加PDA囊泡的检测特异性和灵敏度。
4.1 细菌、病毒的检测
PDA囊泡可以用于检测病毒和细菌,实质是PDA上连接的功能性基团特异性识别微生物表面物质(如病毒表面蛋白)或微生物分泌的物质(如细菌毒素),这种识别作用引起了PDA结构的扰动。
逆转录-聚合酶链反应(RT-PCR)和酶联免疫吸附试验(ELISA)方法是常用的检测病毒的方法[98],然而这些方法成本高,并且需要长时间的样品制备过程和复杂的操作。Seo等[46]以流感病毒M1肽-M1抗体对作为靶-探针模型,开发了DMPA和连接了M1抗体探针的PCDA 共组装的囊泡微阵列,可以灵敏检测甲型流感病毒。Roh等[45]利用乙肝表面抗体(HBsAb)与乙肝表面抗原(HBsAg)发生的特异性反应,制成一种特殊的PDA/HBsAb囊泡荧光探测器(图5),利用PDA囊泡的红色相作为荧光染料检测硝酸纤维素膜(NC膜)上的HBsAg,裸眼检出限在1 ng/mL以下,荧光分析检出限在0.1 ng/mL以下。
PDA囊泡传感器已被用于检测枯草芽孢杆菌[99]、沙门氏菌[100]、耐甲氧西林金黄色葡萄球菌[101]、大肠杆菌[85,102]等多种细菌。Park等[99]开发了胺功能化的PDA囊泡传感系统(图6),通过细菌释放的表面活性素和PDA囊泡之间的特定相互作用检测细菌。该传感器在枯草芽孢杆菌SSB466(革兰氏阳性细菌的无表面活性素菌株)、枯草芽孢杆菌NCIB3610(革兰氏阳性细菌的产生表面活性素的菌株)、铜绿假单胞菌PA14(一种革兰氏阴性细菌)三种不同的细菌中特异性检测NCIB3610。Tao等[101]制备的PDA囊泡可与耐甲氧西林金黄色葡萄球菌(MRSA)分泌的各种成孔毒素(如白细胞介素和α-毒素)结合,他们利用基于数字光处理的3D生物打印技术将PDA纳米粒子组装到明胶甲基丙烯酰水凝胶中, PDA微凝胶在体外和体内(小鼠)都有结合并中和MRSA分泌的成孔毒素的能力,可用于细菌检测, 并治疗细菌感染。
4.2 用于药物控释和疾病诊断
囊泡内部的亲水“核”可以对药物进行包封,外层的端基也可连接药物,其作为药物递送载体进行靶向药物输送的应用被广泛报道[53,103]。An研究组[103,104]制备了多种负载多西紫杉醇(DTX)的PDA囊泡,多西紫杉醇能与乳腺癌细胞发生识别,将多西紫杉醇(DTX)负载在由叶酸衍生物和PDA制备的新型叶酸-PDA囊泡上[104],该囊泡传感器仍然具有良好的生物相容性,在杀死癌细胞方面也表现出更高的效率。这些PDA囊泡在体外模拟和在Bcap-37乳腺癌细胞中都实现了温度控制的抗癌药物释放,药物的疗效显著提高。
Kim等[105]将PCDA单体与磷脂DMPC混合, 开发了PDA/磷脂囊泡,并将外泌体的标志蛋白(CD-63)的抗体连接在囊泡上, 以诱导抗原-抗体相互作用,该复合免疫传感器可以选择性地检测从人血浆中分离出来的外泌体,作为疾病诊断的信号。溶血磷脂酸(LPA)是卵巢癌的一种敏感的生物标志物[106],Wang等[107]制备了咪唑功能化的PDA传感器(iPDA),能對LPA进行快速的特异性检测(图7A),检出限为0.5 μmol/L,远低于在卵巢癌患者体内的血浆LPA浓度。他们还将功能化的PDA装载在硝酸纤维素膜上,成功区分卵巢癌患者和健康人的血样。Wang等[12]设计合成了3种DA单体PCDA-pBA、PCDA-Nap和PCDA-EA(如图7B所示),用苯硼酸(pBA)分子修饰的单体PCDA-pBA用作唾液酸识别的受体,含有萘亚胺(Nap)衍生物荧光团的单体PCDA-Nap被用于增强PDA传感系统的荧光自放大,荧光团的荧光可在PDA囊泡形成过程中直接淬灭,在唾液酸与复合PDA囊泡特异性结合时又开启。该传感器系统可用于人乳腺癌(MCF-7)细胞表面的唾液酸检测和成像。
4.3 检测其它生物分子和离子
汞含量超标会严重影响人体健康, Wang等[31]将富含胸腺嘧啶(T)的单链DNA连接到PCDA单体上并制成囊泡(图8),适体可与Hg2+选择性结合形成胸腺嘧啶-HgⅡ-胸腺嘧啶复合物(T-Hg-T)[108], 从而引起PDA的颜色变化。该传感器可以对未知汞浓度进行定量分析,Hg2+检出限达5 μmol/L。
Wang等[49]设计的PDA囊泡传感器可以定量检测β-葡萄糖苷酸酶; Jannah等[109]利用PDA囊泡的pH敏感性和尿素酶能催化的尿素水解的特性[110],建立了脲酶的比色传感器平台,可以用于脲酶的视觉检测; Kim等[51]设计的PDA囊泡可在3 min内快速检测到CO2; Cho等[16]将DMPC和PCDA以1∶9的比例混合得到的囊泡,在10种类固醇中可以选择性地检测孕激素。
PDA囊泡还常被用于筛选药物载体。 Wang等[111]制备优化的DMPC/PDA囊泡对市售的3种基因载体Lipofectamine 2000、Entranster-H4000和聚乙酰亚胺显示出最敏感的变色反应。该传感器不仅能够预测基因载体的体外膜亲和力,这有助于提高基因转染效率,而且还为具有高细胞亲和力的各种载体材料的高通量筛选提供了方法。
5 总结与展望
自从Wegner等[66]成功合成PDA以来,基于PDA的研究取得了显著进展。本文讨论了PDA的基本属性,介绍了将PDA囊泡应用于医疗检测领域的一些有代表性的研究成果。通过设计不同结构的PDA,使其与目标分子特异性结合,然后利用PDA的光学特性实现定性和定量检测的目的。此传感器具有双重检测能力,能直接输出检测信号,相比于其它传感器更直观、快速; 而且囊泡结构具有很好的仿生特性和生物相容性,这使得PDA囊泡不仅能检测与生命活动密切相关的物质,还有望进行药物的靶向运输以及疾病的诊断和治疗。
但是,到目前为止, PDA传感器在医疗检测领域的应用仍面临着一些挑战。PDA可以对温度、pH值等作出响应,因此检测时温度、分析缓冲液成分、酸碱度等都可能会影响分析结果,干扰检测,排除这些因素对检测结果的干扰有待继续研究。部分PDA传感器的传感信号不足, 在保证检测特异性的情况下放大检测信号、提高PDA系统检测的灵敏度是未来的研究重点。目前PDA系统中的可逆响应已经能通过改变热、酸碱度、紫外光和电流等实现,但用于医疗检测领域的可逆PDA传感器较少,开发可逆的生物和化学PDA传感器也是一个重要的研究方向。
改进PDA传感系统最基本的方法是通过化学方法在PDA传感系统中引入各种功能性基团,不同的功能性基团在一定程度上决定了PDA传感系统的特异性和灵敏性,由于PDA的可逆性与端基的结构密切相关,因此在末端引入可形成氢键、π-π相互作用的基团理论上也有利于增加PDA变色的可逆性,这种化学方法通常涉及有机合成,具有一定的挑战性,而现代有机合成方法与技术的不断发展将为PDA传感器的设计提供更多可能; 在聚合前通过退火处理可以完善组装体的结构,也可以很好地提升PDA的传感性能; 此外,还可以通过在PDA囊泡体系中掺入其它脂质成分增强膜流动性和仿生性,从而放大检测信号。除了优化PDA自身的结构之外,还应考虑将各种新材料与新技术引入PDA囊泡传感体系。近年来,静电纺丝、3D打印等材料领域的热门技术[73,101]被应用到PDA传感器的设计中,研究者还尝试将自组装的PDA负载到纤维支架[112]、石墨烯片[113]、聚偏氟乙烯膜[32,114]等主体基质上, 制备得到各种性能优异的PDA复合材料,这使得PDA传感器的应用更加方便、快捷,大大增强了PDA材料的实用性。随着新材料和新技术的不断涌现,PDA传感器的研究将迎来更多新的机遇。
References
1 Günes S, Neugebauer H, Sariciftci N S. Chem. Rev., 2007, 107(4): 1324-1338
2 Hoeben F J M, Pascal J, Meijer E W, Schenning A P H J. Chem. Rev., 2005,105(4): 1491-1546
3 MA Yun, ZHOU Yan, DU Wen-Qi, MIAO Zhi-Hui, QI Zheng-Jian. Progress in Chemistry, 2015,27(12): 1799-1807
马 昀, 周 妍, 杜文琦, 缪智辉, 祁争健. 化学进展, 2015,27(12): 1799-1807
4 ZHOU Xiao-Yu, ZHAO Jian-Wei, MA Gui-Min, JIA Hong-Xia. Chinese J. Anal. Chem., 2019,47(7): 1006-1013
周晓毓, 赵建伟, 马贵敏, 贾红霞.分析化学,2019,47(7): 1006-1013
5 Thomas S W, Joly G D, Swager T M. Chem. Rev., 2007,107(4) : 1339-1336
6 Zhang Z T, Liao M, Lou H Q, Hu Y J, Sun X M, Peng H S. Adv. Mater., 2018,30(13): 1704261
7 Shi K L, Zhang W F, Gao D, Zhang S Y, Lin Z Z, Zou Y, Wang L P, Yu G. Adv. Mater., 2018,30(9): 1705286
8 Kim Y H, Han M S, Kim J B, Kim E Y. Energy Environ. Sci., 2018,11(8): 2124-2133
9 Su Y W, Lin Y C, Wei K H. J. Mater. Chem. A, 2017,5(46): 24051-24075
10 Xiao S Q, Zhang Q Q, You W. Adv. Mater., 2017,29(20): 1601391
11 Kang D H, Jung H S, Ahn N Y, Lee J, Seo S B, Suh K Y, Kim J S, Kim K S. Chem. Commun., 2012,48(43): 5313-5315
12 Wang D E, Yan J H, Jiang J J, Liu X, Tian C, Xu J, Yuan M S, Han X, Wang J Y. Nanoscale, 2018,10(9): 4570-4578
13 CHENG Huan, ZHU Guang-Ming, SONG Rui. Progress in Chemistry, 2013,25(12): 2113-2118
成 歡, 朱光明, 宋 蕊.化学进展,2013,25(12): 2113-2118
14 Qian X, Stdler B. Chem. Mater., 2019,31(4): 1196-1222
15 Wegner G. Macromol. Chem. Phys.,1972,154(1): 35-48
16 Cho E, Hu Y, Choi Y, Jung S. J. Ind. Eng. Chem., 2018,63: 288-295
17 Nguyen L H, Naficy S, McConchie R, Dehghani F, Chandrawati R. J. Mater. Chem. C, 2019,7(7): 1919—1926
18 Geiger E, Hug P, Keller B A. Macromol. Chem. Phys., 2002,203(17): 2422-2431
19 FAN Yi, ZHANG Li-Gong, HOU Fang-Yu, MA Bao-Liang, SHEN De-Zheng, LI Ya-Jun. Chem. J. Chinese Universities, 2003,24(4): 657-661
范 翊, 張立功, 候芳玉, 马保亮, 申德振, 李亚军.高等学校化学学报,2003,24(4): 657-661
20 Yao D, Li S, Zhu X, Wu J, He T. Chem. Commun., 2017,53(7): 1233-1236
21 Doerflinger A, Quang N N, Gravel E, Ducongé F, Doris E. Int. J. Pharm., 2019,565: 59-63
22 WANG Xue-Jing, MU Wei, HAN Xiao-Jun. Chinese J. Anal. Chem., 2019,47(8): 1134-1144
王雪靖, 穆 韡, 韩晓军.分析化学,2019,47(8): 1134-1144
23 Chance R R, Baughman R H, Müller H, Eckhardt C J. J. Chem. Phys., 1977,67(8): 3616-3618
24 Xu Y Y, Fu S Y, Liu F Y, Yu H Y, Gao J G. Soft Matter, 2018,14(39): 8044-8050
25 Mapazi O, Matabola P K, Moutloali R M, Ngila C J. Sens. Actuators B, 2017,252: 671-679
26 Ahn D J, Lee S M, Kim J M. Adv. Funct. Mater., 2009,19(10): 1483-1496
27 Wu S, Pan L B, Huang Y J, Yang N, Zhang Q J. Soft Matter, 2018,14(33): 6929-6937
28 Lee J, Jun H, Kim J. Adv. Mater., 2009,21(36): 3674-3677
29 Lee J, Kim H Y, Kim J. J. Am. Chem. Soc., 2008,130(15): 5010-5011
30 Gwon Y J, Kim C, Lee T S. Sens. Actuators B, 2019,281: 343-349
31 Wang M, Wang F, Wang Y, Zhang W, Chen X. Dyes Pigm., 2015,120: 307-313
32 Wen J T, Bohorquez K, Tsutsui H. Sens. Actuators B, 2016,232: 313-317
33 Jang Y S, Yoon B, Kim J M. Macromol. Res., 2011,19(1): 97-99
34 Yun D, Cho E, Dindulkar S D, Jung S. Macromol. Mater. Eng., 2016,301: 805-811
35 Carpick R W, Sasaki D Y, Burns A R. Langmuir, 2000,16(3): 1270-1278
36 Carpick R W, Sasaki D Y, Marcus M S, Eriksson M A, Burns A R. J. Phys. Condens. Mat., 2004,16(23): 679-697
37 Charych D H, Nagy J O, Spevak W, Bednarski M D. Science,1993,261(5121): 585-588
38 Charych D H, Spevak W, Nagy J O, Bednarski M D. Mat. Res. Soc. Symp. Proc.,1992,292: 153-161
39 Okada S, Peng S, Spevak W, Charych D. Acc. Chem. Res.,1998,31(5): 229-239
40 Lebègue E, Farre C, Jose C, Saulnier J, Lagarde F, Chevalier Y, Chaix C, Renault N J. Sensors, 2018,18(2): 599
41 Sun X M, Chen T, Huang S Q, Li L, Peng H S. Chem. Soc. Rev., 2010,39(11): 4244-4257
42 Lee J, Seo S, Kim J S. ACS Appl. Mater. Interfaces, 2018, 10(4): 3164-3169
43 Peng H S, Sun X M, Cai F J, Chen X L, Zhu Y C, Liao G P, Chen D Y, Li Q W, Lu Y F, Zhu Y T, Jia Q X. Nat. Nanotechnol., 2009,4(11): 738-741
44 Wen J T, Roper J M, Tsutsui H. Ind. Eng. Chem. Res., 2018,57(28): 9037-9053
45 Roh J, Lee S Y, Park S, Ahn D J. Chem. Asian J., 2017,12(16): 2033-2037
46 Seo S, Lee J, Choi E J, Kim E J, Song J Y, Kim J. Macromol. Rapid Commun., 2013,34(9): 743-748
47 Oliveira T V, Soares N F F, Andrade N J, Silva D J, Medeiros E A A, Badaró A T. Food Chem., 2015,172: 428-432
48 Xia Y, Deng J, Jiang L. Sens. Actuators B, 2010,145(2): 713-719
49 Wang D E, Zhang Y, Li T, Tu Q, Wang J. RSC Adv., 2014,4(32): 16820-16823
50 Park H K, Chung S J, Park H G, Cho J H, Kim M, Chung B H. Biosens. Bioelectron., 2008,24(3): 480-484
51 Kim K W, Lee J M, Kwon Y M, Choi T Y, Kim J Y H, Bae S, Song J A. Macromol. Res., 2018,26(3): 284-290
52 Lee J, Kim J. Chem. Mater., 2012,24(14): 2817-2822
53 Qin G, Li Z, Xia R, Li F, O'Neill B E, Goodwin J T, Khant H A, Chiu W, Li K C. Nanotechnology, 2011,22(15): 155605
54 Eslamian M, Khorrami M, Yi N, Majd S, Abidian M R. J. Mater. Chem. B, 2019,7(2): 224-232
55 Reppy M A, Pindzola B A. Chem. Commun., 2007,39(42): 4317-4338
56 Sarkar A, Okada S, Matsuzawa H, Matsuda H, Nakanishi H. J. Mater. Chem., 2000,10(4): 819-828
57 Hermanson G T. Bioconjugate Techniques. 3nd ed. Academic press, 2013:233-234
58 Kim J M, Ji E K, Woo S M, Lee H, Ahn D J. Adv. Mater., 2003,15(13): 1118-1121
59 Kim J M, Lee Y B, Yang D H, Lee J S, Lee G S, Ahn D J. J. Am. Chem. Soc., 2005,127(50): 17580-17581
60 Friedman S, Kolusheva S, Volinsky R, Zeire L, Schrader T, Jelinek R. Anal. Chem., 2008,80(20): 7804-7811
61 Cheng Q, Yamamoto M, Stevens R C. Langmuir, 2000,16(12): 5333-5342
62 Song J, Cisar J S, Bertozzi C R. J. Am. Chem. Soc., 2004,126(27): 8459-8465
63 Xie F, Chen C, Chen J, Liu M. J. Photochem. Photobiol. A, 2018,355: 283-289
64 Menzel H, Horstmann S, Mowery M D, Cai M, Evans C E. Polymer, 2000,41(22): 8113-8119
65 Sasaki D Y, Carpick R W, Burns A R. J. Colloid Interface Sci., 2000,229(2): 490-496
66 Wegner G. Macromol. Chem. Phys.,1971,145(1): 85-94
67 Kim T, Crooks R M, Tsen M, Sun L. J. Am. Chem. Soc.,1995,117(14): 3963-3967
68 Menzel H, Mowery M D, Cai M, Evans C E. J. Phys. Chem. B,1998,102(47): 9550-9556
69 Sullivan S P, Schnieders A, Mbugua S K, Beebe T P. Langmuir, 2005,21(4): 1322-1327
70 Ma B, Fan Y, Zhang L, Kong X, Li Y, Li J. Colloids Surf. B, 2002,27(2-3): 209-213
71 Li Y, Ma B, Yi F, Kong X, Li J. Anal. Chem., 2002,74(24): 6349-6354
72 Cho E, Jung S. Molecules, 2018,23(1): 107
73 Kim G, Song S, Lee J, Kim J M. Langmuir, 2010,26(23): 17840-17842
74 Kim K Y, Choi H, Lee G S, Ahn G J, Oh M K. Colloids Surf. B, 2008,66(2): 213-217
75 Thet N T, Jamieson W D, Laabei M, Mercer-Chalmers J D, Jenkins A T. J. Phys. Chem. B, 2014,118: 5418-5427
76 Kim J M, Ji E K, Woo S M, Lee H, Ahn D J. Adv. Mater., 2003,15(13): 1118-1121
77 Su Y L. J. Colloid Interface Sci., 2005,292(1): 271-276
78 Stanish I, Santos J P, Singh A. J. Am. Chem. Soc., 2001,123(5): 1008-1009
79 Lim M C, Shin Y J, Jeon T J, Kim H Y, Kim Y R. Anal. Bioanal. Chem., 2011,400(3): 777-785
80 Eaidkong T, Mungkarndee R, Phollookin C, Tumcharern G, Sukwattanasinitt M, Wacharasindhu S. J. Mater. Chem., 2012,22 (13): 5970-5977
81 Pumtang S, Siripornnoppakhun W, Sukwattanasinitt M, Ajavakom A. J. Colloid Interface Sci., 2011,364(2): 366-372
82 Jung S H, Jang H, Lim M C, Kim J H, Shin K S, Kim S M, Kim H Y, Kim Y R, Jeon T J. Anal. Chem., 2015,87(4): 2072-2078
83 Yaji T, Izumi K, Isoda S. Appl. Surf. Sci., 2002,188(3): 519-523
84 Jo S, Yoshikawa H, Fujii A, Takenaga M. Appl. Surf. Sci., 2006,252(20): 7383-7388
85 Yapor J P, Alharby A, Gentry-Weeks C, Reynolds M M, Alam A K M M, Li Y V. ACS Omega, 2017,2(10): 7334-7342
86 Li Y, Wang L, Wen Y, Ding B, Sun G, Ke T, Chhen J, Yu J. J. Mater. Chem. A, 2015,3(18): 9722-9730
87 Tahir M N, Nyayachavadi A, Morin J F, Simon R G. Polym. Chem., 2018,9(22): 3019-3028
88 Traiphol N, Chanakul A, Kamphan A, Traiphol R. Thin Solid Films, 2017,622(331): 122-129
89 Yoon J, Chae S K, Kim J M. J. Am. Chem. Soc., 2007,129(11): 3038-3039
90 Wang D E, Zhao L, Yuan M S, Chen S W, Li T, Wang J. ACS Appl. Mater. Interfaces, 2016,8(41): 28231-28240
91 Lio A, Reichert A, Ahn D J, Nagy J O, Salmeron M, Charych D H. Langmuir,1997,13(24): 6524-6532
92 Eckhardt H, Boudreaux D S, Chance R R. J. Chem. Phys.,1986,85(7): 4116-4119
93 Hankin S H W, Downey M J, Sandman D J. Polymer,1992,33(23): 5098-5101
94 Lee D C, Sahoo S K, Cholli A L, Sandman D J. Macromolecules, 2002,35(11): 4347-4355
95 Chen X, Zhou G, Peng X, Yoon J. Chem. Soc. Rev., 2012,41(13): 4610-4630
96 Su Y L, Li J R, Jiang L. Colloids Surf. B, 2004,39(3): 113-118
97 Su Y L, Li J R, Jiang L, Cao J. J. Colloid Interface Sci., 2005,284(1): 114-119
98 Neumann G, Noda T, Kawaoka Y. Nature, 2009,459(7249): 931-939
99 Park J, Ku S K, Seo D, Hur K, Jeon H, Shvartsman B, Seok H K, Mooney D J, Lee K. Chem. Commun., 2016,52(68): 10346-10349
100 Oliveiraa T V, Soaresa N F F, Coimbraa J S R, Andradea N J, Mourab L G, Medeirosa E A A, Medeiros H S. Sens. Actuators B, 2015,221(31): 653-658
101 Tao J, Xu X, Wang S, Kang T, Guo C, Liu X, Cheng H, Liu Y, Jiang X, Mao J, Gou M. ACS Macro Lett., 2019,8: 563-568
102 Koh J J, Liu S, Zeng W, Zou H, Wang L, Suresh V, Beuerman R, Cao D. Sens. Actuators B, 2013,178: 563-571
103 Yan X, An X. RSC Adv., 2014,4(36): 18604-18607
104 Li L, An X, Yan X. Colloids Surf. B, 2015,134: 235-239
105 Kim C, Lee K. Biomacromolecules, 2019,20(9): 3392-3398
106 Mills G B, Moolenaar W H. Nat. Rev. Cancer, 2003,3(8): 582-591
107 Wang Y, Pei H, Jia Y, Liu J, Li Z, Ai K, Lu Z, Lu L. J. Am. Chem. Soc., 2017,139(33): 11616-11621
108 Liu X, Tang Y, Wang L, Zhang J, Song S, Fan C. Wang S. Adv. Mater., 2007,19(11): 1471-1474
109 Jannah F, Kim J M. Dyes Pigments, 2019,169: 15-21
110 Zambelli B, Musiani F, Benini S, Ciurli S. Acc. Chem. Res., 2011,44(7): 520-530
111 Wang J W, Zheng F, Chen H, Ding Y, Xia X H. ACS Sens., 2019,4: 977-983
112 Haridas V, Sadanandan S, Collart-Dutilleul P Y, Gronthos S, Voelcker N H. Biomacromolecules, 2014,15 (2): 582-590
113 Wang X, Sun X, Hu P A, Zhang J, Wang L, Feng W, Lei S, Yang B, Cao W. Adv. Funct. Mater., 2013,23 (48): 6044-6050
114 Jeong J P, Cho E, Yun D, Kim T, Lee I S, Jung S. Polymers, 2017,9(4): 127
Advances in Fabrication of Polydiacetylene Vesicles
and Their Applications in Medical Detection
HAO Yu-Jia, ZHU Guang-Ming*
(College of Natural and Applied Sciences, Northwestern Polytechnical University, Xi' an 710129, China)
Abstract Polydiacetylenes (PDAs) have received increasing attention as smart materials owing to their unique optical and electronic properties. PDAs are the most commonly synthesized as self-assembled bilayer vesicles via 1,4 addition polymerization. Vesicles are often perceived as closely mimicking the cell membrane, thus functioning as convenient biomimetic platforms. PDAs undergo colorimetric and fluorescent transition in response to external stimuli. Therefore, PDA vesicles can be used for medical detection, such as bacteria, viruses, proteins, and enzymes, etc. In this review, the preparation of PDA vesicle sensing systems and the mechanism of solid phase polymerization are summarized. The relative applications of PDA vesicle sensing systems in medical detection are introduced. Besides, the shortcomings and issues to be solved, and future directions are also discussed and prospected.
Keywords Polydiacetylene; Vesicle; Self-assembly; Solid phase polymerization; Medical detection; Review
(Received 18 September 2019; accepted 4 November 2019)
