硅量子点荧光传感器快速检测鲜奶中的四环素
2020-02-29杨彩玲赵雪珺李建颖赵国虎张丽曹文涛
杨彩玲,赵雪珺,李建颖,赵国虎,2,张丽,曹文涛
1(兰州城市学院 化学化工学院,甘肃 兰州,730070) 2(“城市环境污染控制”甘肃省高校省级重点实验室,甘肃 兰州,730070)3(西北师范大学 化学化工学院,甘肃 兰州,730070)
四环素(tetracycline,TET)是一种价格低廉且最为常用的广谱性抗生素,能有效抑制革兰氏阳性和阴性细菌、立克次体、滤过性病毒、螺旋体和寄生虫等感染[1],作为饲料添加剂和治疗药物被大量用于预防和治疗奶牛乳房炎等严重疾病,但使用不当或滥用会导致牛奶中过量残留,对消费者健康造成危害,如引起过敏反应或抗药性、损害肝脏、使肠胃功能紊乱等[2-3]。国际卫生组织、欧盟和我国规定四环素在牛奶中的最大残留限量为100 μg/L[4-5]。但即使牛奶中残留水平很低,长期饮用也会在人体内蓄积,增大健康风险。我国乳业自“三聚氰胺”事件之后,乳品质量有了很大提高,但迄今为止,鲜牛奶中抗生素残留超标现象还时有发生,特别是一些个体散卖的鲜牛奶[6-9],因此,监测四环素在鲜牛奶中的残留情况十分必要。现有的四环素残留检测方法主要有酶联免疫法、高效液相色谱法、液质联用法、毛细管电泳法等[10]。酶联免疫法抗体制备时间长,稳定性差;色谱法灵敏度高,可以多组分同时测定,但仪器昂贵、操作复杂耗时,还需要专业的操作人员,限制了它们在现场和实时检测中的应用。因此,建立一种简便、快速、灵敏的四环素测定方法,对牛奶质量控制具有重要意义。
近年来,基于量子点的荧光传感分析方法因灵敏度高、选择性好、响应时间短、操作简便及成本低等诸多优点而备受关注,已广泛应用于药物残留[11-14]、生物毒素[15]、违禁添加[16]等食品安全检测。在抗生素检测方面,毛永强[13]、YANG等[17]分别通过制备CdTe量子点和碳量子点对牛奶中的土霉素和鱼肉中的四环素进行了灵敏测定。相比于金属半导体量子点和碳量子点,硅量子点(silicon quantum dots, SiQDs)不仅水溶性好,光稳定性强,无毒,并且拥有高的荧光量子产率和丰富的硅源,在分析检测、生物成像、药物传递等领域应用前景广阔[18-21]。本文以水热法合成硅量子点,利用四环素能有效猝灭硅量子点荧光,首次提出了基于硅量子点荧光传感的四环素检测新方法,应用于鲜牛奶中四环素残留的测定,并对传感机理进行了研究,旨在为四环素残留的快速检测提供一种新思路。
1 实验部分
1.1 仪器与试剂
TECNAIG2型场发射透射电子显微镜,美国FEI公司;FLS920型稳态/瞬态荧光光谱仪,英国EI公司;NEXUS 670型红外光谱仪,美国 Thermo Nicolet公司;RF-5301型荧光分光光度计,日本岛津公司;Tu-1810紫外可见分光光度计,北京普析通用仪器有限责任公司。
无水柠檬酸、KCl、MgCl2、CaCl2、NaCl、硝酸锌、FeCl3,广州化学试剂厂;半胱氨酸、甘氨酸、酪氨酸、L-苯丙氨酸、N-(β-氨乙基)-γ-氨丙基甲基二甲氧基硅烷(AEAPMS),上海阿拉丁试剂公司;磷酸、醋酸、硼酸、维生素C,国药集团化学试剂公司;四环素、土霉素、红霉素,上海恒远生物科技有限公司;葡萄糖、蔗糖,重庆茂业化学试剂有限公司;乳糖、EDTA,成都市科龙化工试剂厂。以上试剂均为分析纯,实验用水为超纯水。
1.2 实验方法
1.2.1 SiQDs的制备
SiQDs的制备参照文献[22]并修改如下:在50 mL锥形瓶中加入5 mL 超纯水,然后在搅拌下依次加入50 mg无水柠檬酸和1.0 mL AEAPMS,充分搅拌后将上述混合溶液转移至聚四氟乙烯高压反应釜中,240 ℃反应2 h,自然冷却至室温。准确移取250 μL SiQDs 溶液加水稀释并定容至50 mL,储存在4 ℃冰箱中备用。
1.2.2 荧光测定
在10 mL比色管中,依次加入一定体积不同浓度四环素标准溶液和30 μL上述稀释后的SiQDs溶液,用pH 7.0的B-R缓冲溶液稀释定容至5.0 mL,摇匀,静置1 min后在室温及激发光波长为370 nm条件下测定体系荧光光谱(激发和发射狭缝宽度均为5 nm)。根据lg(F0/F)与C(四环素浓度)绘制工作曲线(F0和F分别代表未加入和加入 TET 时的荧光强度)。
1.2.3 牛奶样品的处理和测定
生鲜牛奶购自当地7个不同散养售卖点。每个点相隔1 d购买1份,各买3份,共收集样品21份,所有样品均于购买当天处理后冰箱冷藏保存。样品处理过程为:准确移取鲜奶5.0 mL,加入含有20 mmol/L EDTA的McIlvaine buffer 缓冲溶液(pH 5.0)3 mL,质量分数10%的三氯乙酸2 mL,涡旋振荡5 min,之后在4 ℃ 10 000 r/min下离心10 min以脱去蛋白质,再向上清液中加入2 mL氯仿涡旋振荡5 min以除去脂肪并再次离心。取上清液用1 mol/L NaOH溶液调节pH为7.0,经0.45 μm微孔膜过滤后准确移取4.5 mL,按1.2.2的方法制备待测样品溶液进行荧光测定,平行测定3次。
2 结果与讨论
2.1 量子点的形貌结构、光学性质及稳定性

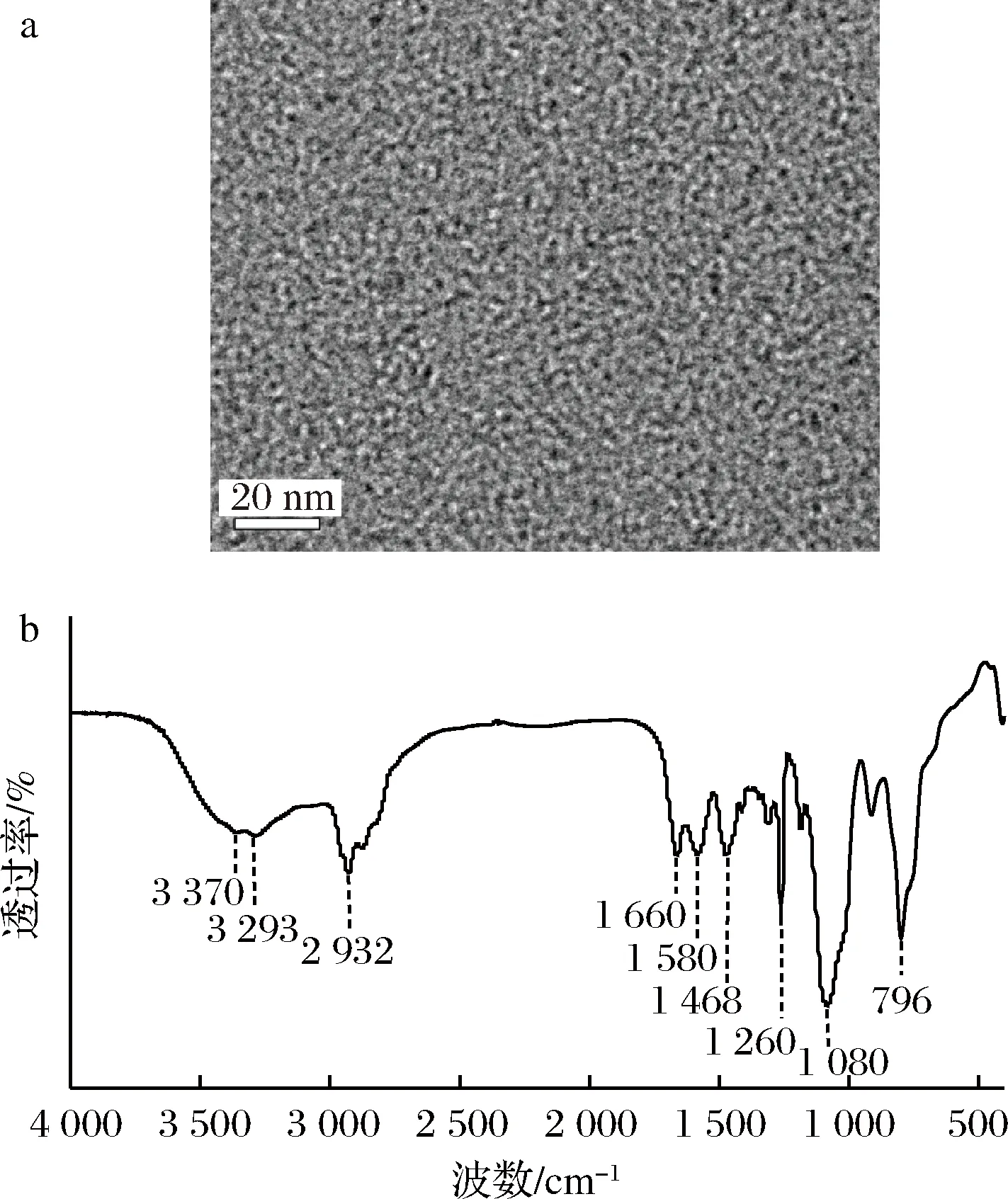
a-SiQDs的TEM图片;b-SiQDs的红外光谱图图1 SiQDs 的表征Fig.1 Characterization of SiQDs
通过FLS920型稳态/瞬态荧光光谱仪测量[23]并计算该量子点的绝对荧光量子产率为18.93%。根据图2-a SiQDs在不同激发波长下扫描的发射光谱图,该量子点发射峰位置与激发光无关,说明所制备的SiQDs的发射光不具有激发光依赖特性,但发射光强度随激发波长的增加先增大后减小,在370 nm达到最大。SiQDs的紫外吸收光谱和荧光激发、发射光谱如图2-b所示,230 nm 处出现的吸收峰可能是羰基发生π-π*电子跃迁引起,同时SiQDs 表面的官能团发生n-π*跃迁造成了352 nm处出峰。SiQDs 最佳激发波长为370 nm,最佳发射波长为465 nm;内插图显示,SiQDs在自然光下接近无色,365 nm紫外光照射下发出明亮的蓝光。
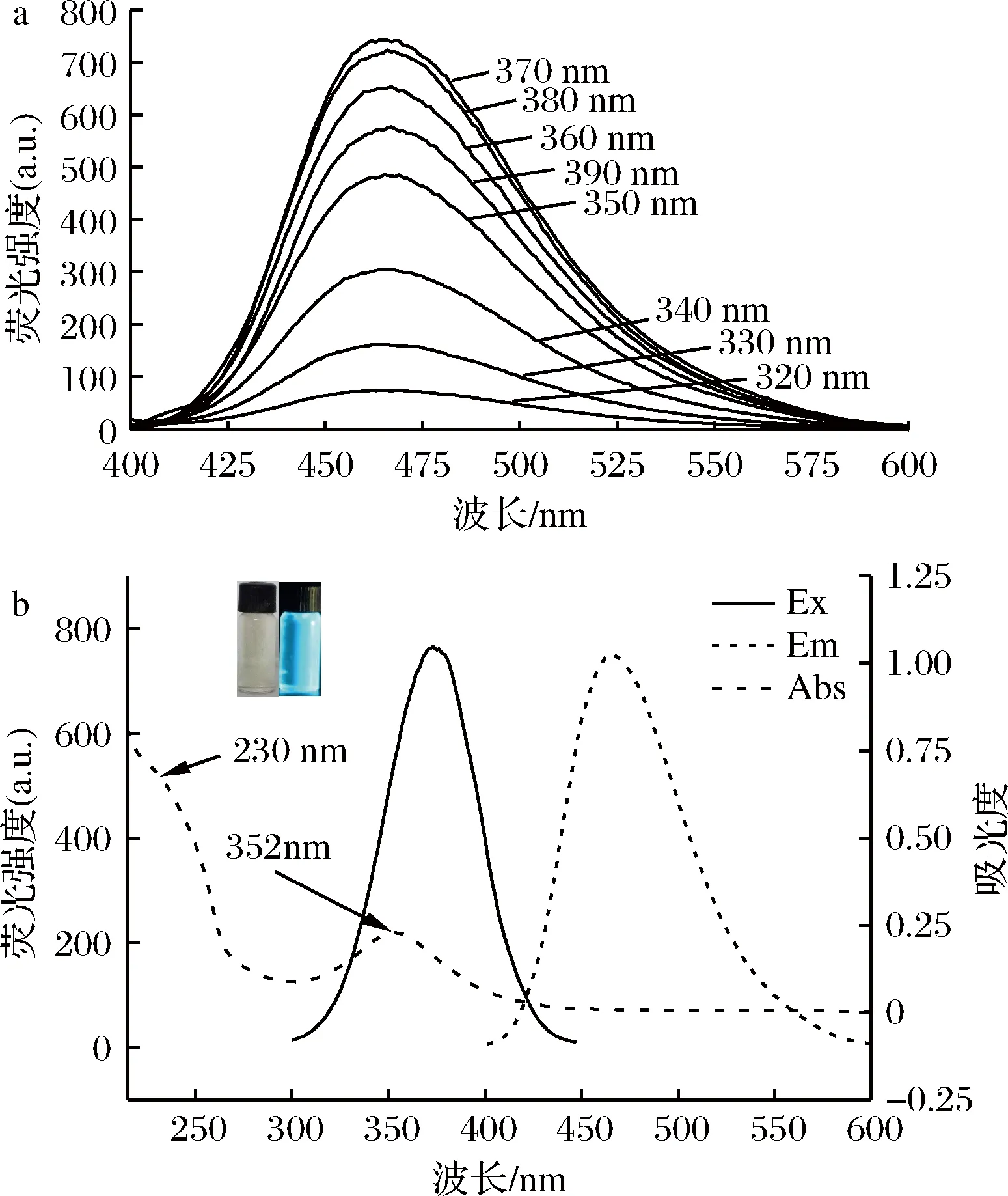
a-不同激发波长下的荧光光谱图;b- UV-vis、荧光激发和发射光谱、自然光和365 nm下照片图2 SiQDs的光谱图Fig.2 The spectrum of SiQDs
测定不同酸度(pH 3~12)B-R缓冲溶液中SiQDs 的荧光强度发现,当pH 3时,SiQDs 的荧光强度相对较低,pH 在4~9之间时,SiQDs 的荧光强度较高且稳定;而当 pH>9 时,其荧光强度又逐渐增大。这主要是由于SiQDs 表面官能团的质子化-去质子化作用引起的。此外,向溶液中加入一定浓度NaCl,观察到SiQDs在盐浓度为0~100 mmol/L的范围内荧光强度没有明显改变。比较在370 nm 激发光连续照射0~30 min以及保持溶液温度分别为20、25、35、45 ℃的条件下SiQDs的荧光强度,发现SiQDs的荧光强度基本不变,以上说明所制备的SiQDs具有良好的稳定性和强的抗光漂白能力。
2.2 溶液酸度和反应时间的选择
溶液酸度会影响量子点的发光性质,通常也会影响量子点与目标分析物之间的相互作用。图3-a是在pH 3~12的测定体系中加入四环素后荧光猝灭效率(F0/F)随pH变化的情况。可以看出,在所测试的pH范围内,pH=7时猝灭最好。因此,实验选择在pH 7的B-R缓冲液中进行测定。图3-b是在pH为7的荧光测定体系中加入四环素分别反应0、0.5、1、2、3、4、5、10、15、20、30 min后测定的荧光强度,由图可见,猝灭在1min内即可达到平衡,说明利用该方法能够实现对四环素的快速检测。
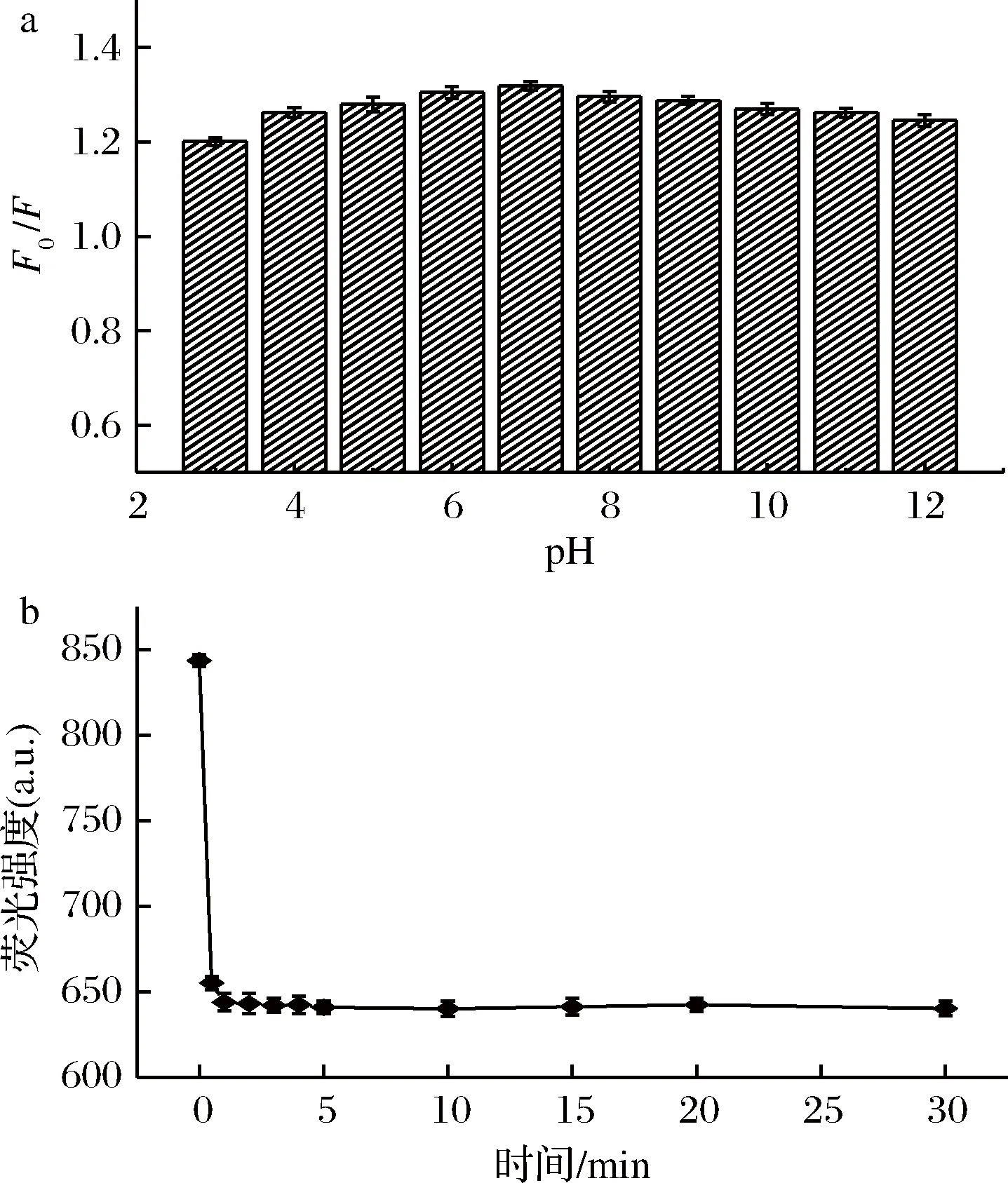
a-溶液酸度对体系荧光猝灭的影响;b-反应时间对体系荧光猝灭的影响图3 实验条件的选择(cTET=6 μmol/L)Fig.3 Selection of experimental conditions
2.3 量子点对四环素的选择性
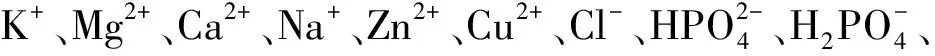
2.4 样品分析
2.4.1 工作曲线
按照1.2.2实验方法,测定加入不同浓度四环素标准溶液后体系的荧光光谱,结果显示:随着四环素浓度的增加,体系荧光强度逐渐降低。四环素在0.05~90 μmol/L的浓度范围内与体系相对荧光强度的对数lg(F0/F)呈良好线性关系,线性方程为lg(F0/F)=0.0118 4c+0.015 78,相关系数R2为0.999 4, 检出限为18 nmol/L (3σ/k),低于鲜乳中规定的四环素限量标准。对含有6.0 μmol/L四环素的荧光体系平行测定8次,相对标准偏差为2.7%,说明该方法具有良好的重现性,能满足实际样品中四环素分析要求。
2.4.2 样品测定结果及回收率
在选定的实验条件下,根据实验方法测定生鲜牛奶中四环素的残留量。结果表明,21份生鲜奶中均未检出四环素,一定程度上说明该地区目前生鲜牛奶中四环素残留风险较小。任取其中一份样品进行加标回收率试验,加标水平为75、100、200 μg/L,处理方法与样品相同,每个浓度水平重复测定6次,测得3个浓度水平的加标回收率为92.36%~104.07 %,相对标准偏差(RSD)为2.1%~4.2%(表1),表明所建立的方法准确可靠,可用于实际乳样分析。

表1 四环素在生鲜奶中的回收率(n=6)Table 1 Recoveries of TET in fresh milksamples(n=6)
注:ND代表低于检测限
2.5 猝灭机理
从图4可以看出,SiQDs 的激发光谱在300~450 nm的波长范围内(曲线a),四环素在此范围内有吸收,吸收峰位于355 nm(曲线b),二者间有相当程度的光谱重叠,满足发生荧光内滤的条件,可以推断猝灭机理主要是内滤效应。因此,当体系中加入四环素后,作为荧光体的SiQDs的激发光能量被荧光受体四环素有效吸收,导致体系荧光强度降低。
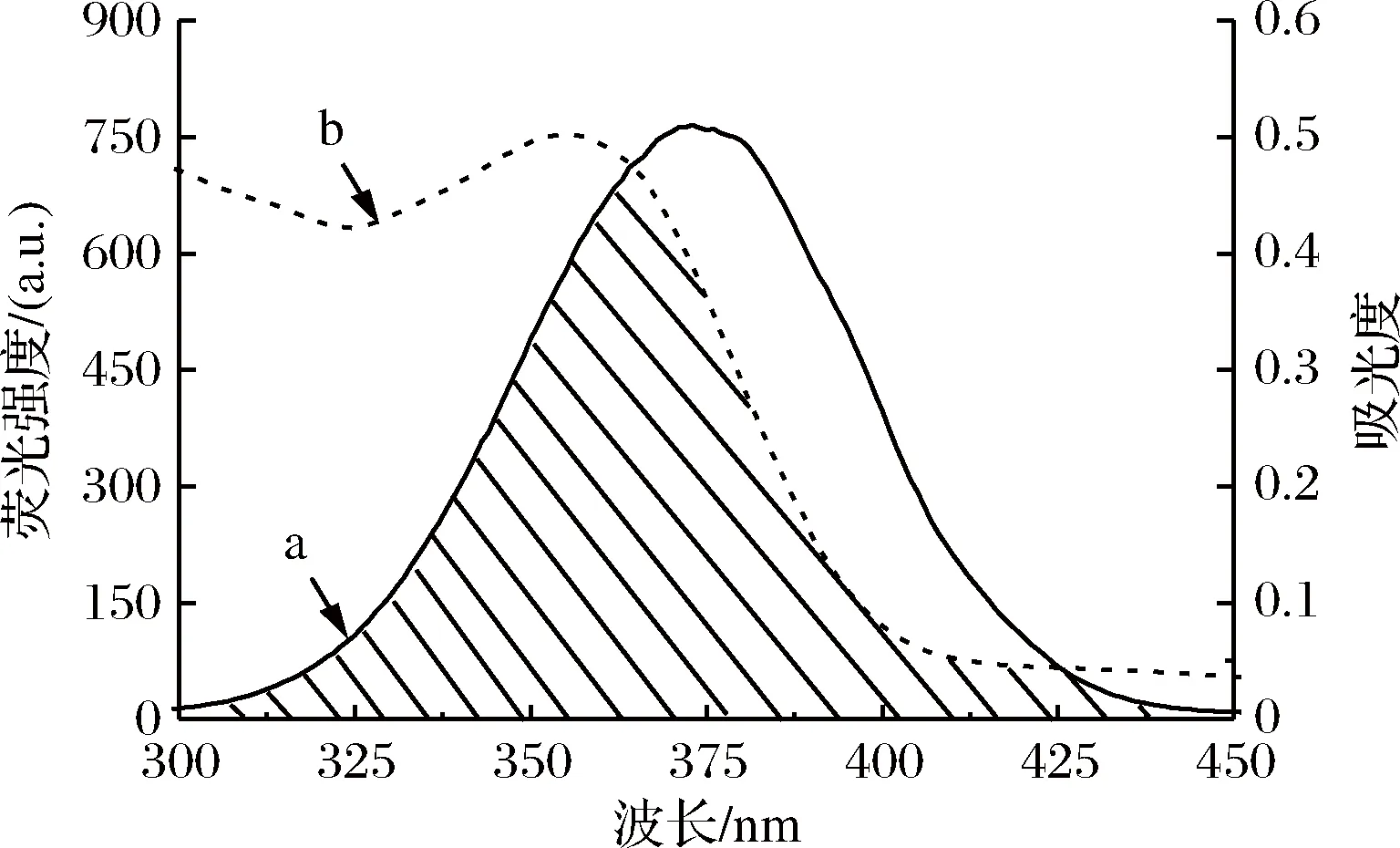
图4 SiQDs 的荧光光谱(曲线a)和四环素的UV-vis吸收光谱图(曲线b)Fig.4 Fluorescence spectra of SiQDs (curve a)andUV-Vis absorption spectra of TET(curve b)
由图5可知,四环素在274 nm 和355 nm各有一个吸收峰,当与SiQDs 相互作用后,274 nm的峰消失,355 nm的峰以及SiQDs 352 nm 的吸收峰发生红移,说明四环素分子与SiQDs中的羧基或氨基通过氢键作用形成了基态复合物,猝灭过程应为静态猝灭。因为动态猝灭只影响荧光分子的激发态,而不改变荧光物质的吸收光谱[24]。
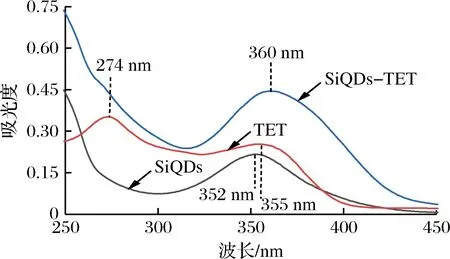
图5 SiQDs、TET以及混合溶液的UV-vis吸收光谱Fig.5 UV-vis absorption spectra of the SiQDs,TET andthe mixture of the SiQDs and TET
进一步通过测量加入四环素前后SiQDs 的荧光寿命进行确定,发现加入四环素后SiQDs 的荧光寿命几乎没有改变(图6),说明猝灭为静态猝灭[25]。因此,可以认为四环素对 SiQDs 的荧光猝灭主要为内过滤效应和静态猝灭协同作用的结果。
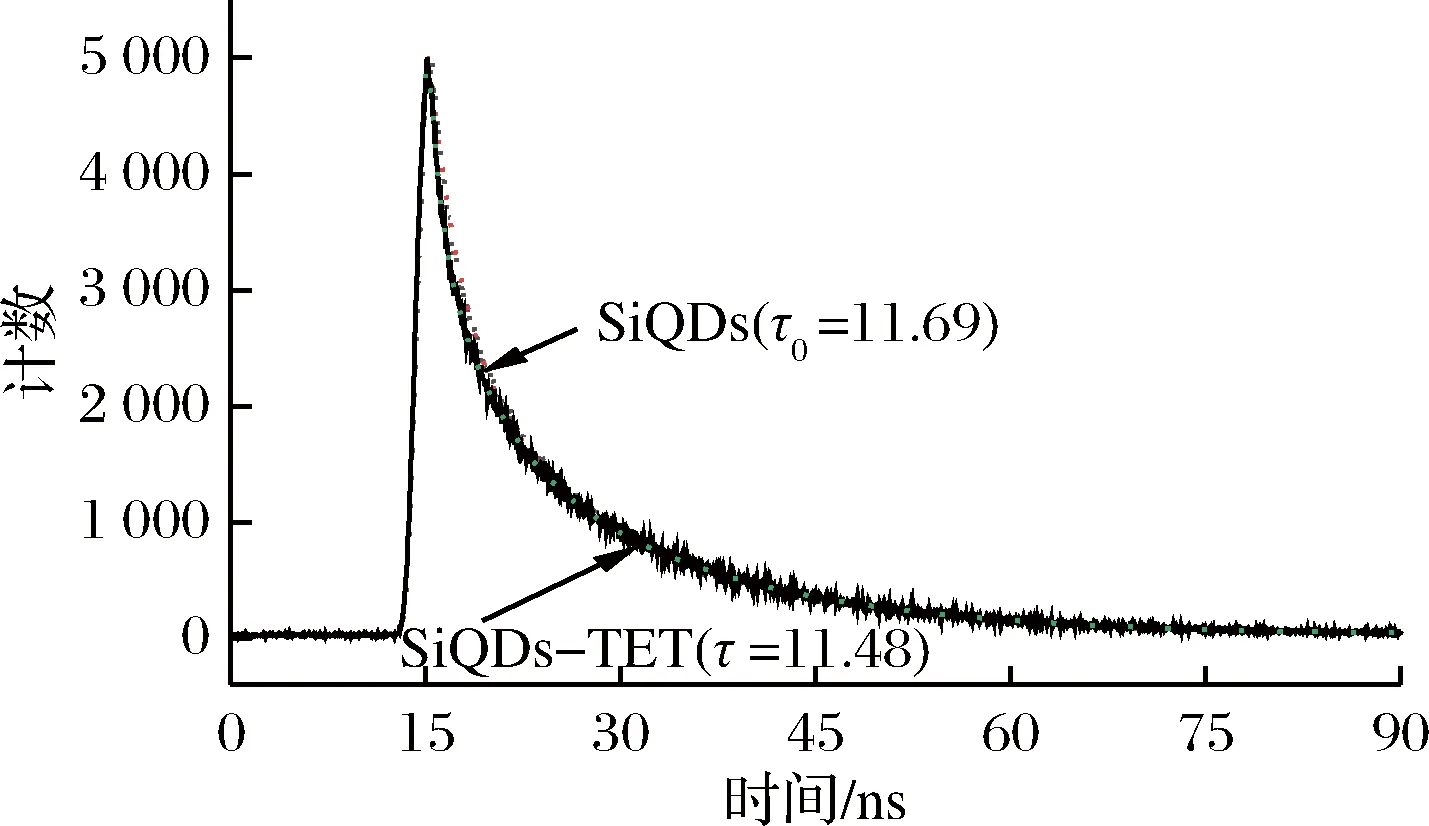
图6 加入TET前后SiQDs 的时间分辨衰减曲线Fig.6 Time-resolved decay curves of SiQDs in theabsence and presence of TET
3 结论
本文通过水热法一步合成了水溶性的荧光硅量子点,合成方法简单,避免了耗时的表面修饰过程,所合成的 SiQDs 具有良好的热稳定性、优异的耐盐性和抗光漂白能力。利用四环素与SiQDs之间存在内过滤效应和静态猝灭的协同作用构建了新型荧光传感器用于鲜奶中四环素测定,方法快速、灵敏、准确,并且不需要昂贵的设备,为鲜奶中四环素残留检测提供了一种新思路。
