在线固相萃取净化-高效液相色谱法测定人血浆中的霉酚酸
2020-02-28许泽君杨新磊
许泽君,景 霞*,孙 芳,吉 超*,杨新磊
(1.南京医科大学 附属儿童医院,江苏 南京 210008;2.安捷伦科技(中国)有限公司,上海 200080 )
吗替麦考酚酯(Mycophenolate mofetil,MMF)是一种肾移植时常用的免疫抑制剂[1],在进入人体后快速水解成霉酚酸而发挥药效[2]。近年来,该药被发现在治疗肾病综合症方面也有着良好的应用前景,并且由于其肾毒性较小,在儿科临床上使用日益增多[3-5]。有研究表明,在固定剂量下,成人体内的药物暴露量有很大差异,个体间药代动力学差异甚至大于10 倍[6],再加上该药的服用疗程较长,这种差异可能造成疗效不足或者不良反应[1,3-5]。为保证合理用药[7],进行霉酚酸的血药浓度监测十分必要。
酶放大免疫法(EMIT)[8-9]、高效液相色谱法(HPLC)[10-13]及液相色谱-串联质谱法(LC-MS/MS)[14-15]是常用的3种血药浓度检测手段。其中,酶放大免疫法快速方便,但特异性较差,代谢物会产生免疫交叉反应,导致结果正偏离[16],且所用试剂盒较为昂贵。高效液相色谱法中,由于血浆含有大量的蛋白和磷脂等大分子杂质,需要对血样进行复杂的前处理后才能进样分析,造成时间、人力及试剂的消耗较大,且还会引入误差。LC-MS/MS同样涉及复杂的样品前处理,且仪器采购与成本维护昂贵,对操作人员的要求较高。基于医院临床的大样本和时效性等特点,传统的液液萃取、离线固相萃取等方法由于其步骤繁琐、重现性欠佳等局限性,不适用于医院检测。而在线固相萃取(Online SPE)是一种基于阀切换的自动化样品前处理技术,具有分析快速、操作简单、重现性好、易于联用等优点。本方法使用限进介质填料的萃取柱,自动化去除经蛋白沉淀后样品中的少量残余蛋白与磷脂,以实现对目标物的富集与净化。进一步将Online SPE与HPLC 联用则可克服HPLC灵敏度不足、干扰较大的局限性,在临床血药浓度检测领域具有良好的应用前景,已用于茶碱[17]、左旋舒必利[18]、氨磺必利[19]等药物的血药浓度监测。本文建立了Online SPE-HPLC联用测定血浆中霉酚酸浓度的分析方法,减少了分析步骤和人为因素引入的误差,节省了试剂消耗,可以满足医院临床监测的需求。
1 实验部分
1.1 仪器与试剂
Online SPE-HPLC系统购自安捷伦公司,包括一维模块(G7111A泵、G7167自动进样器、G7167B柱温箱和G7114A检测器)和二维模块(G7120A泵、G7117B 二极管阵列检测器和G1170A双二位四通阀);十万分之一分析天平(MS205DU,瑞士Mettler Toledo公司);Vortex-5涡旋振荡器(江苏海门市其林贝尔仪器制造有限公司);Abbott离心机( 德国Hettich公司)。
霉酚酸标准品(纯度大于98%,Lot.086M4010V,Sigma公司);甲醇、乙腈(色谱纯,国药集团化学试剂有限公司);纯化水采用二级反渗透装置纯水系统(南京慧城水处理设备有限公司)自制。空白血浆由南京医科大学附属儿童医院提供。
1.2 样本的制备

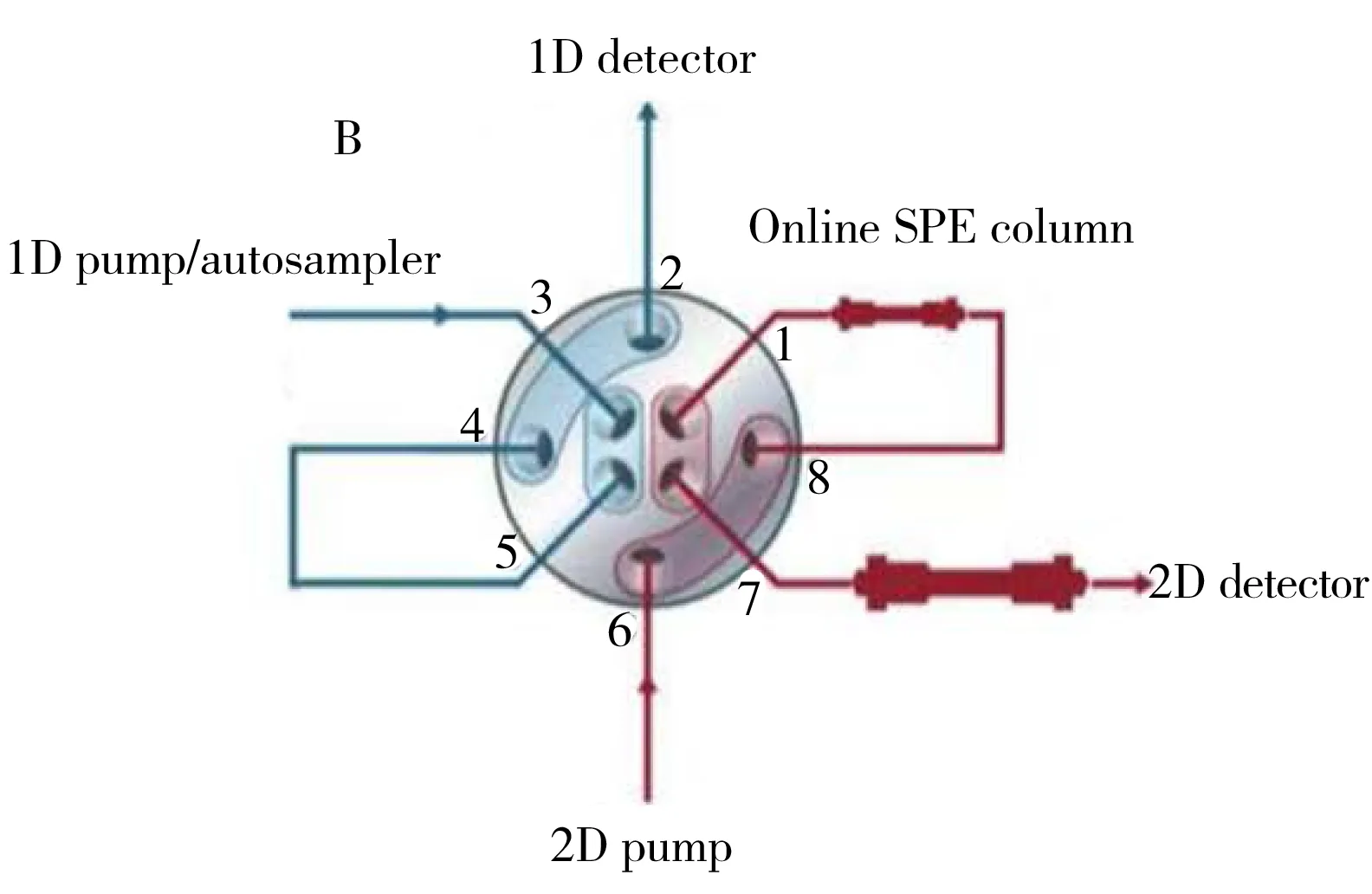
图1 Online SPE系统连接示意图
精密称取霉酚酸标准品12.5 mg至25 mL容量瓶,加甲醇至刻度后,超声2 min。置于-30 ℃冰箱内保存。用空白血浆稀释至目标浓度后,取200 μL置于1.5 mL 离心管中,加入甲醇400 μL,涡旋振荡5 min后,10 800 r/min离心8 min,取上清液,进样检测。
1.3 液相色谱与在线固相萃取条件
固相萃取柱:Capcell PAK MF Ph-1(4.6 mm×10 mm);分析柱:Poroshell 120Å EC-C18柱(4.6 mm×50 mm,2.7 μm)。1D泵流动相A为甲醇,流动相B为0.5%磷酸水溶液,梯度洗脱,流速为1.0 mL/min;2D泵流动相A为乙腈,流动相B为0.1%三乙胺溶液(10%磷酸调节pH至3.5±0.1),流速为0.8 mL/min;柱温30 ℃,检测波长215 nm,进样量20 μL。
Online SPE系统连接如图1所示。实验过程中,0~2.0 min,切换阀处于1~3连接状态,1D泵将样品上样至固相萃取柱,样品中的霉酚酸在固相萃取柱中保留,而蛋白等大分子物质不保留,直接流入废液;2.0~2.5 min,切换阀处于1~7连接状态,2D泵流动相将霉酚酸从固相萃取柱转移至分析柱;2.5~9.0 min,切换阀处于1~3连接状态,1D泵冲洗固相萃取柱并将流动相平衡至初始状态,分析泵继续完成霉酚酸的分离和冲洗平衡,具体洗脱程序和阀切换参数见表1。

表1 在线固相萃取、分析洗脱及阀切换的程序
2 结果与讨论
2.1 样品制备条件的优化
在线固相萃取虽可去除血浆中的蛋白,但将血浆直接进样,会由于蛋白含量过高,影响萃取柱的寿命和方法的稳定性。因此在样品制备过程中,先加入有机溶剂沉淀去除大部分蛋白,再进行固相萃取及分析。考察了常用有机蛋白沉淀试剂甲醇及乙腈对样品中蛋白的去除效果,发现经乙腈处理后的样品溶液经过长时间放置或者冷藏后会再次析出蛋白,可能会造成萃取小柱堵塞。因此实验选择甲醇作为最佳蛋白沉淀试剂。
此外,样品制备时,样品-甲醇的体积比也会影响血浆中蛋白沉淀的效率。随着甲醇比例的增加,沉淀效率略有提高,但同时也会稀释样品中的霉酚酸浓度。考虑到在线固相萃取中还会进一步去除蛋白,为了保证方法的灵敏度,本实验选择样品-甲醇的体积比为1∶2。
2.2 固相萃取条件的优化
固相萃取主要目的是纯化样品,在去除血浆中蛋白质等大分子的同时,保留药物小分子。常规的反相色谱柱对大分子蛋白具有一定的保留作用,而高有机相比例会造成蛋白质析出,长期使用会导致柱头堵塞,使用寿命缩短。限进介质色谱柱是近年发展起来的新型色谱柱,其通过尺寸排阻、键合长链亲水基团等手段,达到降低大分子蛋白在柱内保留的效果,可有效去除样品中残余的蛋白,并保留小分子药物。该类萃取柱的键合相类型较多,如反相C18、C8、苯基、离子交换等。不同的键合相具有不同的化合物选择性。本实验中,由于目标物霉酚酸具有苯环共轭结构,能与苯基柱中的苯环键合相产生Π-Π相互作用,从而形成较好的特异性吸附。此外,苯基柱的反相保留能力比C18弱,将霉酚酸从苯基柱上洗脱时有机相比例无需太高,进入C18分析柱时可再次产生柱头富集效果,避免产生溶剂效应,使目标物峰形更加尖锐。综上考虑,本实验选择苯基型的Capcell PAK MF Ph-1作为萃取柱。该柱不仅纯化效果好,而且可重复使用千次以上[19]。
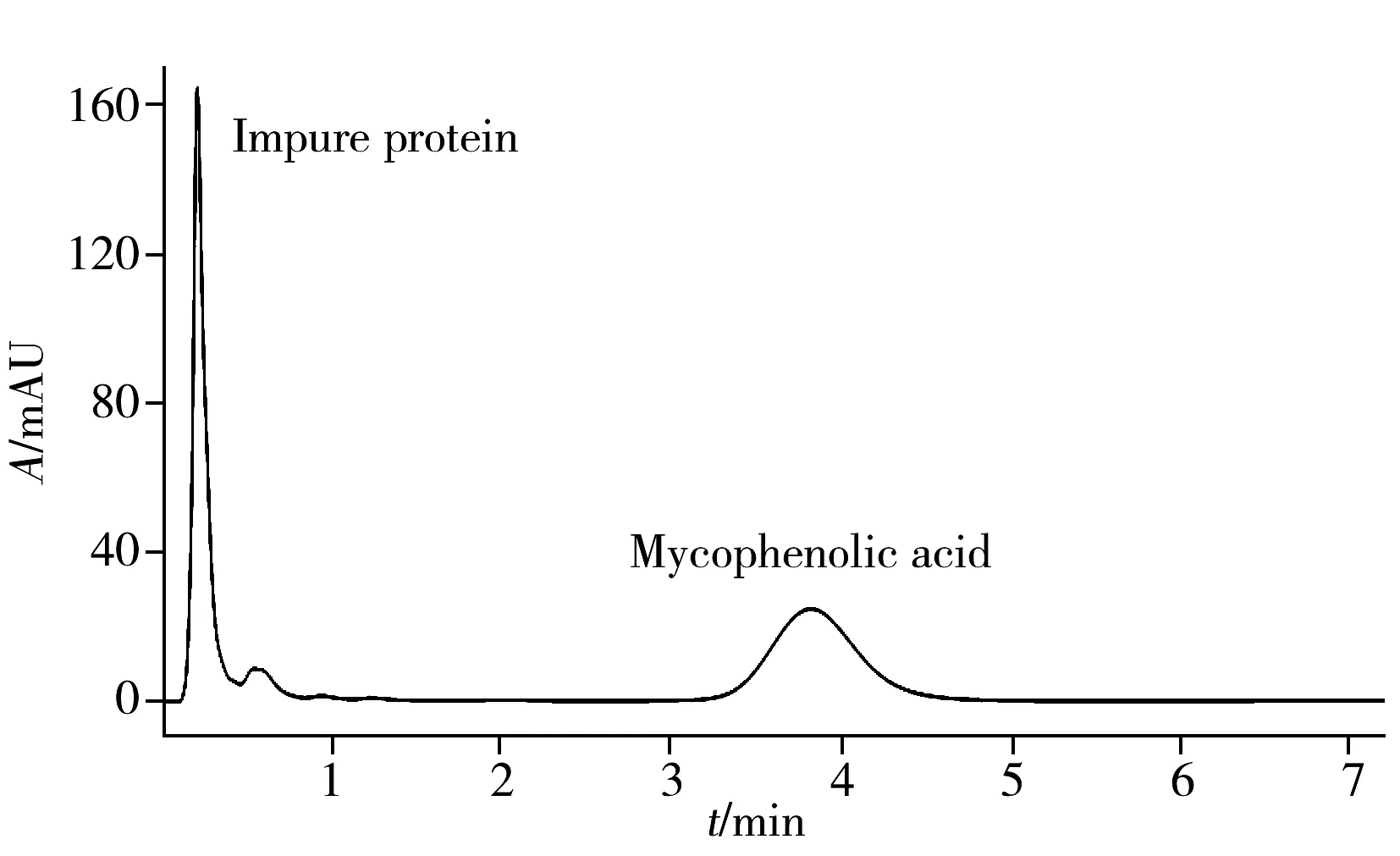
图2 霉酚酸在1D检测器的色谱图(不切换)
由于固相萃取流动相的选择会直接影响蛋白的去除效果及目标物的保留,本实验中,目标物霉酚酸具有羧基及酚羟基两个易电离基团,因此选择在固相萃取的水相中加入0.5%磷酸,使流动相呈酸性,以抑制霉酚酸的电离,增强其在萃取柱上的保留,具体流动相选择见“1.3”。实验结果显示,当流动相中甲醇比例为20%时,样品中的蛋白可快速通过萃取柱,霉酚酸在固相萃取柱的保留时间可达3.7 min左右(见图2)。因此,本实验选择2 min时切换阀,能保证蛋白质已完全洗脱去除,而霉酚酸仍保留在萃取柱中。在2.5 min阀切回时,1D检测器未检出霉酚酸的信号,表明霉酚酸均已进入分析柱(图3)。
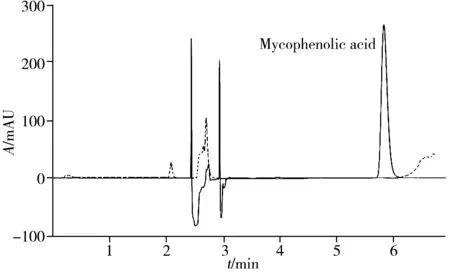
图3 2~2.5 min阀切换时,1D()和2D()检测器的色谱图
2.3 分析条件的优化
2.3.1 流动相的优化比较了乙腈、甲醇作为有机相以及pH值不同(pH 3.5、6.5)的水相等不同流动相组成对霉酚酸峰形和响应的影响。结果表明,以乙腈为有机相时,霉酚酸的响应明显高于甲醇;由于霉酚酸易电离,需要较低pH值产生抑制,因此选择pH 3.5的水相时能得到更好的峰形;为了进一步提高峰形的对称性,实验选择加入0.1%三乙胺抑制霉酚酸拖尾,并选择了水相与有机相的比例为65∶35,以获得适中的保留时间。
2.3.2 波长的优化对标准品进行全波长扫描,发现霉酚酸在215 nm 和254 nm附近均有较强的吸收光谱,且以215 nm处的响应更高,因此实验选择215 nm为最佳检测波长。
2.4 分析方法的评价
2.4.1 专属性在优化实验条件下,分别处理空白血浆和含霉酚酸的血浆,进样分析。结果显示,霉酚酸在分析柱中的保留时间为5.7min,与空白血浆相比,无血浆内源性物质干扰,且峰形良好(图4)。
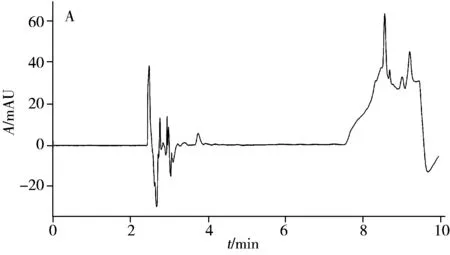
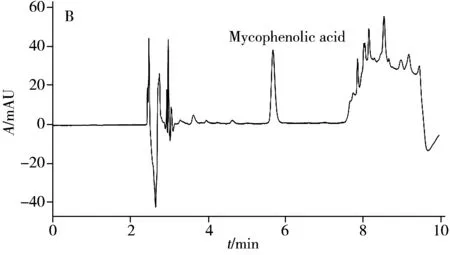
图4 空白血浆(A)和加标血浆样品(B)的色谱图
2.4.2 标准曲线、检出限与定量下限以血浆为基质,配制霉酚酸质量浓度分别为0.20、0.39、0.78、1.56、3.13、6.25、12.50、25.00、50.00 μg/mL的系列基质加标样品。以霉酚酸的峰面积(Y)和对照品质量浓度(X,μg/mL)作线性回归,得到回归方程为Y=58.16X+1.58,r=0.999 8。定量下限(S/N=10)为0.20 μg/mL,检出限(S/N=3)为0.07 μg/mL。
2.4.3 回收率与相对标准偏差配制0.39、25.00、50.00 μg/mL高、中、低3 种霉酚酸质量浓度的血浆样品,每种浓度1 d 内按“1.3”方法平行操作5次,连续测定3 d。根据标准曲线,考察对照品的加标回收率及日内、日间精密度。测得霉酚酸的日内回收率为98.0%~105%,日内相对标准偏差(Intra-RSD)为2.6%~3.1%,日间回收率为96.2%~104%,日间RSD(Inter-RSD)为2.9%~3.3%,方法的准确度与精密度均良好(表2)。

表2 血浆样品中霉酚酸的回收率与相对标准偏差
2.4.4 方法的稳定性考察了含高、中、低3 种质量浓度(0.39、25.00、50.00 μg/mL)霉酚酸的血浆样品在不同温度条件下(室温放置6 h、4 ℃冰箱放置12 h、反复冻融3次)的稳定性。结果显示,霉酚酸在上述3种温度条件下的RSD为1.3%~5.8%,表明霉酚酸在这3种条件下基本稳定(表3)。
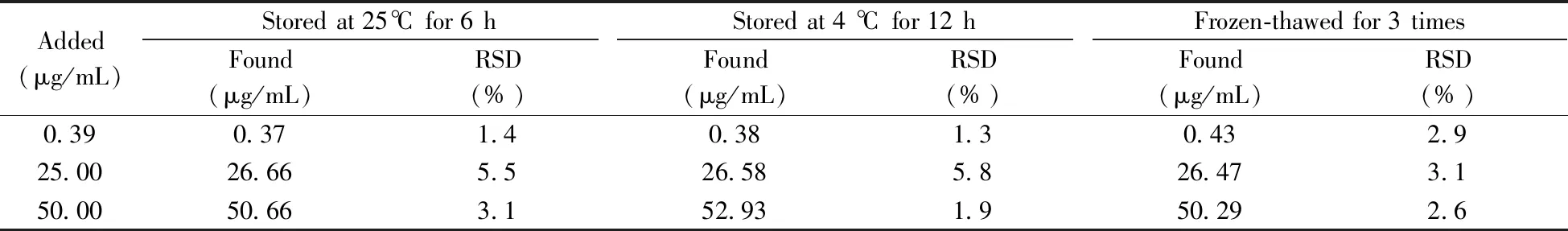
表3 加标血浆样品中霉酚酸的稳定性
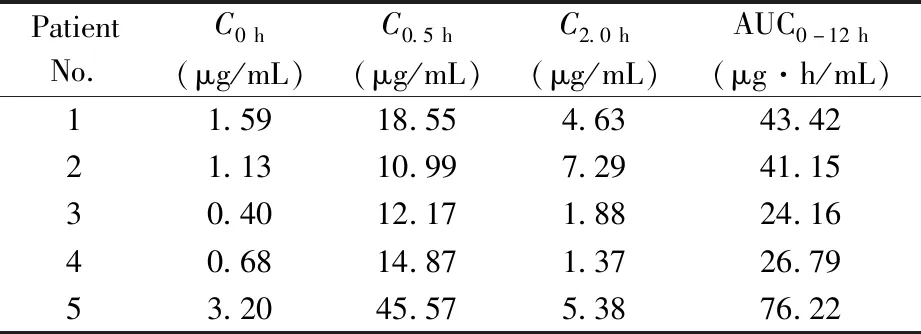
表4 5例患者的霉酚酸测试结果
2.5 临床应用
采集5例服用吗替麦考酚酯的待测患者0、0.5、2.0 h后的血样,高速离心后取血浆按本方法对霉酚酸的质量浓度进行检测(C0 h、C0.5 h、C2.0 h)。结果显示(见表4),霉酚酸的质量浓度均在线性范围内。通过有限采样法可以计算霉酚酸在患者体内的暴露量(AUC0-12 h)[20],以评价霉酚酸的吸收程度及其在体内的暴露特性,从而供临床参考。
3 结 论
本研究建立了血浆中霉酚酸的在线样品前处理-高效液相色谱分析方法。本方法样本前处理简便,分析过程高效快速,准确度和精密度良好,为临床开展霉酚酸的血药浓度监测提供了适宜的分析方法。
