人工腹腔积液辅助射频消融术治疗比邻胃肠道肝癌的临床疗效
2020-02-26张建松侯森郑路敏
张建松,侯森,郑路敏
1许昌市中心医院肝胆外科,河南 许昌461000
2许昌市第二人民医院外科,河南 许昌4610000
肝癌是一种与乙型肝炎/丙型肝炎病毒、酗酒、 肝硬化等密切相关的恶性肿瘤,患者的临床表现包括肝区腹痛、黄疸、腹腔积液及消瘦等[1-2]。射频消融术是无法耐受根治术的肝癌患者的常用治疗术式,可通过电热效应促进肝癌病灶凝固坏死,从而治疗肝癌[3]。然而,对于比邻胃肠道的肝癌病灶,射频消融术的疗效并不佳,与以下因素有关:为避免损伤胃肠道,消融往往需控制在一定范围内,这将导致消融不足,残留的肿瘤将再次恢复活性,最终导致复发[4]。因此,临床开发了人工腹腔积液技术来隔离胃肠道及肿瘤,以避免电热效应损伤胃肠道,同时确保消融范围的有效性[5]。本研究分析了人工腹腔积液辅助射频消融术治疗比邻胃肠道肝癌患者的临床疗效,现报道如下。
1 对象与方法
1.1 研究对象
选取2016 年3 月至2019 年12 月许昌市中心医院收治的76 例比邻胃肠道肝癌患者。纳入标准:①肝癌的诊断参考《原发性肝癌诊疗规范(2011 年版)》[6]中的标准;②经计算机断层扫描(CT)、磁共振成像(MRI)及肝脏穿刺活检证实为肝癌;③术前影像学检查显示单个肿瘤最大直径≤3.0 cm,肿瘤数目≤3 个,肿瘤接近胃肠道,最短距离≤0.5 cm;④患者年龄为19~79 岁:⑤Child-Pugh 分级 为A~B级。排除标准[7-8]:①已发生远处转移;②肿瘤发生胆管侵犯、血管转移;③合并其他部位恶性肿瘤;④合并胃肠道梗阻、穿孔等并发症;⑤合并凝血功能障碍、活动性出血疾病;⑥贫血。采用随机数字表法将76 例患者分为观察组和对照组,每组38例。观察组中,男22 例,女16 例;年龄为48~77 岁,平均(63.8±5.3)岁;术前血清甲胎蛋白(α-fetopro‐tein,AFP)水平为(542.8±96.1)ng/ml;Child-Pugh 分级:A 级20 例,B 级18 例;病灶最大直径为(2.10±0.60)cm;病灶数目为(1.96±0.54)个。对照组中,男20 例,女18 例;年龄为45~79 岁,平均(64.2±7.1)岁;术前血清AFP 水平为(528.1±93.2)ng/ml;Child-Pugh 分级:A 级24 例,B 级14 例;病灶最大直径为(2.01±0.57)cm;病灶数目为(1.89±0.60)个。两组患者的性别、年龄、术前血清AFP 水平、Child-Pugh分级、病灶最大直径及病灶数目比较,差异均无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会审批通过,所有患者及家属均对本研究知情并签署知情同意书。
1.2 手术方法
对照组患者采用射频消融术治疗,患者局部麻醉后,于超声引导下进行射频针穿刺操作,消融仪器为Cool-tip RF Ablation System 内冷型射频电极针,将射频针植入病灶底部,对病灶进行消融,时间为15~20 min,如病灶体积较大,可进行多点重叠消融。消融完毕后,退出消融针,同时对穿刺针道进行消融。消融1 天后对患者进行超声复查,观察是否存在残留病灶,如有可再次消融[9]。
观察组患者采用人工腹腔积液辅助射频消融术治疗,患者局部麻醉后,于超声引导下对病灶区域胃肠道间隙进行穿刺,置入扩管针,扩张腹腔,并接入单腔中心静脉导管,静脉滴注生理盐水。对于存在既往腹腔手术史或存在腹腔器官粘连的患者,可选用注射器进行生理盐水推入。生理盐水滴入或注入量以手术视野清晰且可将胃肠道安全隔离为准(与肿瘤间隙≥5 mm),生理盐水总量为350~2000 ml。随后于超声引导下进行消融操作,具体步骤同对照组。
1.3 观察指标及评价标准
依据实体瘤疗效评价标准(response evaluation criteria in solid tumor,RECIST)[10]评价射频消融治疗效果:完全缓解(complete response,CR),靶病灶完全消失,至少持续4 周;部分缓解(partial response,PR),所有靶病灶的长径总和缩小≥30%,至少持续4周;疾病稳定(stable disease,SD),所有靶病灶的长径总和缩小<30%或增加<20%;疾病进展(progres‐sive disease,PD),所有靶病灶的长径总和增加≥20%或出现新病灶。总有效率=(CR+PR)例数/总例数×100%。依据影像学结果评估两组患者的肿瘤病灶坏死程度:部分坏死,肿瘤病灶的坏死程度为50%~89%;不完全坏死,肿瘤病灶的坏死程度为90%~99%;完全坏死,肿瘤病灶的坏死程度达到100%[11-12]。采用化学发光法检测两组患者术前及术后4 周的血清AFP 水平。采用普朗PUZS-300A/X 全自动生化分析仪检测两组患者术前、术后1 周、术后4 周的肝功能指标,包括天冬氨酸转氨酶(aspartate aminotrans‐ferase,AST)、丙氨酸转氨酶(alanine aminotransfer‐ase,ALT)、总胆红素(total bilirubin,TBIL)[13]。比较两组患者的卡氏功能状态(Karnofsky performance status,KPS)评分及并发症发生情况。
1.4 统计学方法
采用SPSS 21.0 软件对数据进行统计分析,计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料以例数和率(%)表示,组间比较采用χ2检验,等级资料的比较采用Mann-WhitneyU检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 射频消融治疗效果的比较
观察组患者的总有效率为84.21%(32/38),与对照组患者的73.68%(28/38)比较,差异无统计学意义(χ2=1.267,P=0.260)。(表1)
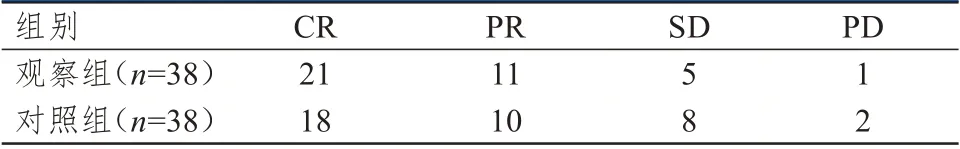
表1 两组患者的射频消融治疗效果
2.2 射频消融病灶坏死程度的比较
观察组和对照组患者射频消融病灶的坏死程度比较,差异无统计学意义(Z=-0.633,P=0.526)。(表2)

表2 两组患者射频消融病灶的坏死程度[n(%)]
2.3 血清AFP 水平和KPS 评分的比较
术前,两组患者的血清AFP 水平和KPS 评分比较,差异均无统计学意义(P>0.05)。术后4周,观察组患者的KPS 评分明显高于对照组,差异有统计学意义(P<0.01);术后4 周,两组患者的血清AFP 水平比较,差异无统计学意义(P>0.05)。(表3)
表3 手术前后两组患者血清AFP水平和KPS评分的比较(±s)

表3 手术前后两组患者血清AFP水平和KPS评分的比较(±s)
注:*与对照组术后4周比较,P<0.01
指标血清AFP水平(ng/ml)KPS评分时间术前术后4周术前术后4周观察组(n=38)542.8±96.1 143.8±43.2 75.2±2.7 81.8±3.3*对照组(n=38)528.1±93.2 151.4±47.3 74.7±2.4 79.5±3.0
2.4 肝功能指标的比较
术前及术后4 周,两组患者的血清ALT、AST、TBIL 水平比较,差异均无统计学意义(P>0.05)。术后1 周,两组患者的血清ALT、AST、TBIL 水平均高于本组术前,差异均有统计学意义(P<0.05);术后1 周,两组患者的血清ALT、AST、TBIL 水平比较,差异均无统计学意义(P>0.05)。(表4)
表4 手术前后两组患者肝功能指标的比较(±s)

表4 手术前后两组患者肝功能指标的比较(±s)
注:*与本组术前比较,P<0.05
指标ALT(U/L)AST(U/L)TBIL(μmol/L)时间术前术后1周术后4周术前术后1周术后4周术前术后1周术后4周观察组(n=38)26.1±5.3 177.3±39.6*27.6±6.0 22.3±5.0 172.1±41.8*23.0±5.5 11.3±3.2 27.2±5.5*13.6±3.7对照组(n=38)25.7±5.5 190.5±41.7*28.3±5.7 23.6±5.8 184.0±56.3*24.2±6.1 12.0±3.9 29.0±6.2*12.5±4.0
2.5 并发症发生情况的比较
术后,观察组患者疼痛、恶心的发生率均低于对照组,差异均有统计学意义(P<0.05);观察组和对照组患者发热、腹胀的发生率比较,差异均无统计学意义(P>0.05)。(表5)

表5 两组患者并发症发生情况的比较
3 讨论
如果肝癌比邻胃肠道,其超声成像将因胃肠道影响而出现边界不清的情况,进而影响射频消融时操作人员对病灶大小、边界以及周围器官关系的判断,最终导致两种结果:一是病灶消融不足,或反复消融;二是消融损伤比邻的胃肠道,引发胆漏、肠漏、出血等并发症,而人工腹腔积液技术可有效避免这两种结果的出现[14]。
人工腹腔积液技术可在肝癌病灶与比邻胃肠道间建立一条人工的腹腔积液隔离带,用以消弭射频消融的电热效应,进而保护胃肠道,确保病灶消融的有效性[15]。为保障腹腔积液隔离带对消融电热效应的有效吸收,其厚度往往需大于2 mm,本研究将腹腔积液隔离带厚度设置为5 mm,旨在吸收消融电热效应的同时保护邻近胃肠道。此外,人工腹腔积液建立后,肝癌病灶的超声成像将不受胃肠道阴影的影响,这对提高病灶成像清晰度、确保穿刺及消融工作的准确性及针对性具有重要意义。需要注意的是,腹腔积液隔离带的电热效应吸收能力可在一定程度上降低病灶消融所需的能量,因此,临床需酌情增加消融针数及消融时间[16]。本研究结果显示,观察组和对照组患者的总有效率和射频消融病灶的坏死程度比较,差异均无统计学意义(P>0.05);术后4 周,观察组患者的KPS评分明显高于对照组,差异有统计学意义(P<0.01)。表明人工腹腔积液辅助射频消融在提高肝癌患者术后生活能力上具有显著优势,其原因可能是人工腹腔积液技术可有效减少消融造成的邻近脏器误损伤情况,这对降低患者胆漏、肠漏的发生率,减轻患者痛苦具有重要作用,因此可提高患者术后生活质量,提高患者的自主生活能力。本研究结果还显示,术后,观察组患者疼痛、恶心的发生率均低于对照组,差异均有统计学意义(P<0.05);观察组和对照组患者发热、腹胀的发生率比较,差异均无统计学意义(P>0.05),这也佐证了前述结论。
ALT、AST、TBIL 是临床常用的肝脏功能评估指标[17]。本研究结果显示,术前两组患者的血清ALT、AST、TBIL 水平比较,差异均无统计学意义(P>0.05)。术后1 周,两组患者的血清ALT、AST、TBIL 水平均高于本组术前,差异均有统计学意义(P<0.05);术后1 周,两组患者的血清ALT、AST、TBIL 水平比较,差异无统计学意义(P>0.05)。表明两种方式均可有效增强患者的肝脏功能,这与消融手术可有效灭杀肝癌细胞、维护健康肝脏细胞的功能有关。超声引导下的消融操作具有极高的准确性,这有效降低了消融电热效应对健康肝脏细胞的损伤率,并加速了患者术后肝脏功能的恢复进程[18]。腹腔脏器粘连将导致肝癌病灶与周围组织器官紧密连接,并增加消融电热效应对周围脏器的损伤率。这一粘连现象同时也将增加人工腹腔积液的建立难度,常规的滴入操作可能无效[19]。因此,本研究选择注射器推入腹腔积液,这一操作成功构建了腹腔积液隔离带,保护了比邻胃肠道,确保了消融的有效性。
人工腹腔积液辅助射频消融术操作时,可实时监控腹腔积液的注入量,确保腹腔积液隔离带厚度的有效性。同时治疗后可通过引流导出腹腔积液,部分留存的腹腔积液往往可在术后2~3 天内吸收。相较于人工胸腔积液辅助射频消融术,人工腹腔积液辅助技术具有操作简便、成本低廉等多种优势,同时还可有效避免胸腔积液、血气胸等并发症的发生,具有极高的推广价值[20]。
综上所述,人工腹腔积液辅助射频消融术治疗比邻胃肠道肝癌患者可在保证手术效果的同时,减少手术并发症,进一步提高术后患者的生活质量。
