新型PPAR-γ调控剂VSP-17对DSS诱导溃疡性结肠炎的抑制作用
2020-02-14徐笑天王宇晖
徐笑天,王宇晖
(桂林医学院,广西 桂林 541004)
0 引言
溃疡性结肠炎(UC)是一种容易反复发作并且难以根治的肠道疾病,临床症状主要表现为腹痛、腹泻、便血、体重减轻等[1],其发病机制尚不明确,目前认为UC的发病与环境因素、饮食因素、遗传因素有关[2-3]。当前临床常使用的罗格列酮不良反应较多,因此研究出一种不良反应少并且高效的药物迫在眉睫[4]。本实验拟通过构建小鼠UC模型,探讨新型PPAR-γ调控剂VSP-17对UC的抑制作用,并比较VSP-17和罗格列酮的抗UC疗效和不良反应,为VSP-17的临床应用提供有效依据。
1 材料与方法
1.1 仪器。XS105DU电子天平(瑞士mettler toledo梅特勒托利有限公司);GENEX单道可调移液器(上海宝予德科学仪器有限公司);正置成像系统显微镜(OIYMPUS DP27上海比目仪器厂);Medium-S800UVF实验室纯水系统(上海和泰仪器有限公司)。
1.2 试剂的配制
1.2.1 2.5%DSS溶液:精密称取12.0 g DSS,溶于480 mL超纯水中,现配现用。
1.2.2 0.01MPBS溶液:称取10 g磷酸缓冲盐粉剂,溶于1000 mL超纯水中。
1.2.3 3%过氧化氢溶液:取9 mL的双蒸水,加入1 mL 30%过氧化氢,混匀。
1.2.4 10 g/L邻甲苯胺溶液:取8.5 mL的冰醋酸,加入1.5 mL的邻甲苯胺,混匀,避光保存。
1.3 实验动物。健康雄性SPF级C57BL/6小鼠53只,6-8周龄,体重18-22 g,由湖南斯莱克景达实验动物有限公司提供,许可证号:SCXK2014-0002。
1.4 实验方法。将53只C57BL/6小鼠随机分为6组,即正常组、模型组、美沙拉嗪组(200 mg/kg)、罗格列酮低剂量组(20 mg/kg)、罗格列酮高剂量组(100 mg/kg)、VSP-17组(20 mg/kg),其中正常组6只,模型组15只,其余每组各8只。正常组自由饮用超纯水,其余各组给予相同体积的2.5%DSS溶液7d建立模型,随后更换超纯水自由饮用3 d。在建立模型期间,除正常组和模型组外,其余的分组每天灌胃给予相应药物,并且每天对小鼠进行称重并记录,收集粪便,观察粪便性状及进行DAI评分。在第10 d灌胃后一小时,颈椎脱臼处死,将小鼠解剖,取小鼠结肠,测量并记录结肠长度,随后用0.01 mol/L PBS溶液清洗结肠,从远心端处取结肠1 cm置于4%组织细胞固定液,用于HE染色,作结肠病理组织学检查,在光学显微镜下观察结肠病变情况。
1.5 统计学分析。利用GraphPad Prism 5.0统计软件进行数据分析。以P<0.05为具有统计学差异。
2 结果
2.1 DAI评分情况。正常组小鼠DAI分数无明显浮动,与正常组相比较,从第2天开始,模型组由于体重不断减轻、粪便出现隐血和稀便的情况,DAI分数逐渐上升,至实验进行的第8天达到高峰值;与模型组相比较,给药组的DAI分数在第8天达到高峰值后逐渐下降,其中VSP-17组的下降最为明显(P<0.05),其次是罗格列酮低剂量组、美沙拉嗪组、罗格列酮高剂量组。说明药物对疾病均有抑制作用且VSP-17的抑制作用最明显,详见表1。
2.2 小鼠结肠长度变化。与正常组相比较,模型组小鼠由于肠道受到刺激,结肠有所缩短;与模型组相比较,VSP-17组、美沙拉嗪组和罗格列酮低剂量组的结肠有所增长,其中罗格列酮低剂量组的结肠长度最长(P<0.05),罗格列酮高剂量的结肠最短。
表1 药物对各组小鼠DAI评分的影响
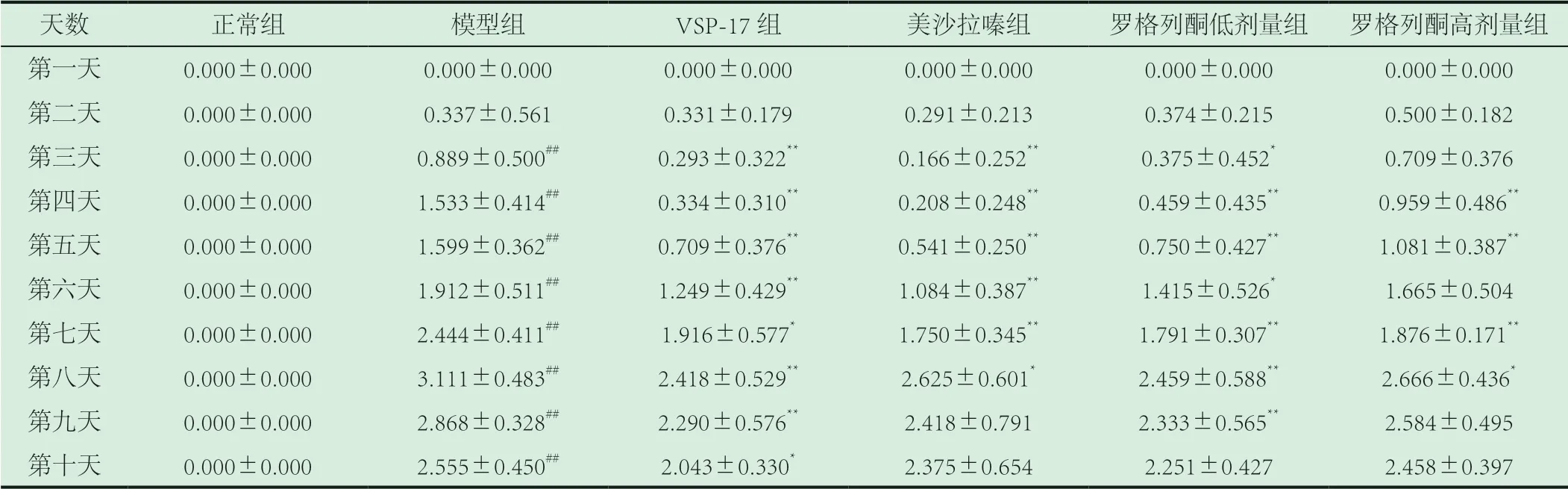
表1 药物对各组小鼠DAI评分的影响
注:##P<0.01,模型组vs正常组;⋆P<0.05,给药组vs模型组;⋆⋆P<0.01,给药组vs模型组。
天数 正常组 模型组 VSP-17组 美沙拉嗪组 罗格列酮低剂量组 罗格列酮高剂量组第一天 0.000±0.000 0.000±0.000 0.000±0.000 0.000±0.000 0.000±0.000 0.000±0.000第二天 0.000±0.000 0.337±0.561 0.331±0.179 0.291±0.213 0.374±0.215 0.500±0.182第三天 0.000±0.000 0.889±0.500## 0.293±0.322⋆⋆ 0.166±0.252⋆⋆ 0.375±0.452⋆ 0.709±0.376第四天 0.000±0.000 1.533±0.414## 0.334±0.310⋆⋆ 0.208±0.248⋆⋆ 0.459±0.435⋆⋆ 0.959±0.486⋆⋆第五天 0.000±0.000 1.599±0.362## 0.709±0.376⋆⋆ 0.541±0.250⋆⋆ 0.750±0.427⋆⋆ 1.081±0.387⋆⋆第六天 0.000±0.000 1.912±0.511## 1.249±0.429⋆⋆ 1.084±0.387⋆⋆ 1.415±0.526⋆ 1.665±0.504第七天 0.000±0.000 2.444±0.411## 1.916±0.577⋆ 1.750±0.345⋆⋆ 1.791±0.307⋆⋆ 1.876±0.171⋆⋆第八天 0.000±0.000 3.111±0.483## 2.418±0.529⋆⋆ 2.625±0.601⋆ 2.459±0.588⋆⋆ 2.666±0.436⋆第九天 0.000±0.000 2.868±0.328## 2.290±0.576⋆⋆ 2.418±0.791 2.333±0.565⋆⋆ 2.584±0.495第十天 0.000±0.000 2.555±0.450## 2.043±0.330⋆ 2.375±0.654 2.251±0.427 2.458±0.397
2.3 小鼠病理组织学变化。HE染色后,将小鼠结肠组织做成切片,在光学显微镜下观察到正常组小鼠的肠壁组织上有完整的杯状细胞,没有充血、水肿等现象;与正常组相比较,模型组随着炎症细胞的浸润,小鼠肠壁上的杯状细胞遭到破坏,并且会伴有糜烂、水肿或充血的现象;与模型组相比较,给药组随着药物的作用小鼠肠壁上原本出现的糜烂、水肿、充血等现象以及炎症细胞的浸润减少,其中VSP-17的效果较好,罗格列酮高剂量组的效果差[5]。
3 结论
通过实验发现VSP-17能改善小鼠体重下降情况,降低
DAI分数,减少粪便隐血,改善结肠缩短情况,减小结肠损伤程度。提示,VSP-17对DSS诱导UC有抑制作用。
