IGF-1介导的丰富环境对成年弱视小鼠视皮层可塑性的影响
2020-02-08罗瑜琳罗诗诗刘政海王曦琅陶利娟吴小影涂艳琼
罗瑜琳,罗诗诗,刘政海,王曦琅,陶利娟,吴小影,涂艳琼
0引言
弱视是一种严重影响视觉功能的常见儿童眼病。在视觉发育关键期内,患者如果得不到及时治疗,不仅影响视力,还可能导致双眼视觉以及立体视功能损害,严重危害家庭及社会。传统观念认为,超过视觉发育关键期的大龄儿童及成年弱视患者视功能及视皮层可塑性难以逆转,治疗无望。但近年来对弱视的研究使该观点受到新的挑战[1]。我们的前期研究已经证实,丰富环境可重塑视皮层突触可塑性,改善成年弱视小鼠的视觉功能,然而其潜在的分子机制尚不十分清楚。胰岛素样生长因子-1(IGF-1)作为一种神经生长因子,具有神经保护及调控神经系统可塑性的作用,可作为研究视皮层可塑性的指标。本研究在建立成年单眼剥夺弱视模型小鼠的基础上,观察不同饲养环境对弱视小鼠视功能及视皮层可塑性的影响,重点探讨IGF-1是否作为可能的关键因子参与弱视的发病,为临床上弱视治疗提供新的可行性思路。
1材料和方法
1.1材料
1.1.1实验动物及分组选取正常新生21日龄昆明小鼠80只。根据随机数字表法分为4组:正常组(Nor),单眼剥夺+标准环境组(MD+SE),单眼剥夺+丰富环境组(MD+EE),单眼剥夺+氟西汀组(MD+FLX)。所有小鼠采购于湖南省斯莱克景达实验动物有限公司(No.43004700018257),许可证号:SCXK(湘)2016-0001。实验得到湖南省儿童医院伦理委员会的批准(审批号HCHLL-2015-35),实验动物的处理按照《湖南省儿童医院实验动物管理与使用指南》实施。
1.1.2主要试剂及仪器全自动视觉电生理检查系统(MetroVision,法国);2.5%戊二醛,1%锇酸,日立H7700投射电镜;IGF-1兔多克隆抗体(ab9572,Abcam,英国),IGF1-R兔多克隆抗体(ab39675,Abcam,英国),IGFBP5兔多克隆抗体(ab125696,Abcam,英国),TUBULIN小鼠单克隆抗体(sc-137179,Santa Cruz美国);乙酸纤维素薄膜(浙江路桥四青生化材料厂);电泳仪(北京六一,中国)。
1.2方法
1.2.1动物模型构建及处理各模型组(MD+SE、MD+EE、MD+FLX)小鼠于出生后21d缝合右侧眼睑,建立单眼形觉剥夺弱视模型[2],在小鼠麻醉状态下,剪除右侧上下眼睑缘组织,然后行褥式缝合。在标准环境(standard enrichment, SE)中饲养2wk后剪开缝合的眼睑,并对剥夺眼行闪光视觉诱发电位检测正常眼及剥夺眼的P100波,剥夺眼的P100波幅较正常眼明显下降,潜伏期明显延长,确定建模成功。建模过程中眼睑裂开或闪光视觉诱发电位检测弱视模型失败的小鼠予以剔除,每组保留18只小鼠进行后续实验。剪开模型小鼠眼睑后,按预先分组:MD+SE组在标准环境中饲养,MD+EE组在丰富环境中饲养,MD+FLX组在标准环境中饲养,但饮用水中添加氟西汀,4wk后行视敏度检测及闪光视觉诱发电位检测(F-VEP)后处死动物,取左侧视皮层组织为后续检测准备。
1.2.2环境干预方法丰富环境条件参照Baroncelli等[3]方法设置,采用1m3的木箱,其垫料上摆放隧道、转轮、小木屋、各色积木及木梯等玩具,玩具隔天更换或交换位置,并定期清洗。MD+EE组小鼠每天置于该环境装置中6h以上,持续4wk;标准环境则按国家标准实验动物环境及设施规定的小鼠笼具原则要求饲养。

注:Nor:正常组;MD+SE:单眼剥夺+标准环境组;MD+EE:单眼剥夺+丰富环境组;MD+FLX:单眼剥夺+氟西汀组。
1.2.3小鼠视敏度检测小鼠视敏度检测方法参照Drapeau等[4]的描述,即前爪触地反射实验。操作方法[5]:用黑色的布遮挡小鼠的正常眼,将其从距离平台大约20cm处缓慢下降,若小鼠在胡须或鼻子触碰到桌面之前前爪出现探爪动作,则视为探爪成功,重复3次,以小鼠探爪成功率作为计量指标。该部分实验检测均由同一实验人员完成,观察与记录均采取盲法。
1.2.4小鼠剥夺眼F-VEP检测视敏度检测完成后,参照ISCEV标准,对各组小鼠的右眼行F-VEP检测,操作方法[6]:小鼠首先置于暗室适应30min,分别在枕骨粗隆、两耳连线与正中线交点及同侧耳处放置银针电极。用闪烁光(刺激频率1.0Hz,通频带宽0.5~85.0Hz)作为刺激光,叠加60次。检查时左眼用不透光眼罩完全遮挡,记录每次测量结果,包括P2波潜伏期及波幅,潜伏期为起点至P2波峰的距离,波幅为N2波谷至P2波峰的距离,连续测量3次,取其平均值。
1.2.5电镜检测小鼠视皮层神经元突触超微结构处死小鼠取左侧视皮层双眼区组织,经2.5%戊二醛、磷酸盐缓冲液固定2h,1%锇酸固定液固定3h,体积分数50%、70%、90%乙醇脱水15min后,90%乙醇、体积分数90%丙酮等体积混合脱水15min,90%丙酮脱水15min,包埋液包埋,60℃烤箱固化,超薄切片机50nm厚切片,质量分数3%醋酸铀-枸橼酸铅双染色。然后将制备的切片于透射电子显微镜下观察,每只小鼠随机观察记录10个突触,每组共记录80个突触进行图像分析。参照多点平均法[7]及Güldner等[8]的方法测量并记录各组小鼠视皮层神经元的突触间隙宽度、突触活性区长度及突触后致密物厚度。
1.2.6 Western Blot法检测小鼠视皮层中IGF-1、IGF-1R及IGFBP5蛋白表达分别收集各组小鼠左侧视皮层双眼区组织总蛋白,蛋白质变性后电泳,转移至PVDF膜上,用含5%牛血清白蛋白的TBST封闭,用一抗IGF-1兔多克隆抗体(1∶500)、IGF-1R兔多克隆抗体(1∶500)、IGFBP5兔多克隆抗体(1∶1000)、TUBULIN鼠单克隆抗体(1∶1000),4℃孵育过夜,TBST洗3次,每次5min,二抗(HRP羊抗兔IgG,1∶1000,Vector)孵育1h,TBST洗3次,每次5min,化学发光法检测蛋白质印迹结果。

2结果
2.1丰富环境对弱视小鼠视敏度的影响通过检测前爪触地成功率判断小鼠视敏度,各组(n=18)间小鼠前爪触地成功率比较差异有统计学意义(F=114.632,P<0.001)。MD+SE组小鼠前爪触地成功率(26.55%±4.66%)明显低于Nor组(91.73%±2.98%),差异有统计学意义(t=15.480,P<0.001);MD+EE组(90.00%±7.86%)及MD+FLX组(87.43%±5.46%)小鼠前爪触地成功率明显高于MD+SE组,差异有统计学意义(t=15.071,P<0.001;t=14.841,P<0.001);与MD+FLX组比较,MD+EE组小鼠前爪触地成功率差异无统计学意义(t=0.238,P=0.816)。
2.2丰富环境对弱视小鼠F-VEP的影响各组小鼠右眼(模型组小鼠剥夺眼)闪光视觉诱发电位检测结果见图1,表1。各组间小鼠F-VEP的P2波的潜伏期比较差异有统计学意义(F=36.510,P<0.01)。MD+SE组小鼠剥夺眼F-VEP的P2波的潜伏期较Nor组比较明显延长,差异有统计学意义(t=10.220,P<0.01);MD+EE组及MD+FLX组小鼠剥夺眼F-VEP的P2波的潜伏期较MD+SE组比较均明显缩短,差异有统计学意义(tMD+EE组 vs MD+SE组=7.051,PMD+EE组 vs MD+SE组=0.003;tMD+FLX组 vs MD+SE组=6.049,PMD+FLX组 vs MD+SE组=0.002);与MD+FLX组比较,MD+EE组小鼠剥夺眼F-VEP的P2波的潜伏期差异无统计学意义(t=1.002,P=0.322);各组间小鼠F-VEP的P2波的波幅总体比较差异有统计学意义(F=34.140,P<0.01)。MD+SE组小鼠剥夺眼F-VEP的P2波的波幅明显低于Nor组,差异有统计学意义(t=10.090,P<0.01);MD+EE组及MD+FLX组小鼠剥夺眼F-VEP的P2波的波幅均明显高于MD+SE组,差异有统计学意义(tMD+EE组 vs MD+SE组=5.030,PMD+EE组 vs MD+SE组<0.01;tMD+FLX组 vs MD+SE组=5.650,PMD+FLX组 vs MD+SE组P<0.01);与MD+FLX组比较,MD+EE组小鼠剥夺眼F-VEP 的P2波的波幅差异无统计学意义(t=0.618,P=0.539)。
2.3丰富环境对弱视小鼠视皮层神经细胞突触超微结构的影响透射电镜下观察各组小鼠左侧(模型组小鼠剥夺眼对侧)视皮层双眼区神经细胞突触超微结构的结果见表1,图2。各组间小鼠视皮层神经细胞突触间隙宽度总体差异有统计学意义(F=8.75,P=0.004)。MD+SE组小鼠视皮层神经细胞突触间隙明显宽于Nor组,差异有统计学意义(t=5.018,P<0.01);MD+EE组及MD+FLX组小鼠视皮层神经细胞突触间隙较MD+SE组明显缩窄,差异有统计学意义(tMD+EE组 vs MD+SE组=3.24,PMD+EE组 vs MD+SE组=0.0035;tMD+FLX组 vs MD+SE组=2.712,PMD+FLX组 vs MD+SE组=0.0075)。各组间小鼠视皮层神经细胞突触活性区长度总体差异有统计学意义(F=17.03,P<0.01)。MD+SE组小鼠视皮层神经细胞突触活性区长度与Nor组比较明显缩短,差异有统计学意义(t=5.772,P<0.01);MD+EE组及MD+FLX组小鼠视皮层神经细胞突触活性区长度与MD+SE组比较均增加,差异有统计学意义(tMD+EE组 vs MD+SE组=4.805,PMD+EE组 vs MD+SE组<0.01;tMD+FLX组 vs MD+SE组=6.545,PMD+FLX组 vs MD+SE组<0.01)。各组间小鼠视皮层神经细胞突触后致密物厚度总体差异有统计学意义(F=29.08,P<0.01)。MD+SE组小鼠视皮层神经细胞突触后致密物厚度与Nor组比较明显变薄,差异有统计学意义(t=8.609,P<0.01)。MD+EE组及MD+FLX组小鼠视皮层神经细胞突触后致密物厚度较MD+SE组均增厚,差异有统计学意义(tMD+EE组 vs MD+SE组=7.181,PMD+EE组 vs MD+SE组<0.01;tMD+FLX组 vs MD+SE组=6.448,PMD+FLX组 vs MD+SE组<0.01)。MD+EE组与MD+FLX组小鼠比较,视皮层神经细胞突触间隙宽度,突触活性区长度,突触后致密物厚度差异均无统计学意义(P>0.05)。
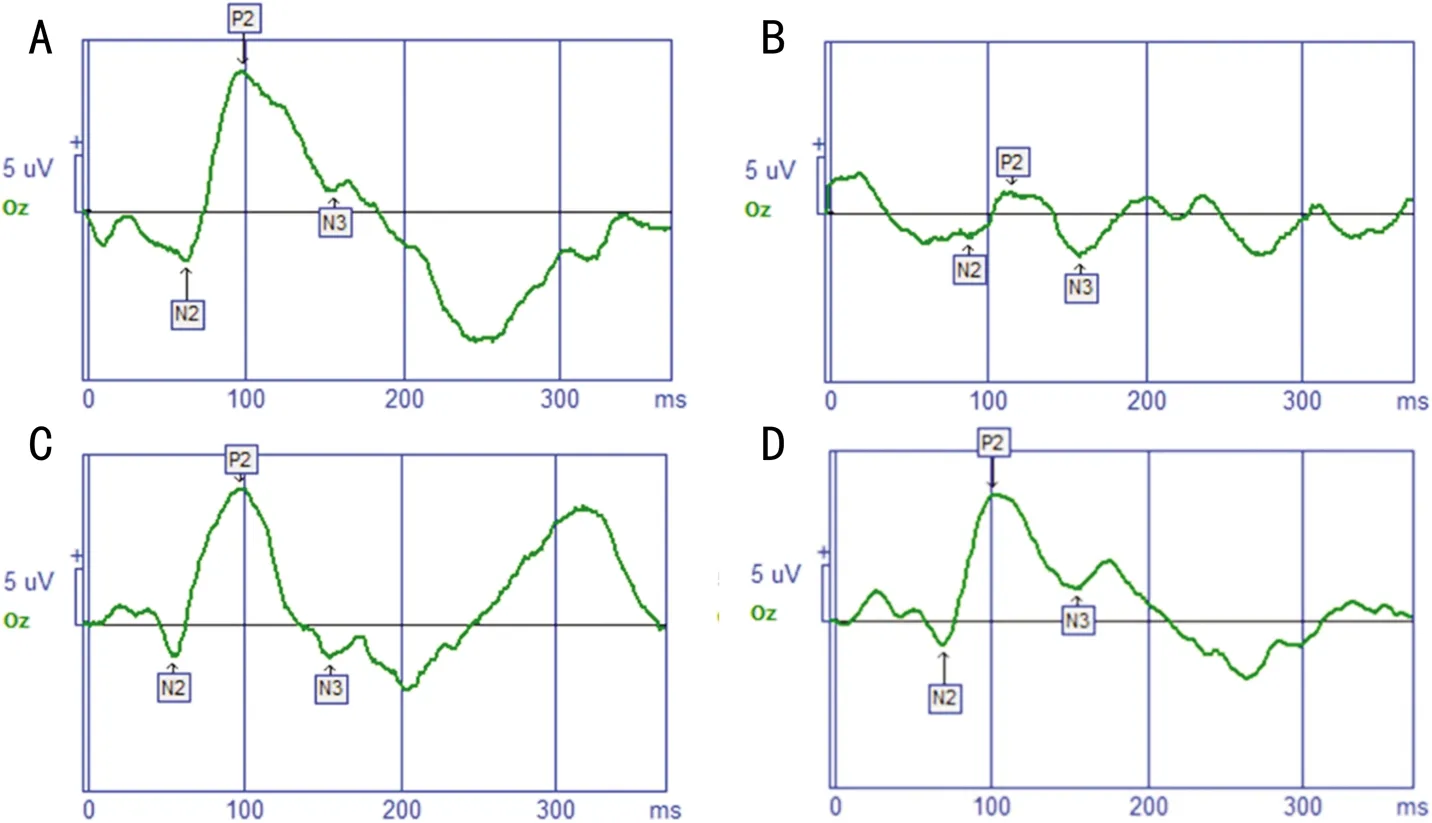
图1各组小鼠闪光视觉诱发电位P2波潜伏期及波幅比较A: Nor组;B:MD+SE组;C:MD+EE组;D:MD+FLX组。

图2电镜观察各组小鼠视皮层神经细胞突触超微结构A:Nor组;B:MD+SE组;C:MD+EE组;D:MD+FLX组。
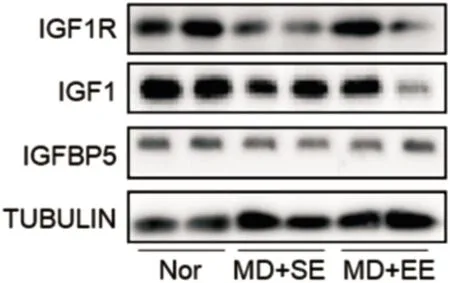
图3 Western-blot检测各组小鼠视皮层IGF-1、IGF-1R及IGFBP5蛋白表达。
2.4丰富环境对弱视小鼠视皮层IGF-1、IGF-1R及IGFBP5蛋白表达的影响Western Blot检测各组小鼠左眼(模型组小鼠剥夺眼对侧)视皮层双眼区组织的IGF-1及IGF-1R蛋白表达见表2,图3,各组间小鼠视皮层双眼区组织IGF-1蛋白表达光密度值总体差异有统计学意义(F=22.00,P<0.01)。MD+SE组小鼠IGF-1蛋白表达明显低于Nor组,差异有统计学意义(t=6.598,P<0.01); MD+EE组小鼠IGF-1蛋白的表达明显高于MD+SE组,差异有统计学意义(t=2.712,P= 0.016),但仍显著低于Nor组,差异有统计学意义(t=3.887,P=0.001)。各组间小鼠视皮层双眼区组织IGF-1R蛋白表达光密度值总体差异有统计学意义(F=67.31,P<0.01)。MD+SE组小鼠IGF-1R蛋白表达明显低于Nor组,差异有统计学意义(t=11.4,P<0.01); MD+EE组小鼠IGF-1R蛋白表达明显高于MD+SE组,差异有统计学意义(t=3.815,P=0.041),但仍显著低于Nor组,差异有统计学意义(t=7.582,P=0.001)。各组间小鼠视皮层双眼区组织IGFBP5蛋白表达光密度值总体差异无统计学意义(F=0.793,P=0.470)。

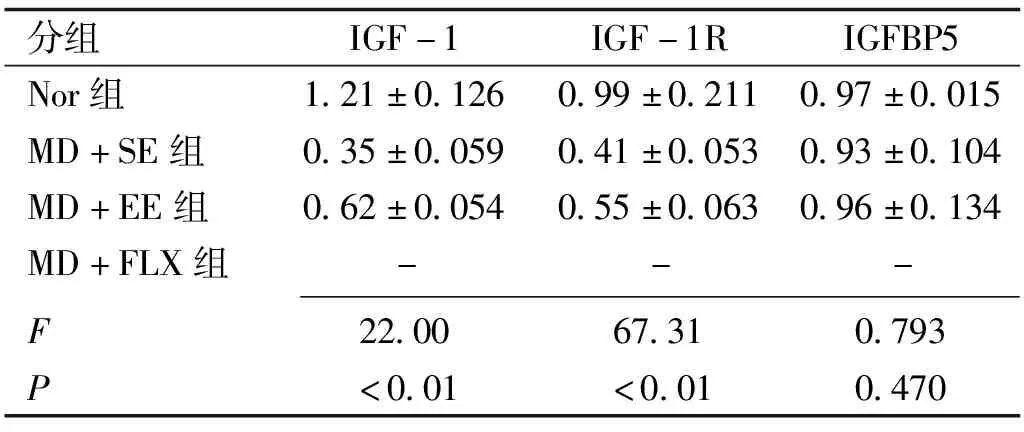
分组IGF-1IGF-1RIGFBP5Nor组1.21±0.1260.99±0.2110.97±0.015MD+SE组0.35±0.0590.41±0.0530.93±0.104MD+EE组0.62±0.0540.55±0.0630.96±0.134MD+FLX组---F22.0067.310.793P<0.01<0.010.470
注:Nor:正常组;MD+SE:单眼剥夺+标准环境组;MD+EE:单眼剥夺+丰富环境组;MD+FLX:单眼剥夺+氟西汀组。
3讨论
人类和哺乳动物出生以后,视觉系统能够根据周围视觉环境的刺激调整和改变视皮层神经元的结构和突触间联系,称为视皮层的可塑性,发生这一改变的时期称为视觉发育的关键期[9]。随着年龄的增长,视皮层神经网络结构逐渐发育成熟,限制了神经元突触轴突及树突的生长,可塑性逐渐被抑制。临床上弱视治疗具有显著的时限性,视皮层可塑性关键期内疗效明显,超过关键期的患者采用传统的遮盖疗法效果不佳。因此如何重新激活超越关键期“被抑制”的视皮层可塑性是目前研究的热点和难点。
单眼形觉剥夺弱视模型是目前研究视皮层可塑性的经典模型[10]。本实验对出生后21d的小鼠行右侧眼睑缝合阻断该侧视觉信息输入,建立单眼剥夺弱视模型。单眼缝合2wk后,我们观察模型小鼠前爪触底反射成功率显著降低,剥夺眼F-VEP P2波的潜伏期延长、波幅下降,证实单眼剥夺弱视小鼠模型建立成功。
丰富环境是研究感觉经验对大脑和行为影响的一个广泛应用的模型,它被定义为“复杂的无生命物与社会刺激的复合体”[11]。丰富环境不仅提供了多感官刺激和运动的机会,而且赋予了相互间社会性情感体验的可能。近年来,丰富环境逐渐被广泛应用于中枢神经系统以及视皮层可塑性机制的研究中[12]。将正常新生小鼠暴露于丰富环境中让其生长,出生后25d视敏度较标准环境中生长的小鼠增加18%,其视敏度基本接近出生后28d的水平,说明丰富环境显著影响着视觉系统的发育,可加速小鼠视功能的成熟[13-14]。我们前期研究证实,丰富环境可通过上调成年单眼剥夺弱视小鼠视皮层中MAP2的表达,调控突触相关蛋白PSD-95及SYP重塑视皮层可塑性,从而促进弱视模型小鼠视觉功能的恢复。本实验以氟西汀干预组作为阳性对照,进一步探讨丰富环境重新激活成年视皮层可塑性的分子机制。结果显示,在单眼剥夺弱视小鼠模型建立成功以后,将其饲养于丰富环境中,4wk后应用前爪触地反射实验观察各组小鼠的主观视敏度,显示丰富环境饲养组模型小鼠前爪触地成功率明显高于标准环境饲养组,与正常小鼠及氟西汀干预的弱视模型小鼠比较无明显差异,提示丰富环境明显改善弱视模型小鼠的主观视敏度。我们同时使用F-VEP检测各组小鼠的客观视功能,与标准环境饲养比较,丰富环境中饲养的弱视模型小鼠剥夺眼F-VEP的P2波潜伏期明显缩短,波幅升高,小鼠客观视功能恢复并接近氟西汀治疗组。近来的多项研究结果证实,氟西汀对包括海马[15]、躯体感觉皮层椎体神经元[16]、视皮层[17-18]在内的成年皮层神经元可塑性具有显著的再激活作用,从而为成年弱视治疗提供新的靶点,因此在我们的研究中将氟西汀干预组作为阳性对照。以上实验结果均提示丰富环境可以重新激活成年弱视小鼠的功能可塑性,显著改善视觉功能,其机制可能是通过重塑视皮层神经元突触结构实现的。
以往研究证实,丰富环境可引起正常成年或衰老动物中枢神经系统结构可塑性的变化,包括皮层重量和厚度、神经细胞数量、树突分支及密度、突触数量及突触接触面积等的变化[19-20]。我们的研究显示,与标准环境相比较,丰富环境饲养条件下的成年弱视模型小鼠,剥夺眼对侧视皮层突触间隙缩小、突触活性区长度增加、突触后致密物厚度增加;突触超微结构参数与正常小鼠及氟西汀干预的弱视模型小鼠比较无明显差异,提示丰富环境可重新激活成年弱视小鼠的结构可塑性,改变突触结构,促进视皮层视觉电冲动的传导。突触是神经元间信息传递的结构基础,丰富环境干预以后,视皮层神经元突触结构发生适应性变化,突触间隙缩小,加快神经递质到达突触后膜的速度,神经递质失活的可能性降低,增强神经元与效应细胞之间的信息沟通,加强突触传递效能。突触界面活性区长度在一定程度上反映神经元功能活动状态,活性区长度的增加使突触前后膜接触面增加,减少递质向周围间隙扩散,有利于递质与受体更有效结合。PSD是突触后膜上的致密物质,主要含有微管蛋白、肌动蛋白、神经丝蛋白及各种酶,丰富环境饲养后的弱视小鼠视皮层神经元突触后致密物厚度显著增加能反映出突触后膜上受体与离子通道的变化,从而在功能上增强突触的传递效率,改善小鼠视觉功能。
胰岛素样生长因子-1(IGF-1)是胰岛素样生长因子家族中的一员,是由70个氨基酸组成的单链碱性多肽,主要由肝脏合成及分泌,具有广泛的生物学效应。IGF-1的生物学活性受IGF-1受体(IGF-1R)和胰岛素样生长因子结合蛋白(IGFBP)的调节。血浆中75%的IGF-1都和IGFBP结合形成无活性的复合物,构成IGF-1的储备库。组织中的IGFBP通过阻止IGF-1与其受体结合,抑制IGF-1发挥生物学作用。此外,IGF-1还可穿过血-脑屏障,与广泛分布于脑组织中的IGFBP5结合形成无活性的复合物,游离的IGF-1则分布于脑组织中与IGF-1R结合而发挥作用[21]。经典的理论认为,IGF-1与哺乳动物中枢神经系统的发生密切相关,包括调控神经细胞增殖及发生,神经元存活、分化,突触发生,髓鞘形成等[22]。近年来研究报道,IGF-1不仅能对神经细胞起到保护作用[23],而且可介导并调控海马以及视皮层可塑性[24-25],参与学习、记忆及弱视的发病机制。本实验结果证实,IGF-1、IGF-1R及IGFBP5在正常小鼠视皮层组织中均有表达,单眼剥夺后剥夺眼对侧视皮层中IGF-1及IGF-1R表达明显下调,IGFBP5表达无明显变化。丰富环境干预后较标准环境饲养小鼠视皮层中IGF-1,IGF-1R表达明显上调,但并不影响IGFBP5的表达。以上结果均提示丰富环境可能通过直接上调IGF-1及受体IGF-1R表达,介导对成年弱视小鼠视皮层可塑性进行调控,重新激活“被抑制”的视皮层神经环路,改变突触结构,增强突触传递效能,在一定程度上改善弱视小鼠的视觉功能。我们推测IGF-1调控视皮层可塑性机制包括以下几种:(1) IGF-1通过调控葡萄糖代谢及体内血糖水平,调控视皮层组织、细胞及突触对外界感觉刺激的反应;(2) IGF-1作为视皮层中突触及神经细胞活动的重要调质,发挥神经营养因子的作用调控视皮层可塑性;(3) IGF-1通过影响PI3K的表达,调控神经细胞传导及突触蛋白表达,重新激活视皮层可塑性。因此,在未来的研究中,我们将对以上可能机制进行深入探究,力求寻找能适合临床大龄及成年弱视患者治疗的有效性、无创性新方法。
