不同部位皮下注射硼替佐米联合治疗方案在初治不适合移植的多发性骨髓瘤患者中的安全性分析探究
2020-02-07梁燕辉沈孝春
梁燕辉 沈孝春
1.广东省江门市中心医院血液内科,广东江门 529200;2.广东省江门市中心医院风湿免疫与介入科,广东江门 529200
多发性骨髓瘤(multiple myeloma,MM)是一种克隆性浆细胞异常增殖的恶性疾病,异常浆细胞及其产物可致骨痛及骨折、贫血、肾功能损害、高钙血症、易罹患感染等一系列靶器官功能障碍和临床表现[1]。MM 占恶性肿瘤的1%,发病率高居淋巴造血系统发病率第二位,欧美洲MM 发病率为4 ~6/10 万, 发病率呈逐年上升趋势[2],我国目前尚缺乏确切的流行病学数据,有学者推测我国MM发病率为1.0 ~2.5/10 万,但随着我国迈入老龄化时代,MM 发病率有增高趋势且呈年轻化态势[3]。MM 是一种无法治愈的疾病,加之患者年龄较大、易产生耐药性且复发率较高,故大多MM 患者以延长生存期、改善生存质量为治疗目的。既往对于MM多以长春新碱、地塞米松、阿霉素等化疗方案为主,但有效率仅10%左右,中位生存期仅24 个月[4]。近年来,随着硼替佐米、来那度胺、沙利度胺等新药被批准应用后MM 患者总有效率和无进展生存期得到了极大程度的提高[5-6]。对于初治MM 患者应考虑是否适合自体造血干细胞移植(ASCT)选择治疗方案,硼替佐米是一种可逆的蛋白酶体抑制剂,可通过不同通路发挥抗肿瘤作用,对于年龄>65 岁或其他并发症等不适合行ASCT 治疗者一线方案以硼替佐米为主的联合用药,但在临床应用中皮下注射硼替佐米的有效性和安全性尚未达成共识,故本研究前瞻性选取初诊不适合移植的MM 患者接受皮下注射硼替佐米联合治疗方案的有效性,且进一步比较不同皮下注射部位是否能进一步提高治疗安全性,旨在为皮下注射硼替佐米联合不同周期剂量的一线治疗方案在初诊不适合移植的MM 患者中的有效性和安全性提供实践依据。现报道如下。
1 资料与方法
1.1 一般资料
本研究经我院医学伦理委员会审核批准,前瞻性选取初诊不适合移植治疗的MM 患者,纳入标准:(1)均符合国际骨髓瘤工作组(IMWG)多发性骨髓瘤的诊断标准(2014 年更新版)[7],初次诊断为MM;(2)经至少2 名专科医生同时确定为不适合移植治疗;(3)年龄>18 岁;(4)根据《赫尔辛基宣言》(2013 年版Fortaleza),均在知情下自愿签署知情同意书等相关协议。排除标准:(1)使用硼替佐米以外其他新药治疗者;(2)已接受1 剂或多剂静脉注射硼替佐米治疗或者经静脉注射改为皮下注射硼替佐米治疗者;(3)不适合移植者,包括对本研究药物过敏者;或者伴其他恶性肿瘤、脑梗死、脑出血等严重疾病者;伴精神神经系统疾病(癫痫、痴呆、严重抑郁、躁狂、阿尔茨海默病等),不能配合治疗者;(4)依从性不佳,临床资料不全者;(5)拒绝接受本研究治疗方案者或同意本研究治疗方案但拒绝参与本研究者。最终纳入2019 年5 月~2020 年3 月间60 例患者,采用随机数字表法将其分为两组,每组各30 例,两组患者在性别、年龄、分型、RISS 分期[8]等一般资料比较,差异无统计学意义(P >0.05),具有可比性,见表1。
1.2 治疗方法
两组患者均接受改良PAD 方案[硼替佐米(意大利BSP Pharmaceuticals SRL,J20171067)+阿霉素(海正辉瑞制药有限公司,H33021980)+地塞米松(天津天药药业股份有限公司,H20033553)]治疗,第1、4、8、11 天硼替佐米1.3mg/(m·d)皮下注射,第1 天阿霉素40mg/(m·d)静脉滴注;第1 ~2、4 ~5、8 ~9、11 ~12 天 地 塞 米 松10mg 静 脉 注射,2 次/d,每28 天为1 个疗程,共进行3 个疗程化疗。对照组患者按临床护理操作规程,在双侧大腿外侧交替注射硼替佐米,观察组在3 个疗程中依次进行8 个部位交替循环的硼替佐米皮下注射。两组患者注射硼替佐米均由经统一培训合格的至少有3 年及以上血液科工作经验的执业护士负责,注射器统一使用洪达公司生产的1mL 注射器(针头长1.8cm)。观察组部位选择依次按照左上腹、左下腹、左大腿外侧近端、左大腿外侧远端、右大腿外侧远端、右大腿外侧近端、右下腹、右上腹顺序交替进行皮下注射,腹部注射部位以脐为中心,左上、左下、右上、右下10cm 范围(脐周1cm 除外),大腿注射部位选取大腿外侧近远端皮下组织丰厚位置,2 次注射点间距2cm 以上,避开皮肤破损、瘢痕以及色素沉着部位。对照组在左右大腿外侧近端皮质丰富处交替注射,注射方法同观察组。在注射过程中首先要将注射器针头用生理盐水排气,保持注射器垂直向下角度抽取适量空气约0.1mL,保证空气始终位于注射器活塞顶端。对于体型消瘦者用手指捏起皮肤后保持45°进针,体型正常和肥胖者可直接垂直进针。下腹注射采用Z 型进针方法,下肢注射时保持45°进针。
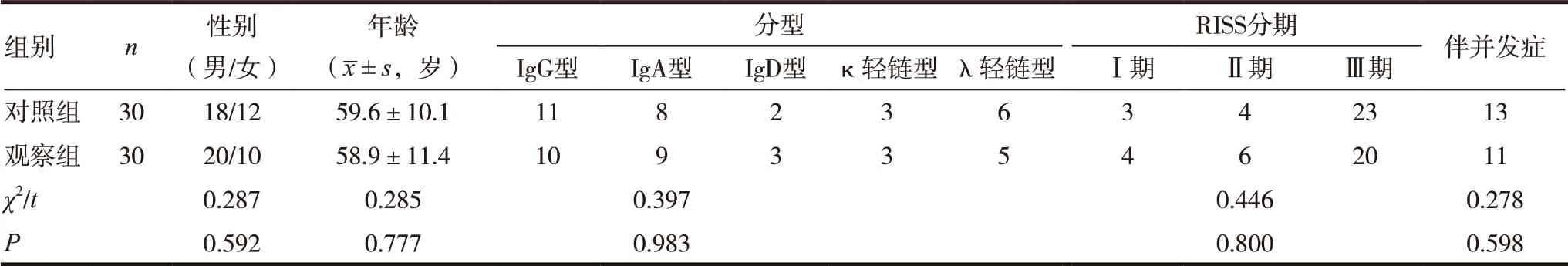
表1 两组患者一般临床资料比较
1.3 观察指标及评估方法
(1)观察两组患者皮下注射硼替佐米后30min疼痛程度,采用视觉模拟评分法(VAS)评估,0 分为无痛、1 ~3 分为轻度疼痛、4 ~6 分为中度疼痛、7 ~9 分为重度疼痛、10 分为剧烈疼痛,得分越高则提示疼痛程度越强。
(2)参照中国多发性骨髓瘤诊治指南(2017 年修订)[9]将疗效分为严格意义的完全缓解(sCR)、完全缓解(CR)、非常好的部分缓解(VGPR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD),总有效率(ORR)=(sCR+CR+VGPR)例数/总例数×100.00%。参照WHO 抗癌药物不良反应分度标准评估不良反应,不良反应按美国国家癌症研究所不良事件常用术语研究标准(National Cancer Institute Common Terminology Criteria for Adverse Events,CTVAE version3.0)判断[10],每天详细观察并记录患者发生相关药物毒副反应等,同时比较两组患者注射后局部不良反应情况。
1.4 统计学处理
应用SPSS18.0 统计学软件进行数据分析,计量资料以()表示,若数据符合正态分布则采用t检验(组内比较行配对t 检验,组间比较行成组t 检验),若数据不符合正态分布则行秩和检验,计数资料和等级资料均采用[n(%)]表示,计数资料采用χ2检验,等级资料采用秩和检验,P <0.05 为差异有统计学意义。
2 结果
2.1 两组患者皮下注射硼替佐米30min VAS评分比较
观察组患者皮下注射硼替佐米30min 后平均VAS 评分为(2.89±0.38)分,明显低于对照组患者评分(4.86±0.35)分(t=20.886,P=0.000)。
2.2 两组临床疗效及药物毒副反应比较
观察组和对照组ORR 分别为90.00%和83.33%,但差异无统计学意义(P >0.05),见表2。观察组药物毒副反应[腹部不适、周围神经病变、贫血、肝功能异常、白细胞(WBC)减少、血小板(PLT)减少]发生率均略低于对照组(P >0.05),见表3。
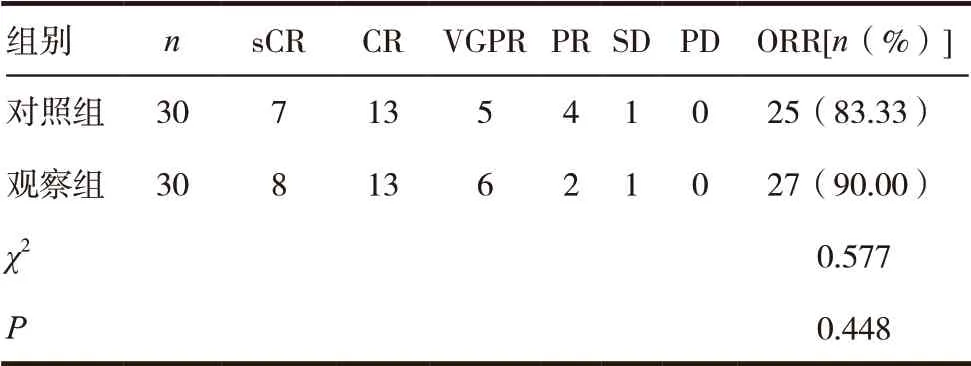
表2 两组患者临床疗效比较
2.3 两组患者注射局部不良反应发生情况比较
两组患者注射硼替佐米后均出现肿胀、外渗、硬结、红斑等不良反应,且观察组发生率(16.94%)明显低于对照组(23.33%)(P <0.05)。见表4。
3 讨论
MM 是恶性浆细胞单克隆增值性血液系统疾病,主要为M 蛋白的出现和溶骨性病变,导致患者出现高钙血症、肾功能损害、贫血、骨破坏等临床表现,但目前病因和病机尚未完全明确。流行病学研究发现MM 多发于中老年人,发病年龄多为50 ~ 60 岁,男性多于女性,近年来发病呈年轻化趋势[11],故本研究中病例选择中以年龄>18岁为标准,同时发现两组平均年龄超过50 岁,和流行病学数据吻合。目前,MM 仍是不可治愈的血液系统疾病,随着对其病因、病机深入研究及靶向治疗药物(蛋白酶体抑制剂、免疫调节药物、组蛋白去乙酰化酶抑制剂等)和自体造血干细胞移植、异体造血干细胞移植等治疗技术的应用,MM 治疗取得了重大突破,明显提高了治疗总有效率,延长了无进展生存和总生存时间[12]。
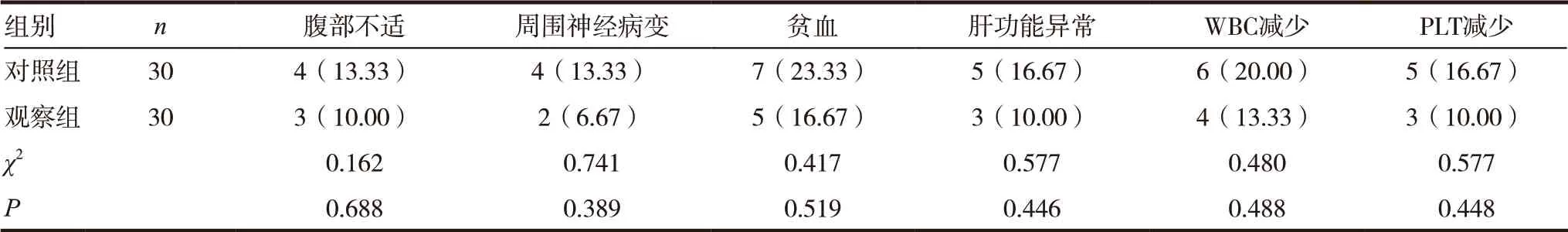
表3 两组患者药物毒副反应比较[n(%)]

表4 两组患者注射局部不良反应发生情况比较
ASCT 仍是适合移植MM 患者一线治疗方案,可有效改善MM 患者预后,目前仍将65 岁或以下作为是否适合移植的年龄界限。近年来,越来越多研究证实诱导治疗后MM 患者缓解程度与移植后无进展生存和总体生存相关[13],建议在移植前诱导治疗延长至4 ~ 6 个疗程。不适合ASCT 患者诱导治疗总疗程不应少于6 个疗程,且在诱导治疗后需进行维持治疗,MM 患者不管是否适合ASCT 治疗均会先进行诱导治疗[14],故本研究为了避免因治疗方案不同对结果产生偏移选择不适合行ASCT 治疗的MM 患者为研究对象。
硼替佐米是一种可逆性的蛋白酶体抑制剂(第一代),选择性地结合蛋白酶体活性位点,阻断蛋白酶对目标蛋白的降解。其可通过多种通路发挥抗肿瘤作用,其中NF-κB 通路在肿瘤细胞凋亡、代谢、增殖、侵袭等方面发挥关键作用,在MM 患者细胞系中可发现NF-κB 持续活化,而硼替佐米通过组织IkB 降解而让NF-κB 不能发挥作用,从而抑制细胞增殖相关基因的表达,诱导肿瘤细胞凋亡[15];可抑制MM 患者骨髓内皮细胞的生长及新生血管的形成,促进MM 细胞凋亡;通过半胱天冬酶-8 依赖性Sp1 蛋白质下调组蛋白去乙酰化酶基因家族I 表达,并诱导组蛋白高度乙酰化,诱导MM 细胞凋亡;在MM 细胞内上调促凋亡蛋白NOXA 表达,让NOXA 与抗凋亡蛋白Bcl-2 相互作用而致MM细胞凋亡[16];此外其还能影响骨髓微环境,发挥抗肿瘤作用,已经成为MM 治疗的一线用药,含硼替佐米方案成为首选,NCCN 和而欧洲肿瘤内科学会(ESMO)均推荐PAD 方案,且众多研究均证实其用于初治、难治性/复发性、维持治疗、ASCT 前预处理治疗取得了显著的效果,较传统药物在有效率、缓解程度及PFS、OS 方面均具有明显优越性[17],故本研究两组患者均选择改良PAD 方案(硼替佐米+阿霉素+地塞米松)治疗3 个疗程。此外,宋岭等[18]比较分析PAD 化疗方案中硼替佐米剂量1.0~1.3mg/m2、1.6mg/m2对多发性骨髓瘤患者疗效发现1.0~1.3mg/m2剂量硼替佐米治疗MM 疗效优于1.6mg/m2剂量治疗效果,安全性更好,故本研究VAD 化疗方案种硼替佐米剂量选择1.3mg/m2。结果显示,观察组和对照组ORR分别为90.00% 和83.33%,药物毒副反应(血小板减少、白细胞减少、腹部不适、周围神经病变、贫血、肝功能异常)发生率方面比较,差异无统计学意义(P >0.05),和孙慧敏[19]研究报道基本一致,ORR 和毒副反应发生率的差异可能是受年龄、临床分型、R-ISS 分期及对药物敏感性等因素的影响。
近年来研究发现,硼替佐米皮下注射和传统静脉给药在疗效、安全性、耐受性比较两种给药方式在药动力学、药效学一致[20],临床疗效相当,皮下注射安全性较静脉给药有所改善,患者局部耐受性更好,且给药更为方便,缩短了注射时间,已经成为患者首选的方式。曹红花等[21-22]比较分析皮下注射和静脉给药注射硼替佐米为主化疗方案治疗MM 发现,皮下注射硼替佐米为主治疗MM 是一种安全、可靠、有效且耐受性好的方式。皮下注射时药物剂量极少,常规注射因注射器存在无效腔,注射后可见针头有残留药液,长期用药可导致药物剂量与应有剂量存在较大差异,进而影响临床疗效[23]。本研究通过留置气泡方式可有效规避因注射器无效腔导致的药液残留,确保了总剂量的准确性,同时为了避免因注射器因素对结果的影响,统一使用洪达公司生产的1mL 注射器,可有效避免偏移。结果显示,观察组注射局部不良反应发生率(16.94%)明显低于对照组(23.33%)(P <0.05),同时还发现观察组患者皮下注射硼替佐米30min 后平均VAS评分为(2.89±0.38)分,明显低于对照组患者评分(4.86±0.35)分,提示通过8 个部位交替进行皮下注射能有效减轻患者注射的疼痛感,还能有效降低因注射所致的局部不良反应,此结果和张黎琴等[24]报道结论基本一致,但因两项研究中皮下注射部位选择存在一定差异,尚需后期大样本试验验证。但本研究尚未完成随访,尚缺乏皮下注射硼替佐米联合治疗方案对不适合移植治疗MM 患者PFS、OS 的影响,待完成随访后补充。
综上所述,皮下注射硼替佐米联合治疗方案对初诊不适用移植的多发性骨髓瘤患者疗效确切,采用8 个部位交替进行皮下注射,可有效降低不良反应,缓解注射后疼痛和局部注射反应,具有较好的推广和应用价值。
