氧掺杂对VN-g-C3N4催化剂光催化固氮性能的影响
2020-01-15赵艳锋孙效龙胡绍争
赵艳锋, 孙效龙, 胡绍争, 王 辉, 王 菲, 李 萍
(辽宁石油化工大学化学化工与环境学部, 抚顺 113001)
氮气是空气的主要组分, 因其化学和生物惰性较强, 导致绝大多数生命体都不能直接吸收利用氮气. 人工固氮产铵技术对现代工业和农业都有着非常重要的影响. 目前, 世界上绝大多数的固氮过程是采用高能耗的Haber-Bosch法, 但该方法已经不能符合现代化工业节能、 绿色、 环保的新要求. 因此, 寻找新的人工固氮技术已经迫在眉睫. 光催化氧化还原技术因具有条件温和、 节能环保等优点而受到越来越多的关注[1~9]. 目前, 该技术在降解有机物、 光解水制氢、 有害气体还原、 有机合成、 制取双氧水等领域的应用研究已有大量报道, 并取得了一系列研究成果[10~14]. 1977年, Schrauzer等[15]发现在Fe掺杂TiO2催化剂上存在光催化固氮作用. 此后, 光催化固氮法被认为是传统的Haber-Bosch法的最佳替代法之一.
石墨相氮化碳是近年来环境和化学领域的研究热点[16], 并已成功应用于多个领域, 如储气、 燃料电池、 光催化等[17~22]. Cao等[23]制备的氨基功能化的超薄g-C3N4催化剂具有大比表面积、 强还原能力、 高电子-空穴分离效率和强固氮能力. Hu等[24]采用熔盐辅助微波法制备了花状Cu掺杂g-C3N4催化剂, 其光催化固氮能力比纯的g-C3N4催化剂提高了35倍. Li等[25]制备了KOH处理的g-C3N4催化剂, 并以CH3OH为质子源考察了催化剂的光催化固氮能力. 结果表明, K+离子的引入提高了电荷分离效率和固氮能力.
由于在光能较低的能量密度和光催化温和的反应条件下氮气分子很难被活化, 使光催化固氮性能不理想. 研究发现, 在催化剂表面引入缺陷态能有效吸附并活化反应物分子. Dong等[26]和Ma等[27]分别报道了氮空穴作为活性中心能有效活化氮气分子并促进光电子在催化剂与反应物分子间的转移, 因此提高光催化固氮能力. Hu等[28]和Li等[29]发现三元金属硫化物中的硫空穴和BiOBr中的氧空穴对光催化固氮性能也有着类似的促进作用.
在常用的金属和非金属掺杂元素中, 氧是最有效的掺杂元素之一[30,31]. 氧引入g-C3N4晶格后能调节催化剂的电子结构和能级结构, 提高光催化性能. 因此, 本文采用介质阻挡放电等离子体法合成了氧原子掺杂的具有氮空穴的g-C3N4催化剂. 与单纯具有氮空穴的g-C3N4催化剂相比, 氧原子的引入提高了氮空穴对氮气分子的活化能力, 提高了光催化固氮性能、 密度泛函理论计算结果证实了该结论.
1 实验部分
1.1 试剂与仪器
所用试剂均为分析纯, 购自天津化学试剂厂, 使用前未经提纯. 所有水溶液均用去离子水配制.
日本岛津公司XRD-7000型X射线衍射仪(CuKα1辐射源, 工作电压40 kV, 工作电流30 mA); 日本电子有限公司JSM 5600LV型扫描电子显微镜(SEM); 日本分光公司UV-550型紫外-可见光谱仪; 赛默飞世尔科技有限公司ESCALAB-250型热电X射线光电子能谱仪(XPS); 德国Elementar公司vario EL cube型元素分析仪; 美国Micromeritics公司2010型物理吸附仪; 美国Quantachrome公司 CHEMBET-3000 TPD型化学吸附分析仪; 瑞士万通公司AUTO-LAB PGSTAT30型电化学工作站.
1.2 催化剂的制备
将双氰胺研磨30 min后转入带盖的坩锅中, 于马弗炉中在Ar气氛、 520 ℃下焙烧2 h, 制备的g-C3N4催化剂命名为NCN. 采用介质阻挡等离子体放电法制备氧原子掺杂的具有氮空穴的g-C3N4: 将0.3 g NCN置于石英管中, 通入5 min Ar气将石英管中的空气排出, 然后持续通入氢气, 流速为40 mL/min. 打开等离子体发生器, 调节电压至10 kV, 放电时间为30 min, 频率10 kHz. 放电结束后, 得到的氮空穴掺杂的催化剂命名为CN(VN). 保持相同的放电条件, 用氧气替换氢气继续放电30 min, 氧气流速20 mL/min, 得到共掺杂的催化剂命名为OCN(VN). 为了对比, 将NCN直接在氧气条件下放电, 条件相同, 得到的氧掺杂催化剂命名为OCN.
1.3 模拟计算
所有密度泛函理论(DFT)计算均基于平面波方法展开, 使用剑桥连续总能量计算包(CASTEP)进行模拟. 对电子交换和相关相互作用使用广义梯度近似(GGA)中的Perdew-Wang 91函数进行计算, 并用OBS(奥尔特曼-贝希斯特-施密特)方法进行DFT色散校正(DFT-D), 考虑弱的相互作用. 所有结构使用的K点均以0.2/nm进行分隔, 截断能量设定为400 eV. g-C3N4模型在z方向上的真空层为2.0 nm, 以消除相邻周期单元之间的相互作用.
1.4 活性评价
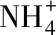
2 结果与讨论
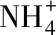
当反应体系采用N,N-二甲基甲酰胺(DMF)取代去离子水时, 没有铵离子生成; 当体系中加入AgNO3捕获光电子时, 铵离子产率显著降低[图1(B)]. 由这些结果能初步推断出光催化固氮反应机理, 即光电子为反应活性物种, 水为反应提供质子源, 反应方程如下:

(1)
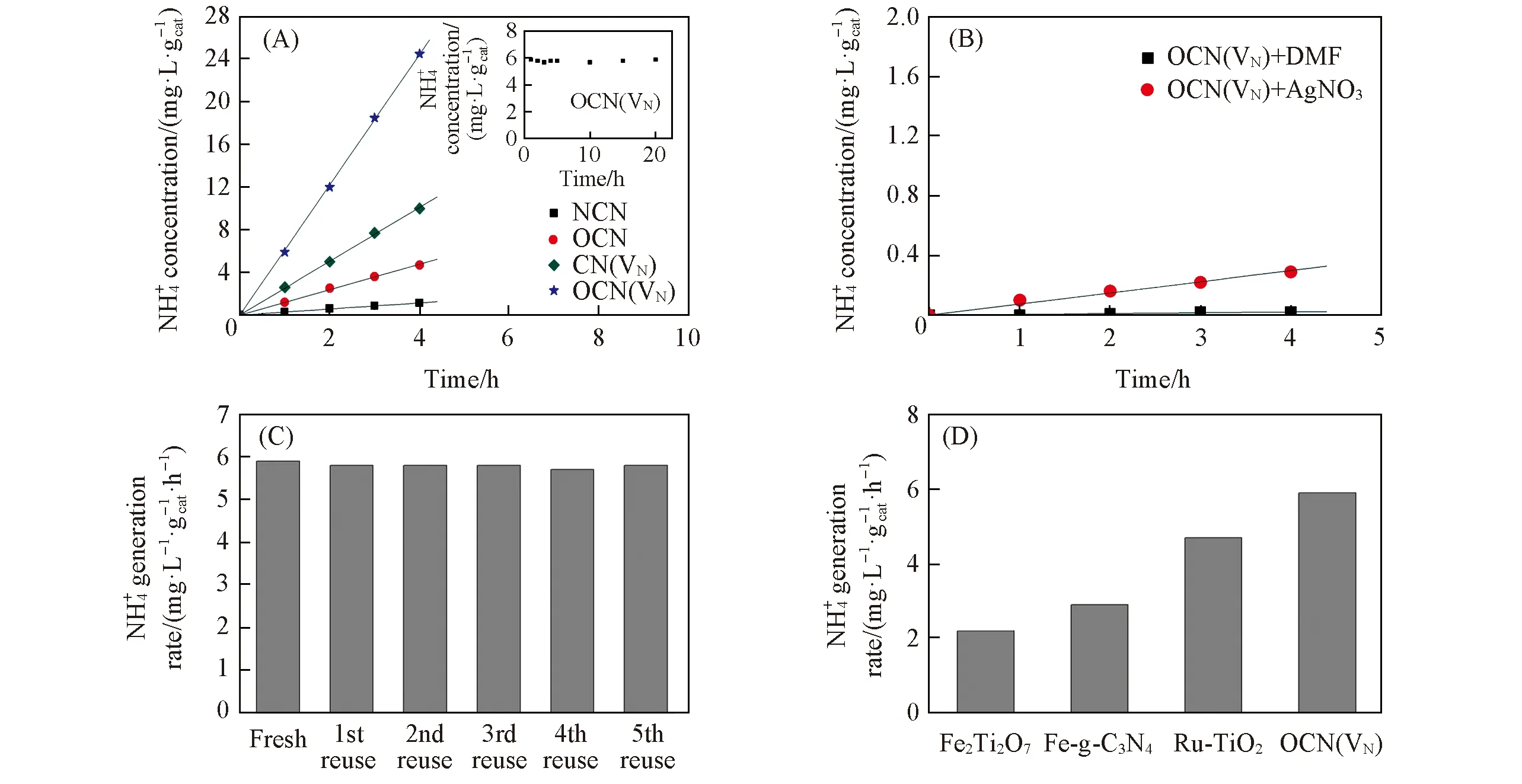
Fig.1 N2 photofixation ability over as-prepared catalysts(A), production ability of OCN(VN) in aprotic solvent DMF or using AgNO3 as the electron scavenger(B), N2 photofixation ability of reused OCN(VN)(C) and comparison of production rate over OCN(VN) and other catalysts(D)

Fig.2 Mass spectra of the indophenol prepared from different atmosphere
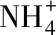
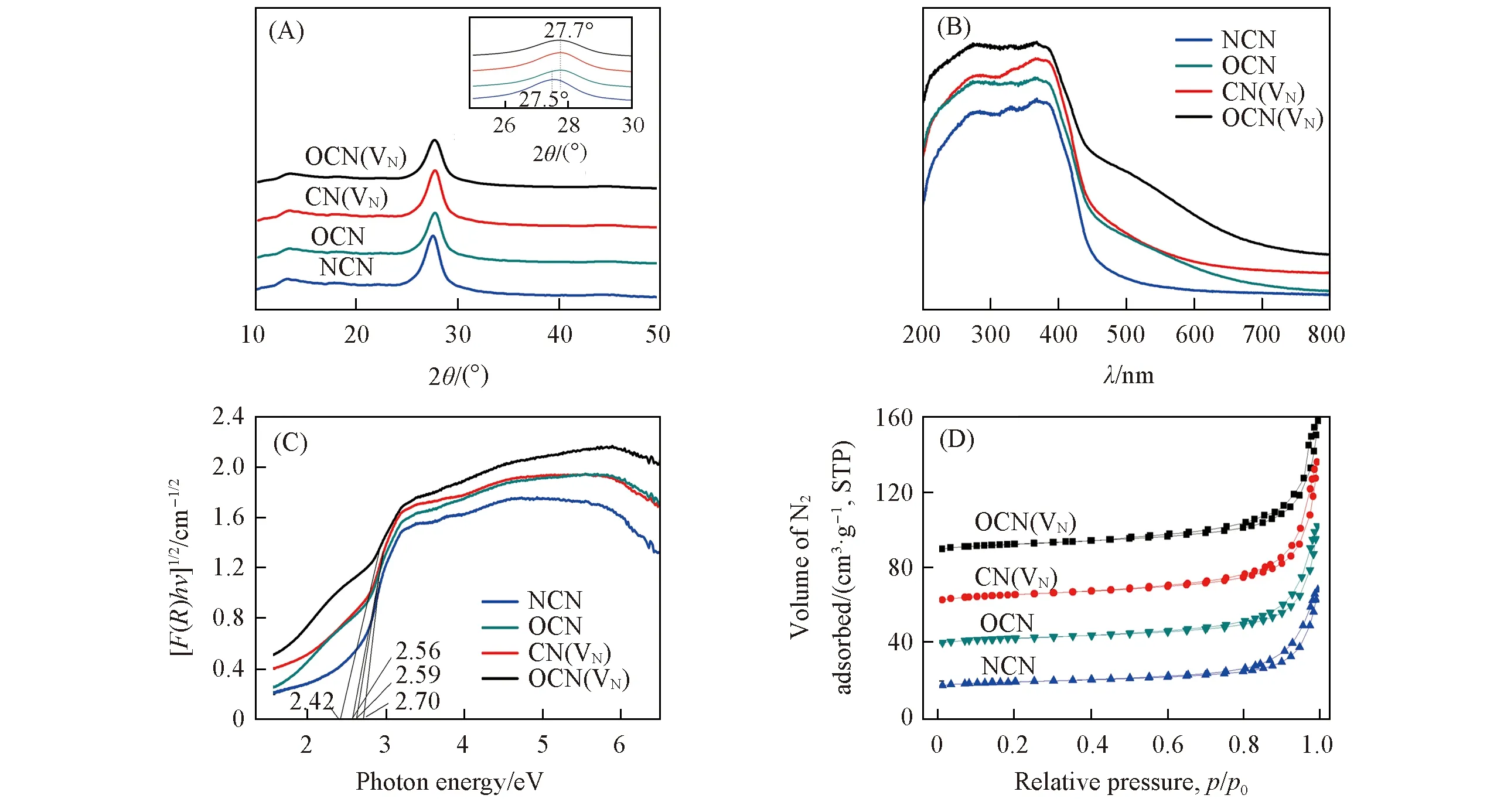
Fig.3 XRD patterns(A), UV-Vis spectra(B), plots of transformed Kubelka-Munk function vs. the energy of light(C) and N2 adsorption-desorption isotherms(D) of as-prepared catalysts
图3(A)的XRD谱图结果显示, NCN的两个特征峰分别位于2θ=13.1°和27.5°处, 分别归属于石墨相氮化碳(JCPDS No.87-1526)的(100)和(002)晶面. 等离子体处理后, 催化剂显示出了与NCN类似的晶体结构, 但衍射峰位置向高角度发生了位移. 这可能是由于氧原子和氮空穴引入了氮化碳晶格所导致的. 研究发现, 引入氮空穴能改变催化剂的晶体结构[27,35]. 而掺入的氧原子与被取代的碳原子或氮原子相比, 其更强的电负性能导致氮化碳层间更强的相互作用, 使层间距变小, 也能改变催化剂的晶体结构. UV-Vis光谱结果[图3(B)]显示, NCN的吸收边界约为460 nm. CN(VN)和OCN的吸收边界发生了明显的红移现象. 由于氧掺杂与氮空穴的共同作用, OCN(VN)的红移现象更加显著. 根据Kubelka-Munk公式[36]计算得出, NCN, CN(VN), OCN和OCN(VN)的能带宽度分别为2.70, 2.59, 2.56和2.42 eV[图3(C)]. 图3(D)所示为各催化剂的N2吸附-脱附曲线. 由图可知, 所有催化剂为Ⅳ型等温线. NCN, CN(VN), OCN和OCN(VN)的比表面积分别为8.8, 8.9, 8.6和9.1 m2/g. 可见等离子体处理对催化剂的比表面积没有显著影响. 为了确定氮空穴的存在, 采用元素分析测试了催化剂的C/N摩尔比. 结果显示, NCN的C/N比为0.74, 而CN(VN)的C/N比为0.78, 证实了氮空穴被成功引入催化剂晶格. 此外, OCN的C/N比为0.76, 也明显高于NCN的C/N比. 这可能是由于氧原子取代了氮原子掺入氮化碳晶格, 导致C/N比的增加. 而OCN(VN)的C/N比高达0.8, 可能是由于氧掺杂与氮空穴的共同作用引起的.
由图4(A)可见, NCN为无规则块状结构, 这些块状结构由许多层状结构相互堆砌而成. 在HRTEM照片中能看到催化剂晶格, 其晶格间距为0.33 nm, 与石墨相氮化碳(002)晶面间距相吻合[37]. CN(VN), OCN和OCN(VN)的形貌与NCN相比没有明显区别[图4(B)~(D)], 说明等离子体处理没有显著改变催化剂的形貌.

Fig.4 SEM and HRTEM(inset) images of NCN(A) and SEM images of CN(VN)(B), OCN(C) and OCN(VN)(D)

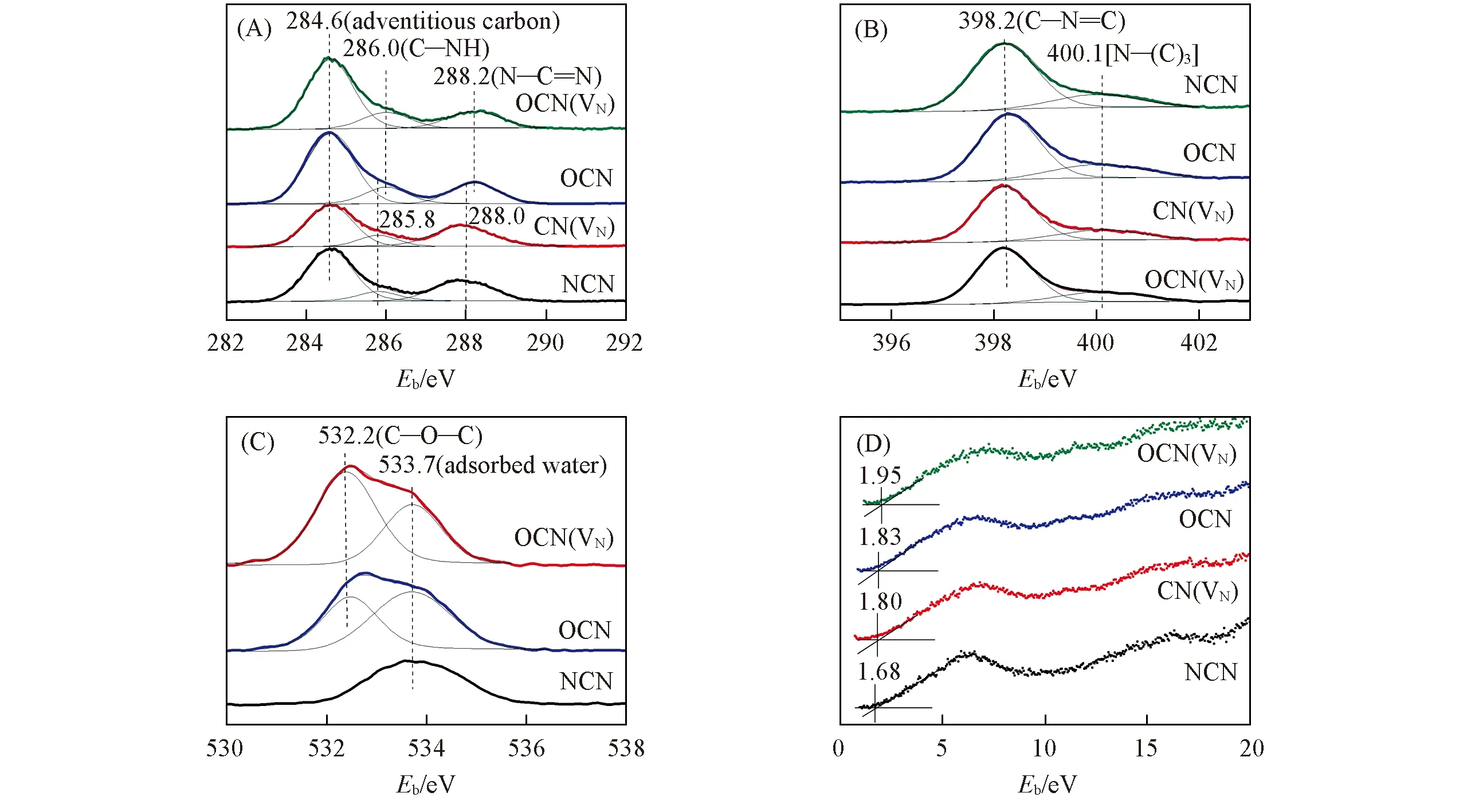
Fig.5 XPS spectra in the region of C1s(A), N1s(B), O1s(C) and VB XPS(D) of as prepared catalysts
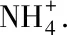
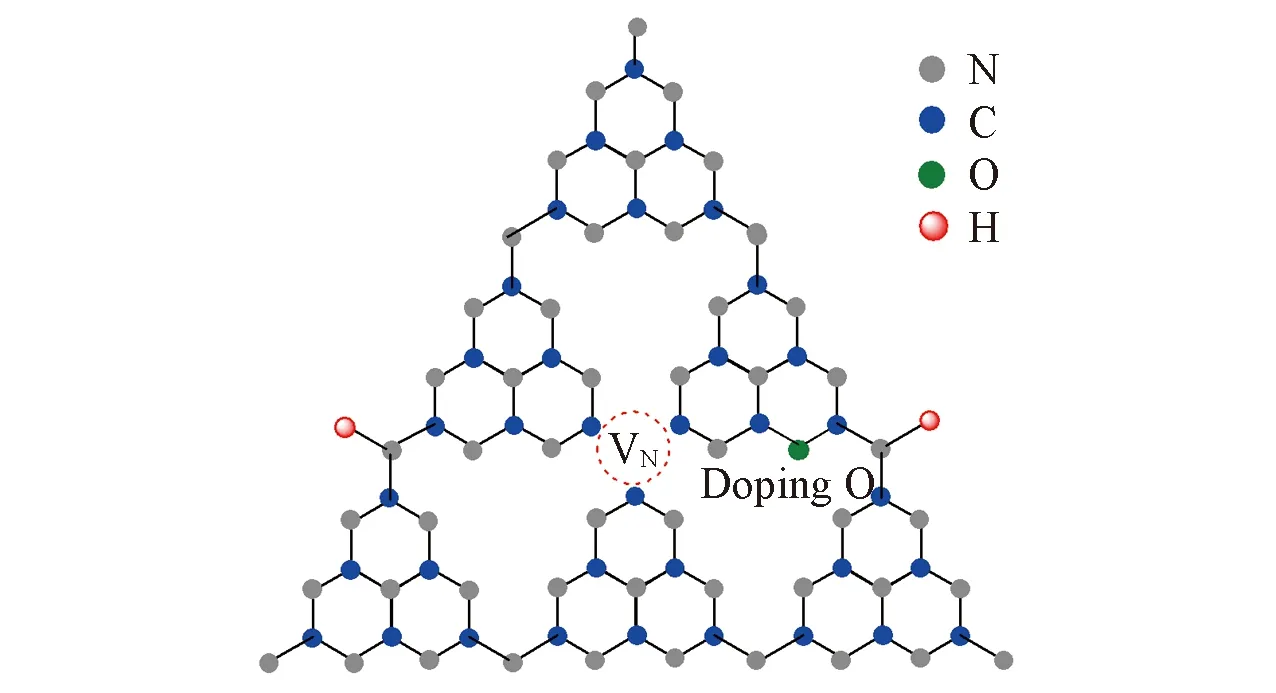
Fig.6 Diagram of possible structure of OCN(VN)
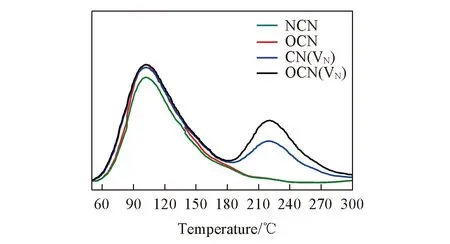
Fig.7 N2-TPD curves of as-prepared NCN, CN(VN), OCN and OCN(VN)
在多相催化反应中, 化学吸附是活化反应物分子的关键步骤. 图7为催化剂的N2-TPD表征结果. NCN在100~110 ℃的脱附峰应归属于N2在催化剂表面的物理吸附[44]. OCN的脱附曲线与NCN相似. 在CN(VN)和OCN(VN)的脱附曲线中, 除了100 ℃附近的物理脱附峰, 在220 ℃附近还出现了一个新的脱附峰, 应归属于N2在催化剂表面的化学吸附. 值得注意的是, 具有氮空穴的催化剂才发生化学吸附, 说明氮空穴是N2发生化学吸附的活性中心, 这与此前的研究结果相一致[26,27]. 此外, 图中明显看出, OCN(VN)在220 ℃的脱附峰面积比CN(VN)的脱附峰面积大得多, 说明氧原子的引入能提高催化剂中氮空穴对氮气的活化能力.
EIS结果[图8(A)]显示, NCN的圆弧半径最大, 表明其电荷转移电阻大, 不利于电荷传输. OCN和CN(VN)的阻抗弧半径与NCN相比有所减小, 说明氧掺杂和引入氮空穴都能提高催化剂的电子-空穴分离效率. OCN(VN)的阻抗弧半径最小,表明该催化剂具有最高的光生电子-空穴对分离效率. 图8(B)为各催化剂在氮气气氛下的PL光谱. NCN样品在460 nm附近有很宽的荧光发射峰, 归属于光激发而产生的带边荧光现象. CN(VN), OCN和OCN(VN)谱图的形状和NCN样品相似, 但是荧光发射峰的强度明显减弱, 这说明氧掺杂和引入氮空穴都能有效提高催化剂的电子-空穴分离效率[45,46]. 图8(C)对比了各催化剂在Ar和N2气氛下的PL光谱强度. NCN和OCN催化剂在2种气氛下的PL光谱强度基本一致; 但CN(VN)和OCN(VN)催化剂在N2气氛下的PL峰强度显著低于在Ar气氛下的峰强度, 说明气氛对具有氮空穴的催化剂的电荷分离效率有显著影响. 这可能是由于氮空穴能捕获光电子, 并将光电子转移至吸附的氮气分子表面. 由于氮气分子的2个成键轨道已被占满, 转移的光电子只能占据高能的反键轨道, 导致氮气分子的活化, 如图8(C)的插图所示. 然而在Ar气氛下不能发生这种电子转移现象, 因此导致了不同的电荷分离效率.
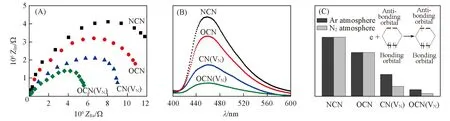
Fig.8 EIS(A) and PL(B) spectra of NCN, CN(VN), OCN and OCN(VN) and comparison of their PL intensity under Ar and N2 atmospheres(C) and the possible electrons transfer route(inset)(C)
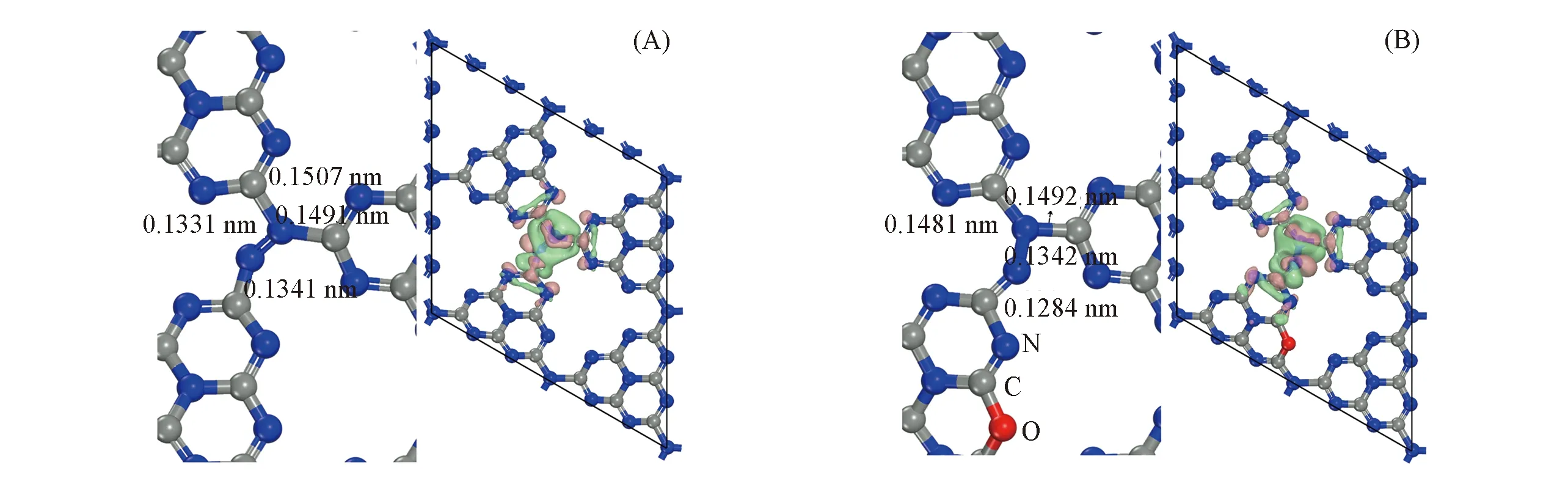
Fig.9 Optimal N2 adsorption model and the charge density difference of the N2 molecule adsorbed on CN(VN)(A) and OCN(VN)(B)
采用DFT计算确认了氧掺杂对氮气分子活化的促进作用. 图9所示为N2在CN(VN)和OCN(VN)表面的最佳吸附模式和电荷差分密度图. 可以看出, 在2个催化剂上, 氮气分子均吸附在氮空穴上并与相邻的3个碳原子成键. 根据文献[24,34]报道, 氮气分子的N≡≡N键的键长为0.1157 nm. 如图9所示, 当氮气分子吸附在CN(VN)上时, 其N≡≡N键的键长增大到0.1331 nm. 而氮气分子吸附在OCN(VN)上时, 其N≡≡N键的键长进一步增大到0.1342 nm. 此外, 氮气分子在CN(VN)和OCN(VN)上的吸附能(Eab)分别为-3.52 eV和-4.59 eV. OCN(VN)的吸附能更低, 说明其吸附能力更强. 由此得知, 氧原子的引入能提高氮空穴对反应物氮气分子的活化能力.
此外, 图9还比较了CN(VN)和OCN(VN)催化剂的电荷差分密度. 图中粉色和绿色部分分别表示发生了电子积累和电子消耗. 如图所示, 在2个催化剂上, 电子均在N≡≡N键上发生积累, 而在邻近的碳原子上发生消耗. 此结果确认了电子从氮空穴转移至吸附的氮气分子表面. 此外, 氮气分子吸附在OCN(VN)上的电子密度为-0.09 e, 高于吸附在CN(VN)上的电子密度(-0.05 e). 此结果证实了氧的引入赋予了氮空穴更强的电子供给能力, 使氮气分子更容易被活化, 因此导致了更高的光催化固氮能力.
综上所述, 推断CN(VN)的光催化固氮反应机理如下: 光照催化剂产生电子-空穴对后, 光电子被氮空穴捕获. 由于氮空穴上还同时吸附着反应物氮气分子, 光电子通过氮空穴转移至氮气分子表面. 由于氮气分子的两个成键轨道已被占满, 转移的光电子只能占据高能的反键轨道, 导致氮气分子活化, 进而与水中氢离子作用生成产物氨气分子. 氧原子的引入赋予了氮空穴更强的电子供给能力, 使氮气分子更容易被活化, 因此OCN(VN)催化剂表现出更高的光催化固氮能力.
3 结 论
感谢大连理工大学超级计算中心提供密度泛函理论计算.
