金纳米粒子荧光增强法测定食用油中PG的研究
2020-01-14李满秀任光明王苗苗
李满秀,任光明,王苗苗,孙 越,贾 佳
(忻州师范学院 化学系,山西 忻州 034000)
没食子酸丙酯(PG)亦称棓酸丙酯,是食品工业中常用的抗氧化剂,我国GB 2760—2014《食品安全国家标准 食品添加剂使用标准》规定:PG用于含油脂食品中最大使用量为0.1 g/kg(以油脂中的含量计)。研究表明,过量使用PG会对人体健康造成危害[1],如导致肾脏受损或引起接触性皮炎等。因此,对PG的定量检测非常必要。目前,测定PG的方法主要有高效液相色谱法[2-4]、液质联用法[5-6]、化学发光法[7]和分光光度法[8-10]等,使用金纳米荧光法测定PG的应用未见报道。
金纳米粒子(AuNPs)是近年来推出的新型纳米材料,因其制备方法简单及独特的光学性质受到普遍关注[11-12],在化学及生物医学等领域应用广泛[13-15]。本实验采用聚乙烯亚胺作保护剂,利用THPC还原氯金酸制备了一种稳定性好,发光强度高的金纳米溶液。根据PG增强金纳米溶液的荧光强度,建立了快速测定痕量PG的新方法,并成功用于食用油中PG的测定,可为食用油中PG的测定提供参考。
1 材料与方法
1.1 实验材料
氯金酸、PG,国药集团化学试剂有限公司;THPC((CH2OH)4PCl),梯希爱(上海)化成工业发展有限公司;聚乙烯亚胺,阿拉丁试剂(上海)有限公司;磷酸二氢钠、磷酸氢二钠、氢氧化钠、乙酸铵,天津市福晨化学试剂厂;福临门花生油、神池胡麻油,本地超市购买。所用试剂均为分析纯,实验用水为超纯水。
F-4600型荧光分光光度计,日本日立公司;UV-2550型紫外可见分光光度计,日本岛津公司;pHS-3B型酸度计,上海精密科学仪器有限公司;85-2型恒温磁力搅拌器,上海司乐仪器厂;AL-204电子天平,梅特勒-托利多仪器有限公司。
1.2 实验方法
1.2.1 AuNPs的制备[16]
在100 mL小烧杯中依次加入45 mL水、0.5 mL 1 mol/L NaOH溶液、1 mL THPC搅拌5 min,再加入1.5 mL 1 mmol/L的氯金酸搅拌15 min,然后滴加25滴聚乙烯亚胺,搅拌30 min,溶液呈金黄色,室温避光放置片刻,将AuNPs溶液转移到容量瓶中,于4℃避光保存。
1.2.2 AuNPs溶液紫外和荧光光谱测定
取1 mL稀释10倍的AuNPs原液于10 mL比色管,再取1 mL稀释10倍的AuNPs原液和1 mL 0.21 μg/mL PG于另一10 mL比色管,均加入2 mL pH 7.8的磷酸盐缓冲液后用超纯水定容,分别测定其紫外和荧光光谱。
1.2.3 PG含量的测定
取10 mL比色管,依次加入1 mL稀释10倍的AuNPs原液、1 mL 0.21 μg/mL PG溶液、2 mL pH 7.8的磷酸盐缓冲液,用超纯水定容。25℃反应20 min后,在激发波长333 nm下,测定380 nm处的荧光强度(激发和发射狭缝宽度均为10 nm)。
1.2.4 样品处理
称取10 g食用油样品,用100 mL石油醚溶解,移入分液漏斗中,加20 mL乙酸铵溶液(16.7 g/L)振摇2 min,静置分层,将水层放另一分液漏斗中,石油醚层再用20 mL乙酸铵溶液(16.7 g/L)重复提取两次,合并水层。石油醚层用水振摇洗涤两次,每次15 mL,水洗涤液并入同一分液漏斗中,振摇静置。将水层通过干燥滤纸滤入100 mL容量瓶中,用少量水洗涤滤纸,加2.5 mL乙酸铵溶液,加水至刻度,摇匀。将此溶液用滤纸过滤,弃去初滤液的20 mL,收集滤液供测定用。
2 结果与讨论
2.1 AuNPs的光谱表征
AuNPs及AuNPs与PG作用的荧光光谱如图1所示。
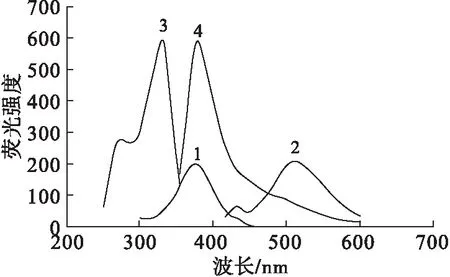
注:1、2分别表示AuNPs的荧光激发、发射光谱;3、4分别表示AuNPs+PG的荧光激发、发射光谱。
图1 AuNPs及AuNPs与PG作用的荧光光谱
由图1可知,AuNPs的荧光激发波长在375 nm,发射波长在513 nm。于pH 7.8的磷酸盐缓冲液,加入PG后,荧光发生明显蓝移且强度显著增强,其激发波长变为333 nm,发射波长变为380 nm。
AuNPs的紫外吸收光谱见图2。

图2 AuNPs的紫外吸收光谱
由图2可知,最大吸收波长为373 nm,证明制备的产物为AuNPs。
2.2 PG测定条件的优化
2.2.1 缓冲体系pH的影响
在缓冲体系pH分别为5.8、6.2、6.6、7.0、7.4、7.8、8.0的条件下测定体系的荧光强度,结果见图3。
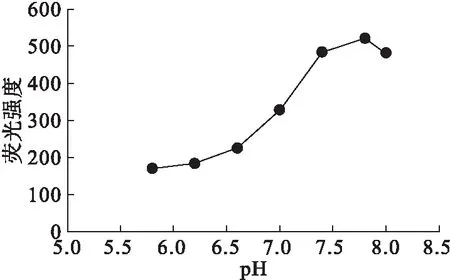
图3 pH对体系荧光强度的影响
由图3可知,加入pH 7.8的磷酸盐缓冲溶液条件下,体系最稳定,PG对AuNPs的荧光增强作用最好。实验选择pH 7.8的磷酸盐缓冲溶液为反应介质。
2.2.2 反应时间的影响
在反应时间分别为10、20、30、40、50、60 min条件下测定荧光强度,结果见图4。

图4 反应时间对体系荧光强度的影响
由图4可知,在不同反应时间,体系的荧光强度基本不变。实验选择反应时间为20 min。
2.2.3 反应温度的影响
分别将反应温度控制在15、25、35、45、55、65℃,测定荧光强度,结果见图5。
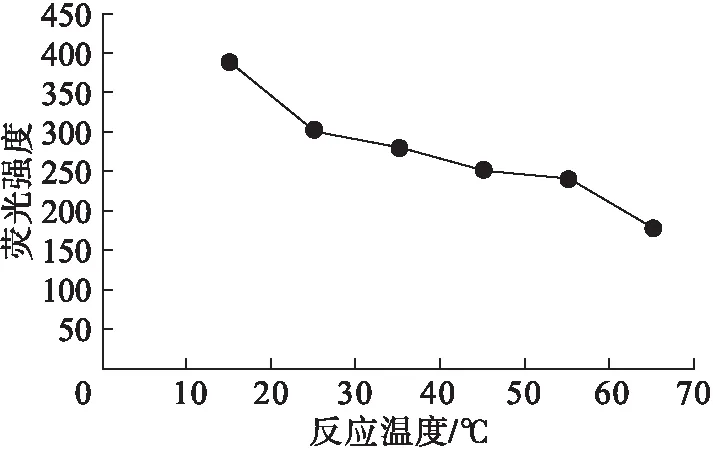
图5 反应温度对体系荧光强度的影响
由图5可知,随着反应温度的升高,体系的荧光强度不断降低。综合考虑,选择反应温度为25℃。
2.2.4 AuNPs溶液浓度的影响
AuNPs溶液浓度会影响PG检测的灵敏度和线性范围,实验探究了不同浓度AuNPs溶液对PG检测效果的影响。分别将AuNPs原液稀释不同倍数进行实验,结果发现将AuNPs原液稀释10倍时,检测效果最好。实验选择AuNPs原液稀释10倍后使用。
2.3 干扰实验
基于PG质量浓度为0.21 μg/mL,在优化实验条件下考察了常见离子及糖类物质对体系测定的影响(相对误差在±5%范围内)。结果表明,下列共存物质的允许量如下(以PG质量浓度的倍数计):K+、Na+500倍;Ca2+300倍;Mg2+200倍;Al3+10倍;Cu2+25倍;Fe3+5倍;葡萄糖、果糖 1 000倍;维生素C、淀粉 100倍。
2.4 工作曲线、检出限及精密度
配制PG系列(0.02、0.04、0.06、0.08、0.21、0.42、0.64、0.85、1.06 μg/mL)标准工作溶液,在最佳实验条件下测定体系的荧光强度,以PG的质量浓度为横坐标,荧光强度为纵坐标绘制标准曲线,结果见图6。
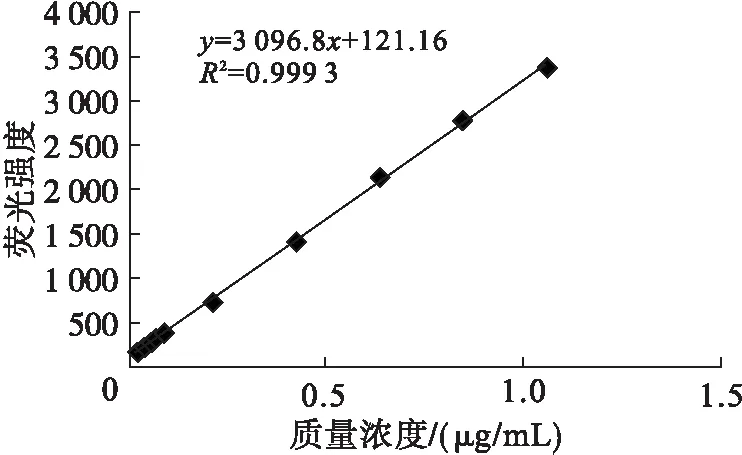
图6 PG标准曲线
由图6可知,在0.02~1.06 μg/mL范围内,PG质量浓度与AuNPs体系荧光强度呈良好的线性关系,线性方程为y=3 096.8x+121.16,相关系数(R2)为0.999 3。以3倍标准偏差计算本法对PG测定的检出限为9.7×10-3μg/mL。平行测定10组质量浓度为0.21 μg/mL的PG溶液,其相对标准偏差为1.3%。
2.5 样品加标回收率测定
采用加标回收法测定两种食用油(花生油,胡麻油)样品中PG含量,加入3种不同质量浓度的PG标准溶液平行测定5组,计算回收率,同时采用光度法(GB/T 5009.32—2003)进行对照实验,结果如表1所示。
由表1可以看出,两种方法测定值基本一致,该方法的加标回收率为92.1%~104.1%,说明该方法准确可靠,能用于实际样品中PG含量的测定。

表1 样品加标回收率
3 结 论
本文以AuNPs与食用油中的PG相互作用,在优化条件下建立一种以AuNPs为荧光探针测定PG含量的新方法。得到检测PG的最佳条件为:缓冲体系pH 7.8,反应时间20 min,反应温度25℃,AuNPs原液稀释10倍。在最佳条件下,PG与金纳米体系荧光强度在0.02~1.06 μg/mL范围内呈良好的线性关系,相关系数(R2)为0.999 3,检出限为9.7×10-3μg/mL。该方法用于食用油中PG的检测,加标回收率为92.1%~104.1%。该方法灵敏度高、选择性好、操作简单、线性范围宽,在食用油中PG含量测定方面具有较好应用价值。
