CeOx对低温选择性催化还原脱硝催化剂FeOx-MnOx/TiO2的改性研究*
2020-01-14肖雨亭张亚平
肖雨亭 吴 鹏 王 玲 张亚平#
(1.江苏龙源催化剂有限公司,江苏 无锡 214123;2.东南大学能源热转换及其过程测控教育部重点实验室,江苏 南京 210096)
煤炭在我国能源消费结构中占有重要比重,然而燃煤产生大量SOx、NOx、粉尘等大气污染物。其中NOx活性高、氧化性强,是造成我国复合型大气污染的主要污染物,威胁人民群众的身体健康,因此脱硝已成为当前迫切需要解决的问题[1]。选择性催化还原(SCR)因其NOx去除率高、无二次污染等优点而成为国内外广泛应用的脱硝技术[2]。随着我国绝大多数燃煤电厂的脱硝改造完成,非电行业正在成为进一步脱硝的领域。根据《2017年脱硫脱硝行业发展评述和2018年发展展望》,非电行业的煤消耗量已占到50%。但是由于非电行业烟气温度普遍较低(120~180 ℃),而燃煤电厂使用的催化剂多为V2O5-WO3/TiO2或V2O5-MoO3/TiO2,它们的工作温度一般远高于120~180 ℃[3],难以直接应用于非电行业。因此,研究在120~180 ℃具有较好催化活性的催化剂,对于非电行业烟气脱硝具有重要意义。
大量研究发现,铁基或锰基催化剂在低温条件下表现出较高的脱硝效率。KIJLSTRA等[4]制备了MnOx/Al2O3催化剂,150 ℃时脱硝效率可达72%。QI等[5]221-222研究发现,FeOx负载到MnOx/TiO2催化剂上形成铁基和锰基催化剂可以进一步提高锰基催化剂的脱硝效率。但是实际烟气中由于含有水蒸气和SO2,会导致催化剂失活[6]。因此,提高铁基和锰基催化剂的抗水性和抗硫性也是其实际应用中需要解决的重要研究课题。
由于稀土元素Ce极好的储存氧和释放氧的能力,其氧化物CeOx对铁基和锰基催化剂的低温SCR脱硝、抗水性及抗硫性有很大的改进作用[7]。刘炜等[8]研究表明,添加CeOx后,MnOx/TiO2催化剂的抗水性明显提升。WEI等[9]指出,SO2会优先与CeOx反应生成硫酸铈,从而可以保护MnOx,而且生成的硫酸铈可以产生新的Brönsted酸位,提高催化剂的低温催化活性。JIN等[10]也研究证实,CeOx的掺杂能够显著提高低温脱硝过程中催化剂的抗水性和抗硫性。由此可见,铁基和锰基催化剂具有优异的SCR脱硝活性,同时CeOx的掺加可以进一步提升低温脱硝性能,增强催化剂的抗水性和抗硫性。
本研究制备了一系列不同CeOx负载量的 FeOx-MnOx/TiO2催化剂,进行低温SCR脱硝活性测试,同时结合催化剂结构和性能的表征探究CeOx对FeOx-MnOx/TiO2的改性作用。
1 方 法
1.1 材 料
Fe(NO3)3·9H2O、Mn(CH3COO)2·4H2O、Ce(NO3)3·6H2O,均为分析纯;TiO2,粒径为30 nm,纯度为99.9%。
1.2 催化剂制备
选择(FeOx)0.1-(MnOx)0.4/TiO2(其中0.1、0.4分别为FeOx、MnOx与载体TiO2的摩尔比)催化剂进行改性研究[5]219-221,[11],[12]4961,[13]。首先,称取3 g TiO2,再根据CeOx、FeOx、MnOx与TiO2的摩尔比称取相应质量的Fe(NO3)3·9H2O、Ce(NO3)3·6H2O和Mn(CH3COO)2·4H2O。然后,将TiO2加入到40 mL去离子水中,再分别加入Fe(NO3)3·9H2O、Ce(NO3)3·6H2O和Mn(CH3COO)2·4H2O,先在25 ℃下均匀搅拌4 h,再在80 ℃下继续搅拌至水分近蒸干,于110 ℃下干燥12 h,冷却后研磨至粉末状,然后置于马弗炉(SX-20-10)中以5 ℃/min从25 ℃升温至450 ℃后煅烧4 h,冷却即得CeOx改性的FeOx-MnOx/TiO2催化剂,记作(CeOx)n-(FeOx)0.1-(MnOx)0.4/TiO2(其中n为CeOx与载体TiO2的摩尔比)。
1.3 催化剂活性测试
图1为催化剂活性测试的装置示意图。通过耐高温石英棉将催化剂粉末固定在不锈钢反应器内,由带温控系统的管式炉提供脱硝反应所需的温度。模拟烟气基本成分由NO、NH3、O2和N2配制而成,其中NO、NH3、O2的体积分数分别为0.08%、0.08%、10.00%,SO2和水蒸气的体积分数根据实验设计确定,N2为平衡气,总烟气流量为100 mL/min,空速为20 000 h-1。水蒸气由微量注射泵将去离子水加热气化而成。用烟气分析仪(testo 350-XL)测量进出气取样口的NO和NO2,并计算脱硝效率。

1—高压气瓶;2—减压阀;3—球阀;4—质量流量计;5—气体混合器;6—进气取样口;7—微量注射泵;8—加热器;9—催化剂床层;10—管式炉;11—不锈钢反应器;12—温控仪;13—出气取样口;14—尾气吸收装置图1 催化剂活性测试装置结构示意图Fig.1 Schematic diagram of the catalysts activity evaluation device
1.4 分析方法
采用比表面积及孔径分析仪(Fsorb3400)测定催化剂比表面积、总孔体积和平均孔径。
催化剂晶体的表征采用X射线衍射仪(D2 PHASER,德国布鲁克AXS公司),Cu靶,扫描范围为10°~80°,扫描速率为4°/min。
催化剂的氧化还原能力用程序升温化学吸附仪(FINSORB3010)的H2程序升温还原(H2-TPR)图谱表征。
催化剂NH3吸附行为的表征采用原位漫反射傅立叶红外光谱仪(Nicolet6700,美国赛默飞世尔公司),扫描范围为1 100~2 000 cm-1,分辨率为4 cm-1。
2 结果与讨论
2.1 催化剂活性测试
2.1.1 不同CeOx负载量的催化剂活性
不同CeOx负载量的催化剂脱硝效率如图2所示。总体而言,随着CeOx负载量的增加,催化活性显著增强,并且最佳催化温度降低。(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂在160~180 ℃时催化活性最高,并且保持稳定,脱硝效率达到99%以上。(CeOx)0.10-(FeOx)0.1-(MnOx)0.4/TiO2催化剂的活性与(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2相差不大,也是在160~180 ℃时催化活性最高,并且保持稳定,脱硝效率达到99%以上,因此也就没必要继续提高CeOx负载量了。由此说明,适量CeOx可以提高FeOx-MnOx/TiO2催化剂的脱硝效率,并且能降低最佳催化温度,可以用于非电行业烟气脱硝。下面抗水性和抗硫性研究使用(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂。
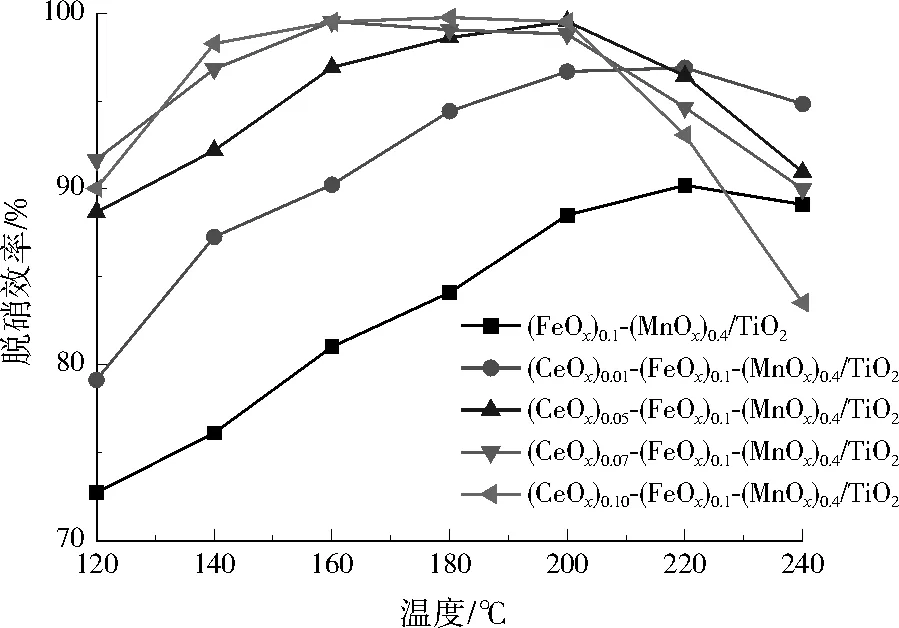
图2 不同CeOx负载量的催化剂脱硝效率Fig.2 NOx conversion of catalysts with different CeOx loadings
2.1.2 (CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂的抗水性和抗硫性
图3研究了模拟烟气中含有水蒸气时(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂的抗水性。水蒸气明显影响了脱硝效率,并且随水蒸气体积分数增大,脱硝效率大幅下降,水蒸气体积分数小于等于10%,基本能保证脱硝效率达到90%以上。180 min时切断水蒸气,脱硝效率可以恢复。因此,水蒸气对(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂的影响是可逆的,只要保证水蒸气体积分数小于等于10%,(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂能有良好的抗水性。
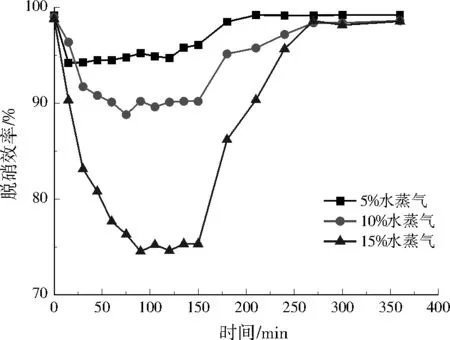
图3 水蒸气对催化剂脱硝效率的影响Fig.3 Effect of water vapour on NOx conversion of catalysts
图4研究了模拟烟气在10%水蒸气的条件下又有SO2存在时,(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂的抗水性和抗硫性。SO2同样会使脱硝效率降低,且随着SO2体积分数增大,脱硝效率大幅下降。SO2体积分数小于等于0.02%,脱硝效率仍能保持90%左右,且150 min时切断SO2和水蒸气后脱硝效率可以恢复。当SO2体积分数为0.04%时,脱硝效率迅速降至约20%,即使提前到90 min时切断SO2和水蒸气,脱硝效率也无法恢复。因此,SO2可对(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂造成不可逆影响,要保证催化剂良好的抗硫性,SO2体积分数须小于等于0.02%。

图4 SO2对催化剂脱硝效率的影响Fig.4 Effect of SO2 on NOx conversion of catalysts
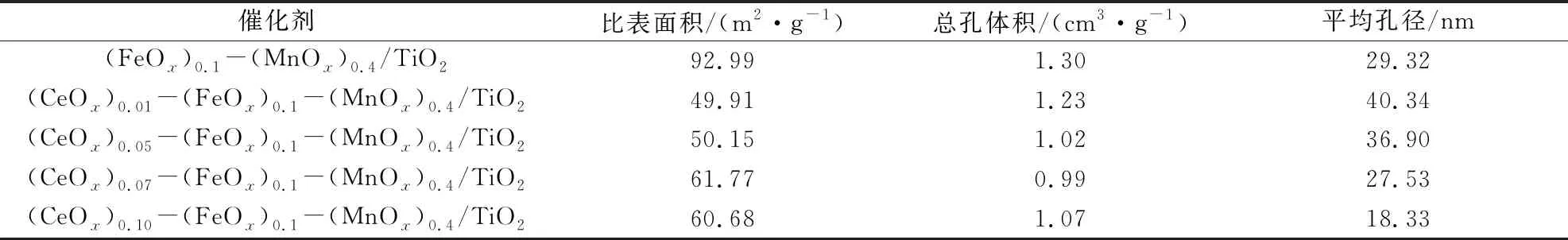
表1 催化剂的比表面积、总孔体积和平均孔径
2.2 催化剂表征
2.2.1 催化剂孔隙结构分析
由表1可见,(FeOx)0.1-(MnOx)0.4/TiO2催化剂的比表面积最大,总孔体积也最大。当n由0.01提高到0.07,催化剂比表面积由49.91 m2/g逐渐增大至61.77 m2/g,总孔体积由1.23 cm3/g减小到0.99 cm3/g,Mn2O3和CeO2形成固溶体结构可能是催化剂比表面积增大和总孔体积减小的原因[14]。继续增大n,催化剂比表面积反而有所减小,而总孔体积反而有所增大。当n为0.01、0.05时,(CeOx)n-(FeOx)0.1-(MnOx)0.4/TiO2催化剂平均孔径比(FeOx)0.1-(MnOx)0.4/TiO2大,而当n为0.07、0.10时,(CeOx)n-(FeOx)0.1-(MnOx)0.4/TiO2催化剂平均孔径比(FeOx)0.1-(MnOx)0.4/TiO2小。由此看来,催化剂的孔隙结构并不是催化剂活性高低的最主要因素。
2.2.2 催化剂晶相分析
图5为不同CeOx负载量催化剂的X射线衍射图谱。所有催化剂均能观察到锐钛矿TiO2(JCPDS,21-1272)的特征峰,大部分催化剂表面Mn2O3(JCPDS,65-7467)的特征峰也比较明显,但所有催化剂均未能观察到FeOx、CeOx的特征峰,这是因为活性组分FeOx和CeOx的结晶度低,不发生团聚,以无定形态分散在催化剂表面,或者是形成的晶体颗粒尺寸过小[15]。当n为0.07或 0.10时,锐钛矿TiO2的相对结晶度基本达到最低,有利于催化活性的提高。
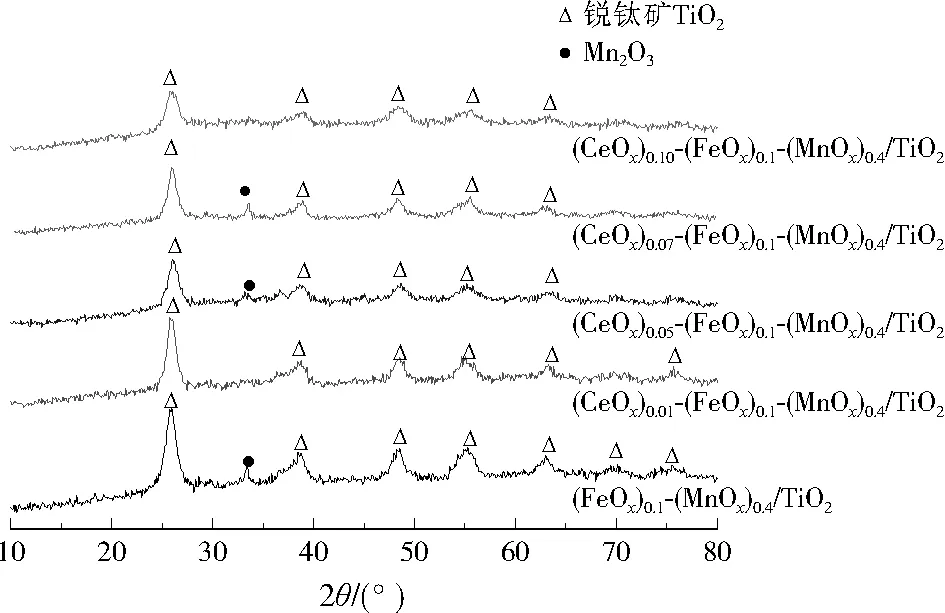
图5 催化剂的X射线衍射图谱Fig.5 X-ray diffractions patterns of the catalysts
2.2.3 催化剂氧化还原能力分析
图6为(CeOx)n-(FeOx)0.1-(MnOx)0.4/TiO2催化剂的H2-TPR图谱,Gauss拟合得到5个耗氢还原峰,表2为各个耗氢还原峰的面积。峰Ⅰ、峰Ⅱ和峰Ⅳ分别对应MnO2→Mn2O3、Mn2O3→Mn3O4、Mn3O4→ MnO 3个过程的耗氢还原峰[16],而峰Ⅲ和峰Ⅴ分别对应Fe2O3→Fe3O4、Fe3O4→FeO 2个过程的耗氢还原峰。由图6可知,n≤0.07的催化剂均有5个耗氢还原峰,而n=0.10的催化剂仅有峰Ⅰ、峰Ⅱ、峰Ⅲ和峰Ⅴ 4个耗氢还原峰。(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂耗氢还原峰温度最低,并且面积较大(见表2),此时低温氧化还原能力最强[17],这就是该催化剂具有较好的低温催化活性的原因之一。
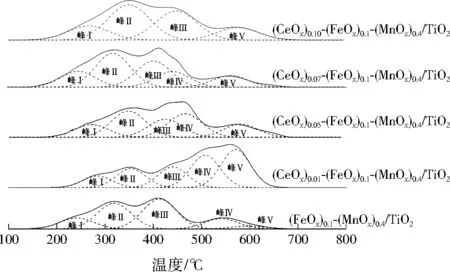
图6 催化剂的H2-TPR图谱Fig.6 H2-TPR profiles of the catalysts
2.2.4 催化剂NH3吸附行为分析
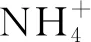

表2 催化剂的耗氢还原峰面积

图7 催化剂的NH3吸收原位漫反射傅立叶红外光谱Fig.7 NH3 adsorption in situ diffuse Fourier infrared spectra of the catalysts
分析图7可知,(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂在Lewis酸位上的NH3最稳定,300 ℃时仍稳定存在,这也说明(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂最为稳定。
3 结 论
(1) 适量负载CeOx,可以显著提高(CeOx)n-(FeOx)0.1-(MnOx)0.4/TiO2催化剂的低温SCR脱硝催化活性。当n=0.07时,(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂160~180 ℃时的催化活性最高,脱硝效率达到99%以上。同时,该催化剂对水蒸气、SO2体积分数分别小于等于10%、0.02%的情况,具有较好的抗水性和抗硫性。
(2) X射线衍射分析表明,当n为0.07时,锐钛矿TiO2的相对结晶度低,有利于催化活性的提高。 H2-TPR分析结果显示,(CeOx)0.07-(FeOx)0.1-(MnOx)0.4/TiO2催化剂耗氢还原峰温度最低,并且面积较大,低温氧化还原能力最强。其表面Lewis 酸位上的NH3最稳定,也有利于其低温SCR脱硝。
