碘酸钾滴定法测定阳极泥中锡含量
2020-01-09向春
向 春
(云南锡业研究院有限公司,云南 个旧 661000)
阳极泥由于其成分复杂,在对其中锡的含量进行测定时,通常会受到很多其它元素的干扰。测定锡含量的常用方法是碘酸钾滴定法,运用广泛,但是阳极泥中杂质元素含量较高且影响锡的测定[1-2]。
本文通过对试样的分解、铁粉、铝粒及淀粉溶液的用量进行了试验研究,并对其中影响测定锡的杂质元素进行了分离。试样经焙烧后再用锌粉-硼砂-硼酸混合熔剂烧结分解,以盐酸浸出,还原铁粉分离杂质元素,金属铝还原锡,以淀粉为指示剂,碘酸钾标准滴定溶液滴定至终点测定锡含量。
1 实验部分
1.1 主要试剂
金属锡[w(Sn) ≥99.99%];
还原铁粉:粒度小于0.2mm,含铁量大于93%;
铝粒:含量99.5%以上,颗粒状;
锌粉:(工业纯,粒度为0.074~0.18mm);
无水硼砂(Na2B4O7),分析纯;
硼酸,分析纯。
锌粉-硼酸-无水硼砂混合熔剂:称取20g 无水硼砂、10g 硼酸在乳钵中磨细后,加90g 工业锌粉,混匀,放入磁盘中,置于100~105℃烘箱中烘1h,冷后研磨,保存于磨口玻璃瓶中。
淀粉溶液(5g/L):称取2.5g 木薯粉(可溶性淀粉),置于50mL 烧杯中,称取1g 氢氧化钠置于盛有约50mL 蒸馏水的烧杯中,摇动溶解后,立即用水将木薯粉移入氢氧化钠溶液中,摇动至试液清亮,用水稀释至500mL,混匀。
碘化钾溶液(100g/L);三氯化钛溶液(15%)。
锡标准溶液:称取2.0000g 金属锡 [w(Sn)≥99.99%]于500mL 烧杯中,加入盐酸200mL,盖表面皿,低温加热溶解完全,取下冷却至室温,以水转移入1000mL 容量瓶中,用水稀释至刻度,混匀。此溶液每毫升含锡2mg。
碘酸钾标准滴定溶液 [ C(1/6KIO3)=0.05mol/L]的配制:
称取17.75g 碘酸钾、10g 无水碳酸钠于1L 烧杯中,加入800mL 水,加热并搅拌至完全溶解,加入90g 碘化钾,搅拌至溶解,冷却后以水稀释至10L,混匀。
标定:称取0.1000g 金属锡 [w(Sn) ≥99.99%]置于300mL 锥形瓶中,加入1g 还原铁粉,80mL 盐酸,将锥形瓶连接于还原台上。低温加热使锡溶解完全后,加20mL 水。加入1.5g铝粒,连续摇动锥形瓶至大部分铝粒溶解,加热煮沸试液至铝粒溶解完全,并产生大气泡。通入二氧化碳气体,在二氧化碳气体保护下,将锥形瓶放入冷水槽中冷却至室温。取下锥形瓶,塞上橡皮塞,移至滴定台,加入5mL 淀粉溶液,立即用碘酸钾标准溶液滴定至浅蓝色为终点。同时进行空白试验。
按下面公式计算碘酸钾标准滴定溶液的实际浓度
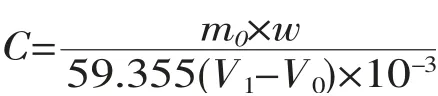
式中:C 为碘酸钾标准溶液滴定溶液的实际浓度,单位为mol/L;m0为称取金属锡的质量,单位为g;w 为金属锡中锡的质量分数,%;V1为标定时滴定金属锡所消耗的碘酸钾标准溶液的体积,单位为mL;V0为标定时空白试验所消耗的碘酸钾标准滴定溶液的体积,单位为mL;59.355 为锡(1/2Sn)的摩尔质量,单位为g/moL。
平行标定三份,其极差不大于1×10-4mol 时,取其平均值,否则重新标定。
1.2 实验方法
称取0.2000g 试样于5mL 瓷坩埚中(同时做空白),在500~550℃的马弗炉中焙烧15~30min,取出,冷却至室温后加入2g 混合熔剂,用细玻璃棒搅匀,用毛刷净玻璃板,覆盖1g 混合熔剂,1g 氯化钠。移入马弗炉中在750~800℃中熔融20~30min。取出冷却后放入盛有50mL 盐酸(1+1)的250mL 烧杯中盖上表皿,连接好还原装置,加热至熔融物溶解,浸取完全。加入2 滴10%碘化钾溶液,加入1~1.5g 还原铁粉,加热微沸至剩余少量铁粉时,立即在流水中冷却,用棉花加少量纸浆过滤于300mL 锥形瓶中,以盐酸(1+1)洗涤烧杯及沉淀3~5 次,控制试液体积约100ml,弃去沉淀。补加盐酸(1+1)至120mL,往锥形瓶中加入0.8mL 三氯化钛溶液和1~2g 氯化钠,连接于还原台上,加入1~1.5g 铝粒,持续摇动锥形瓶,使还原作用完全,绝大部分铝溶解,煮沸至小气泡消失,在二氧化碳其他保护下流水中冷却至室温,停止通入二氧化碳气体,取下锥形瓶,塞好橡皮塞并移至滴定台,快速加入5mL 淀粉溶液,立即用碘酸钾标准滴定溶液滴定至浅蓝色为终点。
2 结果与讨论
2.1 混合溶剂的选择试验
经查阅资料[3-7]及实际工作中的经验,本次试验选择锌粉-硼砂-硼酸混合熔剂烧结分解试样。以下按试验方法测定,结果见表1。
从表1 看出,试样采用的熔剂所测得Sn 的结果与参考值相近,本次试验采用此熔剂。
2.2 铁粉用量的选择
加入铁粉的目的主要是起还原作用,消除溶解氧的影响。测定结果见表2。
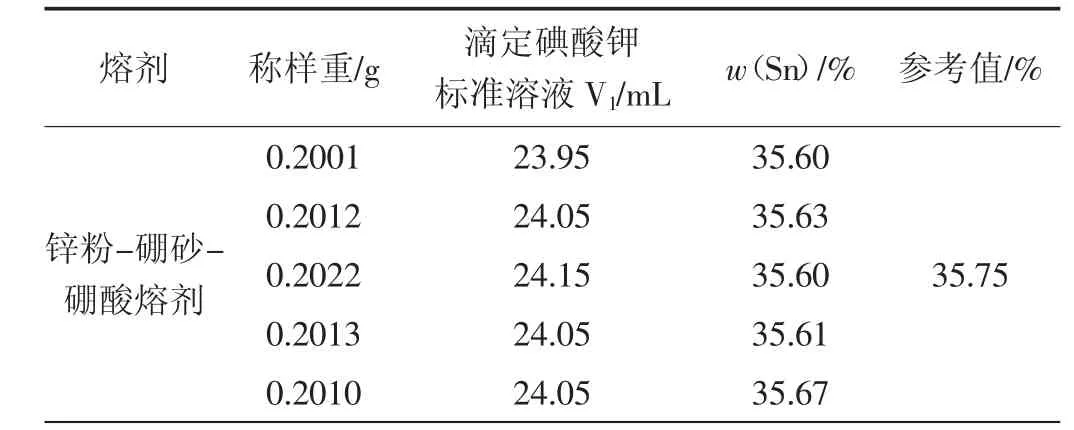
表1 试样分解测定结果
从表2 中看出,铁粉的加入量在1.0~2.0g 对锡的测定结果无明显影响,本试验还原铁粉的用量选择1.0g。
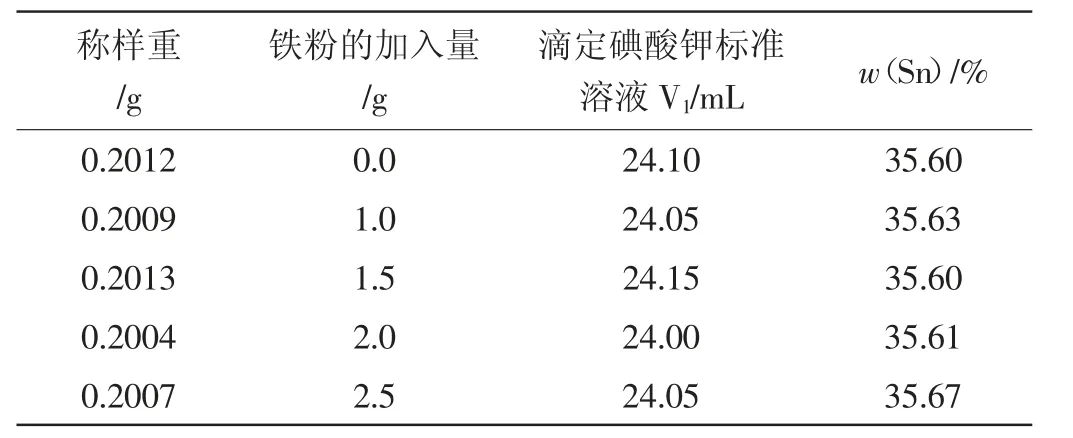
表2 铁粉用量的试验结果
2.3 铝粒用量的试验
加入金属铝粒的主要目的是将锡还原为二价锡,结果见表3。
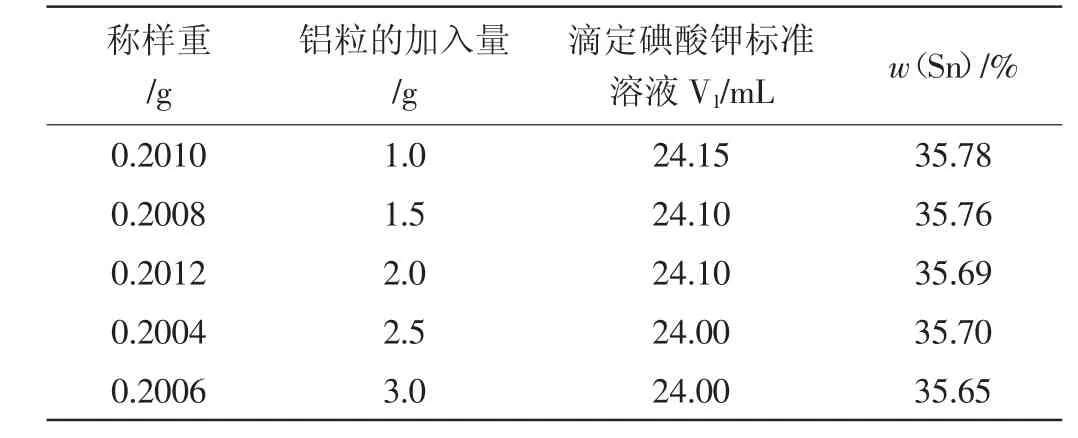
表3 铝粒用量的试验结果
从表3 看出,铝粒的加入量在1.0~2.5g 对测定锡的结果无明显影响,试验方法中的铝粒的加入量选择1.5g。
2.4 淀粉溶液用量试验
碘与淀粉的反应必须有一定量的碘离子存在下方能形成有色吸附物。
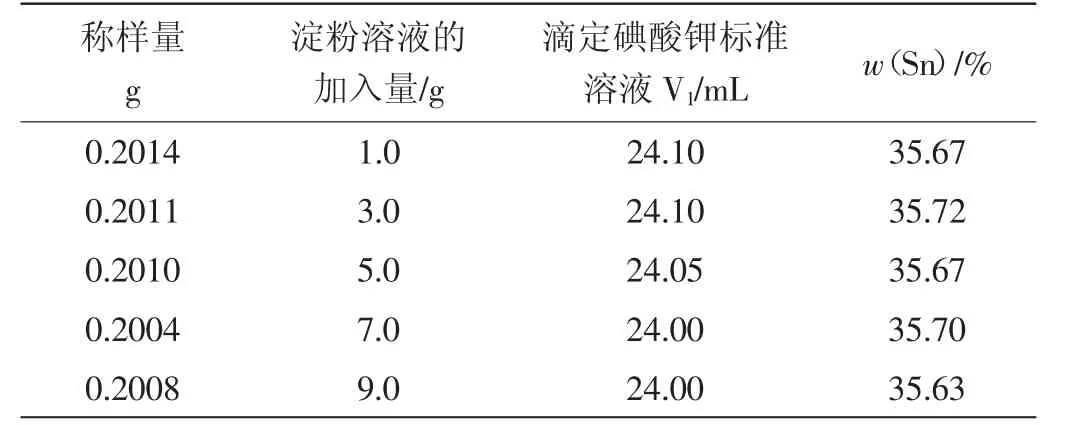
表4 淀粉溶液用量试验
从表4 看出,淀粉的加入量在1~9mL 对测定锡没有明显影响,本试验淀粉的加入量选择5.0mL。
2.5 共存元素的影响与消除
在锡阳极泥中,测定锡时的干扰元素主要有铜、砷、钨、钼、锑、铋、锗、铬、钒、铌。试样经发射光谱半定量分析,阳极泥中主要含有锡、锑、铜、砷、铋等金属元素,其中影响测定锡含量的杂质元素含量见表5。
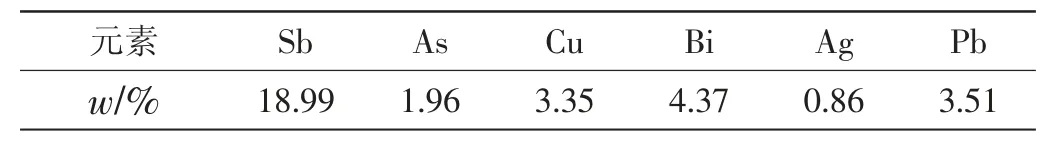
表5 试样中杂质元素含量
表5 中锑、砷、铜对测定锡含量有影响,必须对其进行分离消除。
2.5.1 杂质元素的分离消除
测定锡含量时,共存元素的允许量见表6。

表6 共存元素的允许量
试样经过焙烧及烧结分解后,干扰元素砷挥发近90%,锑挥发近70%。砷挥发后的含量已经不影响锡的测定。利用As3+、Sb3+、Bi3+、Cu2+的氧化还原反应,加入铁粉,可使溶液中锡与其它干扰元素分离。
将烧结冷却至室温的坩埚置于盛有50mL 盐酸(1+1)的250mL 的烧杯中盖上表皿,加热浸出完全,加入2 滴100g/L 碘化钾溶液,1~1.5g 还原铁粉,加热微沸至剩余少量铁粉时,立即在流水中冷却,用棉花加少量纸浆过滤于300mL 锥形瓶中,以盐酸(1+1)洗涤烧杯及沉淀3~5 次,控制总试液体积约100mL。
对分离后的滤液用AAS 法进行检测,铜、砷、锑、铋的含量均在共存元素允许的范围内,不再对锡的测定产生干扰。
2.6 精密度和准确度
按拟定的分析步骤进行测定,结果如表7 所示。
从表7 看出,测定结果稳定,标准偏差和RSD 都较小。
2.7 试样加标回收试验
称取适量试样,加入10mL 锡标准溶液,按拟定分析步骤进行测定,结果见表8。
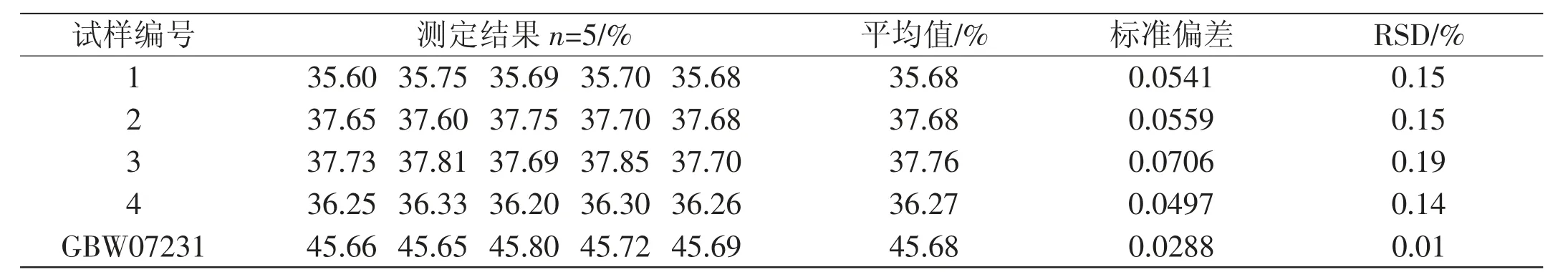
表7 试样中w(锡)分析结果
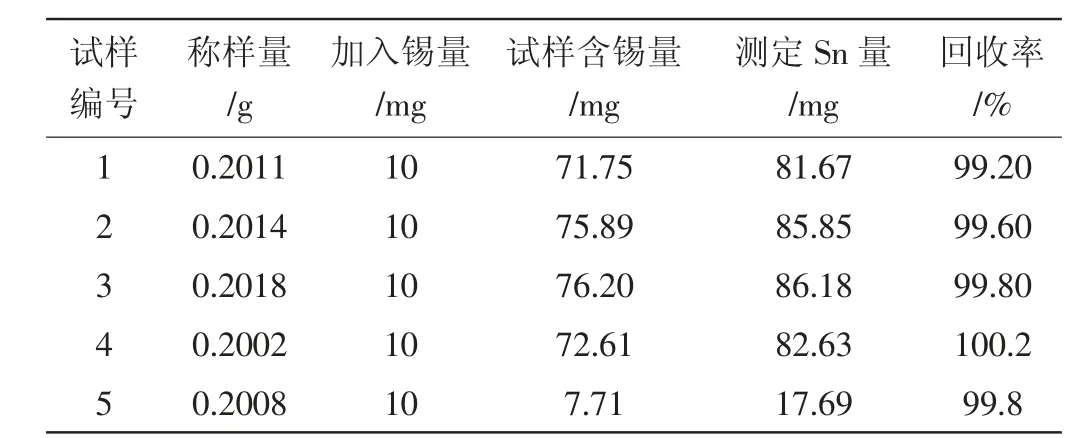
表8 试样加标回收试验
从表8 中看出,试样的加标回收率在99.2%~100.2%之间,满足测定要求。
3 结论
试验结果表明,试样先经焙烧,挥发部分砷及其它杂质元素后经锌粉-硼砂-硼酸混合熔剂烧结分解试样,盐酸(1+1)浸出,还原铁粉分离杂质元素,用碘酸钾标准溶液滴定法测定阳极泥中的锡,精密度高,试样加标回收率高,本方法准确度可靠。
