挥发性有机物与非甲烷总烃的相关性研究
2020-01-09邢利利张晓旭谢永洪吴晓峰
李 佳,陈 勇,张 渝,邢利利,张晓旭,谢永洪,谢 翔,吴晓峰
(1.成都市环境监测中心站,四川 成都 610072; 2.四川省生态环境监测总站,四川 成都 610072)
0 引 言
挥发性有机物(volatile organic compounds,以下简称VOCs)是一类有机化合物质的统称,世界卫生组织将其定义为“熔点低于室温而沸点在50 ℃~260 ℃之间的挥发性有机化合物的总称”[1-2]。由于VOCs是形成臭氧(O3)和细颗粒物(PM2.5)污染的重要前体物,且部分物质具有高毒性,生态环境部印发《2018年重点地区环境空气挥发性有机物监测方案》加强对VOCs的监测,其中甚至将乙烷等沸点远低于50 ℃的有机物也作为了VOCs进行监测。VOCs作为环境监测的重要指标,目前常用的监测方法主要有气相色谱-质谱法(gas chromatographymass spectrometry,简称GC-MS)、气相色谱-氢火焰离子化检测器法(gas chromatography-hydrogen flame ionization detector,以下简称GC-FID)、气相色谱-电子捕获检测器以及液相色谱法[3-5],我国针对大气中VOCs多组分的监测主要有《环境空气 挥发性有机物的测定 罐采样/气相色谱-质谱法》(HJ 759-2015)、《环境空气 挥发性有机物的测定 吸附管采样-热脱附/气相色谱-质谱法》(HJ 644-2013)等方法,但VOCs种类繁多、成分复杂,暂时还无法对所有组分进行监测。由于绝大部分VOCs在FID上都有不同灵敏度的响应,因此在环境标准中通常使用适用性受限的非甲烷总烃(non-methane hydrocarbon,以下简称NMHC)作为挥发性有机化合物总量的指标[3]。这影响了对VOCs总量核算的科学性和准确性,更忽视了不同组分在大气化学中的作用差别,以及高危组分的浓度情况。
NMHC是指除甲烷气体外,在气相色谱仪的氢火焰离子化检测器上有响应的气态有机化合物的总和[6-8]。即在FID上有响应的碳氢化合物的衍生物也属于NMHC范围,在FID上没有响应的有机物则不属于非甲烷总烃,所以NMHC与VOCs在物质组成上有重叠,但不等同。另外,由于不同类型VOCs在FID上响应不同[9-11],所以NMHC与VOCs两者在数值上不相等,但存在相关性。为研究NMHC与VOCs的数量关系,本文运用不同实验方法所得的实验结果建立了NMHC与VOCs的简单数学模型,实现了VOCs与NMHC之间的数量转换。
1 实验部分
1.1 实验原理与实验仪器
实验采用目前环境监测领域中3种不同原理的GC-FID方法对各类标准气体和实际样品进行NMHC的测定,3种方法分别是:六通进样阀双色谱柱法(以下简称双柱法)、十通进样阀单色谱柱法(以下简称单柱法)以及便携式催化-GC-FID法(以下简称催化法)。
双柱法:样品经六通阀进样,分别在甲烷柱和总烃柱上测得甲烷和总烃的含量,两者之差即为NMHC,同时以除烃空气代替样品,测得氧在总烃柱上的响应值,以扣除样品中氧对总烃测定的干扰[6-7]。检测仪器为4890D气相色谱仪(美国HP公司),其甲烷柱为内填充了粒径为60~80目GDX-502的不锈钢填充柱(2 m×3.2 mm),总烃柱为内填充了粒径为60~80目硅烷化玻璃微珠的不锈钢填充柱(2 m×3.2 mm)。仪器流路详见图1。
单柱法:样品通过十通进样阀进样,由载气将样品带入Porapak Q填充柱中分离,当氧气和甲烷出峰后,通过阀的切换,其余组分一起反吹进入FID,形成一个NMHC合峰[12]。检测仪器为Trace GC Utra气相色谱仪(美国Thermo公司),其色谱柱为Porapak Q填充柱(美国Restek公司,2 m×3.2 mm)。仪器流路详见图2。
催化法:气体样品分别进入总烃检测单元和甲烷催化转换单元,经FID检测器分别测定总烃及甲烷的含量,两者之差即为NMHC的含量[13]。检测仪器为PF-300便携式甲烷/总烃/非甲烷总烃测试仪(意大利Pollution公司),仪器配有采样系统、催化装置和FID检测器。
实际样品中VOCs的测定:106种VOCs组分测定参考《环境空气 挥发性有机物的测定 罐采样/气相色谱-质谱法》[14],用内壁惰性化处理的不锈钢罐采集样品,经预浓缩仪热解析后,进入气相色谱仪分离,用质谱检测器进行定性与定量分析。检测仪器为7200预浓缩仪(美国Entech公司),7890B-5977B气相色谱质谱联用仪(美国Agilent公司),其色谱柱为DB-624(美国Agilent公司,60 m×0.250 mm×1.4 μm);甲醛的监测方法为《空气质量甲醛的测定 乙酰丙酮分光光度法》(GB/T 15516-1995)[15],检测仪器为UV5500PC紫外可见分光光度计(上海元析仪器有限公司)。
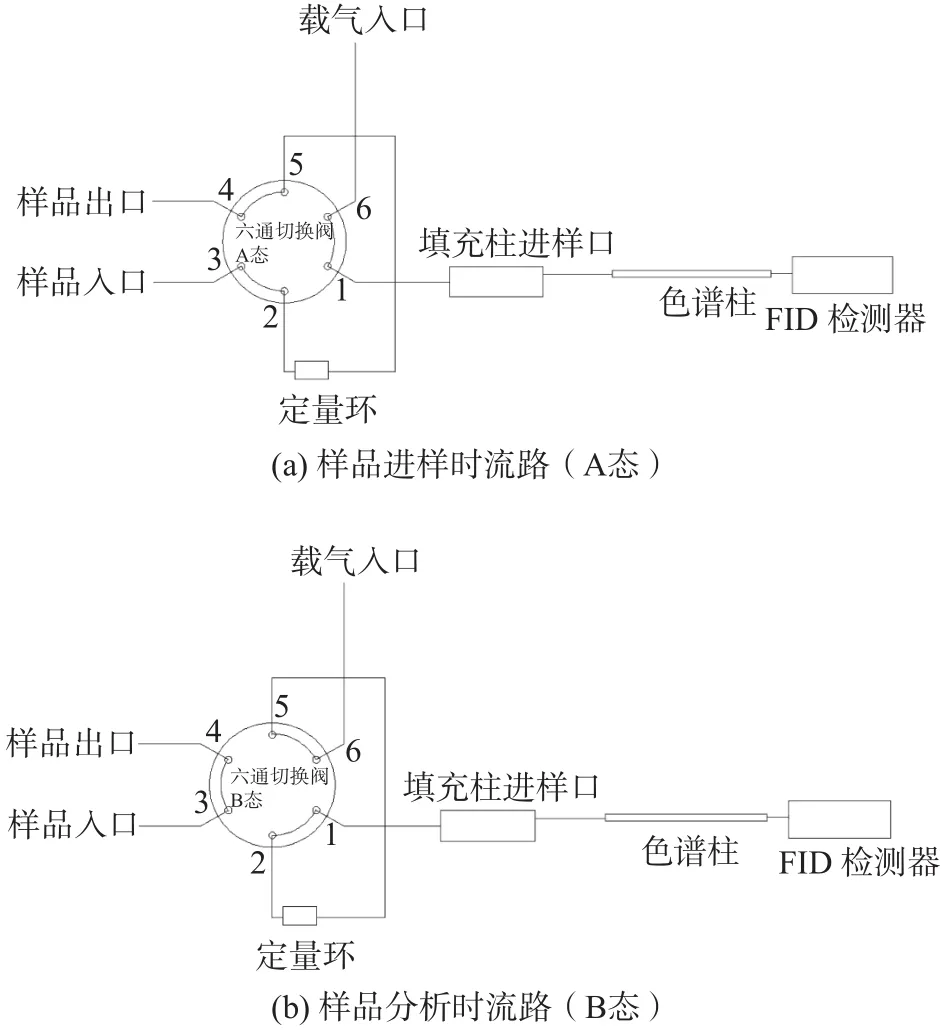
图1 双柱法仪器流路图
标准液体样品的测定:实验采用液体标准样品直接进样,由载气带入色谱柱中分离,经FID检测。检测仪器为7890B(美国Agilent公司)气相色谱仪,其色谱柱为BD-624毛细管柱(美国Agilent公司、30 m×0.25 mm×1.4 μm)。
1.2 实验耗材
高纯氮气(≥99.999%),标准气体1为内含66种组分的TO15(四川中测标物科技有限公司,140 mg/m3),标准气体2为内含57种组分的PAMS(美国Restek公司,205 mg/m3),标准气体3为内含5种组分的有机硫(四川中测标物科技有限公司,5.89 mg/m3),标准气体4为内含两种组分的醛类(四川中测标物科技有限公司,16.1 mg/m3),标准气体5为内含两种组分的NMHC(四川中测标物科技有限公司,甲烷为150 mg/m3,丙烷为296 mg/m3),标准气体6为甲烷气体(意大利Pollution公司,甲烷为40.0 mg/m3和120 mg/m3)。各类标准气体浓度均以碳计,混合标准气体浓度为各组分浓度之和。
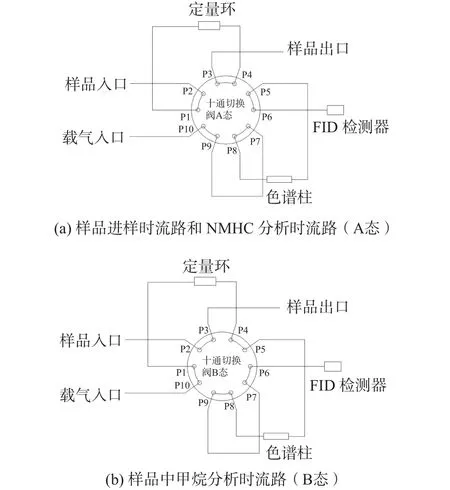
图2 单柱法仪器流路图
使用4700静态稀释仪(美国Entech公司)将各类标准气体稀释至硅烷化真空罐(美国Entech公司)中,得到不同浓度值(以碳计)样品。标准气体5配制成5个不同浓度值(甲烷浓度为:1.00 ,2.00 ,10.00 ,30.0 ,50.0mg/m3;总烃浓度为:3.00 ,6.00 ,30.0 ,90.0 ,150 mg/m3;NMHC浓度为:2.00 ,4.00 ,20.0 ,60.0 ,100 mg/m3);标准气体1和标准气体2配制成浓度60.0 mg/m3的样品;标准气体3和标准气体4配制成浓度为4.00 mg/m3的样品。以下若无特别说明,浓度值均以碳计。
1.3 实验条件
双柱法:进样系统(包含进样管路与六通阀)温度20 ℃、65 ℃和150 ℃;进样口恒压30.0 kPa;进样口温度150 ℃;进样量1.0 mL;检测器250 ℃;氢气压力200 kPa;空气压力350 kPa;总烃柱温150 ℃、甲烷柱温100 ℃。
单柱法:进样系统(进样管道与十通阀)温度100 ℃;柱箱100 ℃保持4.0 min;载气30.0 mL/min、氢气40.0 mL/min、空气300 mL/min;检测器温度250 ℃;十通阀切换时间分别是0.01 min和0.60 min。
催化法:采样流量800 mL/min;进样口温度180 ℃;检测器温度190 ℃;催化模块温度280 ℃;点火阶段氢气流量30.0 mL/min、空气流量300 mL/min;样品测定阶段氢气流量:25.0 mL/min、空气流量:225 mL/min。
标准液体样品的测定:进样口温度220 ℃;柱流量1.5 mL/min;柱温35 ℃保持6 min,10.0 ℃/min升温至220 ℃保持6 min;检测器温度220 ℃;空气流量400 mL/min;氢气流量30.0 mL/min。
2 结果与讨论
2.1 色谱图与校准曲线
2.1.1 色谱图
除催化法无色谱柱外,双柱法和单柱法的色谱图如图3、图4所示。其中图4中两个未标注的色谱峰为十通阀两次切换形成的杂峰。
2.1.2 校准曲线
除催化法使用甲烷标准气对仪器进行单点校准外,双柱法与单柱法均使用NMHC标准气体的浓度与峰面积绘制了校准曲线,其相关系数均大于0.999。校准曲线与相关系数见表1。
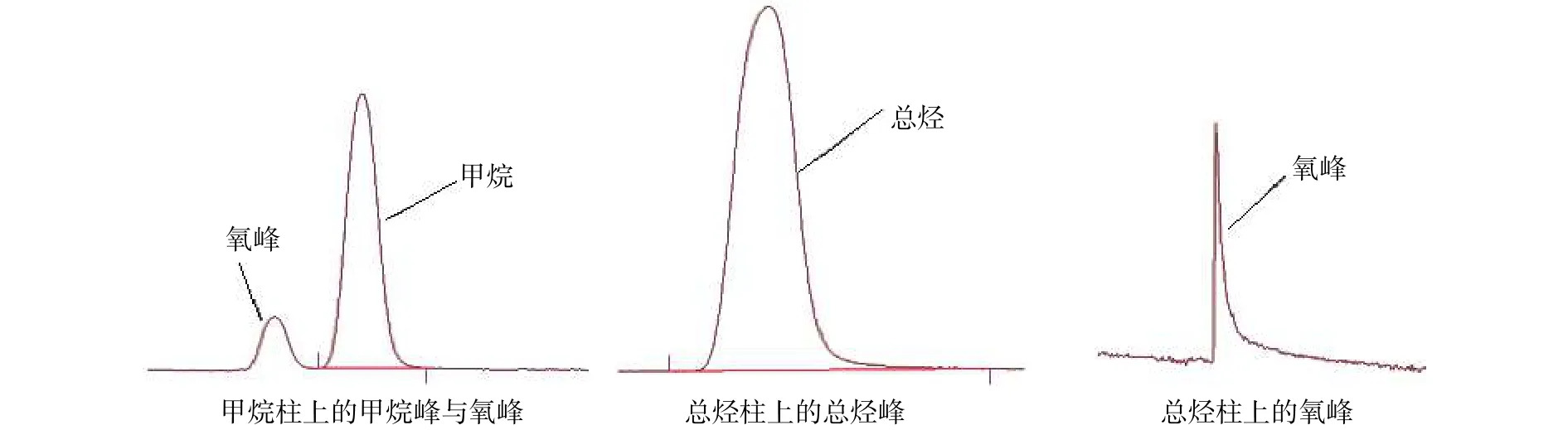
图3 双柱法色谱图
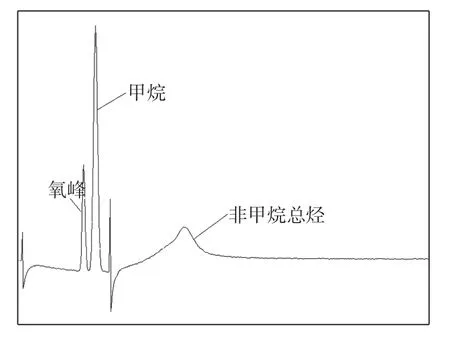
图4 单柱法色谱图

表1 不同方法的校准曲线与相关系数汇总表
2.2 实验条件的优化
双柱法测定样品时,由于VOCs组分复杂,可能存在强吸附性、较高沸点的物质,在进样流路中易因吸附冷凝造成损失,最常见的解决办法是提高进样系统的温度。由于烃类物质在FID上的响应与其含碳数呈现正相关[8-11],本实验选用PAMS标准气体(为C2~C12的烃类,包括了较高沸点的VOCs组分)考察进样系统的温度对实验结果的影响,便于判断损失情况。综上,为考察进样系统温度对测定结果的影响,实验采用双柱法分别在进样系统为20 ℃(常温)、65 ℃和150 ℃(接近部分厂家切换阀的耐受上限温度)时测定PAMS标准气体样品。实验时每个样品均平行测定了3次(n=3)并取均值,将其除以理论值得到回收率。
不同进样系统温度测定PAMS标准气体结果如图5。实验测定值随着进样系统温度的升高而增加,原因是VOCs各组分在进样过程中有不同程度的吸附,温度升高可以有效地降低吸附,当温度升高至150 ℃后,吸附现象基本消失,测定值与理论值基本一致。因此,本文的后续实验,进样系统的温度均设置为150 ℃。
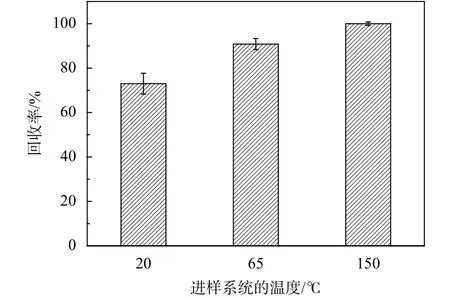
图5 不同进样系统温度测定PAMS标准气体结果汇总图
单柱法测定标准气体样品时,由于Porapak Q对组分的保留能力与其极性、分子量呈正相关,分析含有强极性和较高分子量组分的样品时,柱箱温度可能影响结果的准确性。为考察柱箱温度对实验结果的影响,实验时分别在柱箱温度为80 ℃、100 ℃、140 ℃和160 ℃时测定PAMS标准气体样品。如图6所示,图中两个未标注的色谱峰为十通阀两次切换形成的杂峰。
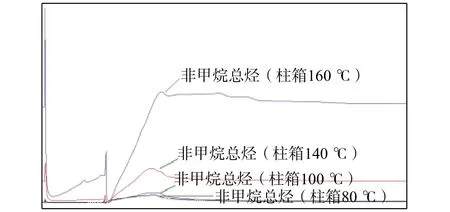
图6 不同柱温下测定PAMS标准气体色谱图
不同柱箱温度下测定PAMS所得色谱图如图6。若柱箱温度较低,极性或沸点达到一定水平的组分很难出峰,若升高柱箱温度,仪器基线会随温度升高而急剧上升,基线对色谱峰的掩盖造成无法对色谱峰进行有效积分。综上,实验选择柱箱温度100 ℃作为最佳实验条件,但是此实验条件NHMC色谱峰依然有不同程度的拖尾现象,自动积分会有较大偏差,结果处理时采用了手动积分,手动积分结果RSD≤3.5%。
2.3 标准气体测定结果
3种方法测定各类标准气体的回收率(测定值除以理论值)详见图7。实验结果表明:1)双柱法、单柱法测定各类标准气体样品呈现很好的一致性;2)催化法测定PAMS和TO15的回收率均较低,并且在测定TO15时,仪器显示甲烷的测定值为4.72 mg/m3,而TO15标准气体组分中并没有甲烷,甲烷理论上应为未检出。原因是催化剂对VOCs各组分的催化效率不同,导致样品并没有完全转变为CO2和H2O,所以,当分析难催化分解物质时,催化剂的催化效率可能会影响实验结果的准确性。3)PAMS回收率为100%,但TO15、有机硫与醛类的测定值均低于理论值,回收率最低为醛类。原因是PAMS组分为烷烃、烯烃和芳香烃类物质,而TO15组分为烷烃、芳香烃、卤代烃以及其他含氧化合物,有机硫组分为二甲基二硫醚、乙硫醚、甲硫醚、乙硫醇和甲硫醇,醛类组分为甲醛和乙醛,物质中含非碳氢原子使其在FID上的响应与同数碳烷烃类物质的响应不同,正如盛立彦[16]等人提出关于醇醚类物质在FID上响应会降低一样,因含氧原子增加了碳正离子形成的难度,从而降低了分子的有效碳数,使得物质在FID上的响应降低。本文标准气体样品的测定结果也正好验证了不同类型VOCs在FID上的摩尔响应值存在差异[16-18]。为考察不同类型VOCs在FID上响应的差异性,实验采用液体标样直接进样、GC-FID分析的方式,考察单一组分在FID上的响应。
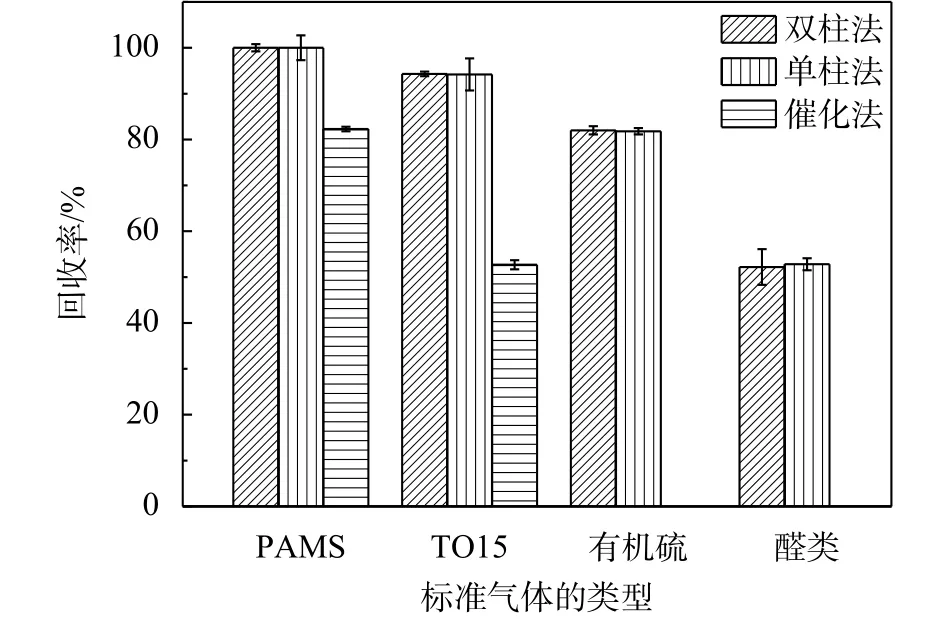
图7 3种方法测定标准气体结果汇总图
2.4 VOCs单一组分在FID上的响应以及VOCs与NMHC的相关性
由FID原理可知,当物质进入FID燃烧的氢气火焰中,与氧气进行了化学电离反应。以苯为例,其在FID的反应如下[9]:
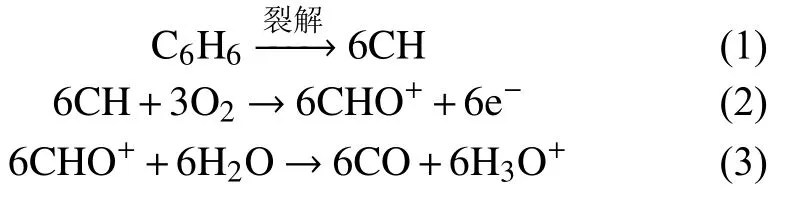
反应表明,电流产生的正离子和电子形成了微电流信号经电流放大器放大后,由仪器记录仪画出色谱峰。故本文使用等质量组分、且VOCs类别包含烷烃类、烯烃类、芳香烃类、酮类、醇类、酯类以及卤代类有机化合物的3种液体标样分别直接进样后经色谱柱分离,由FID检测器检测得到单一组分在FID上的色谱峰面积,如图8所示。
GC-FID法测定等质量VOCs标准液体结果详见图8。比较每一种组分在FID上的响应可以发现:只含碳氢的分子在FID上的响应与碳原子数量呈现一比一正比关系;含有极性共价键的分子在(1)反应中,若碳原子与非碳原子的共价键断裂形成的碳原子基团倾向于失去电子,将会抑制反应式(2)的进行,物质在FID上的响应减弱;相反,若倾向于得到电子,将会促进反应式(2)的进行,物质在FID上的响应增强。
物质在FID上的响应值最终以峰面积呈现,若用A表示某一种物质在FID上的总有效响应值,那么:
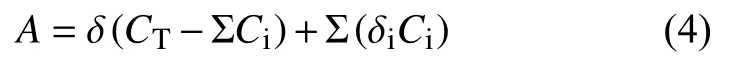
式中:δ——摩尔碳的有效响应值;
CT——物质的总碳数;
Ci——极性共价键的碳原子;
δi——极性共价键的碳原子摩尔响应值;
D——极性共价键的电负性,其中δi=f(δ,D)。
理论上可通过极性共价键的电负性D算得所有物质的A,即当没有标准物质的情况下,也能够通过其他物质的响应来推算无标待测组分的浓度。但实际上受实验条件的限制,本文难以准确测定所有极性共价键的电负性,故建立了简化的响应计算数学模型:将物质中碳碳相连的碳原子视为摩尔碳响应值均为δ,根据本文GC-FID测定VOCs标准液体的实验结果,以FID上碳原子离子化效率为100%的苯为基准,计算得到碳原子在FID上的摩尔碳响应值δ,与非碳原子相连的碳原子视为摩尔碳响应值为δi,假设δi与δ的比值为di,结合在本文实验条件下得到的标准气/液体在FID上的响应值,对不同官能团的δi计算,根据δ与δi可以对di值进行估算,以此建立VOCs与NMHC的简单数学模型。上段的公式则可以转变为:A=δ∑(diCs)=δd表征,公式中Cs为物质含的碳元素,对于只与碳氢原子相连的Cs,其对应di值为1,其他部分官能团的di值与Ci值见表2。
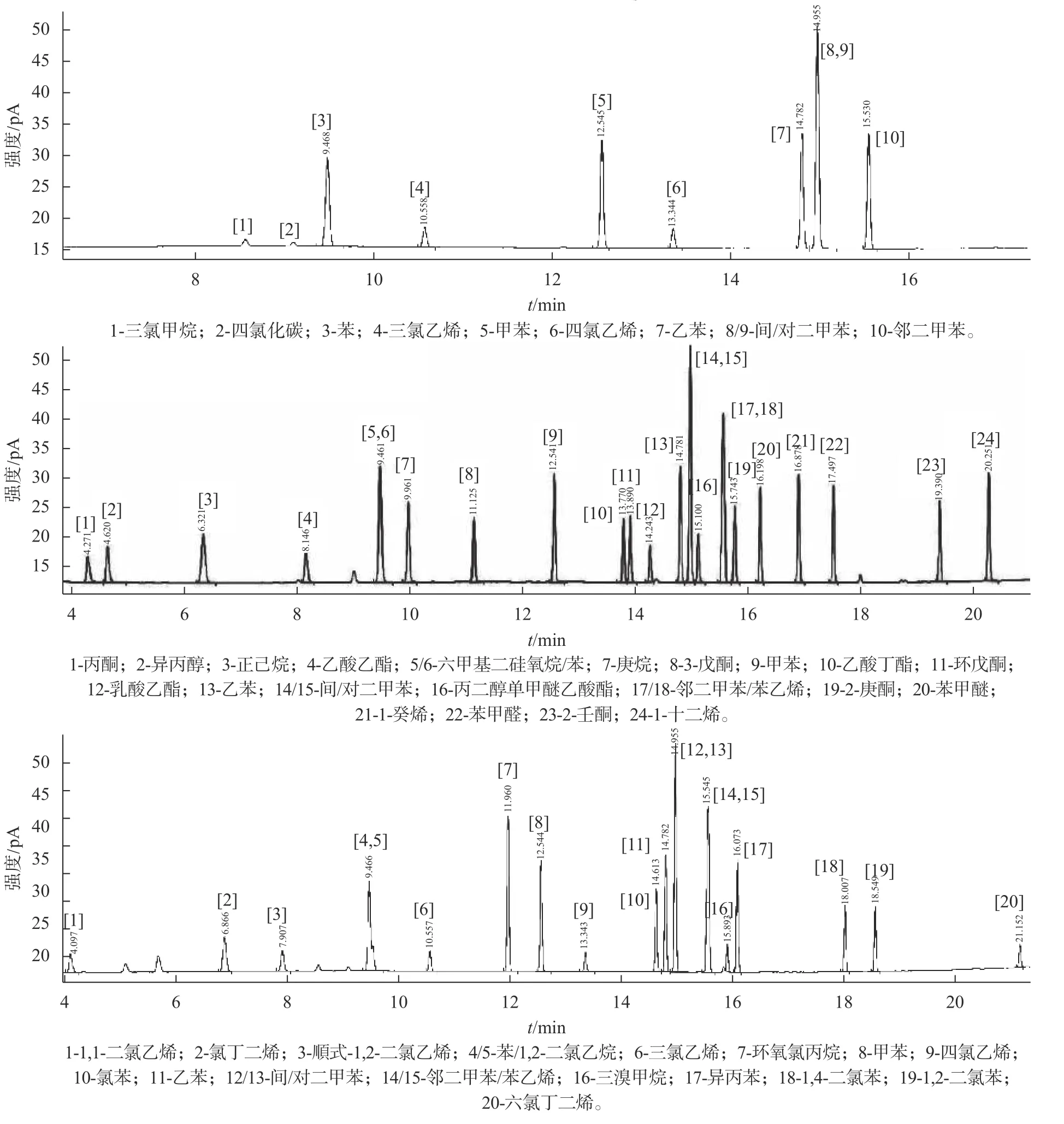
图8 GC-FID法测定标准液体结果汇总图(等质量响应值)

表2 部分官能团的di值与Ci值汇总表
取代官能团会抑制或促进反应式(2),从而造成物质在FID上的响应降低会增加,但根据结果分析,取代官能团难以完全的抑制或无限的促进有机分子在FID上的响应,所以根据实验结果将模型方程式拟合为较接近实际情况的指数函数或幂函数。
2.5 标准气体结果分析
运用数学模型对各类标准气体的理论响应值进行修正,得到修正理论值,计算双柱法的测定值与理论修正值的百分比值(修正回收率),同时将标准气体测定值与理论值计算所得百分比值(实测回收率)进行比较。
双柱法测定各类标准气体的实测回收率与修正回收率的比较详见图9。如图,通过数学模型的修正后,各类标准气体回收率均达到了98.1%~100%。
2.6 实际样品结果分析
实验使用单柱法和双柱法测定了实际样品的NMHC,同时使用预冷浓缩/GC-MSD测定实际样品中106种有机组分(主要有烷烃、烯烃、芳烃和少量醇、酮类),以及使用乙酰丙酮分光光度法测定样品中甲醛的含量(106种组分中不包括甲醛,而甲醛是室内重要有机物指标)。
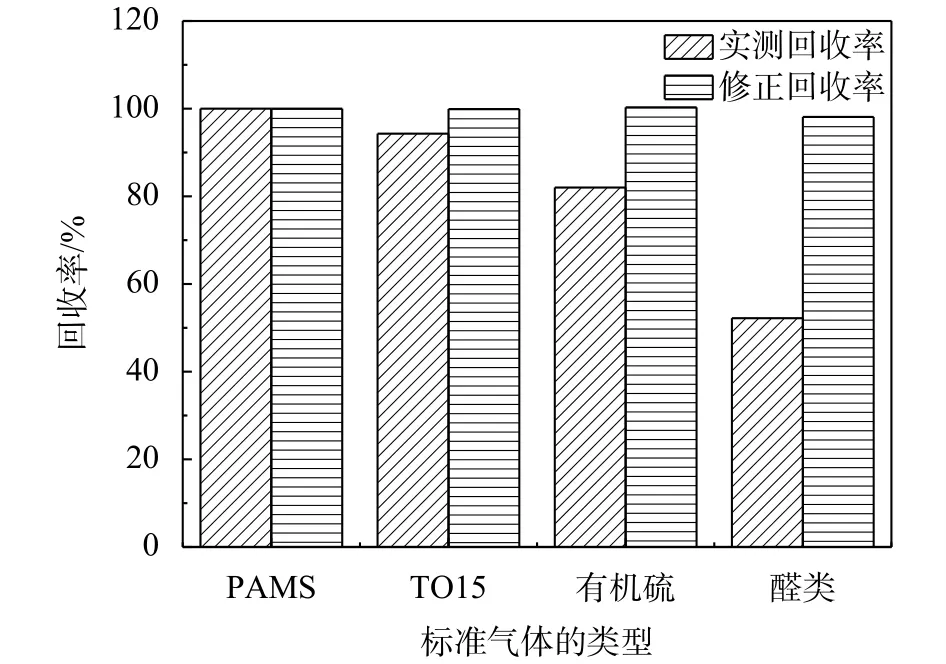
图9 各类标准气体实测回收率与修正回收率比较图
实际样品的NMHC与VOCs(包括甲醛在内的107种有机物组分的质量体积浓度之和)的测定结果详见图10。实验结果比较发现:样品NMHC的测定值高时,VOCs的测定值也普遍较高,两者存在一定程度的正相关关系;由于实际样品中VOCs的种类繁多,而实验室能检测的种类有限,所以VOCs的各组分浓度之和低于NMHC。
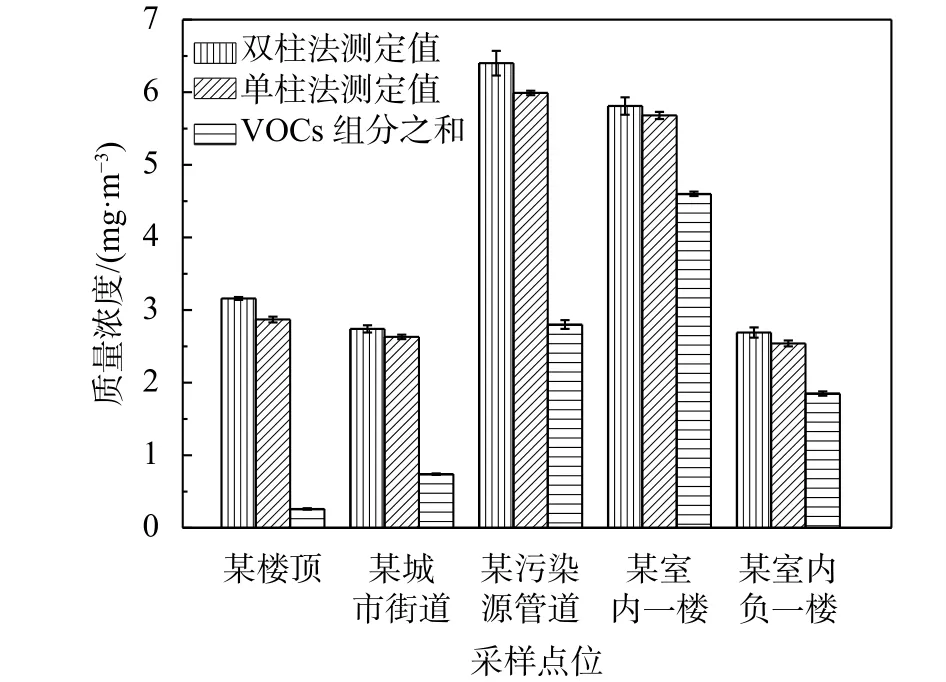
图10 实际样品NMHC测定值与VOCs结果比较图
3 结束语
综上,VOCs与NMHC之间有相关性,但并不等同。从物质组成上,NMHC与VOCs有重叠,但不完全相同。从数值上,双柱法、单柱法和催化法3种实验方法所得测定值已表明NMHC与VOCs两者之间存在一定的数量关联:当样品中只含碳氢化合物时(如PAMS和苯系物),VOCs与NMHC的数值十分接近,此时可以用NMHC作为VOCs的总量指标;当VOCs分子含有取代官能团时,其在FID上的响应系数与碳氢化合物的响应系数不同,NMHC与VOCs的数值有较大差异,此时用NMHC将难以对VOCs总量做出科学准确的评估。
此外,NMHC仅为总量型的指标,而且对含官能团的VOCs分子响应一般偏低,因此无法对甲醛、1,1,1-三氯乙烷、四氯化碳等高毒VOCs物质的浓度进行有效监测或评估,存在环境监测方面难以弥补的缺陷。
本文结合标准气体与标准液体的在FID上的测定结果建立了NMHC与VOCs之间的简单数学模型,且运用该模型计算得出各类标准气体的VOCs理论修正值,NMHC的回收率为98.1%~100%,数学模型可信。
