神经生长因子在慢性阻塞性肺疾病大鼠血、肺组织、支气管灌洗液中的表达
2020-01-09李渺苗邵宏涛李宁孔铖英孙丽蒋涛
李渺苗 邵宏涛 李宁 孔铖英 孙丽 蒋涛
(1浙江大学医学院附属第四医院呼吸与危重症学科,浙江 义乌 322000;2南京中医药大学附属中西医结合医院;3江苏省中医药研究院)
慢性阻塞性肺疾病(COPD)是一种以气流受限为特征的疾病,气流受限不完全可逆、并呈进行性发展〔1〕。吸烟是COPD的主要危险因素,慢性炎症是COPD发病的中心环节,但令人费解的是,即使戒烟后肺部的炎症仍然存在,所以炎症一旦启动,就会一直持续存在,并进行性加重,形成恶性循环〔2〕。目前缺乏统一标准的COPD动物模型构建方法,尤其是在停止造模干预后仍显示出COPD的特征性变化的造模方法。神经生长因子(NGF)在肺组织中广泛表达,在不同微环境下,NGF通过表达变化及介导细胞功能的发挥参与肺部疾病的发生发展,如支气管哮喘、肺结节病、肺癌、肺纤维化等〔3〕。研究发现香烟刺激COPD大鼠肺巨噬细胞高表达NGF〔4〕。因此观察NGF在COPD、戒烟COPD中的表达变化有助于进一步阐述COPD炎性持续存在的发病机制。
1 材料与方法
1.1实验动物 健康雄性SD大鼠24只,平均体重(145±15)g,清洁级,由南京军区南京总医院比较医学科提供。实验动物合格证号:SCXK(军)2012-0014。
1.2试剂与仪器 大丰收牌香烟由中国烟草总公司监制(含焦油量11 mg,烟气烟碱量0.9 mg,烟气一氧化碳量14 mg);NGF上下游引物由南京金斯瑞公司合成;总RNA提取试剂盒购自北京天根生化科技有限公司;逆转录试剂盒及实时荧光定量PCR试剂盒购自Takara大连宝生物有限公司;实时荧光定量PCR仪为美国ABI StepOne定量PCR仪;大鼠NGF ELISA试剂盒购自武汉博士德生物工程有限公司。
1.3动物模型的建立 将24只大鼠按随机数字表法分为正常对照组、COPD组,戒烟1个月COPD组,每组8只。采用单纯烟熏法建立COPD大鼠模型:将大鼠置于自制的熏箱(70 cm×50 cm×30 cm)内,每次点燃5只香烟,2次/d,共暴露2 h/d,每周5 d,连续6个月。戒烟1个月COPD组:按COPD大鼠模型进行香烟刺激6个月后,停止香烟刺激1个月。正常对照组亦同时放入另一相同自制熏箱做伪暴露,余饲养条件相同。
1.4肺组织病理HE染色 2%戊巴比妥钠腹腔麻醉大鼠(30 mg/kg),心脏抽血处死,将右上肺浸入4%多聚甲醛中固定24 h,石蜡包埋,4 μm连续切片,脱蜡,HE染色,脱水,透明,封片,光学显微镜下观察。
1.5支气管肺泡灌洗进行细胞分类计数 麻醉大鼠后,75%酒精浸泡消毒2~3 min,移至超净工作台,固定四肢,逐步暴露气管后,丝线结扎上端气管防止灌洗液倒流,静脉留置针行气管穿刺,成功后退金属内芯并将塑料套管缓慢送入气管约1 cm,经套管注入PBS行支气管肺泡灌洗,每次5 ml,共6次,灌洗时轻柔按摩双肺1 min后回吸。收集灌洗液后,1 000 r/min离心10 min,DMEM重悬细胞,在光镜下行有核细胞计数。吸取100 μl细胞悬液行细胞涂片,经瑞士吉姆萨染色。
1.6酶联免疫吸附试验(ELISA)测定3组大鼠血、肺组织、支气管肺泡灌洗中NGF蛋白表达 取3组大鼠右下肺0.5 mg左右,充分剪碎,研磨,加入约 500 μl磷酸盐缓冲液(PBS),充分混匀,5 000 r/min离心10 min,取上清。取3组大鼠血液2 ml,1 000 r/min离心5 min,取上清。收集支气管灌洗液后,1 000 r/min离心10 min,取上清。配制1 000.0 pg/ml,500.0 pg/ml,250.0 pg/ml,62.5 pg/ml,31.3 pg/ml,15.6 pg/ml的标准品,并依次加入一排7个孔中,1孔只加样品稀释液做为零孔。其余孔加入样品稀释液稀释的上清液100 μl,酶标板加上盖,37℃反应90 min,甩去酶标板的液体,对着吸水纸拍4次,不洗,加入NGF抗体工作液100 μl,37℃反应60 min,甩去液体,PBS洗3次,每次1 min,加入100 μl ABC工作液,37℃反应30 min,甩去液体,PBS洗5次,每次1 min,加入90 μl TMB显色液,37℃避光反应25 min,加入100 μl TMB终止液,用酶标仪在460 nm测定OD值。
1.7实时荧光定量PCR检测3组大鼠肺组织、支气管灌洗液NGF mRNA表达 按照总RNA提取试剂盒提取的总RNA,并测量RNA的浓度,根据逆转录试剂盒操作合成cDNA,反应条件(30 μl反应体系)为:37℃ 30 min,85℃ 5 s。NGF上游序列为5′-CACTCTGAGGTGCATAGCGT-3′,下游序列为5′-GCTTCAGGGACAGAGTCTCC-3′,内参照GAPDH上游序列为5′-TCAAGAAGGTGGTGAAGCAG-3′,下游序列为5′-AGGTGGAAGAATGGGAGTTG-3′。实时荧光定量PCR反应体系采用SYBR GreenⅠ,其最终反应体系为20 μl,采用两步法扩增,最后得到荧光阈值循环数(Ct值)。NGF mRNA相对表达量用2-ΔΔCt进行比较。ΔCt目的基因=Ct目的基因-Ct内参基因,ΔΔCt=ΔCtCOPD组-ΔCt正常对照组。
1.8统计学方法 采用SPSS18.0统计软件包进行单因素方差分析、LSD检验。
2 结 果
2.1大鼠肺组织HE染色 COPD组、戒烟1个月COPD组大鼠肺组织HE染色均可见肺泡壁变薄、肺泡间隔破裂、肺泡腔不规则扩大,部分融合形成肺大疱,肺气肿形成明显,见图1。
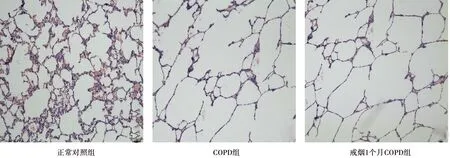
图1 各组肺组织病理改变(HE,×100)
2.2大鼠肺功能检测结果 相比正常对照组,COPD组、戒烟1个月COPD组肺顺应性和每分钟通气量均明显下降,气道阻力明显升高(均P<0.05)。见表1。COPD组戒烟1个月COPD组均出现气流受限,肺通气功能障碍,即使戒烟,COPD大鼠仍存在肺通气功能障碍。
2.3支气管肺泡灌洗液细胞分类 正常对照组支气管灌洗夜中白细胞总数及肺泡巨噬细胞,明显少于COPD组、戒烟1个月COPD组(P<0.05)。肺泡巨噬细胞、中性粒细胞、淋巴细胞所占比例在3组无明显差异(P>0.05)。见表2。
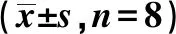
表1 各组肺功能检测结果
与正常对照组比较:1)P<0.05,下表同
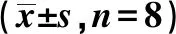
表2 各组支气管肺泡灌洗液中白细胞总数及细胞分类
2.4NGF蛋白的表达 正常对照组、COPD组、戒烟1个月COPD大鼠血中NGF蛋白表达无明显差异(P>0.05)。相比正常对照组,COPD组、戒烟1个月COPD组大鼠肺组织、支气管肺泡灌洗液中NGF蛋白表达明显升高,但两组间无明显差异(P>0.05)。见表3。

表3 各组NGF蛋白在血、肺组织、支气管肺泡灌洗液中的表达
2.5NGF mRNA的表达 COPD组、戒烟1个月COPD组大鼠血中NGF mRNA表达分别是正常对照组的(1.76±0.25)倍及(1.34±0.15)倍,但3组间差异无统计学意义(P>0.05)。COPD组、戒烟1个月COPD组大鼠肺组织及支气管肺泡灌洗液中NGF mRNA分别是正常对照组的(24.76±5.99)倍、(25.32±5.45)倍及(23.34±3.50)倍、(26.32±7.45)倍,差异有统计学意义(P<0.05)。COPD组与戒烟1个月COPD组大鼠肺组织、支气管肺泡灌洗液NGF mRNA表达无明显差异(P>0.05)。
3 讨 论
目前根据COPD的致伤因素把COPD模型的建立方法分为单一因素诱导、复合因素诱导模型〔5〕。单一因素包括:吸入有毒、有害气体(香烟烟雾、二氧化硫、氯化镉等)〔6〕;气管内注入猪胰弹性蛋白酶、中性粒细胞弹性蛋白酶、木瓜蛋白酶、LPS等化学药物;鼻多次吸入肺炎克雷伯杆菌、肺炎链球菌;基因调控模型〔7〕。复合因素建立在慢性烟雾暴露基础上联合气管内注入蛋白酶或脂多糖〔8〕。关于采用何种动物模型,主要根据临床上常见的诱因、研究目的、动物种属和实验条件决定。吸烟是导致COPD发生发展的最主要环境因素,90%的COPD患者为吸烟者,香烟烟雾中含有一氧化碳、氮氧化物、氨、丙烯醛、对苯二酚、烟碱、氢氰酸等在内的4 500多种化合物。吸入这些有害物质可以使气道纤毛脱落、倒伏、不规则,纤毛运动发生障碍,降低局部清除能力,并直接损伤气道上皮细胞,增加病毒及细菌的感染,引起支气管痉挛,增加气道阻力〔9〕,长期的烟雾刺激还使黏膜下腺体过度增生,杯状细胞分泌过多,加强气道阻塞,大量氧化剂和自由基可以激活巨噬细胞、T细胞(尤其是CD8+T细胞)、中性粒细胞在肺部浸润,激活的这些炎性细胞分泌白细胞介素-1、白细胞介素8、肿瘤坏死因子等多种炎性因子及中性粒细胞蛋白酶、基质金属蛋白酶、α-胰蛋白酶等蛋白酶类从而引起气道、肺实质、肺血管的慢性炎症和肺组织的破坏〔10〕。因此单一烟熏模型更符合COPD的发病过程和病理改变,被动吸烟可以诱导出最真实的COPD〔11〕,因此本实验采用单一烟熏法建立COPD模型。
烟雾暴露的时间要长达数月〔12〕,如6个月或者更长时间可使肺气肿形成越典型,可能是因为肺实质的修复相关的基因在香烟暴露3个月时明显下降,6个月时下调更明显,从而造成肺实质的破坏,形成肺气肿〔9〕,其中以大鼠、小鼠、豚鼠最为常用。有研究显示SD大鼠每天暴露于10支香烟的烟雾中,连续16 w,肺病理显示肺气肿形成,支气管周围及血管周围炎性细胞浸润,可以成功复制COPD模型〔13〕。若每次同时点燃5支香烟,每天暴露4次,每周6 d,连续80 d,肺功能及肺组织病理提示也可以成功建立COPD模型。若采用早晚各1次,每次1 h,1支香烟燃烧约15 min,间隔5 min,再燃烧另1支,每次共燃烧3支香烟的方法,连续36 w,24 w时成功复制肺气肿及气道重塑模型,但肺功能在36 w时才有统计学差异〔14〕。在临床中,即使戒烟,COPD的炎症仍继续发展,肺功能仍在下降,建立戒烟后COPD模型利于对COPD发病机制的探讨〔5〕。因此延长被动吸烟时间、加大烟雾刺激量,采用6个月单纯烟烟熏法建立的COPD模型,即使戒烟,大鼠肺组织HE染色仍证实肺气肿、肺大泡的形成,肺功能证提示气流仍受限,支气管灌洗液中炎性细胞持续浸润,这对研究COPD发生发展的机制提供良好的动物模型。
体内外实验证明NGF介导细胞的存活、增生、分化和活化。NGF在肺组织的结构细胞及炎性细胞有一定的基础量表达,这有助于细胞的存活及生理功能的发挥〔15〕。有研究表明如果肺组织缺乏NGF受体,动物的早期死亡率升高,NGF可能通过上调bcl-2表达及激活核转录因子κB抑制单核细胞、肥大细胞、上皮细胞、B细胞的凋亡〔16〕。本实验结果提示NGF持续参与COPD肺部炎性反应。
本实验观察到香烟刺激的大鼠气管灌洗夜中中性粒细胞、巨噬细胞数目明显增多,这与相关研究相同〔17〕。肺泡巨噬细胞强大的吞噬作用、抗原提呈能力,分泌及调节炎性因子和蛋白酶的功能在COPD发病中起到关键作用〔18〕,在COPD急性发作期,中性粒细胞浸润增多〔19〕。研究表明NGF可以上调单核巨噬细胞表面趋化因子受体4,增强其趋化性。在脂多糖刺激下,单核巨噬细胞高表达NGF和TrkA,并呈浓度、时间依赖性,高表达的NGF通过结合单核细胞表面的TrkA激活ERK1/2及部分c-Jun氨基末端激酶上调肿瘤坏死因子-α表达,而预先用NGF抗体拮抗内源性NGF后,在脂多糖刺激下单核巨噬细胞凋亡明显增多〔20〕。以上研究提示在急性炎症时,NGF介导巨噬细胞的存活并调节功能的发挥。在我们前期研究发现,香烟刺激COPD大鼠肺泡巨噬细胞高表达NGF及其受体〔4〕,增多的NGF与受体TrkA结合是否介导肺泡巨噬细胞、中性粒细胞在肺部的存活及调控细胞功能,从而参与COPD的进程,这需要深入研究。
