酸碱滴定反应的计算及模拟研究
2019-12-30贾明瀚
贾明瀚


摘 要:随着利用质子平衡方程建立了酸碱滴定的数学模型,并借助Visual Basic编程工具设计开发了一个软件对模型进行了求解。该软件可计算酸碱滴定混合溶液任一滴定百分数的pH值,计算酸碱滴定反应的化学计量点及突跃起点、突跃终点的pH值,并可为反应选择合适的指示剂,并计算酸碱滴定的滴定误差,软件还可绘制酸碱滴定曲线用以模拟酸碱滴定反应进程中溶液的pH值变化。
关键词:酸碱滴定;计算机模拟;滴定曲线;Visual Basic
中图分类号:O655.22-4 文献标识码:A 文章编号:1671-2064(2019)21-0239-04
1 研究背景
酸碱滴定分析是化学分析的一个重要类型,是分析化学教学的重点与难点,在常量滴定分析中应用很广,但酸碱滴定分析特别是多元酸碱的滴定分析由于概念多,公式推导繁琐,计算量大,学生学习中往往感到理解困难,很多计算需要简化才能进行。查阅已有文献,王进平[1]等人根据林邦副反应思想,用Origin软件绘制酸碱滴定曲线,但这对学生的Origin软件掌握水平要求较高,且应用过程中需要设置函数操作,比较复杂;孙晓波[2]与赵鑫[3]等人分别设计了酸碱滴定曲线的绘制软件,但软件没有指示剂的选择及滴定误差的计算等功能;CurTiPot软件可计算各种溶液体系pH值,并可模拟绘制滴定曲线,但软件操作比较复杂,需对软件进行系统的学习才可以掌握。
2 酸碱滴定过程的数学模型
对于某一混合酸碱体系,若溶液中n元弱酸HnA的浓度为,m元弱碱B(OH)m的浓度为,此外溶液中还有amol·l-1的一元强酸和bmol·l-1的一元强碱,选用H2O、HnA、B(OH)m作为基准物质,根据质子平衡理论,可写出平衡方程式:
3 酸碱滴定软件的开发
3.1 程序界面及功能设计
程序由主界面和滴定曲线绘制界面构成。程序主界面分为三块:输入区域,操作区域,计算结果显示区域,分别由三个Frame框架控件来对三个功能区的控件分隔开,程序主界面如图1所示。“输入区域”用Label控件标示输入的数据的意义,组合框里面的选项代表了不同的酸碱类型,可供用户选择,文本框响应用户输入的数据;“操作区域”有三个命令按钮组成,点击可弹出一个文本输入框,提示输入对应的滴定分数T,此时可在计算结果显示区域输出相对应的pH值。点击按钮,可进入滴定曲線绘制界面。滴定曲线绘制界面里用图片框显示所生成的滴定曲线,单击则程序可在“计算结果”框中显示出化学计量点、突跃起点和终点,并显示出可参考的指示剂及滴定终点误差。单击按钮,则程序提示输入滴定分数的下限、上限和刻度,即可在图片框中生成滴定曲线图,并用红色表示滴定突跃范围,横坐标轴为滴定分数,纵坐标轴为pH。
3.2 软件计算功能的设计
利用VB语言强大的计算和绘图功能,开发了酸碱滴定计算软件,根据酸碱滴定的不同类型,定义了三种情况下pH值和滴定误差的计算子程序,即强强型(强碱滴定强酸或强酸滴定强碱)、强弱型(强碱滴定弱酸或强酸滴定弱碱)、弱强型(弱酸滴定强碱或弱碱滴定弱酸),软件对pH值的计算主要是通过二分法求解质子平衡方程,计算对应的滴定分数时酸碱混合溶液的pH值,滴定曲线的绘制主要采用line函数,circle函数,指示剂的变色点和颜色变化主要通过软件所建立的数组予以保存,软件通过计算出化学计量点的pH值,由此寻找数组中和计量点pH值最接近的变色点,由此找出合适的指示剂。滴定误差主要通过式(4)和式(5)进行计算。强弱型酸碱滴定pH计算子程序代码如下。
Public Sub phjisuanqr(ct0!,cbt0!,t!,dd!,pk2!(),n2%,ph!)强弱型滴定pH值计算子程序,ct0为滴定剂浓度,cbt0为被滴定物质浓度,t为滴定分数,dd指示滴定剂酸碱性,pk2()为被滴定物质的逐级解离平衡常数,n2表示被滴定物质为n元弱酸或n元弱碱,ph返回计算的溶液的ph值。
4 计算实例
4.1 一元强碱滴定一元弱酸
0.1000mol·L-1 NaOH滴定0.1000mol·L-1 HAc溶液,计算化学计量点的pH值及滴定突跃范围并选择合适的指示剂,画出滴定曲线。
运行软件,选择滴定剂为“一元强碱”,被滴定物质为“一元弱酸”,分别输入相对应的浓度及HAc的解离平衡常数,其pKa值为4.75,则软件运算结果及绘制的滴定曲线如图2所示。从图2可以看出,化学计量点时溶液pH值为8.724,突跃起点的pH值为7.745,突跃终点的pH值为9.704,软件推荐的合适指示剂为百里酚蓝,其滴定误差为0.0088%,指示剂的颜色变化为黄色变蓝色。
4.2 一元强碱滴定三元弱酸
0.1000mol·L-1 NaOH滴定0.1000mol·L-1 H3PO4溶液,计算各化学计量点的pH值及滴定突跃范围并选择合适的指示剂,画出滴定曲线。
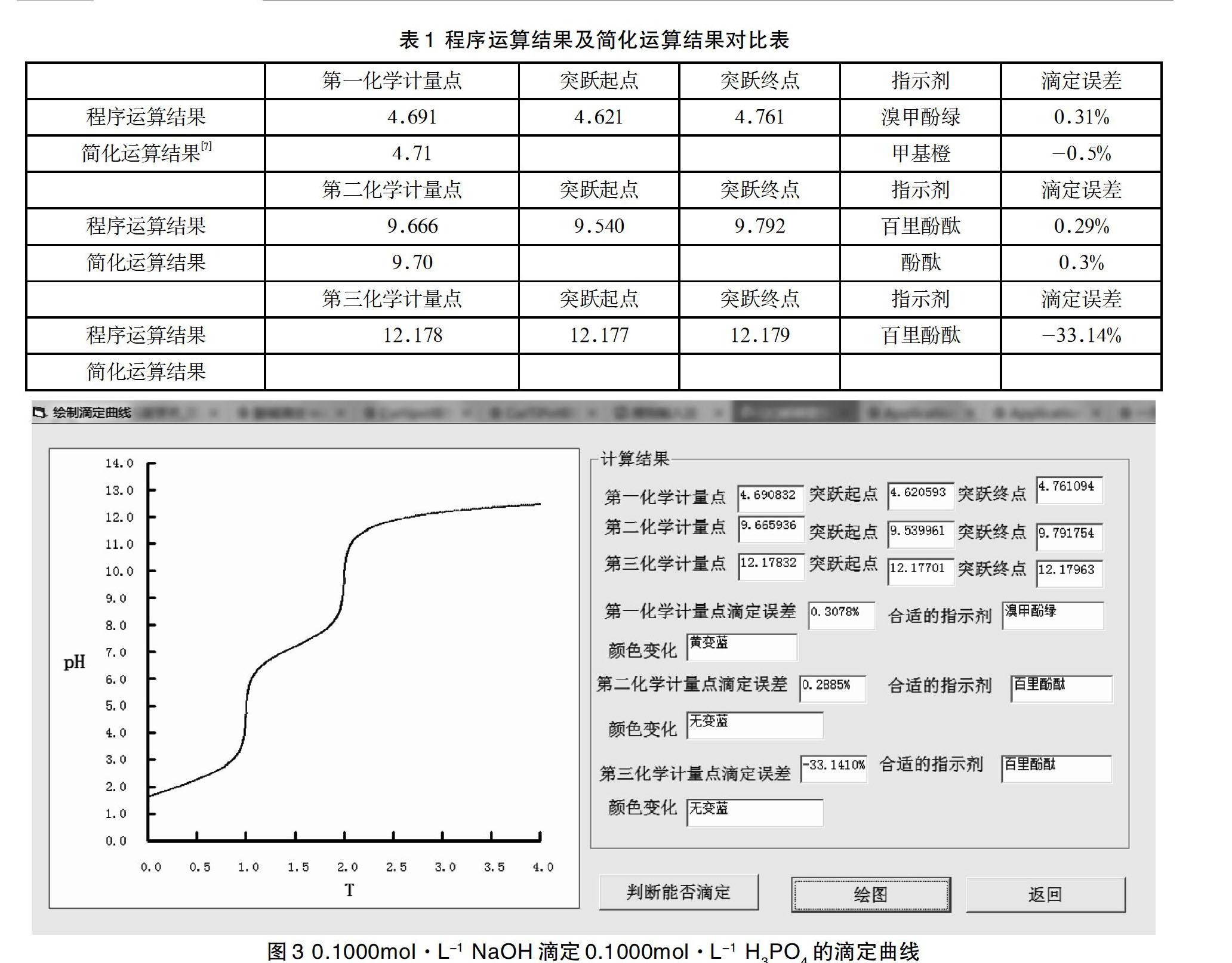
运行软件,选择滴定剂为“一元强碱”,被滴定物质为“三元弱酸”,分别输入相对应的浓度及H3PO4的各级解离平衡常数,其pK1,pK2,pK3值分别为2.12,7.2,12.36,则程序运算结果如表1所示。
从表1可以看出,程序运算结果和简化运算结果数值接近,但程序运算结果可提供更多的信息,如第三化学计量点当选择指示剂为百里酚酞时,滴定误差为-33.14%,可知采用第三化学计量点作为滴定终点不可行。程序绘制的滴定曲线如图3所示。
5 研究结论
本文利用质子平衡方程建立了酸碱滴定时酸碱混合溶液的pH值计算模型,并推导了酸碱滴定的滴定误差的计算公式,利用VB可视化语言编程工具开发了酸碱滴定的计算软件,并运用软件计算了两个酸碱滴定反应的实例。所编写的软件界面友好,简便易学,计算准确快速,软件可绘制酸碱滴定曲线用来预测酸碱滴定反应进程中溶液的pH值变化,并为酸碱滴定反应选择合适的指示剂,软件还可计算化学计量点剂、突跃范围、滴定误差等,判断酸碱滴定的可行性,软件可作为酸碱滴定反应研究的计算工具,也可应用于酸碱滴定反应课程的教学中。
参考文献
[1] 王进平,孙晓波.Origin在精确绘制酸碱滴定曲线中的应用[J].大学化学,2014,29(6):29-33.
[2] 孙晓波,李琳,王秀霞,等.滴定分析模型的统一、MATLAB解析及曲线绘制[J].大学化学,2016,31(5):78-84.
[3] 陆晨刚.Curtipot软件在酸碱平衡和酸碱滴定中的应用[J].化学教学,2017(10):92-97.
