基于Sb2S3阳极的钠离子电池性能评价综合实验设计
2019-12-20顾修全
顾修全,家 珊
(中国矿业大学 材料科学与工程学院,江苏 徐州 221116)
0 引 言
20世纪90年代,锂离子电池与钠离子电池并行发展。锂离子电池具有Li+/Li电化学标准电位较低和Li+较小的尺寸,钠离子电池不具备这特点,没有实现商业化。锂与钠同主族,理化性质极其相似。在商业化应用中,锂离子电池的负极材料主要为石墨类的碳,这种碳具有良好的可充电性能和安全性能,但因其比容量(372 mAhg-1)较低,已不能满足实际应用中高容量的要求。同锂离子电池相比,钠离子电池具有以下优点:钠资源地壳储量丰富,分布广泛,而且价格低廉;因其电压平台高,安全性更高[1-2]。在正常的充放电情况下,钠离子在正负极间的嵌入脱出不会破坏电极材料的基本化学结构;从充放电的可逆性来看,钠离子电池反应是一种可逆的反应[3-4]。作为钠离子电池的负极材料金属硫化物因其具备高容量和高度可逆的氧化还原反应近年来得到极大的发展[5]。基于以上,发展大规模的储能应用的金属硫化物型的钠离子电池具有重要的战略意义。锑基的负极材料具有比较高的理论比容量,如Sb(660 mAh/g)、Sb2S3(946 mAh/g)、Sb2O3(1 103 mAh/g)、Sb6O(1 256 mAh/g)等,且Sb的嵌锂电压为0.8 V,在此电压下,能有效地避免锂枝晶出现,从而提高锂离子电池的安全性能[6-7]。本论文以SbCl3为锑源、乙二醇为溶剂,采用溶剂热法和原位氧化聚合法制备Sb2S3,作为金属硫化物的一种,Sb2S3原料来源广、制备工艺简单及制备成本低和高的理论容量等特点,是一种很有潜力的电极材料[8-9]。
鉴于Sb2S3作为钠离子电池负极材料的重要性以及水热法容易开展学生综合性实验等特点,在满足实验室安全性的前提下,本文旨在通过实验室里的Sb2S3的制备过程培养大学生动手能力及创新意识,并巩固课堂所学的钠离子电池相关知识。通过Sb2S3的形貌表征和电化学性能测试,加深学生对SEM、蓝电系统等仪器设备的认识与了解,培养学生的科研意识。
1 实验部分
1.1 主要实验试剂与仪器
(1)试剂。三氯化锑(分析纯),乙二醇(分析纯),硫脲(分析纯),去离子水,无水乙醇(分析纯),羧甲基纤维素钠(CMC),乙炔黑,高氯酸钠电解液(分析纯)。
(2)仪器。磁力搅拌器,扫描电子显微镜,透射电子显微镜,恒温箱,离心机、真空干燥箱,管式炉,精密电子天平。
1.2 实验方法
将0.75 g硫脲溶于60 mL的乙二醇中,磁力搅拌2h。将上述溶液快速倒入SbCl3溶液(0.75 g SbCl3溶于60 mL乙二醇)中,继续磁力搅拌4 h。将反应溶液移到150 mL的反应釜中,在炉子中密封好,180 ℃下加热2 h。反应釜冷却到室温后,通过离心再用无水乙醇和去离子水清洗得到黑色的沉淀,黑色沉淀在80 ℃下真空干燥12 h。所得产品在450 ℃下碳化2 h(Ar2氛围,3 ℃/min加热)[10]。
2 结果与讨论
2.1 SEM和TEM分析
为了进一步考察Sb2S3的形态,对其进行了SEM和TEM形貌分析,如图1所示。水热法合成的Sb2S3材料呈现簇状微米棒结构形态[见图1(a)、(b)],微米棒呈立方体结构,尺寸分布较为均匀。这种簇状的结构可以为电极与电解液提供充足的接触区域,从而提供大量的活性位点,而且Na+的扩散路径也会缩短,这可以为电极材料提供更优的动力学条件。TEM图像表明Sb2S3呈棒状形态,与SEM图像以及之前文献报道的结果一致[11-13]。棒的平均长度约为0.5~2 μm[见图1(e)],直径约为0.3 μm[见图1(f)]。如图1(c)所示,Sb2S3具有清晰的晶格条纹,所以Sb2S3为结晶性较高的单晶材料,其晶面间距约为0.35 nm,与标准的Sb2S3(JCPDS 42-1393)材料的晶面间距一致[15-16]。





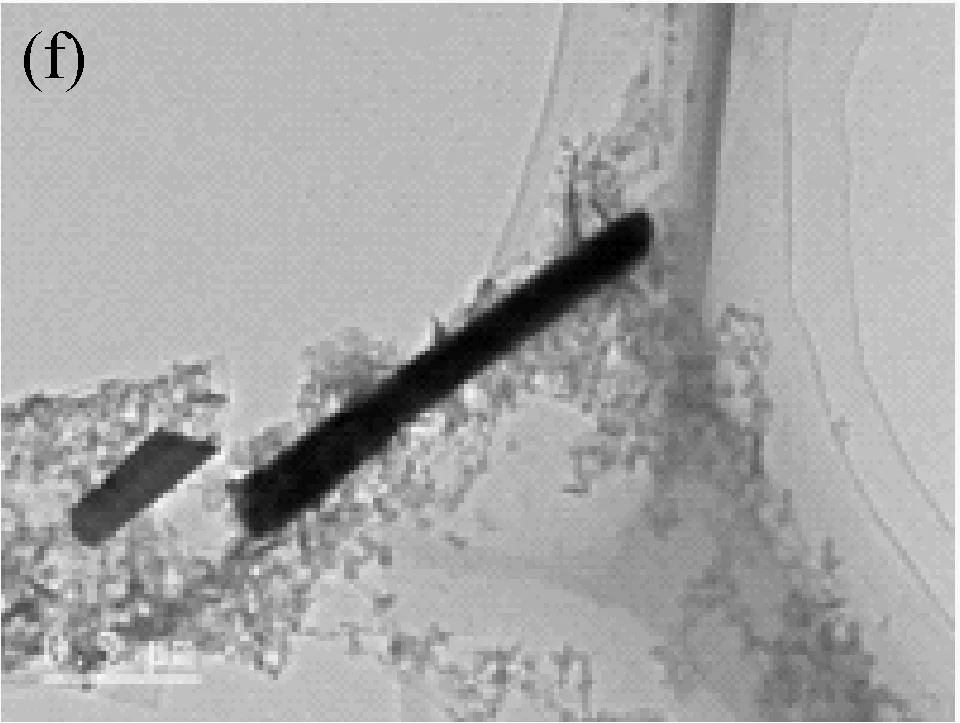
图1 Sb2S3纳米棒的SEM图(a-b),TEM图(c-f)
2.2 Sb2S3电化学性能分析
图2所示为Sb2S3在0.1 A/g的电流密度下的充放电曲线。电池的初始库伦效率为67.19%,容量损失为32.81%。损失的部分可归结为两个方面:① 在首次充放电过程中,电解液和电极材料在固液相界面上反应,形成了一层覆盖在电极材料表面的钝化层,即“固体电解液界面膜”(SEI膜);② Sb2S3表面的电解质发生了分解,这也是容量损失的原因之一。而且,在充放电过程中由于产生巨大的体积膨胀,致使Sb2S3发生粉化而从集流体上脱落,最终导致材料差的循环性能。在充放电电压曲线中,在≈0.87 V处形成了一个电压平台,这与Sb2S3脱锂的过程相关。
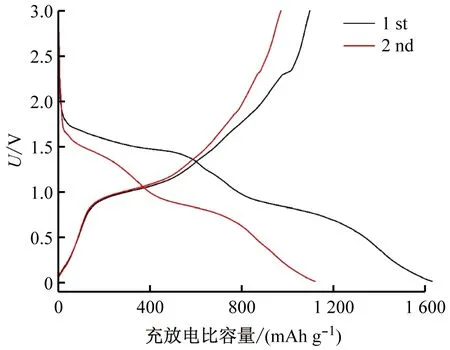
图2 Sb2S3基钠离子电池在0.1 Ag-1的电流密度下的充放电曲线
图3所示为Sb2S3第1~200圈充放电曲线。循环次数为1、10、50、100、150、200时库伦效率分别为69.19%、97.26%、97.27%、99.11%、97.85%、98.77%,放电比容量依次为1 633.2、755.7、345.4、216.5、226.9、269.8 mAh/g,充电比容量依次为1 097.3、735.0、335.9、214.5、222.0 mAh/g。值得注意的是:放电比容量稳定在220 mAh/g后,又有所提升,证明了Sb2S3材料在钠离子电池中有应用的价值。同时由图可知,随着循环圈数的增加,充放电曲线有重合的趋势,侧面反映了电池的容量趋于稳定。
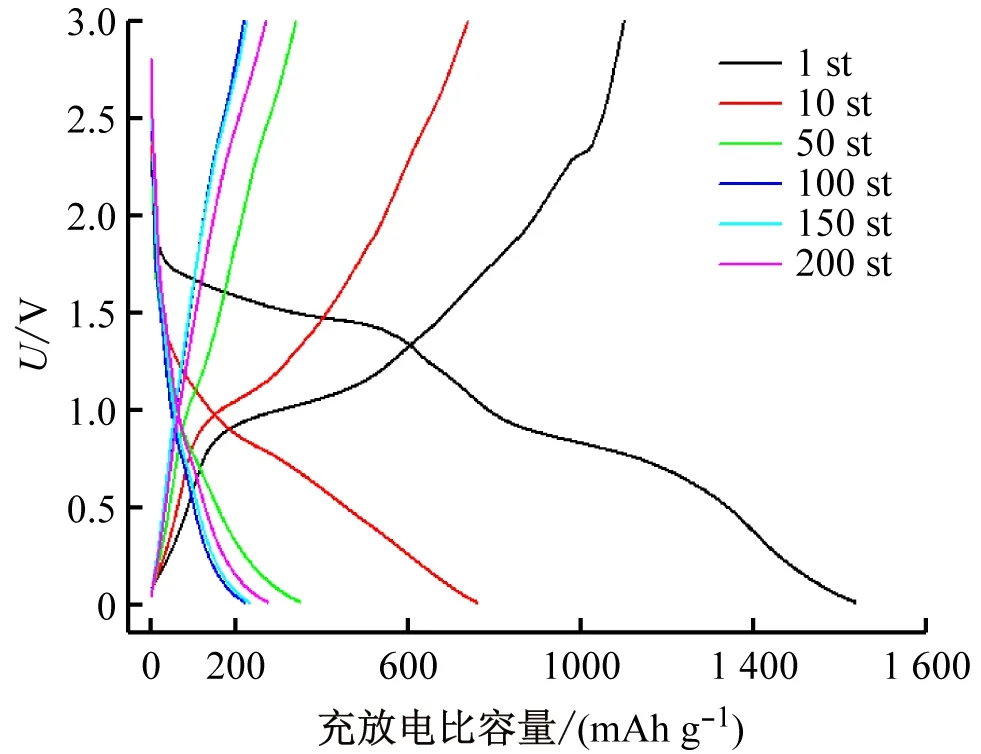
图3 Sb2S3在0.1 Ag-1的电流密度下的第1、10、50、100、150、200圈充放电曲线
图4所示为Sb2S3基钠离子电池在100 mA的电化学循环性能,由图可见,Sb2S3初次循环展示了较高的放电比容量,1 633.2 mAh/g。经过了200圈循环后,电池的比容量稳定在290 mAh/g左右。电池容量相比于初始衰减的原因可能是由于在钠离子脱出与嵌入的过程中局部的体积有较大变化,导致了微观形态内部的结构塌陷,活性物质发生粉化从集流体上脱落,从而容量有较大范围的衰减现象。
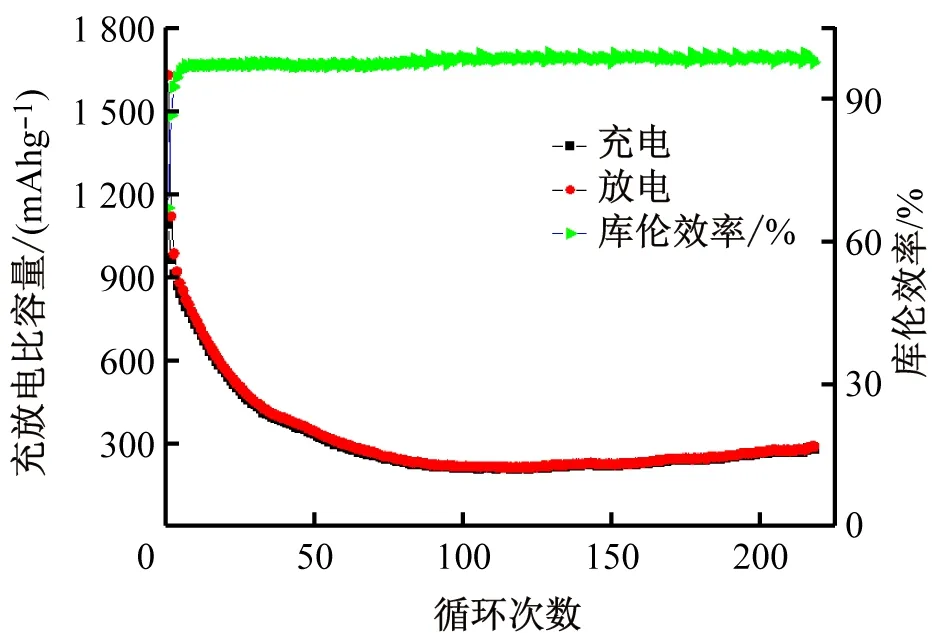
图4 Sb2S3的简单循环曲线
图5所示为Sb2S3基钠离子电池的倍率性能曲线。电流密度为0.1、0.2、0.5、1、2、5 C时,电池的可逆容量分别为413.4、208.5、169.5、101.1、74.7、56.2 mAh/g。当电流密度恢复到0.1 C时,电池的可逆容量可以恢复到252 mAh/g。可见,随着电流密度的上升,电池的比容量下降较大,这是由于在电流密度较高的时候,库伦效率非常接近100%,在放电的过程中由于电位升高而储钠难度增加。值得注意的是,电流密度由2 C增加到5 C时,容量保持率在75.2%,变化范围不大。
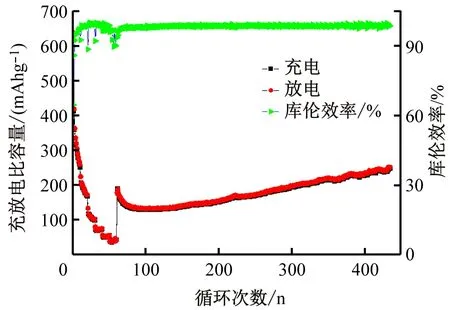
图5 Sb2S3的倍率性能曲线
3 结 语
该实验通过水热法制备Sb2S3粉末,以作为钠离子电池的负极材料。采用了SEM和TEM等测试手段对样品进行了表征分析,并采用电化学测试手段对样品进行了电化学性能分析,得到如下结论:
(1)SEM和TEM分析结果表明:Sb2S3这种材料呈簇状微米棒状结构,且Sb2S3是一种结晶性较高的单晶材料。
(2)电化学测试分析表明:电池的初始库伦效率为67.19%,经过200次循环后,最终容量稳定在290 mAh/g左右。
(3)该实验材料采用水热法制备,流程相对简单,较易操作,可重复性高,易于学生上手掌握。且该实验采用Sb2S3制备钠离子电池,可将理论知识与实际操作相结合。将现代材料分析技术、材料化学以及电化学知识相串联,通过该实验的学习,可使学生巩固理论知识,锻炼动手操作能力和分析讨论的科研能力。
(4)学生在完成规定的实验内容后,对于有兴趣的学生,可以在导师的指导下,自行设计方案进行拓展性研究,从而培养学生的创新能力与创新意识。
