分子筛吸附与微滤耦合工艺去除废水中Cu2+
2019-12-20安卫华余金鹏夏思奇
安卫华 余金鹏 夏思奇 朱 琳
1陕西延长石油榆神能源化工有限责任公司(陕西榆林 719302)2上海绿强新材料有限公司(上海 201806)
采矿、冶炼、电镀、化工等工业领域会产生大量含铜废水,这些废水造成土壤、水源、生物体内的铜超标,对人体和环境产生危害[1,2]。随着国家对环保的重视,国家对高密度开发区的废水排放标准不断提高,其中工业废水中总铜的排放质量浓度由现有的1.0 mg/L降低到0.1 mg/L[3]。因此,开发深度脱除废水中铜的相关技术尤为必要。
目前含铜废水的处理技术主要有絮凝沉淀法、物理化学法、电化学法、生物法、物理吸附等[4]。初级含铜工业废水经加酸加碱沉淀之后,Cu2+可被脱除至1.0~2.0 mg/L,但还需对其进行深度脱除。吸附法因材料便宜易得、成本低、能深度脱除重金属而成为水体重金属污染修复研究的重点。用于处理含铜废水的吸附材料主要有沸石分子筛[5]、粉煤灰[6]、凹凸棒土[7]、离子交换树脂[8]等,其中沸石分子筛是一种多孔结构的硅酸盐矿物,A型[9]、X型[10]等分子筛被广泛应用于重金属的吸附去除。工业上使用的分子筛大多是1~3 mm的分子筛颗粒,用作液相环境的吸附材料时,其颗粒内部传质阻力较大,影响使用效果[11]。然而将分子筛原粉直接用于脱除废水中的重金属时,后续固液分离困难,易形成新的工业污泥,这种工业污泥因重金属离子的富集对环境的二次污染危害性更大[12]。膜过滤技术的发展可有效解决固液分离问题,研究发现[13]膜分离技术在固液分离方面具有巨大优势(操作费用低),特别是陶瓷膜[14],其理化性能稳定,在水处理方面具有广泛应用。
针对目前工业中存在的吸附剂使用效率不高、分子筛原粉使用过程中易产生工业污泥等问题,本研究旨在将分子筛原粉与膜分离技术相结合深度脱除工业废水中的铜。选用13X分子筛为吸附剂,当13X分子筛原粉吸附饱和后,使用微滤技术回收,再生后重复使用,从而实现分子筛的循环使用,降低使用成本。
1 实验与方法
1.1 实验材料及仪器
材料:EDTA-2Na溶液、Cu标准溶液;商用13X分子筛原粉、13X分子筛颗粒、微孔陶瓷管(截留孔径为 0.8μm)。
用X射线衍射仪(XRD)对吸附材料进行表征,结果如图1所示。由图1可知,13X分子筛结晶度良好、无杂峰,微孔陶瓷管由纯晶相的α-Al2O3组成。
仪器:Ultima IV组合型多功能水平X射线衍射仪,日本理学株式会社;TAS-990型原子吸收分光光度计,北京普析通用仪器有限公司。
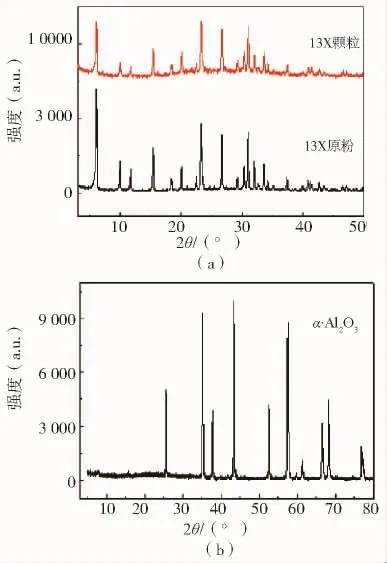
图1 分子筛、陶瓷管的XRD谱图
1.2 静态吸附实验
使用静态吸附实验测定不同材料对Cu2+的吸附性能,选用模拟的低质量浓度(0.1~5.0 mg/L)Cu2+废水溶液,将一定体积废水置于锥形瓶中,加入一定量吸附材料,置于摇床中,转速设定为200 r/min,室温。吸附一段时间后,测定废水中Cu2+的质量浓度。
1.3 耦合工艺装置
实验采用的分子筛吸附与微滤分离耦合工艺装置如图2所示。通过泵,以10~30 mL/min的流速将模拟的低质量浓度(0.1~0.5 mg/L)Cu2+废水打入反应池中,反应池在200 r/min的转速下连续搅拌,出口处接一直径为12 mm、长50 mm的陶瓷管,通过泵将净化的液体打出,流速为10~30 mL/min。为保证处理过程中废液体积与分子筛的用量不变,将含有13X分子筛原粉的悬浮溶液 (0.001~0.100 g/mL)以0.1~1.0 mL/min的流速泵入反应器中,来模拟工业处理时的连续操作工况。
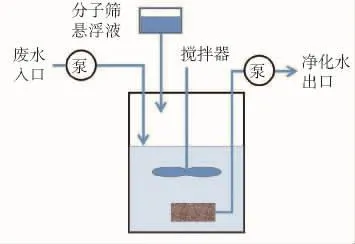
图2 分子筛吸附与微滤耦合工艺
1.4 计算公式
分子筛对重金属离子的吸附容量可依据质量平衡来计算,具体公式见式(1):

其中:q为每单位质量沸石吸附重金属离子的量,mmol/g;V为液体的体积,L;m为干基分子筛的质量,g;c0与cf分别为溶液初始和最终金属离子浓度,mmol/L。
采取Lagergren拟一级动力学模型和拟二级动力学模型描述分子筛的瞬时吸附容量,公式分别见式(2)、式(3)。
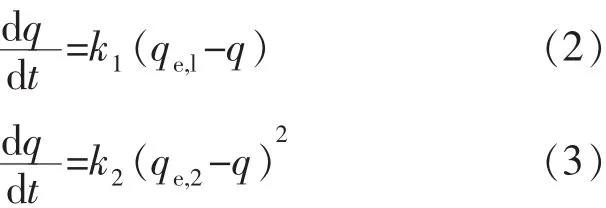
分别对公式(2)、(3)从 t=0、q=0 到 t=t、q=qt,进行积分,得到结果:
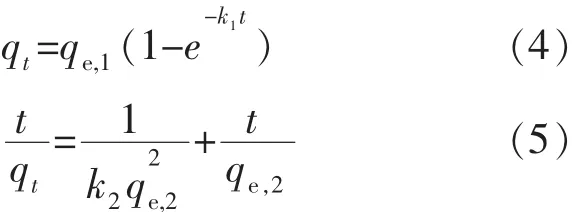
其中:qe,1,qe,2分别为 Lagergren 拟一级动力学模型和拟二级动力学模型的平衡吸附容量,mmol/g;
k1为一阶速率常数,min-1;
k2为二阶速率常数,g/mmol/min。
2 结果与讨论
2.1 分子筛形状对Cu2+的脱除效果
称取13X分子筛原粉、13X颗粒、微孔陶瓷管(α-Al2O3)各 0.2 g,分别置于 1.2 L 废水中(液固比为6000 mL/g),进行重金属吸附实验;废水中Cu2+的初始质量浓度为5.0 mg/L、pH=5~7。结果如图3所示。13X分子筛原粉、13X分子筛颗粒、微孔陶瓷管在120 min时对废水中Cu2+的吸附容量分别为0.445,0.201和0.005 mmol/g,对应的Cu2+脱除率依次为94.3%、43.2%、1.1%。由此可见,13X分子筛原粉对废水中Cu2+的吸附量远大于13X分子筛颗粒;微孔陶瓷管对废水中的Cu2+几乎没有吸附作用。另外,13X分子筛原粉对Cu2+的吸附到达吸附平衡的时间最短,约20 min;而13X分子筛颗粒在120 min时仍未达到吸附平衡。这说明13X分子筛颗粒内部传质阻力大于13X分子筛原粉,影响其吸附效果。
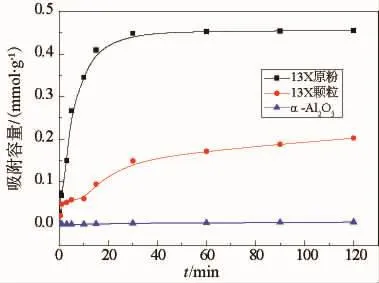
图3 不同吸附材料对Cu2+的脱除效果
综上所述,相对于分子筛颗粒,选用分子筛原粉对废水中的Cu2+进行脱除,可以降低分子筛内部传质阻力,提高分子筛利用率,表现出较高的吸附性能。因此,后续实验中,选择13X分子筛原粉直接应用于重金属的脱除。
2.2 不同Cu2+初始质量浓度对脱除效果的影响
选用液固比为6 000 mL/g,分别将分子筛原粉置于初始质量浓 度为 0.5,1.0,2.0,5.0 mg/L 的含Cu2+废水中,分子筛对不同质量浓度Cu2+废水的脱除效果如图4所示。由图4可知,初始质量浓度由低到高的吸附容量分别为 0.029,0.076,0.163及 0.445 mmol/g,它们的平衡吸附时间分别约为 3,15,15,30 min。由此可见,废水中Cu2+质量浓度越低,分子筛对其吸附达到平衡的时间也就越短,说明在低质量浓度废水中,分子筛原粉能对Cu2+进行快速脱除。
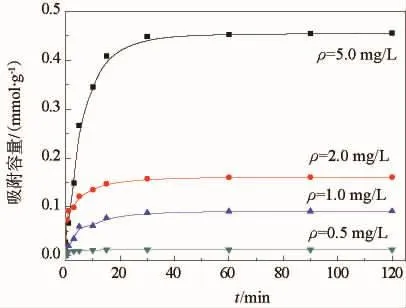
图4 不同Cu2+质量浓度对脱除效果的影响
2.3 不同分子筛用量对Cu2+脱除效果的影响
在绝大多数情况下,提高吸附剂分子筛的用量,可以提高废水中重金属的脱除率[15]。废水中Cu2+初始质量浓度为0.5 mg/L。随着分子筛用量增加(液固比降低),Cu2+脱除率逐步趋近于稳定值1,当液固比小于1000 mL/g时,脱除率增长趋缓。所得结果如表1所示。进一步运用Lagergren拟一级动力学方程和拟二级动力学方程拟合分析不同液固比时吸附容量随时间的变化曲线,结果发现,拟二级动力学模型的相关系数R2比拟一级动力学模型的相关系数更接近于1,即Cu2+在13X分子筛上的吸附符合拟二级动力学模型。这说明13X分子筛吸附重金属过程中的速率控制步骤为化学吸附,即吸附为离子交换的过程[16]。随着分子筛用量增多,分子筛平衡吸附容量逐渐减小,这说明分子筛原粉的离子交换位点未充分使用。但为使重金属脱除率达到95%以上,仍需使用小于1000 mL/g的液固比。
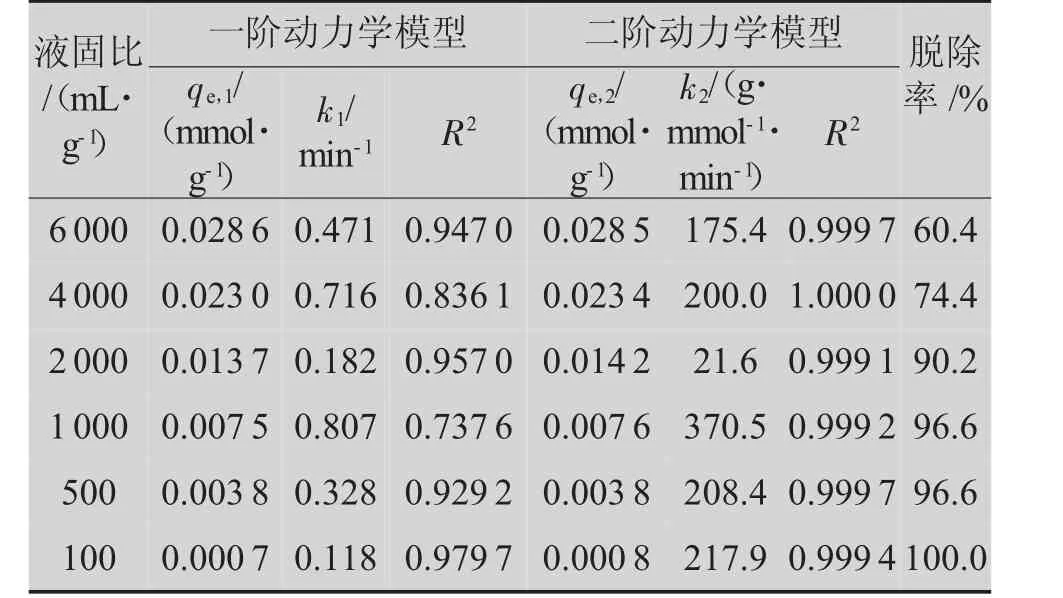
表1 13X分子筛原粉吸附动力学参数
2.4 分子筛吸附与微滤耦合工艺脱除Cu2+
选用0.5 mg/L的Cu2+废水溶液,通过泵以24.5 mL/min的流速将废水打入反应池中;反应池体积为250 mL;分子筛悬浮液泵入速率为0.5 mL/min,其中分子筛固含量为0.05 g/mL,分子筛用量相当于1 g/L(液固比为1 000 mL/g);反应池在200 r/min的转速下连续搅拌,出口处接一直径为12 mm、长50 mm的微孔陶瓷管,通过泵将净化后的液体打出,泵的流速为25 mL/min。模拟工业废水连续处理工况,脱除Cu2+的效果见图5。
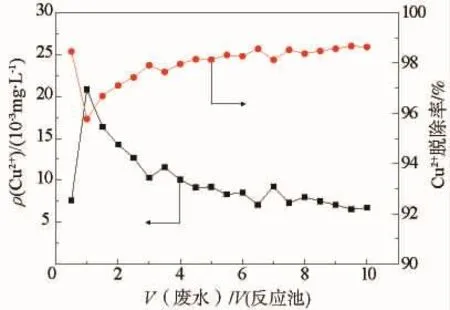
图5 分子筛吸附-微滤耦合工艺脱除Cu2+效果
由图5可知,横坐标为被处理液体体积与容器体积之比,左纵坐标为微孔陶瓷膜出口泵出液体中Cu2+的质量浓度,右纵坐标为低质量浓度废水中Cu2+的脱除率。当被处理废水与反应池体积比为0.5时,Cu2+的脱除率达98.4%;随着废水和分子筛溶液泵入反应器内,Cu2+脱除率呈先减小后增大的趋势,并且随着系统的运行,对Cu2+的处理能力逐渐趋于稳定(脱除率约为98.5%)。整个系统运行过程中,运用分子筛原粉与微滤膜分离组合脱除废水中的Cu2+,脱除率均能达到95.8%以上,出口处Cu2+质量浓度小于0.021 mg/L,远低于特殊排放限值0.1 mg/L。这说明13X分子筛吸附-微滤耦合工艺能对低质量浓度废水中的Cu2+进行深度脱除。
当被处理废水与反应池体积比为10时,停止装置,对反应器内的分子筛原粉进行再生实验。使用0.01 mol/L EDTA-2Na溶液浸泡使用过的分子筛原粉,其中固液比为100 mL/g;以200 r/min的速率室温振荡15 min,微滤膜过滤,30℃干燥2 h后置于450℃马弗炉中处理2 h,冷却后再次投入使用。再生之后的分子筛原粉的脱除率与再生液的洗脱率如表2所示。
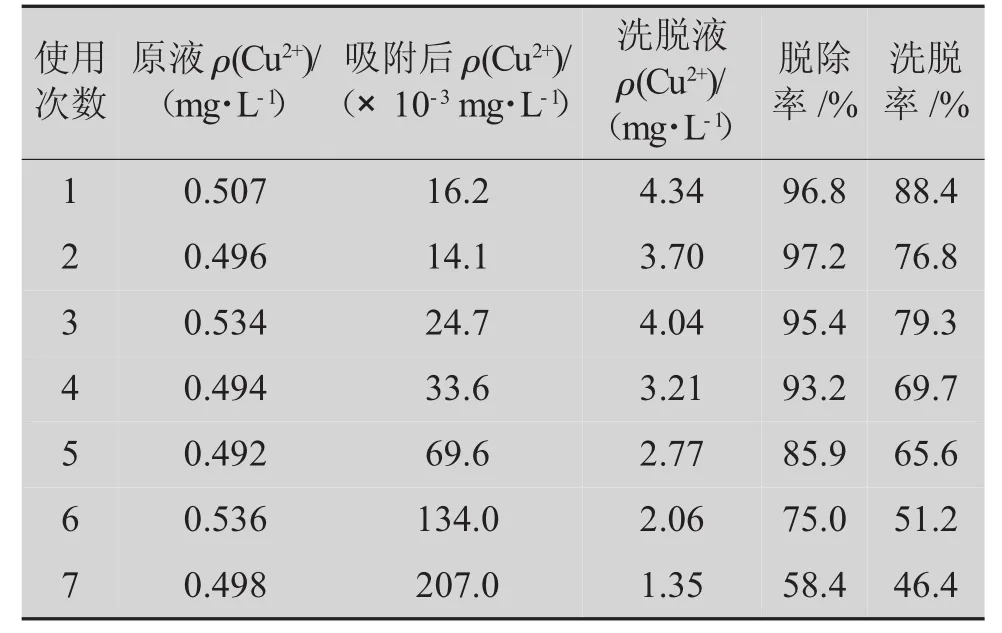
表2 分子筛原粉再生实验结果
由表2可知,随着再生次数的增加,分子筛原粉对Cu2+的脱除能力逐步下降,洗脱率也逐步降低。这可能与分子筛中吸附的Cu2+洗脱不完全有关。13X的晶胞组成为 Na86Al86Si106O384·264H2O,Na+在分子筛结构中主要起平衡骨架结构内部负电荷的作用[17],这部分Na+可与其他二价金属离子进行交换。Cu2+进入分子筛孔道取代Na+,1个Cu2+可取代2个Na+,从而被13X分子筛吸附脱除。当用EDTA-2Na溶液洗脱时,Cu2+需先被Na+交换下来,再被EDTA2-离子螯合,从而被除去。一般来说,13X分子筛与二价金属阳离子的结合力强于一价金属阳离子。因此,13X分子筛骨架中的Cu2+难以洗脱完全[17]。进行5次再生之后的分子筛对废水中的Cu2+同样能达到深度脱除效果。但当再生次数达到6~7次时,分子筛原粉对低质量浓度废水中Cu2+的脱除能力显著下降。建议分子筛重复使用5次后更换新分子筛,或对分子筛进行多次洗脱以恢复其吸附能力。
3 结论
(1)当废水中Cu2+初始质量浓度为5.0 mg/L、吸附时间为120 min时,13X分子筛原粉、13X分子筛颗粒对废水中Cu2+的吸附容量分别为0.445,0.201 mmol/g,对应的 Cu2+脱除率依次为94.3%、43.2%。这说明13X分子筛原粉内部传质阻力小于13X分子筛颗粒,对Cu2+脱除效果较好。
(2)在同一固液比条件下,分别对Cu2+初始质量浓度为 0.5,1.0,2.0,5.0 mg/L 的废水进行脱除,发现废水中Cu2+初始质量浓度越低,13X分子筛原粉达到吸附平衡的时间越短。运用Lagergren动力学方程对13X分子筛原粉吸附Cu2+的过程进行拟合,结果表明13X分子筛吸附Cu2+的控速步骤可能为离子交换过程。
(3)运用分子筛吸附-微滤耦合工艺处理低质量浓度Cu2+废水,脱除率在95.8%以上,能够达到深度净化标准。将使用后的分子筛原粉再生,重复使用5次之后,Cu2+脱除率降至85.9%,仍可达到深度净化标准。分子筛吸附-微滤耦合工艺能深度脱除废水中的重金属离子,具有一定的应用前景。
