参茸鹿胎膏有效成分的定性鉴别及含量测定
2019-12-20田旭张红梅周微侯淑丽
田旭,张红梅,周微※,侯淑丽
(1.吉林大学第一医院药学部,长春 130021;2.吉林省医药中等职业学校,长春 130031)
膏方又称膏剂,是中医药的8 种剂型(丸、散、膏、丹、酒、露、汤、锭)之一,它以大规模复方汤剂为基础,经浓缩煎煮后加入蜂蜜或阿胶后制成的一种浓稠的半固体剂型。参茸鹿胎膏为棕褐色块状物,具有轻微的腥味和略带咸味的味道,该药物由人参、当归、川穹、鹿茸、鹿胎、化橘红、附子(制)等45 种中药组成,其主要功能为补虚生精、益肾壮阳的功效,主治经血不足、妇女虚寒。
本组方中的人参为五加科植物人参(Panax ginseng C.A.Mey.)的根茎,主要成分是皂苷类、糖类、挥发油等;当归为伞形科植物当归(Angelica sinensis)的根,主要成分是有机酸、挥发油、糖等;川芎为伞形科植物川芎(Ligusticum chuanxiong Hort.)的根茎,主要含有阿魏酸、川芎嗪等;附子是毛茛科植物乌头(Aconitum carmichaeli Debx.)的子根加工品,主要含有生物碱等,由于含有的乌头碱类生物碱有毒,因此需要进行乌头碱的限量检查[2];化橘红为芸香科植物化州柚(Citrus grandis Tomentosa)或柚〔C.grandis(L.)Osbeek〕的果皮,主要含有机酸、环烯醚萜苷等。本研究通过薄层色谱法定性鉴别制剂中的人参、当归、川芎3 种成分;根据《中国药典》(2015 年版一部)化橘红项下含量测定方法,采用高效液相色谱法测定化橘红中柚皮苷的含量,以柚皮苷作为指标性成分控制参茸鹿胎膏的内在质量,建立参茸鹿胎膏质量控制方法。
1 材料与仪器
1.1 材料与试剂
参茸鹿胎膏、人参、当归、川芎(吉林省天强制药有限公司);参茸鹿胎膏-2、参茸鹿胎膏-3、参茸鹿胎膏-4(委托吉林省天强制药有限公司制备,除分别不含有人参、鹿茸和化橘红外,其他原料和生产工艺与参茸鹿胎膏完全相同);硅藻土(灵寿县汇资矿产品有限公司);柚皮苷标准品、人参皂苷Rg1 标准品、乌头碱标准品(中国药品生物制品检验所);硅胶G(青岛海洋化工厂);三氯甲烷、甲醇、正丁醇、氨水试液、石油醚(分析纯);水为纯化水。
1.2 仪器
Agilent 1200series 高效相色谱仪(美国安捷伦公司);Shimadzmn UV-2450 紫外分光光度计、FA1104 天平(上海精密科学仪器有限公司);RE-52-99 旋转蒸发仪(上海亚荣生化仪器厂);GZX-9140MBE 电热鼓风干燥箱(上海博讯实业有限公司);D ZF-6050 真空干燥箱(上海博讯实业有限公司);
2 方法与结果
2.1 人参成分的鉴定
2.1.1 参茸鹿胎膏供试溶液的制备 取参茸鹿胎膏样品10 g,切碎置于锥形瓶中,加入10 g 硅藻土,混匀、研磨,加入100 mL 甲醇,加热回流过滤30 min,将滤液蒸发干燥,加入30 mL 水溶解残渣后,倒入分液漏斗中,用50 mL 三氯甲烷对残渣进行振摇提取,放置待分层后弃去三氯甲烷溶液,保留水溶液层,用20 mL水饱和的正丁醇提取水溶液3 次,合并提取液,40 mL氨水试液洗涤,除去氨水层,将正丁醇层蒸干,药物残渣用1 mL 甲醇溶解作为供试品溶液。
2.1.2 人参阳性供试夜的制备 取人参0.5g,加入40mL三氯甲烷,加热回流1 h,弃去三氯甲烷液,将药渣中的溶剂挥发干净,然后于残渣中加入0.5 mL水进行搅拌加湿,再于残渣中加入10 mL 水饱和正丁醇溶液,将溶液进行超声处理约30 min,吸取超声处理后的上清溶液,加入3 倍量氨试液,将其振摇均匀,然后将其放置,待分层后,取出上层液并蒸发至干,再于残渣中加入1 mL 甲醇溶液,用甲醇溶液将残留物进行溶解,作为供试品溶液。
2.1.3 人参皂苷Rg1 标准液的制备 取人参皂苷Rg1对照品,于对照品中加入一定量的甲醇溶液,将其制备成每1 mL 含1 mg 的溶液,作为人参皂苷Rg1 标准品溶液。
2.1.4 阴性对照液的制备 取参茸鹿胎膏-2 样品10g,并按照“2.1.1”项下相同的方法制备成阴性对照溶液。
2.1.5 薄层色谱分析 根据薄层色谱法(中国药典2015 年版一部附录ⅥB)试验,吸取上述溶液各5µL,在同一硅胶G 薄层板上点样,用三氯甲烷-乙酸乙酯-甲醇-水(15∶40∶22∶10)放置在 10 ℃以下的下层溶液作为展开剂[1]展开,用10%硫酸乙醇溶液进行喷雾,并在105 ℃加热至斑点显色清晰。在供试品的色谱中,在与对照药材和对照品色谱相对同的位置上,分别显相同颜色的斑点,且斑点清晰,表明阴性对照无干扰,可以定性鉴别为该处方中的人参,结果见图1。
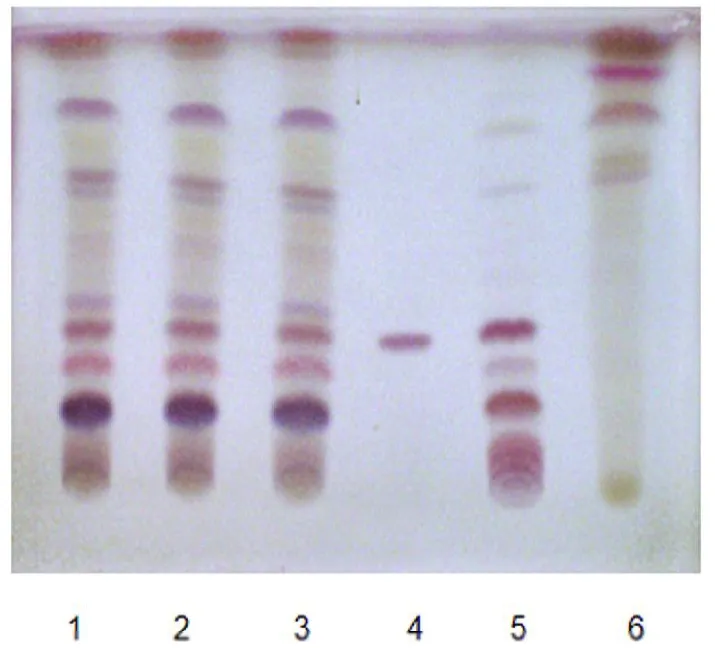
图1 人参薄层色谱图Fig.1 Thin layer chromatogram of P.ginseng
2.2 当归和川芎成分的鉴别
2.2.1 参茸鹿胎膏供试溶液的制备 取参茸鹿胎膏样品10 g,切碎置于锥形瓶中,加入30 mL乙醚浸泡至过夜,将浸泡完全的样品进行超声处理约10 min,超声处理后将其过滤,将滤液进行浓缩,直至浓缩约2 mL,将其作为供试品溶液。
2.2.2 当归、川芎阳性供试液的制备 另外取1 g 当归对照药材以及1g川芎对照药材,加入20mL乙醚浸泡,采用“2.2.1”项下同样的方法制备出对照药材溶液。
2.2.3 阴性对照液的制备 取参茸鹿胎膏-3 样品10g,并按照“2.2.1”项下相同的方法制备成阴性对照溶液。
2.2.4 薄层色谱分析 根据薄层色谱法(中国药典2015 年版一部附录Ⅵ B)试验中提到的方法,吸取上述4 种溶液各2L,置于同一硅胶G薄层板,以展开剂:正己烷-乙酸乙酯(9∶1)展开,在紫外光灯(365 nm)下检视[2-3]。在供试品的色谱中,在与对照药材色谱相同的位置上,显相同颜色的荧光斑点,且斑点清晰,表明阴性对照无干扰,可以用于定性鉴别该处方中的当归和川芎,结果见图2。
2.3 柚皮苷含量测定
2.3.1 供试品溶液制备 取参茸鹿胎膏样品5 块,切碎后混合均匀,精密称量置于锥形瓶中,浸泡过夜后,超声处理约40 min,取出并称定重量,用50%乙醇补足失掉的重量,摇匀同时滤过,取滤液,即制备成供试品溶液。
2.3.2 阳性对照品溶液制备 精密称取柚皮苷对照品适量,加甲醇配制成每1 mL 含70µg 的溶液,振摇均匀即制备成了对照品溶液。
2.3.3 阴性样品溶液制备 取参茸鹿胎膏-4,并按照“2.3.1”项下相同的方法制备成阴性对照溶液。
2.3.4 色谱分析与含量测定 色谱柱:AgilentC18(4.6mm 200 mm,5 µm);流动相:甲醇-0.1%冰醋酸(31∶69);流速:1.0 mL/min;柱温:35 ℃;检测波长:283 nm;理论板数按柚皮苷峰计算应不低于3 000。
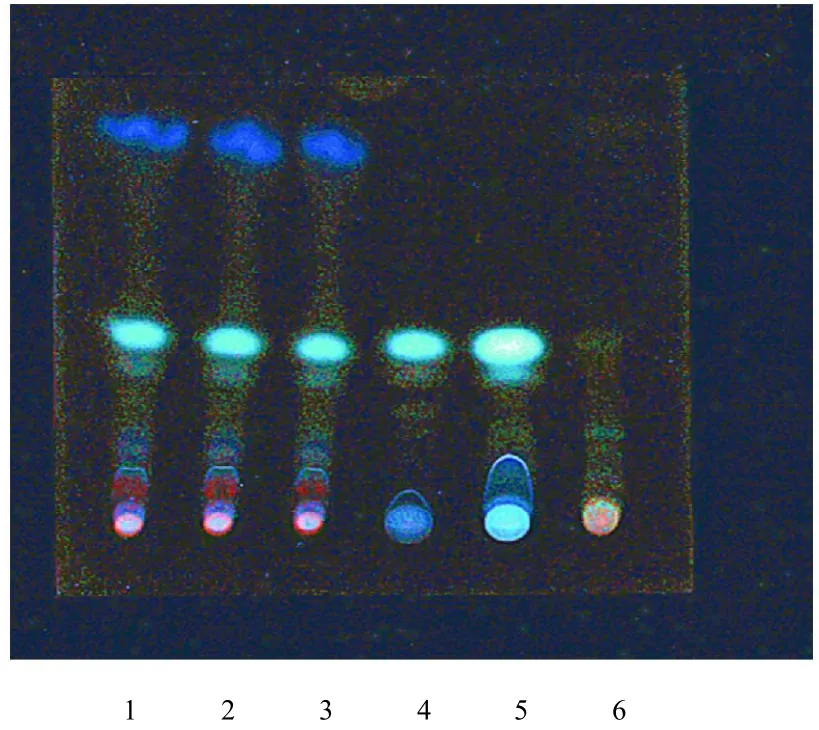
图2 当归和川芎薄层色谱图Fig.2 Thin layer chromatogram of A.sinensis and L.chuanxiong
精密吸取供试品溶液、对照品溶液和阴性对照品溶液各10µL,按“2.3.4”项下色谱条件进样,在对照品色谱图出峰的保留时间位置上,供试品溶液色谱图也出现相应的色谱峰,且阴性对照品色谱图无干扰。结果见图3。

图3 柚皮苷对照品溶液(A)、样品溶液(B)及阴性样品溶液(C)色谱图Fig.3 Chromatograph of naringin reference solution(A),sample solution(B)and negative sample solution(C)
2.3.5 线性关系考察 精密称取适量的柚皮苷对照品,加入甲醇制成0.076 7 mg/mL 的溶液,分别精密吸取 1、2、3、4、5 µL 测定,以对照品进样量为横坐标、峰面积为纵坐标绘制标准曲线,得出回归方程为y= 3.343+2 009.66x(r=0.999 9)。结果表明,柚皮苷在0.1~0.4 mg 呈线性关系。
2.3.6 精密度试验 精密吸取5µL对照品溶液,注入高效液相色谱仪,重复6 次,测定色谱峰面积值,得出RSD 为0.3%,表明该方法精密度良好。
2.3.7 重复性试验 取同一批次样品,按照“2.3.1”项下方法制备供试品溶液,按“2.3.4”项下色谱条件进行6 次独立测定,测得RSD 为1.1%,表明该方法重复性良好。
2.3.8 稳定性试验 取同一批次样品,根据“2.3.5”项下色谱条件分别在 0、2、6、12 和 24 h 进行测定,结果发现峰面积积分值变化的RSD 为1.2%,表明24 h 内供试品溶液中柚皮苷的含量基本稳定。
2.3.9 加样回收率试验 取已知含量的供试品6 份,每份0.50 g 左右,分别精密加入20 mL 对照品溶液(0.009 13 mg/mL,50%乙醇配制),按照“2.3.4”项下色谱条件进样测定,计算回收率(表1),该方法回收率较好、准确度较高。
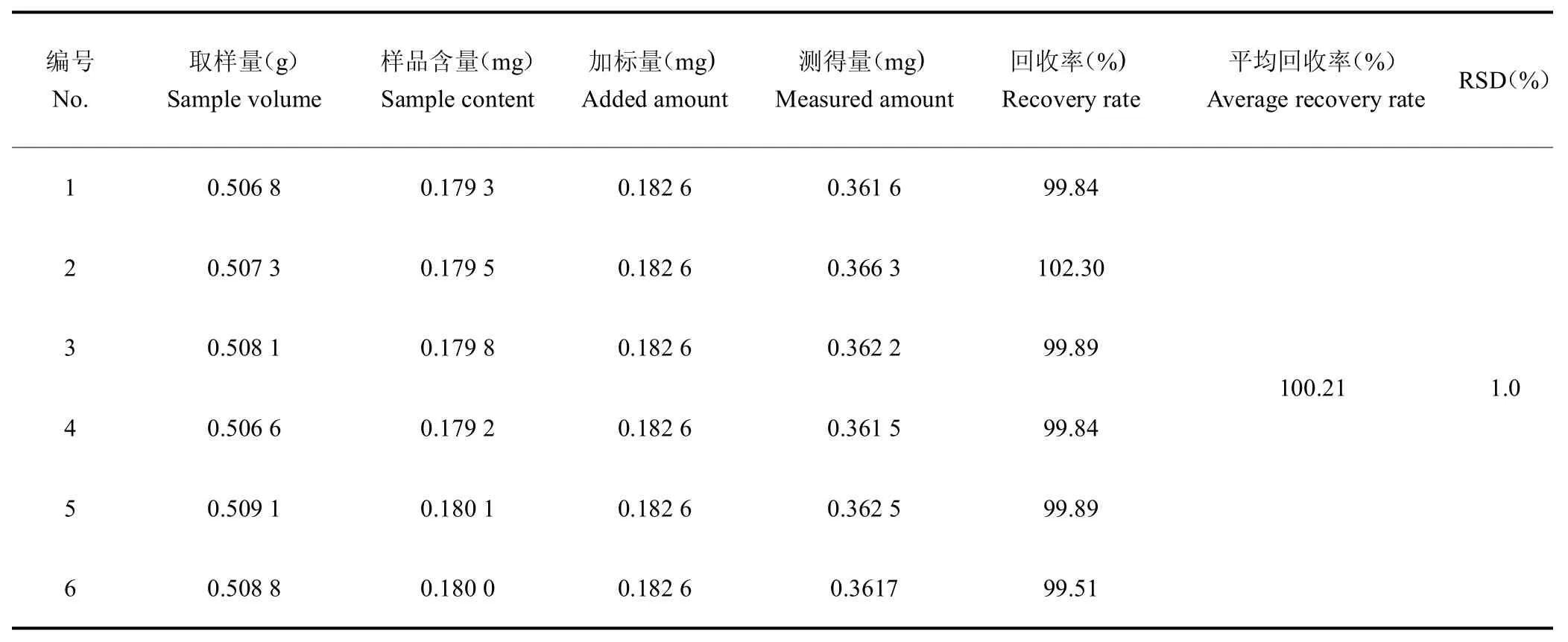
表1 回收率试验Table 1 Recovery rate test
2.3.10 样品含量测定 按照“2.3.1”项下方法及“2.3.4”项下色谱条件,测定3 批样品(171001、171002、171003)所示,结果发现,3 批样品的平均含量分别为1.81、1.82、1.83 mg/丸,该样品含量测定结果表明,根据《中国药典》(2015 年版一部)化橘红的含量测定限度和该处方中化橘红的量,暂定本品每丸含化橘红以柚皮苷(C27H32O14)计,不得少于 1.6 mg。
2.4 乌头碱限量检查
2.4.1 参茸鹿胎膏供试样品的制备 取参茸鹿胎膏样品17 g,切碎置于锥形瓶中,于具塞锥形瓶中加入150 mL 乙醚,将两者进行振摇约10 min,然后加入10 mL氨试液,继续振摇30 min,放置1~2 h,分离醚层,蒸发至干,于残渣中加入1 mL 的无水乙醇,并使之溶解,作为供试品溶液。
2.4.2 乌头碱阳性标准品的制备 取乌头碱标准品,加入一定量的无水乙醇,制成1mg/mL 的溶液作为标准品溶液。
2.4.3 薄层色谱分析 根据薄层色谱法(中国药典2015 年版一部附录ⅥB)试验,取12µL 供试品溶液、5 µL 对照品溶液,分别置于同一硅胶G 薄层板上,以展开剂:甲苯-乙酸乙酯-二乙胺(14∶4∶1)展开[4],用稀碘化铋钾试液喷雾。在供试品色谱中,与对照品色谱相应的位置上未出现斑点。结果见图4。

图4 乌头碱限量薄层色谱图Fig.4 Thin layer chromatogram of aconitine limit
3 结论与讨论
本试验采用高效液相色谱法测定参茸鹿胎膏中柚皮苷的含量,在研究流动相的选择过程中,对多种流动相以及流速进行了考察,曾试用乙腈 0.088%甲酸水溶液(23.3∶76.7)、甲醇 0.2%冰醋酸、甲醇-醋酸-水(30∶4∶70)作为流动相[5-7],但制剂中柚皮苷色谱峰分度较差,最终采用甲醇 0.1%冰醋酸(31∶69)作为本试验流动相,通过对色谱条件的考察及方法学的考察证明,该操作可行,精密度、重复性、稳定性和准确性良好,可以作为本试验的流动相。
综上所述,本试验分别通过薄层色谱鉴别法、限量检查以及高效液相色谱法对参茸鹿胎膏进行定性鉴别和定量分析,为参茸鹿胎膏的质量控制提供了一定参考。
