刺云实胶与黄原胶复配体系质构及流变性研究
2019-12-19牛海佳刘爱国刘立增高晓夏月王鹏程
牛海佳 - 刘爱国 - 刘立增 -高晓夏月 -- 王鹏程 - 强 锋
(1. 天津市食品生物技术重点实验室,天津 300134;2. 天津商业大学生物技术与食品科学学院,天津 300134;3. 天津明哲天翊科技有限公司,天津 300350)
刺云实胶(Tara gum,TG)也称刺云豆胶,是从豆科灌木刺云实的胚乳中提取的一种植物多糖胶,分子结构类似于刺槐豆胶(locust bean gum,LBG)与瓜尔胶(Guar gum,GG),其分子是由β-D-吡喃型甘露糖残基与α-D-吡喃型半乳糖残基以1∶3的数量比通过β-1,6-糖苷键组成的大分子多糖[1-3]。TG的水溶液为假塑性流体,具有良好的热稳定性、化学稳定性和胶体复配性,但单独使用时,硬度大、弹性小,加工性能差,导致应用范围较窄[4]。因此,通常将TG与其他胶体混合,利用协同增效作用,达到更高的稳定性和更好的使用功效,可作为增稠剂、胶凝剂和稳定剂广泛应用于食品工业中[5-7]。
黄原胶(Xanthan gum,XTG)又称黄胶、汉生胶,是由D-葡萄糖、D-甘露糖、D-葡萄糖醛酸、乙酸和丙酮酸组成的“五糖重复单元”的结构聚合体[8]。XTG分子的一级结构由β-1,4键连接的D-葡萄糖基主链及含3个糖单元的侧链组成的双螺旋链,侧链则由两个D-甘露糖和一个D-葡萄糖醛酸的交替连接而成。XTG分子链上有氢键、阴离子、缠结起来的侧链对主链的保护,使其具有高黏度,高耐酸、碱、盐,高耐热稳定性,悬浮性和触变性等[9]。在食品加工中常被用作增稠剂、乳化剂、悬浮剂和稳定剂,也是最广泛应用的一种食品胶体。
研究[10]发现,XTG与半乳甘露聚糖侧链可以相互作用形成热可逆凝胶,凝胶化能力与甘露聚糖侧链的数量和分布以及XTG链的无序程度有关。魏艳霞等[11]发现XTG能与LBG相互作用产生明显的协同作用,在体积比为4∶6时复配胶黏度最大。赵正涛等[12]研究发现XTG与GG存在协效性,在总浓度为0.5%时,XTG与GG比例为9∶1时复配体系具有最大黏度。王元兰等[13]研究发现,在XTG与GG浓度为0.3%、质量比为5∶5时黏度具有最大的协同增效作用。蒋建新等[14]研究表明XTG能与TG共混形成凝胶。Wu等[15]的研究有相同发现,TG与XTG存在明显的协同增效作用,在复配总浓度为0.5%、质量比为6∶4时凝胶强度最大。但均未对TG与XTG复配体系及最佳比例的质构和流变学特性进行系统的研究。
试验拟将TG与XTG按一定比例复配制得总浓度为1%的复合凝胶TG/XTG,通过质构仪、流变仪研究不同质量比的TG与XTG复合凝胶体系的凝胶特性和流变性能,确定TG与XTG最佳复配比例,并研究pH值、Na+和Ca2+对最佳复配体系流变特性的影响,再通过扫描电镜技术,对TG与XTG最佳复配比例进行观察,以期拓宽刺云实胶的应用范围,为TG与XTG在果冻、果酱、软糖等凝胶类新产品开发中的应用提供理论指导。
1 材料与方法
1.1 材料与试剂
刺云实胶:食品级,青岛德慧海洋生物科技有限公司;
黄原胶:食品级,内蒙古阜丰生物科技有限公司;
无水氯化钙、氯化钠:分析纯,天津市化学试剂供销公司第二分公司。
1.2 仪器与设备
流变仪:MCR301型,奥地利安东帕中国有限公司;
质构仪:TA.Xtplus型,英国SMS公司;
数显型顶置式机械搅拌器:RW20型,上海泰坦科技股份有限公司;
恒温水浴锅:HH-4型,常州国华电器有限公司;
扫描电子显微镜:ZEISS型,上海卡尔蔡司管理有限公司;
酸度计:pHS-25型,上海圣科仪器设备有限公司;
冷冻干燥机:Biosafer-10C型,北京博医康实验仪器有限公司;
电子天平:ESJ-S型,沈阳龙腾电子产品有限公司。
1.3 方法
1.3.1 不同比例TG/XTG复配体系的制备 准确的TG与XTG分别按照质量比为0∶10,1∶9,2∶8,3∶7,4∶6,5∶5,6∶4,7∶3,8∶2,9∶1,10∶0复配,称取4 g复配后的混合物缓慢加入396 g预先加热的80 ℃蒸馏水中,配制成浓度为1%的溶液。置于80 ℃恒温水浴锅中,用保鲜膜封口,以150 r/min搅拌3 h,取出,添加80 ℃蒸馏水定容,于室温下静置12 h,使其充分水合。
1.3.2 不同pH值TG/XTG复配体系的制备 准确称取12份总质量为4 g,质量比为6∶4的TG与XTG,分别缓慢加入350 g预先加热的80 ℃蒸馏水中,置于80 ℃恒温水浴锅中,用保鲜膜封口,以150 r/min搅拌3 h,取出。然后用0.1 mol/L的HCl和0.1 mol/L的NaOH调节pH值分别为2,3,4,5,6,7,8,9,10,11,12,将未调节pH的作为对照组。最后添加80 ℃蒸馏水至400 g,于室温下静置12 h,使其充分水合。
1.3.3 不同Na+浓度TG/XTG复配体系的制备 准确称取6份总质量为4 g,质量比为6∶4的TG与XTG,分别缓慢加入396 g不同浓度(0.0%,0.2%,0.4%,0.6%,0.8%,1.0%)的氯化钠溶液中,置于80 ℃恒温水浴锅中,用保鲜膜封口,以150 r/min搅拌3 h,取出,添加80 ℃蒸馏水定容,于室温下静置12 h,使其充分水合。
1.3.4 不同Ca2+浓度TG/XTG复配体系的制备 准确称取6份总质量为4 g,质量比为6∶4的TG与XTG,分别缓慢加入396 g不同浓度(0.0%,0.2%,0.4%,0.6%,0.8%,1.0%)的氯化钙溶液中,置于80 ℃恒温水浴锅中,用保鲜膜封口,以150 r/min搅拌3 h,取出,添加80 ℃蒸馏水定容,于室温下静置12 h,使其充分水合。
1.3.5 凝胶强度测定 将100 g溶胶样品置于100 mL烧杯中,用保鲜膜封口,静置12 h使其形成凝胶,用质构仪测定凝胶强度,选择P/0.5R测试探头,测前速率0.5 mm/s,测试速率与测后速率均为1 mm/s,触发力10 g,压缩距离为10 mm,记录凝胶破裂时的最大力即为凝胶强度。
1.3.6 流变性测定
(1) 静态剪切扫描:采用平板pp50系统,板间距1 mm,剪切速率范围0.01~100.00 s,测量温度25 ℃,观察不同比例TG/XTG复配体系的黏度随剪切速率的变化趋势。
(2) 动态频率剪切扫描:采用平板pp50系统,板间距1 mm,测量温度25 ℃,采用振荡模式进行参数设定,角频率变化范围1~100 rad/s,应变1%(保证在线性黏弹区内),观察在不同频率范围内,不同比例TG/XTG复配体系储能模量(G′)、损耗模量(G″)之间的变化趋势。
(3) 动态温度剪切扫描:采用平板pp50系统,板间距1 mm,测量温度85~25 ℃,采用降温模式,降温速率5 ℃/min,应变1%。观察在不同温度范围内,不同比例TG/XTG复配体系储能模量(G′)、损耗模量(G″)之间的变化趋势。
1.3.7 扫描电子显微镜测试(SEM) 准确称取3份总质量为4 g,质量比为0∶10,10∶0,6∶4的TG与XTG,分别缓慢加入396 g预先加热的80 ℃蒸馏水中,置于80 ℃恒温水浴锅中,用保鲜膜封口,以150 r/min搅拌3 h,取出定容。在培养皿中分装适量溶胶样品,放入-80 ℃冰箱中冷冻6 h,取出,然后进行72 h的冷冻干燥,将干燥好的样品用保鲜袋封装。取少量冷冻干燥好的样品,经过喷金粉后,利用扫描电子显微镜观察其表面微观结构。加速电压3 kV,放大倍数2 000倍。
1.4 数据分析
所有试验均重复3次,每次测试均需更换样品。质构数据使用SPSS 16.0进行统计分析,通过单因素方差分析比较组间数据(P<0.05),最终结果以(平均值±标准差)表示,并利用Origin 9.1做图。
2 结果与分析
2.1 不同比例TG/XTG的复配体系质构分析
在试验中发现单一的TG和XTG没有凝胶化作用。在加热处理时,XTG分子链能够伸展,从无序变为有序,形成具有很多均匀联结点的网络结构,与TG的侧链之间存在明显的协同增效作用[16]。由图1可知,在不同比例的复配凝胶中,随着TG质量的逐渐增加,凝胶强度随之增大,在质量比为6∶4时,凝胶强度最大;在质量比高于6∶4时,凝胶强度又减弱。这一结果与Wu等[15]研究总浓度为0.5%的TG与XTG复配体系结果一致。这是由于在加热条件下,TG中半乳糖支链中含有的羟基和半乳甘露聚糖侧链上没有支链的区域可以与XTG的双螺旋结构通过氢键、静电力作用、空间位阻效应形成稳固的空间网络结构[17-19]。此时,分子之间密度增大,分子链的运动受到阻碍,产生拓扑缠结。在室温下的静置冷却过程中,两者分子形成的网络结构吸收结合水而形成凝胶。
2.2 不同比例TG/XTG复配体系的静态剪切测定
由图2可知,不同比例TG/XTG复配体系的黏度随着剪切速率的增大而逐渐降低,表现出明显的非牛顿流体剪切稀化现象,所有复配体系的流动曲线都符合假塑性流体的特性。单一的黄原胶在低剪切速率下黏度比刺云实胶高出4倍,但在剪切速率较高时,黄原胶黏度下降较快,溶液黏度较刺云实胶低。在不同比例的复配胶中,当刺云实胶质量所占比例高时,溶液黏度较高,但并没有呈现出规律性的变化。在相应的剪切速率下,几乎所有的复配体系的黏度都高于单一胶体的黏度,说明刺云实胶与黄原胶之间存在协同作用,当复配比例在质量比为6∶4时,黏度达到最大值,与凝胶强度的测定结果一致。因此,可以确定,当刺云实胶与黄原胶总浓度为1%时,TG/XTG的最佳复配质量比为6∶4。

图1 不同比例TG/XTG复配体系的凝胶强度
Figure 1 Gel strength of different ratio TG/XTG compound system

图2 不同比例TG/XTG复配体系流动曲线
Figure 2 Flow curve of different ratio TG/XTGcompoundsystem
利用Carreau模型对TG/XTG复配体系的流动曲线进行拟合,Carreau模型方程见式(1)。
(1)
式中:
η——黏度,Pa·s;
η0——零剪切黏度,Pa·s;
η∞——无穷剪切黏度,Pa·s;
γ——剪切速率,s-1;
c——破坏流体结构的时间常数,s;
p——剪切变稀时黏度与剪切速率的关联程度。
通过比较表1的数据可得,在温度为25 ℃条件下,除了10∶0以外,所有TG/XTG复配体系与Carreau模型拟合的拟合度R2都在0.99以上,说明TG/XTG复配体系的流动曲线符合Carreau模型。
表1不同比例TG/XTG复配体系Carreau模型拟合参数

Table 1 Carreau model fitting parameters of different ratio TG/XTG compound system
Carreau模型中,p值可以反映出黏度对剪切速率的依赖程度。当p为0时,样品为牛顿流体,黏度η会随着剪切速率的增大趋于某一固值保持稳定。p值越大,样品非牛顿性越强,反之,非牛顿性弱[19-20]。从表1中可以得出,在所有的复配比例中,p值都不为0,说明TG/XTG复配体系都为非牛顿流体。c值是破坏流体结构的时间常数,其倒数1/c是剪切变稀的临界速率,c值越小,说明破坏结构所需的剪切速率就越大。0∶10的c值在所有复配体系中为最大值,10∶0的c值为最小值,分别为3.479和0.512,说明破坏单一的XTG所需的剪切速率最小,破坏单一的TG所需的剪切速率最大。其余复配比例除1∶9,9∶1以外,c值都保持相对稳定,说明复配体系的稳定性较好,破坏体系结构稳定性的时间相差不大,剪切速率稳定。所有复配体系的η0随着TG所占比例的增大而逐渐上升,在6∶4时达到最大值,然后η0又逐渐降低,也进一步说明所有复配体系中TG与XTG质量比为6∶4时黏度最大。
2.3 不同比例TG/XTG复配体系的频率剪切测定
在流变学研究中,频率扫描是通过对储能模量(G′)、损耗模量(G″)随角频率(ω)或频率(Hz)的变化曲线,其中G′又称为弹性模量,G″又称为黏性模量[21-23]。
在温度为25 ℃的条件下,G′和G″随ω的变化趋势如图3所示。G′和G″随ω增大而上升,在ω为1~100 rad/s时,G′>G″,并且几乎接近平行,复配体系表现

图3 不同比例TG/XTG复配体系的频率扫描图
出弹性的性质,说明复配体系中有弹性凝胶的存在[24]。在低频区,模量随着频率的增大增势缓慢,但在高频区,模量随频率的增大出现急增或骤减的抖动趋势,表明高频率下,可以使复配体系的结构遭到破坏[25]。通过图3中的(a)、(b)图比较得出,TG/XTG复配体系在质量比为6∶4时表现出最大的G′和G″,此时凝胶强度最大。其次是质量比为5∶5,说明TG/XTG复配最佳复配比例为6∶4,其次是5∶5,与凝胶强度测试结果相一致。以上分析可以得出TG和XTG在适当的复配比例时可以促进凝胶的形成。
2.4 不同比例TG/XTG复配体系的温度剪切测定
一个凝胶体系一旦形成,必定会存在一个相转化温度,这个温度即为储能模量(G′)与损耗模量(G″)的交叉点[26]。图4为不同比例的刺云实胶与黄原胶储能模量(G′)与损耗模量(G″)在85~25 ℃温度变化范围内的扫描曲线。在TG/XTG复配比例为9∶1,8∶2,7∶3时存在G″与G′的交叉点,此点为凝胶-溶胶相转化温度,低于此温度时,G′>G″,体系主要以凝胶状态存在,表现出较强的弹性行为;高于此温度时,G′

图4 不同比例TG/XTG复配体系的温度扫描图
Figure 4 Temperaturey scanning of different ratios of TG/XTG compound system
由图4还发现所有复配体系有相同的变化趋势,随着温度的降低G″与G′逐渐增大,且G′的增幅更加显著。可以将G′随温度变化的曲线分为两部分,第一部分是温度为85~45 ℃时,G′增大的速度较慢,是由于在此温度范围内,黄原胶的分子结构发生了从有序到无序的变化,体系的弹性开始缓慢上升;第二部分是温度低于45 ℃时,G′显著增加,可能是此时刺云实胶与黄原胶分子紧密缠绕,水分子虽然在吸收热量后开始运动,但刺云实胶与黄原胶之间的分子缠绕已经不能被已有的热运动所解开,导致凝胶结构急剧收缩,G′迅速增大。
2.5 pH值对最佳TG/XTG复配体系稳定性的影响
图5是不同pH条件下最佳TG/XTG复配体系流动曲线图。从图5可知,酸度对复配体系黏度影响较大,pH为2,3时的黏度明显低于其他pH值条件下的黏度,并且在试验中发现pH为2,3时,复配体系不能形成凝胶,说明在过酸条件下,对复配体系结构破坏较大。普凤仙等[5]的研究发现,pH对TG的黏度几乎没有影响;朱慧等[27]研究发现,在H+浓度过高时,会直接影响XTG分子之间以及与水分子之间的相互作用,使XTG的水化作用增大而直接改变XTG的流变特性。所以,在复配体系中,当pH值较低时,酸度主要是对XTG有影响。当pH值为4时,黏度开始增大,在较高剪切速率下,黏度和对照组(未调pH,pH=7.03±0.20)很接近。pH为5~10时,黏度变化不大并且和对照组几乎重合,说明在此pH条件下最佳复配体系具有良好的稳定性。pH为11,12时,黏度在低剪切速率下较大,但随着剪切速率的增大,黏度又接近于对照组,可能是TG的加入能够加强最佳复配体系的耐碱性。

图5 不同pH条件下最佳TG/XTG复配体系流动曲线
Figure5 Flow curve of optimal TG/XTG compound system under different pH conditions
由表2可知,pH值为5~10时,TG/XTG复配体系流动曲线的R2都在0.98以上,相关性较好,黏度变化较小。但在其他pH条件下,TG/XTG复配体系R2降低。当pH值为2,3时,η0显著降低,可能是强酸性使XTG分子链及形成的氢键出现部分断裂,使得η0显著下降。在偏碱性条件下,复配体系的稳定性要优于偏酸性条件,由此可知,最佳复配体系的耐碱性强于耐酸性。
表2不同pH条件下最佳TG/XTG复配体系Carreau模型拟合参数
Table 2 Fitting parameters of carreau model for optimal TG/XTG compound system under different pH conditions

pHc/spη0/(Pa·s)η∞/(Pa·s)R220.6020.86621.660.0360.945 6230.5750.97636.030.0460.939 2241.0670.984192.610.0000.915 3351.9040.965360.510.0000.981 0961.9190.921322.620.0000.981 9771.9520.894328.380.0000.989 2181.6170.968319.150.0000.987 6891.5420.978329.170.0000.988 57101.3770.953338.190.0000.988 65113.5460.947376.410.0000.967 78126.1390.869525.890.0220.944 82
2.6 盐离子对最佳TG/XTG复配体系稳定性的影响
图6(a)是NaCl浓度在0%~1%范围内最佳复配体系流动曲线图。从图6(a)可以看出,添加Na+的复配体系黏度均低于未添加Na+的,并且TG/XTG复配体系黏度随着Na+浓度的增加而一直呈现下降趋势,说明Na+加入后破坏了复配体系原有的空间结构,使得黏度降低。图6(b)是CaCl2浓度在0%~1%范围内最佳复配体系流动曲线图。可以看出Ca2+的加入对TG/XTG复配体系黏度的影响与Na+有相同的趋势,但是添加Ca2+的复配体系具有更低的黏度,可能是Ca2+比Na+的价态高所导致[26]。有研究[28]发现,XTG体系加入Na+后,由于XTG带负电荷,在Na+浓度逐渐增大时,能够中和XTG侧链上的负电荷,使XTG主侧链更好的交联,分子结构从无序向有序转化。Ca2+中和负电荷的能力更强,此时XTG分子链变柔顺,从而使得XTG与TG结构结合位点减少,结合能力减弱,直接造成体系黏度下降[29]。
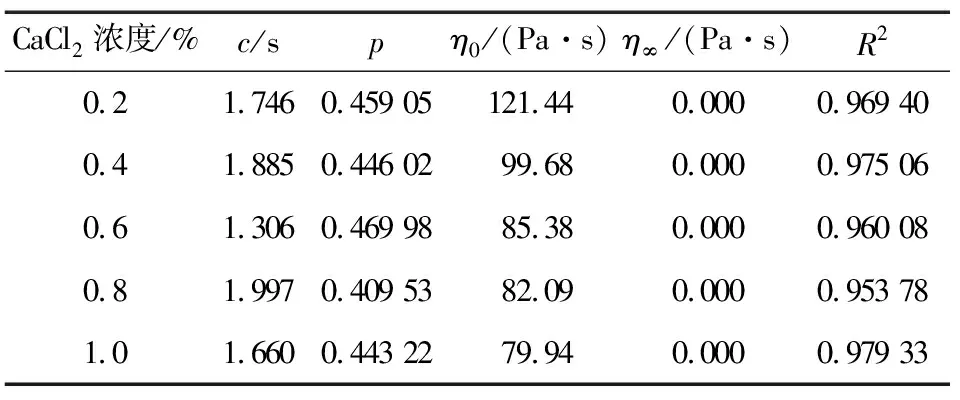
通过不同盐离子浓度对最佳TG/XTG复配体系的流动曲线进行Carreau模型拟合(见表3、4),发现所有的R2都在0.95以上,拟合度较高。在添加Na+后,所有体系的η0(见表3)值随着Na+添加量而逐渐减小。Ca2+添加后,复配体系的η0(见表4)值下降趋势更大,表现出更低的黏度。这也说明高价态的盐离子比低价态的盐离子有更强中和XTG主侧链上负电荷的能力[30],所以,在同浓度添加量下,添加Ca2+的复配体系的黏度低于添加Na+时的黏度。

图6 不同盐离子浓度下最佳TG/XTG复配体系流动曲线
Figure 6 Flow curve of optimal TG/XTG compound system with different salt ion concentration
表3不同NaCl浓度下最佳TG/XTG复配体系Carreau模型拟合参数
Table 3 Fitting parameters of carreau model for optimal TG/XTG compound system with different NaCl concentrations

NaCl浓度/%c/spη0/(Pa·s)η∞/(Pa·s)R20.29.7850.373247.080.0000.970 400.47.1320.393240.530.0000.976 040.65.5320.409192.530.0000.953 340.85.1530.409184.090.0000.983 441.03.9620.426174.240.0000.951 06
表4不同CaCl2浓度下最佳TG/XTG复配体系Carreau模型拟合参数
Table 4 Fitting parameters of carreau model for optimal TG/XTG compound system with different CaCl2concentrations
CaCl2浓度/%c/spη0/(Pa·s)η∞/(Pa·s)R20.21.7460.459 05121.440.0000.969 400.41.8850.446 0299.680.0000.975 060.61.3060.469 9885.380.0000.960 080.81.9970.409 5382.090.0000.953 781.01.6600.443 2279.940.0000.979 33
由以上分析可得,未添加盐离子复配体系的黏度均高于添加了盐离子复配体系的黏度,表明盐离子对TG/XTG复配体系的结构具有破坏作用。
2.7 SEM测定结果分析
图7是XTG、TG及TG/XTG复配体系在质量比为6∶4时的扫描电镜图。从图7(a)中可以看出,单一的XTG表面呈丝绒状、孔径较大、结构疏松。图7(b)中可以看出,单一的TG表面结构不平整,呈立体状,有较大缝隙存在。但图7(c)中TG/XTG复配体系的微观结构发生明显的变化,混合体系表面更加平整、细密;丝片状和凹洞显著减小,观察不到立体状。由此可以表明刺云实胶与黄原胶共混后,在水合的作用下二者分子之间具有良好的交联和相溶作用,形成了稳定的空间网络结构,使得复配体系的凝胶强度、黏弹性大大提高。

(a) XTG (b) TG (c) TG/XTG
图7 XTG、TG及TG/XTG复配体系电镜扫描图
Figure 7 SEM images of XTG TG and TG/XTG compound system
3 结论
采用质构仪和流变仪研究了总浓度为1%时的TG/XTG复配体系的凝胶特性与流变特性,并利用电镜扫描技术分析复配体系网络形成机理。得到以下结论:经质构和流变测定结果表明,在TG/XTG质量比为6∶4时有最大的凝胶强度、最大表观黏度以及最大的动态黏弹性。因此,TG/XTG的最佳复配比例为6∶4。对最佳复配体系稳定性进行研究可知,在pH为5~10时,黏度保持相对稳定。当添加盐离子后,最佳复配体系黏度降低,且在相同添加量下,Ca2+比Na+降低的趋势更为显著。扫描电镜结果表明,在水合的作用下,TG与XTG之间存在明显的协同增效作用,可以形成良好的凝胶网络结构。通过对TG/XTG复配体系质构与流变学特性进行完整、系统的研究,利用二者优良的凝胶可以进一步为TG/XTG在食品、化工、医药等领域的应用和相关产品的质构以及加工性能提供理论依据。在后续的研究中,将对TG/XTG复配体系对具体食品品质的质构、风味及感官等的影响进行研究,以便为TG/XTG在食品中的应用提供更完善的参考。
