氧化石墨烯电催化高效降解有机染料RBk5
2019-11-28周玉莲于永波吴丽颖洪俊明
周玉莲,于永波,黄 湾,吴丽颖,洪俊明,张 倩*
氧化石墨烯电催化高效降解有机染料RBk5
周玉莲1,2,于永波1,2,黄 湾1,2,吴丽颖1,2,洪俊明1,2,张 倩1,2*
(1.华侨大学环境科学与工程系,福建 厦门 361021;2.福建省工业废水生化处理工程技术研究中心,福建 厦门 361021)
电化学高级氧化技术是处理有机染料废水的有效技术方法之一,但其应用受传统贵金属电极成本高、易毒化失活等缺陷的限制.本研究采用廉价易得的石墨粉材料,制备氧化石墨烯(GO)催化剂,用于活性黑5(RBk5)染料废水的电催化氧化降解研究.利用透射电子显微镜、X射线光电子能谱、红外光谱、拉曼光谱、循环伏安法和电化学阻抗谱分析材料的结构特性及电化学性能.结果显示,氧化石墨烯具有较高的电子迁移速率,良好的亲水性和电催化活性.不同的RBk5浓度、外加电流、电解质、初始pH值等条件对RBk5的降解效率也有一定程度的影响.其中,电解质因素对材料性能影响最为显著.在RBk5浓度为10mg/L、外加电流为20mA、反应时间为35min、电解质为NaCl的条件下,电催化降解效率可以达到100%.
氧化石墨烯;电催化氧化;降解染料
随着时代发展,工业印染技术越来越发达,染料的使用也越来越多,导致大量印染废水排放至环境体系中,对环境造成了极大的危害.因此,寻找一种新型、高效的催化降解技术去除废水中的染料类有机污染物迫在眉睫.
近年来,为解决上述污染问题,高级氧化技术方法得到了广泛关注,该方法具有氧化能力强、处理效率高的优点[1].其中电催化氧化技术相较于其他高级氧化技术而言,能有效避免氧化剂或催化剂流失造成的二次环境污染问题(如芬顿法、过硫酸盐氧化法)[2],是一种环境友好型的技术手段.但电催化氧化技术的效率受电极材料影响巨大,传统的贵金属纳米粒子催化剂虽然具有分散性好、活性高、催化性能好的特点[3],但同时也具有价格高昂、易毒化失活等缺点.因此具有大比表面积、高机械强度与柔韧性、强导电能力等特性的碳材料成为替代贵金属电极的最佳材料[5].尤其自2004年二维片层的石墨烯成功制备以来,其兼具的金属材料的特性(消失的费米面)和半导体材料的特性(零能隙)使其在氧化还原反应,析氧反应和析氢反应等电催化领域得到广泛应用[6].现阶段纯度较高的石墨烯材料制备困难、产量低、成本高,但利用化学法合成氧化型石墨烯,制备过程简单且产量较高,因此氧化石墨烯替代石墨烯将大幅度降低材料的制备成本,并且氧化石墨烯表面的氧化基团亦能有效增强材料的亲水特性,使其更易在液相溶液中与污染物接触,进而增加处理效率.
基于这一研究思路,采用改进的Hummers法[5]制备氧化石墨烯做电催化阳极材料,处理活性偶氮染料RBk5染料废水,利用透射电子显微镜、X射线光电子能谱、红外光谱和拉曼光谱等技术手段探究了氧化石墨烯的微观结构特征和表面官能基团,对比氧化石墨烯与还原型石墨烯对于污染物的处理效率,考察了RBk5浓度、初始电流、电解质和初始pH值等因素对降解过程的影响,通过电化学测试分析氧化石墨烯的电化学催化性能,以期为氧化石墨烯作为催化剂电催化处理难降解有机废水提供参考.
1 材料与方法
1.1 材料
石墨粉,购自上海阿拉丁生化科技股份有限公司;H2SO4、NaOH、NaNO3、KMnO4、NaNO2、NaCO3、NaSO4、30%H2O2,分析纯,均购自国药集团化学试剂有限公司;NaCl、HCl,优级纯,均购自国药集团化学试剂有限公司;淬灭用甲醇,分析纯,购自汕头市西陇科学股份有限公司;液相色谱用甲醇,色谱纯,(含量³99.9%),购自Sigma公司.
1.2 氧化石墨烯的制备
采用改进的Hummers法[5]制备氧化石墨烯,制备过程主要有低温、中温、高温3个反应阶段及清洗处理部分.低温阶段:取50mL的浓硫酸到三颈烧瓶,加入1g硝酸钠,在冰浴环境下磁力搅拌直至溶解完全,然后加入1g石墨粉;最后缓慢加入6g高锰酸钾,至全部加入后在冰浴条件下搅拌30min;中温阶段:上述过程之后去掉冰浴,用滴管逐滴加入去离子水,使反应温度保持在35℃~40℃.高温阶段:继续加入去离子水使反应物温度升到95℃,转移到95℃的油浴锅中继续搅拌30min,至溶液变成棕黄色.清洗处理:在反应物中加入100mL的去离子水稀释,加入30wt%的双氧水并持续搅拌,气泡不再产生时终止反应;加入100mL稀盐酸溶液(1:10),充分搅拌后静置;用无水乙醇离心清洗下层沉淀3次;干燥:30℃真空烘箱干燥48h.将得到的产物研磨并收集得到GO.
将上述制备的GO超声1h溶解后放入聚四氟乙烯反应釜中,180℃反应6h后冷却,清洗烘干即得到还原氧化石墨烯(GN).
1.3 实验方法
在室温下,取200mL浓度为10mg/L的RBk5于烧杯中,加入0.2g氯化钠电解质,磁力搅拌至完全溶解.用天平取80mg的GO用导电胶均匀涂布在大小为2.5cm2的洁净的碳布上,干燥.以氧化石墨电极为阳极,阴极为1.0cm的铜片.2个电极之间的距离设为1cm.电解过程中,采用磁搅拌器连续搅拌,外加电流由PS-12阳极极化仪(欧亚中兴技术)控制. 每组设置2个平行样取平均值.
1.4 分析方法
催化剂的表面形貌通过透射电镜(TEM)图像(JEOL-2100F)进行观察;采用ESCALAB250Xi PHI单色Al Ka辐射(1486.6eV)的X射线光电子能谱(XPS,ESCALAB250XiX)分析材料内部键合;利用傅里叶变换红外光谱(FTIR,Thermo Scientific)分析材料表面的官能基团.采用拉曼光谱仪(Raman)分析碳材料表面缺陷;在波长为600nm处采用紫外可见分光光度计检测RBk5;用电化学工作站(CHI660E,晨华)进行峰值电流强度电化学测试.工作电极为自制材料.分别用Ag/AgCl电极和Pt板作为参比电极和对电极.电解液为0.1mol/L的KOH溶液.
染料浓度测定采用TU-1900双光束紫外可见分光光度计,在600nm波长下测定,通过公式:/0=/0计算其降解效率.式中:0为初始RBk5的吸光度值,为时刻RBk5的吸光度值,0为溶液的初始浓度,为溶液时刻的浓度.
2 结果与讨论
2.1 催化剂的表征
2.1.1 透射电子显微镜(TEM)分析 为了解自制氧化石墨烯的微观形态,研究利用透射电镜(TEM)对其进行分析.如图1所示,可以看出制备的GO材料具有明显的片状结构和褶皱缺陷.片层边缘呈透明无序、褶皱的薄纱状.氧化石墨烯在液相中的整体分散性较好,没有大规模的团聚现象,这是由于氧化石墨表面的含氧官能基团的强亲水性造成的[26].
2.1.2 X射线光电子能谱(XPS)分析 研究采用X射线光电子能谱(XPS)分析GO的元素组成及化学价态.在100~700eV的结合能范围分析C、O元素的形态.如图2(a)所示,XPS总谱图中,存在C、O2个特征峰(286.12,531.60eV),通过计算,得到C、O元素的原子含量分别为78.76%、21.24%.C1s谱图如2(b)所示,存在C—C(283.81eV)、C=C(284.8eV)、O—C=O(288.70eV)和C=O(288.02eV)4种形式的特征峰,其中284.8eV处碳sp2特征峰,增大了材料的导电性,提高了氧还原反应(ORR)中电子的传导能力;O1s谱图如2(c)所示,存在C=O(531.10eV)、O—C=O(532.15eV)、O—H(532.20eV)、C—O(532.8eV)和C—OH(534.20eV)5种形式的含氧特征峰,表明石墨在氧化的过程中形成了大量的含氧官能团.GO催化剂表面吸附水中的HO.形成C—OH(534.20eV)键的伸缩振动峰,促进了ORR催化活性[7].丰富的含氧官能团为GO提供了大量的缺陷和活性位点,有利于催化剂性能的提高.

图1 GO的透射电子显微镜
2.1.3 红外光谱(FTIR)分析 利用红外光谱分析材料内部和表面官能团.结果显示(图3),在3435cm-1处的吸收峰归属于GO表面吸附水中O—H键的伸缩振动[8];在1760cm-1处的吸收峰,归属于石墨环骨架中C=O的伸缩振动,表明在氧化过程中,石墨中的C=C键断裂,生成了羧基和羰基[9];在1366cm-1的吸收峰对应于C—OH键的伸缩振动;在1084cm-1处形成的吸收峰则是CO键的伸缩振动,这是由于生成了酚、醇等物质的缘故[27];在400~1000cm-1范围内出现的吸收峰是由于羟基、环氧基和烷氧基团的伸缩振动[24].以上红外数据证明了GO的成功制备,清晰展现出其表面富含的羟基、醚键、环氧键等多种含氧官能团.
2.1.4 拉曼光谱(Raman)分析 为表征材料中碳的晶体缺陷,对GO进行拉曼光谱分析,结果如图4所示,GO和石墨均在1345cm-1(D峰)和1596cm-1(G峰)表现出2个特征峰[10].其中,D峰与石墨烯层缺陷数量(如边缘、非六原子环、杂原子掺杂和功能化)有关,G峰与石墨烯的晶体和石墨结构有关[11].因此,D峰/G峰强度比值(D/G)可以直接反映碳材料的缺陷程度.计算制备的GO与石墨粉和GN的D/G比值,结果显示GO的D/G比值(0.8867)高于GN(0.8746),并且远大于石墨(0.5525),表明GO的缺陷程度比GN高,同时也证明本方法制得GO内部片层规整度良好,且在Raman压片测试过程中仍能保持少层状态,表明GO内部堆积度较低[28].


图3 GO的红外光谱

图4 GO的拉曼光谱
2.1.5 电化学循环伏安法(CV)分析 为了解GO的氧还原活性,对其进行电化学循环伏安分析(CV).图5为GO在100mV/s扫描速率下的循环伏安曲线,如图所示,GO的循环伏安曲线在0~-1.0V之间,有2个明显的氧化还原峰,表明GO含有易发生氧化还原反应的官能团,其主要是因为石墨烯具有良好的电子传递性能和导电能力,可以促进电极表面的电荷转移,使电极反应的灵敏度增高[18].这也是GO电催化氧化催化性能好的原因.
2.1.6 电化学交流阻抗(EIS)分析 电化学交流阻抗是研究电极与电解质界面发生电化学过程的有力工具[21].为研究GO具有良好催化活性的主要原因,对GO进行了电化学交流阻抗分析,以评估材料的电荷传输能力.如图6显示,GO在低频区对应的斜率大,说明表现出良好的双电层电容行为[29].高频区曲线与横坐标轴交点为电极材料的等效串联内阻[22].所制备的GO的为4.03Ω.这主要归因于所制备的GO薄膜中含有大量的亲水含氧官能团,导致GO薄膜的交流电阻较大[22].但是大量的含氧官能团也为GO提供了丰富的缺陷位点,有助于电催化反应的提高.

图5 GO在0.1mol/L KOH和10mg/L的RBk5下的循环伏安曲线

图6 GO的交流阻抗分析
2.2 GO材料处理RBk5溶液
2.2.1 GO电催化性能研究 为研究GO的电催化性能,将其与GN的电催化降解RBk5作比较.如图7(a)所示,在反应时间为35min时,GO电催化降解RBk5(10mg/L)的效率(100%)远大于GN的降解效率(55%);并且如图7(b)所示,在相同条件下GO电催化降解罗丹明B和亚甲基橙染料(10mg/L),去除效率分别为95.7%、91.6%,表明GO对于其他类型的染料而言也具有良好的催化性能.原因是:综合以上FTIR和Raman对GO和GN的结构分析,GO的缺陷程度比GN高,其结构内含有大量的含氧官能团,暴露出丰富的缺陷位点.张倩等[29]采用密度泛函理论(DFT)证明石墨烯边缘羟基和石墨烯平面上的羟基为石墨烯催化作用的主要活性位点.在这些活性位点上,H2O分子很容易发生自发吸附现象.羟基的电子密度高,所以羟基很容易将吸附的 H2O分子转化成活性物质—羟基自由基(HO.),提高了反应活性和反应速率.具有强氧化性的HO.,首先攻击RBk5 的N=N使其脱掉两侧的支链,从而形成短链的化合物.随后HO·不断进攻RBk5的C—S,C—N和C—C等化学键,经过化学键的断裂及脱羧基反应后最终生成H2O和CO2[30].活性物质HO.的生成是石墨烯间接电催化氧化的主要机理.而GN在高温还原的过程中含氧官能团受损,活性位点减少,导致电催化性能下降.

2.2.2 RBk5浓度的影响 在外加电流为20mA,电解质为NaCl(1g/L)、初始pH=4.68的条件下,针对不同初始浓度的RBk5废水进行电催化降解研究.结果如图8(a)所示,35min内不同浓度的RBk5降解效率均达到100%.在15min时,随着RBk5浓度的降低,降解效率随之增加,当浓度从5.0mg/L上升到20.0mg/L时,降解效率从99%下降到50.7%.产生这一现象的原因是,在相同条件下单位时间内电催化GO表面产生的羟基自由基是有限的,RBk5的浓度越高,羟基自由基降解RBk5的速率就越慢.以下研究的因素实验中,RBk5的浓度均选择10mg/L.
2.2.3 外加电流的影响 外加电流是影响降解效率的一个重要操作变量.因此,在RBk5染料浓度为10mg/L,电解质为NaCl (1g/L)、初始pH=4.68的条件下,研究了外加电流对RBk5染料的氧化降解性能的影响,如图8(b)所示.当施加电流从10mA增加到20mA时,在外加电流的作用下,RBk5的降解效率增加.当电流增加到30mA时,RBk5降解效率浓度略有下降.这种下降是由于在过高电流条件下,发生竞争性副反应,在阳极上产生氧气[12](式(1)),而不是羟基自由基(式(2)).此外,在较高的电流下,阳极电极表面上的H2O的氧化可能形成弱氧化剂(如O3) (式(3)),而O3(2.07V)的氧化电位相对于羟基(2.8V) 较低[13-14],造成RBK5降解速率降低.
2H2O→O2+4H++4e-(1)
H2O→HO.+H++e-(2)
H2O→O3+H++e-(3)
2.2.4 电解质的影响 电解液的特性会影响电化学氧化的效率,因为HO.-会与电解过程产生的其他氧化剂发生二次氧化竞争[16].因此,在外加电流为20mA,RBk5的浓度为10mg/L、初始pH=4.68的条件下,研究NaCl、NaCO3、NaSO4及NaNO24种不同的电解质对RBk5降解效果的影响,结果图8(c)示.采用Cl-作为支撑电解质时,RBk5的降解效率达到100%.相比之下,SO42-作为支撑电解质时RBk5降解效率较低(16%).使用Cl-去除RBk5达到较高效率是氯离子氧化所产生的活性氯参与反应造成的(式(4)),.在电催化反应中氯离子受激发产生主要的活性物质—活性氯,活性氯可以快速水解成次氯酸,与氯离子达到平衡状态(式(5~6)),[17].在此条件下,不仅HO.(2.8V)[14]有利于RBk5的降解,HClO(1.61V, 式(7))[19]、O3(2.07V)[14]、H2O2(1.77V)、Cl2(aq)(1.358V)等二次氧化剂也协同参与RBk5的降解.
Cl-→Cl2(aq)+2e-(4)
Cl2(aq)+ H2O→HClO+ H++e-(5)
HClO→ClO-+ H+(6)
HClO+organics→CO2+H2O+HCl (7)
2.2.5 不同的初始pH值对RBk5降解的影响 溶液的初始pH值不仅影响催化剂的表面化学状态和自由基生成过程[20],而且影响水溶液中有机物的吸附和氧化.因此,在外加电流为20mA,RBk5的浓度为10mg/L,氯化钠为电解质(1g/L)的条件下,不同的初始pH值对RBk5降解效率的影响如图8(d)所示.在初始pH=4.68时,降解速率最快,降解效率达到100%;pH=4的酸性条件下的体系对RBk5降解较初始pH=4.68而言反应速率较慢,降解效率也可达到100%;pH=6时,RBk5降解效率为80.14%;相比在pH=8和10的碱性条件下,降解效率为79.55%和68.34%.这是因为RBk5染料表面带负电荷,GO在酸性条件下表面带正电荷,RBk5分子在电荷的相互吸引作用下被吸附到催化剂表面,增加了GO催化剂和RBk5的接触,从而提高了电催化降解的效率.羟基自由基也表现为弱酸性,在中性和碱性条件下与OH-反应生成O-,不利于染料的脱色降解反应.pH值不仅会对电极产生影响,还将决定着羟基自由基的生成,进而影响随后·OH与有机污染物的降解脱色反应效率.
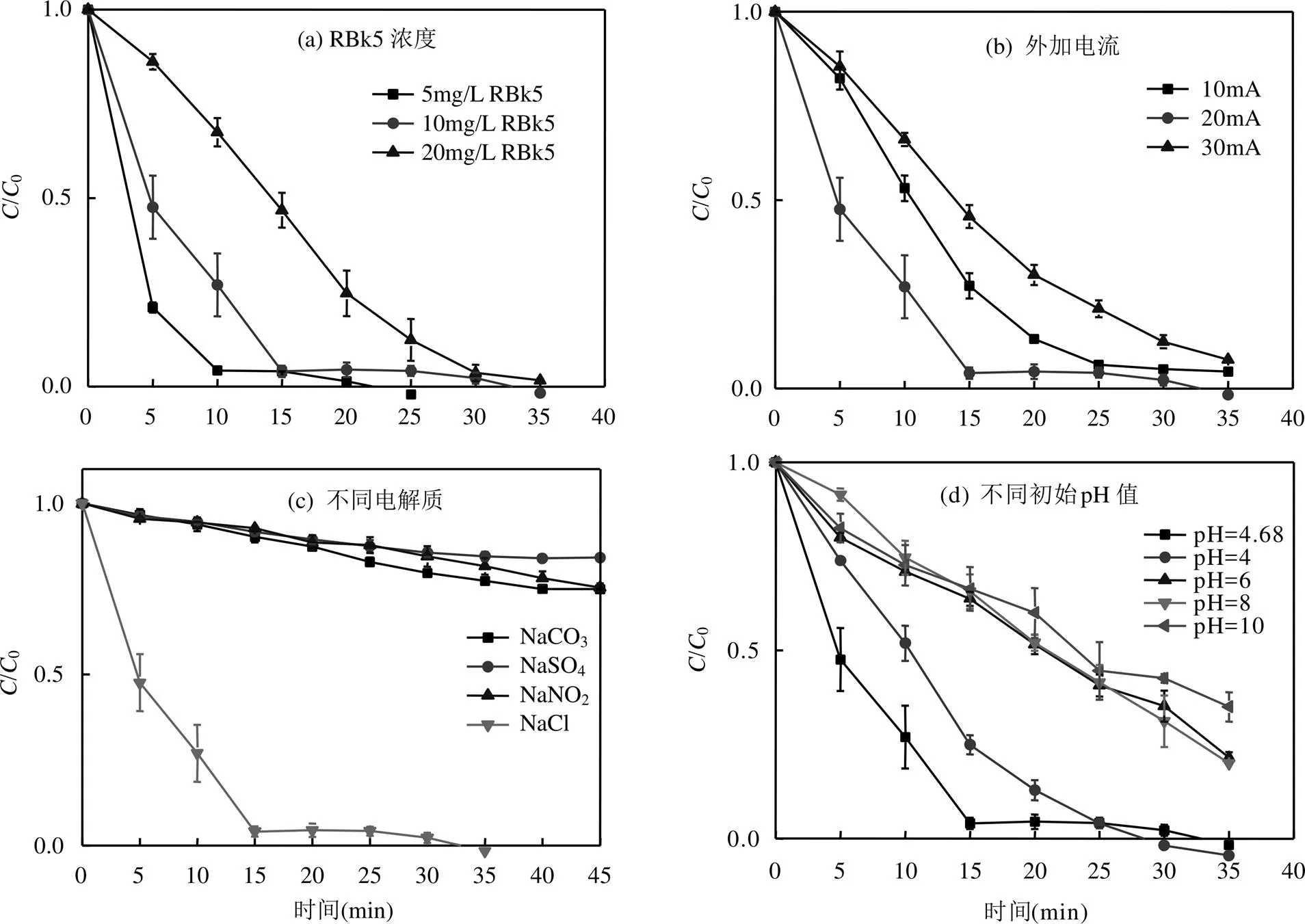
图8 不同初始条件对RBk5降解效率的影响
3 结论
3.1 研究采用水热法成功制备GO催化剂,特性表征结果表明,GO材料的表面缺陷均匀,电化学性能较好,交流阻抗大,材料中的亲水含氧官能团多.GO相较于GN而言,对于电催化技术降解有机物具有明显优势.
3.2 利用GO进行RBK5电催化氧化降解在反应时间为35min,RBk5降解效率可达到100%.
3.3 RBk5初始浓度、外加电流、电解质和初始pH值均对RBk5的降解效率有影响.其中电解质因素对材料的性能影响最大,使用氯化钠电解质,降解效率达到100%;pH值在酸性条件下降解效率好;RBk5浓度及外加电流对材料性能影响较小,具有应用优势.
[1] 董正玉,吴丽颖,王 霁,等.新型Fe3O4@α-MnO2活化过一硫酸盐降解水中偶氮染料[J]. 中国环境科学, 2018,38(8):3003-3010.Dong Z Y, Wu L Y, Wang J, et al. Novel Fe3O4@α-MnO2activated peroxymonosulfate degradation of azo dyes in aqueous solution [J]. China Environmental Science, 2018,38(8):3003-3010.
[2] 吴丽颖,王炳煌,张圆春,等.凝胶球负载零价铁活化过硫酸盐降解偶氮染料废水[J]. 化工进展, 2017,36(6):2318-2324. Wu L Y, Wang B H, Zhang Y C, et al. Degradation of Reactive Black 5(RBK5) by gelatin balls loading iron activating sodium persulfate [J].Chemical Industry and Engineering Progress, 2017,36(6):2318-2324.
[3] 刘 腾,刘 洋,白雪峰.石墨烯负载纳米贵金属催化剂的制备与应用进展[J]. 化学与黏合, 2018,40(6):440-444.Liu T, Liu Y,Bai X F.Progress in Preparation and Application of Graphene Loading Noble Metal Nanocatalyst [J].Chemistry and Adhesion, 2018,40(6):440-444.
[4] 于永波,黄 湾,董正玉,等.N原子杂化石墨烯高效活化过一硫酸盐降解RBk5染料废水[J]. 环境科学, 2019,40(7):1-12. Yu Y B, Huang W, Dong Z Y, et al.Degradation of RBk5 with peroxymonosulfate efficiently activated by N-Doped graphene [J]. Environmental Science, 2019,40(7):1-12.
[5] 吴 波,陈梦唯,吴永亮,等.纳米纤维素/还原氧化石墨烯透明导电薄膜的制备及表征[J/OL]. 林业工程学报, 2019,4(2):106-112. Wu B, Chen M W, Wu Y L, et al. Fabrication and characteristics of cellulose nanofibrils/reduced graphene oxide transparent conductive films [J/OL].Journal of Forestry Engineering, 2019,4(2):106-112.
[6] 刘 腾,刘 洋,白雪峰.石墨烯负载纳米贵金属催化剂的制备与应用进展[J]. 化学与黏合, 2018,40(6):440-444.Liu T, Liu Y,Bai X F. Progress in preparation and application of graphene loading noble metal nanocatalyst [J].Chemistry and Adhesion, 2018,40(6):440-444.
[7] Xiong B, Zhou Y K, Shao Z P, et al. Facile single-step ammonia heat-treatment and quenching process for the synthesis of improved Pt/N-graphene catalysts [J]. Applied Surface Science, 2013,266:433- 439.
[8] Thuy-Duong Nguyen-Phan,Viet Hung Pham,Eun Woo Shin, et al. The role of graphene oxide content on the adsorption-enhanced photocatalysis of titanium dioxide/graphene oxide composites [J]. Chemical Engineering Journal, 2011,170(1):226-232.
[9] Tran Van Khai, Han Gil Na, Dong Sub Kwak, et al. Influence of N-doping on the structural and photoluminescence properties of graphene oxide films [J]. Carbon, 2012,50(10):3799-3806.
[10] Sitansu Sekhar Nanda, Min Jik Kim, Kwi Seok Yeom, et al. A. An, Heongkyu Ju, Dong Kee Yi. Raman spectrum of graphene with its versatile future perspectives [J]. Trends in Analytical Chemistry, 2016,80:125-131.
[11] Ignasi Sirés, Enric Brillas, Mehmet A. et al. Electrochemical advanced oxidation processes: Today and tomorrow. A review [J]. Environmental Science and Pollution Research, 2014,21(14):8336-8367.
[12] Cristina Flox, Pere-Lluís Cabot, Francesc Centellas, et al. Solar photoelectro-Fenton degradation of cresols using a flow reactor with a boron-doped diamond anode [J]. Applied Catalysis B, Environmental, 2007,75(1):17-28.
[13] Neyens E, Baeyens J. A review of classic Fenton's peroxidation as an advanced oxidation technique [J]. Journal of Hazardous Materials, 2003,98(1-3):33-50.
[14] Natija Barhoumi, Lazhar Labiadh, Mehmet A. et al. Electrochemical mineralization of the antibiotic levofloxacin by electro-Fenton-pyrite process [J]. Chemosphere, 2015,141:250-257.
[15] Enric Brillas, Carlos A. Martínez-Huitle. Decontamination of wastewaters containing synthetic organic dyes by electrochemical methods. An updated review [J]. Applied Catalysis B: Environmental, 2015,166-167.
[16] Ignasi Sirés, Enric Brillas. Remediation of water pollution caused by pharmaceutical residues based on electrochemical separation and degradation technologies: A review [J]. Environment International, 2012,40:212-229.
[17] 彭 莹,季露露,汪 娇,等.双酚A在石墨烯修饰电极上的电化学行为[J]. 安徽工业大学学报(自然科学版), 2017,34(4):356-359,378. Peng Y, Ji L L, Wang J, et al. Electrochemical behaviors of bisphenol A on graphene modified electrode [J].J. of Anhui University of Technology (Natural Science), 2017,34(4):356-359,378.
[18] Panizza M, Delucchi M, Sirés I, Electrochemical process for the treatment oflandfill leachate [J]. Appl. Electrochem, 2010,40:1721– 1727.
[19] Liang C J, Wang Z S, Clifford J, et al. Influence of pH on persulfate oxidation of TCE at ambient temperatures [J]. Chemosphere, 2006, 66(1):106-113.
[20] 朱守超,陶华超,杨学林,等.还原氧化石墨烯泡沫的制备及电化学性能研究[J]. 电源技术, 2018,42(10):1529-1532,1539. Zhu S C, Tao H C, Yang X L, et al. Preparation and electrochemical performance of reduced graphene oxide foam [J].Power Technology, 2018,42(10):1529-1532,1539.
[21] 阙龙坤,张 龙,张 勇,等.基于氧化石墨烯与豆渣的复合碳材料制备及性能表征[J]. 功能材料, 2019,50(2):2101-2106+2114. Que L K, Zhang L, Zhang Y, et al. Preparation and characterization of graphene oxide and bean dregs derived for supercapacitors application [J].Functional Materials, 2019,50(2):2101-2106+2114.
[22] Barhoumi N, Labiadh L, Oturan M A, et al. Electrochemical mineralization of the antibiotic levofloxacin by electro-Fentonpyrite process, Chemosphere 2015,141:250–257.
[23] Nguyen-Phan T D, Pham V H, Shin E W, et al. The role of graphene oxide content on the adsorption-enhanced photocatalysis of titanium dioxide/graphene oxide composites [J]. Chemical Engineering Journal, 2011,170(1):226-232.
[24] 李珅珅,苏苗军,刘威华,等.球状多孔Fe-N-C复合催化剂的制备及其氧还原催化性能[J]. 化学研究, 2018,29(4):396-400. Li S S, Su M J, Liu W H. Preparation of spherical porous Fe-N-C composite catalysts andtheir catalytic performance for oxygen reduction [J]. Chemical Research, 2018,29(4):396-400.
[25] Liu R, Wu D, Feng X, et al. Nitrogen-doped ordered mesoporous graphitic arrays with high electrocatalytic activity for oxygen Reduction [J]. Angewandte Chemie, 2010,122(14):2619-2623.
[26] 罗祖云,林 义,张 笛,等.RGO/BaTiO3复合材料的制备与性能研究[J/OL]. 现代化工, 2019,39(5):141-145. Luo Z Y, Lin Y, Zhang D, et al. Preparation of RGO/BaTiO3composites and property study [J/OL].Modern Chemical Industry, 2019,39(5):141-145.
[27] Pei Z, Li L, Sun L, et al. Adsorption characteristics of 1, 2, 4-trichlorobenzene, 2, 4, 6-trichlorophenol, 2-naphthol and naphthalene on graphene and graphene oxide [J]. Carbon, 2013,51:156-163.
[28] Zhang Q, Huang W, Yu Y B, et al. Catalytic performance and mechanism of graphene electrode doped with S and N heteroatoms for-(4-hydroxyphenyl) ethanamide electrochemical degradation [J]. Journal of Hazardous Materials, 2019,368:316-325.
[29] 梁 潇,陶 红,张 倩,等.石墨烯纳米钛管处理染料与扑热息痛的研究[J]. 广州化工, 2015,43(3):97-99. Liang X, Tao H, Zhang Q, et al. Study on the Degradation of the Mixture of Dye and Paracetamol by Graphene Titanium Nanotubes [J].Guangzhou Chemical Industry, 2015,43(3):97-99.
致谢:本实验的实验指导工作由华侨大学化工学院张倩副教授等协助完成,在此表示感谢.
Electrocatalytic degradation of organic dye RBk5by oxide graphene.
ZHOU Yu-lian1,2, YU Yong-bo1,2, HUANG Wan1,2, WU Li-ying1,2, HONG Jun-ming1,2, ZHANG Qian1,2*
(1.Department of Environmental Science and Engineering, Huaqiao University, Xiamen 361021, China;2.Industrial Wastewater Treatment Engineering Research Center of Fujian Provincial, Xiamen 361021, China)., 2019,39(11):4653~4659
Advanced electrochemical oxidation is one technical method for organic dye wastewater treatment, its application is limited by the high cost, easy toxicity and deactivation of noble metal electrode. Therefore, the cheap and easily prepared Graphene oxide (GO) instead of Graphene (GN) was used for the reactive black 5 (RBk5) dye electrocatalytic degradation. The structure and electrochemical properties of the prepared material was analyzed by transmission electron microscopic (TEM), X-ray photoelectron spectroscopy (XPS), Fourier transform infrared (FTIR), Raman spectroscopy, cyclic voltammetry (CV), and electrochemical impedance spectra (EIS). It was indicated that the GO had high electronic transfer rate, excellent hydrophilicity and electrocatalytic activity. Effects of various factors such as different concentration of RBk5, applied current, electrolyte and initial pH were evaluated and investigated. The results showed that the electrolyte had a great influence on the material performance. The removal rate of RBk5could reach 100% under the conditions of RBk5concentration of 10mg/L, applied current of 20mA, reaction time of 35min and NaCl as electrolyte.
graphene oxide;electrocatalytic oxidation;degradation of dyes ferrite
X703.5
A
1000-6923(2019)11-4653-07
周玉莲(1996-),女,广西玉林人,华侨大学硕士研究生,主要从事水污染控制工程研究.发表论文1篇.
2019-04-10
福建省科技计划项目(2019I01010015);厦门科技计划项目(3502Z20173050,3502Z20140057);泉州市科技计划项目(2018Z002);华侨大学研究生科研创新基金资助项目(18013087057)
*责任作者, 副教授, qianzhang@hqu.edu.cn
