温敏性聚(N-异丙基丙烯酰胺)-b-聚(L-谷氨酸)的合成与表征
2019-11-23吴瑕刘大军王琪李荣王薇
吴瑕,刘大军,王琪,李荣,王薇
(长春理工大学 化学与环境工程学院,长春 130022)
如今,癌症已经成为威胁人类健康的严重疾病之一。传统抗癌药物因为是小分子,存在稳定性差、代谢快、缺乏选择性、药物利用率低、毒副作用大等问题。将药物与适当的纳米载体相结合,可以使其更好的发挥作用[1]。纳米载体指能有效负载和传递药物及影像探针的纳米粒子,具有较大的比表面积、表面可功能化的特点[2]。由于实体瘤具有“高渗透和强滞留效应”,纳米载体相比于正常组织更容易聚集在肿瘤组织附近,实现对肿瘤的被动靶向[3]。高分子胶束是一种常见的纳米药物载体,由两亲性分子在一定条件下自组装形成,具有亲水的外壳和疏水的内核,广泛应用于疏水性药物传送[4]。
然而,传统的高分子胶束不具有肿瘤主动靶向功能,无法对外界环境变化做出响应。近年来,具有pH敏感性、温度敏感性、还原响应性等环境刺激响应的胶束作为药物载体已被报道[5-7]。聚(N-异丙基丙烯酰胺)(PNIPAM)是目前研究最广泛的温敏性聚合物之一,它的水溶液在32℃左右发生迅速的可逆相转变[8]。由于和人体生理温度接近,因此被广泛地用于生物医用材料领域。N-异丙基丙烯酰胺(NIPAM)聚合浓度的改变、聚合过程中引入其它聚合物等行为都可能对温敏材料的温敏行为产生影响[9-11]。
选用具有温度敏感的NIPAM单体、通过ATRP法得到聚合物PNIPAM。脱去PNIPAM的叔丁氧羰基保护基得到大分子引发剂,引发γ-苯甲基-L-谷氨酸-N-内羧酸酐单体(BLG-NCA)进行开环聚合,成功得到聚合度不同的嵌段聚合物PNIPAM100-b-PLGA20、PNIPAM60-b-PLGA20。以阿霉素(DOX)为药物模型,制备载药胶束,并在37℃、pH=7.4的磷酸缓冲溶液(PBS)中研究药物的释放行为。结果表明,聚合物胶束具有较高的载药量,约为40%,同时具有较高的包封率,约为60%,DOX的最终释放量高达70%~80%。因此,聚合物载药胶束能高效负载阿霉素,可应用为药物载体。
1 实验
1.1 药品精制及测试条件
所用药品中,四氢呋喃(THF)使用前经Na回流,并蒸馏。N,N-二甲基甲酰胺(DMF)使用前经氢化钙(CaH2)回流,并减压蒸馏。γ-苯甲基-L-谷氨酸-N-内羧酸酐(BLG-NCA)使用前重结晶三次。
傅里叶变换红外光谱(IR)由FTIR-8400s光谱仪测得,用KBr压片法,波数范围为4 000~400 cm-1。核磁共振氢谱(1HNMR)由Bruker AV 500M核磁共振仪测得,以四甲基硅烷(TMS)为内标。凝胶渗透色谱(GPC)采用Waters 5414凝胶色谱仪进行检测,以DMF为流动相。动态光散射(DLS)测试使用WyattQELS仪器,光源为垂直偏正He-Ne激光,有效测试范围为10~1 000 nm,样品浓度为0.05 mg/mL。透射电子显微镜(TEM)通过JEOL JEM-1011透射电镜进行测试,测试电压为100 kV,制备0.1 mg/mL的聚合物水溶液,滴到铜网上,干燥制得透射电镜样品。临界胶束浓度(CMC)用荧光光谱法测定,用Perkin-Elmer FLS-920 Edinburgh荧光光谱仪检测波长393 nm处的激发光谱。DOX累积释放曲线通过Shimadzu UV-2401PC UV-Vis型紫外分光光度计测量。
1.2 新型多功能引发剂的合成
将碳酸氢钠(8.4 g,0.1 mol)与乙醇胺(6.0 g,0.1 mol)溶于THF和水的混合溶液(体积比为1∶2),后将二碳酸二叔丁酯溶解于50 mL THF溶液并使用恒压滴液漏斗使其滴入碳酸氢钠与乙醇胺的混合溶液中。反应在冰浴条件下进行30 min,后室温下反应过夜。过滤,滤液用过量的乙醚萃取后用无水NaSO4干燥,密封过夜。旋转蒸发除去溶剂,得到产物(2-羟基乙基)氨基甲酸叔丁酯(BEA)。
取BEA置于反应瓶中,加入80 mL甲苯130℃回流2 h共沸除水。向反应瓶中加入40 mL THF溶液稀释,加入三乙胺7.6 mL(0.1 mol)。将22.9 g(0.1 mol)溴异丁酰溴溶于10 mL THF溶液,使用恒压滴液漏斗将其滴入反应瓶中。冰浴反应30 min后移到室温下,反应过夜,用G4漏斗过滤,余液用旋转蒸发仪浓缩。浓缩后用乙醚稀释,并用去离子水洗两次、5%的NaHCO3洗一次、5%盐酸溶液洗两次、3.5%的NaCl溶液洗一次,上层有机相用无水Na2SO4干燥过夜,真空抽干。抽干后得到的物质过硅胶柱,得到最终产物2-溴-2-甲基丙酸-2-叔丁氧羰基氨基乙酯(BEA-Br)。
1.3 PNIPAM的合成
以BEA-Br为引发剂,单体NIPAM,三(2-二甲氨基乙基)胺为络合剂(Me6),CuCl为催化剂进行ATRP反应。将BEA-Br(0.031 g,0.1 mmol)、NIPAM(1.132 g,10 mmol)、Me6(53.4 μL)加入到反应瓶中,最后加入4 mL干燥的异丙醇作为反应的溶剂。用液氮使反应液冷冻后抽真空半小时,后通氮气用水解冻,如此重复三次,以便除净反应体系内的氧气。在第三次反应液冻成固体时迅速加入CuCl(0.020 g,0.2 mmol),抽真空40 min,通入氮气用水解冻。待反应液恢复到室温后,将反应瓶置于70℃的油浴中反应6 h后迅速冷却使反应停止。反应液用中性氧化铝层析,以THF为淋洗液,除去铜离子。浓缩后用冷乙醚沉降三次,室温下真空干燥24 h,得到白色固体粉末为最终产物PNIPAM100。用同样的方法制备聚合物PNIPAM60。
1.4 带端位氨基的大分子引发剂(PNIPAM-NH2)的合成
称取0.6 g PNIPAM100溶解于4 mL三氟乙酸(TFA)和二氯甲烷的混合溶液中(体积比为1∶1),室温下反应1 h后用冷乙醚沉降两次,室温下真空干燥24 h,产物为白色固体粉末PNIPAM100-NH2。以同样方法制备聚合物PNIPAM60-NH2。
1.5 聚(N-异丙基丙烯酰胺)-b-聚(L-谷氨酸)(PNIPAM-b-PLGA)的合成
以PNIPAM100-NH2为引发剂,引发BLG-NCA进行开环聚合,得到聚(N-异丙基丙烯酰胺)-b-聚(L-谷氨酸酯)(PNIPAM-b-PBLG),脱去PNIPAM-b-PBLG的苯甲基保护基得到产物PNIPAM-b-PLGA。以聚合物PNIPAM100-b-PLGA20为例。首先称取PNIPAM100-NH2(0.5 g)和20 mL无水甲苯进行共沸除水,弃去甲苯并接冷阱抽干残留的少量甲苯。向反应瓶中加入BLG-NCA(0.4 g)溶解于10 mL DMF中,氮气保护,在室温下反应三天。反应结束后用冷乙醚沉降三次,固体产物在室温下真空干燥24 h,得到白色固体产物PNIPAM100-b-PBLG20。以同样方法制备PNIPAM60-b-PBLG20。
室温下将产物 PNIPAM100-b-PBLG20(0.5 g)溶解在5 ml二氯乙酸(DCA)溶液中,加入1.5 mL氢溴酸/乙酸(HBr/CH3COOH 33 wt%)溶液,反应液在30℃下缓慢搅拌1 h。反应液用过量的丙酮沉降,并用丙酮洗涤多次,沉降物在室温下真空干燥24 h,得到产物PNIPAM100-b-PLGA20。以同样的方法制备聚合物PNIPAM60-b-PLGA20。PNIPAM-b-PLGA的具体合成方案如图1所示。

图1 PNIPAM-b-PLGA的合成方案
1.6 阿霉素(DOX)的负载和释放实验
取一定量的聚合物材料(20 mg)以及DOX(20 mg),均匀分散于pH=7.4的水溶液中,恒温45℃水浴2 h后立即进行超速离心,真空抽干,得到载药胶束。载药胶束的体外释放行为是在37℃、pH=7.4的磷酸缓冲溶液(PBS)中进行的。取载药胶束溶解于2 mL PBS溶液中后,装透析袋(3500Da)密封,放入20 mL PBS溶液中,恒温37℃下进行释放实验。每隔一段时间取2 mL释放介质,并补加2 mL PBS溶液。DOX的释放通过紫外分光光度法(λ=480 nm)进行检测[12]。
2 结果与讨论
2.1 聚合物的核磁共振氢谱分析
图2为PNIPAM与EA-PNIPAM的核磁共振氢谱图,试剂为氘代氯仿。如图2中(a)所示,1.00 ppm(g+c)处的共振峰归属于甲基(-CH3),1.15 ppm(h)处的共振峰归属于端位叔丁氧羰基上的甲基((CH3)3-C-O-)。3.12 ppm(a)与3.98 ppm(b)处的共振峰归属于主链上的亚甲基(CH2-CH2-O-,CH2-CH2-O-)。1.44 ppm(d)与1.79 ppm(e)处的共振峰分别归属于重复单元上的亚甲基(-CH2-CH-)以及次甲基(-CH2-CH-)。3.65 ppm(f)处的共振峰归属于NIPAM重复单元异丙基上的次甲基(-(CH3)2-CH-),证明PNIPAM成功合成。图2(b)中叔丁氧羰基上甲基的共振峰(h)消失,说明叔丁氧羰基成功脱去,得到大分子引发剂EA-PNIPAM。PNIPAM的聚合度由d处与a处的信号峰面积比算得,经计算PNIPAM的聚合度分别为89、46。

图2 PNIPAM(a),EA-PNIPAM(b)的核磁共振氢谱图
图3为聚合物PNIPAM-b-PBLG、PNIPAM-b-PLGA的核磁共振氢谱图,试剂为氘代三氟乙酸。如图3中(a)所示,3.13 ppm(a)与4.12 ppm(b)处的共振峰均归属于主链上的亚甲基(CH2-CH2-O-,CH2-CH2-O-)。1.00 ppm(g+c)处的共振峰归属于甲基(-CH3)。2.25 ppm(d)处的共振峰归属于PNIPAM重复单元上的亚甲基(-CH2-CH-)。3.65 ppm(f)处的共振峰归属于侧链异丙基上的次甲基(-(CH3)2-CH-),1.75 ppm处PBLG结构单元的亚甲基峰(i)(-CH2-CH2C(O)-)与PNIPAM结构单元次甲基峰(e)(-CH2-CH-)重合。4.42 ppm(h)处的共振峰是PBLG中质子的特征峰。2.20 ppm和1.88 ppm(j)处出现的是PBLG侧基的亚甲基的振动峰(-CH2-CH2C(O)-)。4.75 ppm(k)、6.92 ppm(l)处为PBLG结构单元上的亚甲基(-(O)CH2-)以及苯环上的次甲基的振动峰(-C6H5),证明PBLG成功合成。通过峰h与峰b的积分面积可算出PBLG结构单元的聚合度,经计算两组聚合物中PBLG的聚合度分别为16、12。图3(b)中k、l处的共振消失证明了苯甲基保护基的成功脱除,聚合物PNIPAM-b-PLGA成功制备。

图3 PNIPAM-b-PBLG(a),PNIPAM-b-PLGA(b)的核磁共振氢谱图
2.2 聚合物的红外光谱分析

图4 不同聚合物的红外光谱图
如图4(a)PNIPAM的红外光谱图中所示,1 660 cm-1处碳碳双键的伸缩振动峰消失,3 170 cm-1处烯烃的C-H键的伸缩振动峰消失,1 040 cm-1处出现酯键的特征峰,说明NIPAM单体成功聚合。图(4b)PNIPA-b-PLGA的红外光谱图中,3 060 cm-1处苯环上C-H伸缩振动吸收峰消失,1 432 cm-1处出现的峰为羧基上-OH的特征峰,证明苯甲基脱保护成功,得到最终产物PNIPAM-b-PLGA。
2.3 聚合物的凝胶渗透色谱(GPC)分析
用凝胶色谱仪对制备的不同聚合物的分子量及分子量分布进行测试。结果如表1所示,PNIPAM60、PNIPAM100的分子量成比例增加,脱去丁氧羰基保护基后的聚合物EA-PNIPAM60、EA-PNIPAM100分子量降低。引发BLG-NCA开环聚合后PNIPAM60-b-PBLG20、PNIPAM100-b-PBLG20的分子量均出现相应的增长。脱掉聚合物重复单元的苯甲基保护基,分子量降低。测试结果从分子量的角度 证 明 了 PNIPAM60-b-PLGA20、PNIPAM100-b-PLGA20的成功合成。

表1 不同聚合物的分子量及分子量分布指数
2.4 低临界溶解温度(LCST)的测定
PNIPAM聚合物的LCST为32~34℃,聚合物溶液由透明迅速转变至浑浊。此外,聚合物浓度的改变、其他聚合物的引入均会导致其LCST发生变化。使用紫外分光光度法测定λ=500 nm处聚合物溶液透过率的变化确定其LCST值[13]。如图5所示,PNIPAM100-b-PLGA20与PNIPAM60-b-PLGA20在pH=7.4的水溶液中的低临界溶解温度分别为36℃、37℃。碱性条件下聚L-谷氨酸的侧链羧基转化为羧酸盐,在水溶液中的溶解性很好,并且随着温度的升高其溶解度增大,由于亲水链段PLGA的引入,导致聚合物的LCST升高。

图5 λ=500 nm下聚合物溶液的透过率随温度变化曲线
2.5 聚合物胶束
以疏水性的芘为荧光探针测试聚合物的临界胶束浓度(CMC)并讨论聚合物的组成对胶束性能的影响[14]。聚合物CMC测试表明,PNIPAM100-b-PLGA20与PNIPAM60-b-PLGA20在温度低于LCST、pH=7.4的水溶液中芘的荧光强度没有出现红移即不成胶束。但当温度高于LCST时,如图6所示,芘的荧光强度会出现从334.69 nm到336.28 nm的红移,形成以疏水性的PNIPAM为核,亲水性的PLGA为壳的胶束。以聚合物荧光强度之比(I336.28/I334.69)为纵坐标,样品浓度值的对数(lg c)为横坐标作图,图中水平线与切线的交点为CMC值(图7)。PNIPAM100-b-PLGA20与PNIPAM60-b-PLGA20的CMC值主要受到链段PNIPAM的影响。当温度升高时,PNIPAM发生由亲水到疏水的转变,疏水链段比例的增加,聚合物的CMC降低。因此PNIPAM100-b-PLGA20的CMC值(3.715×10-3g/L-1)低于PNIPAM60-b-PLGA20的CMC值(13.81×10-3g/L-1)。

图6 温度高于LCST时,相同浓度的芘在不同浓度的PNIPAM100-b-PLGA20溶液中的激发光谱(λ=393 nm)
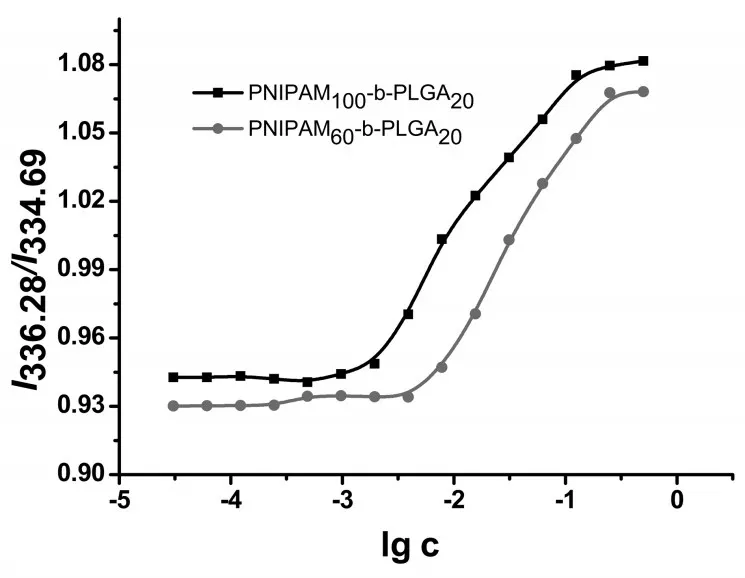
图7 聚合物激发光谱强度之比(I336.28/I334.69)对lg c的曲线
图8是聚合物胶束在pH=7.4、45℃的水溶液中的流体力学半径(Rh)以及透射电镜图(TEM)。PNIPAM60-b-PLGA20胶束的Rh值为(96.7±7.6)nm(图8(a)),PNIPAM100-b-PLGA20胶束的Rh值为(78.4±2.1)nm(图8(c))。TEM结果表明两组聚合物纳米胶束均呈球形,形状较为规则,PNIPAM60-b-PLGA20胶束的粒径为58 nm(图8(b))、PNIPAM100-b-PLGA20胶束的粒径为44 nm(图8(d))。由TEM所测得的粒径低于由DLS所测得的粒径,这主要是由于在TEM测试中,高能电压的强烈作用使胶束粒子明显收缩[15]。PNIPAM100-b-PLGA20胶束的Rh值低于PNIPAM60-b-PLGA20胶束的Rh值,这是由于温度高于LCST时,PNIPAM发生由亲水向疏水性转变,疏水段的比例高导致疏水段相互作用增强。综上,聚合物的组成对Rh值有影响。
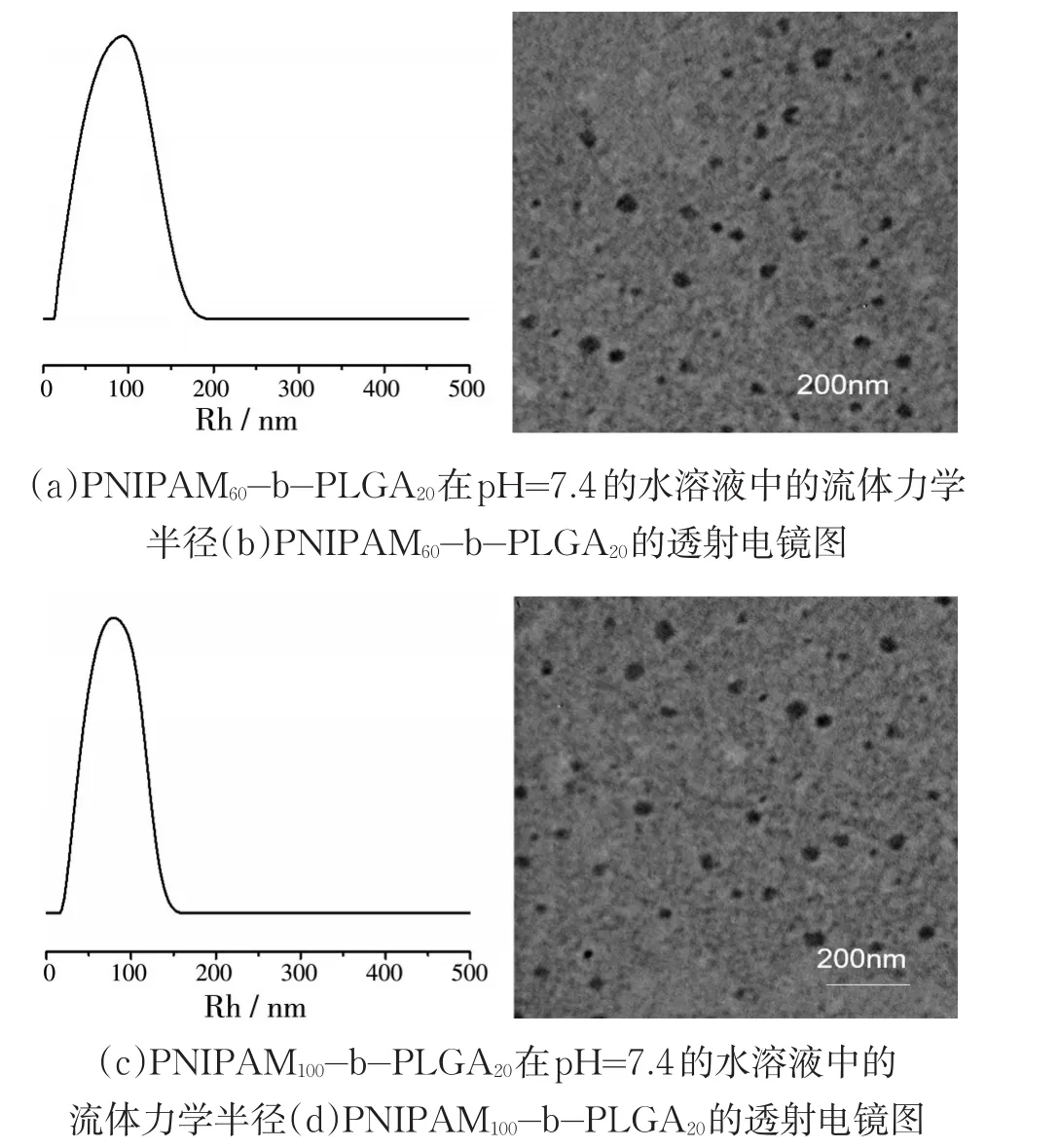
图8 聚合物胶束在pH=7.4的水溶液中的流体力学半径(Rh)及透射电镜图
2.6 DOX的体外释放研究
DOX广泛应用于治疗不同类型的癌症。聚合物胶束PNIPAM100-b-PLGA20与PNIPAM60-b-PLGA20作为纳米级载体,可实现DOX的负载。聚合物胶束的载药量(DLC)、包封率(DLE)如表2所示。聚合物PNIPAM100-b-PLGA20胶束的DLC、DLE高于聚合物胶束PNIPAM60-b-PLGA20。这是由于疏水嵌段比例的增加使胶束的核收缩的同时提高了阿霉素的负载量。图9是两组聚合物载药胶束在37℃、pH=7.4的PBS缓冲溶液中的累积释放曲线。如图9所示,载药胶束的缓慢释放长达72 h,PNIPAM60-b-PLGA20与PNIPAM100-b-PLGA20载药胶束最终释放量分别为原始载药量的78.2%、69.8%。此外,由于PNIPAM100-b-PLGA20载药胶束在高于其LCST时,疏水部分比例高,其胶束内核的疏水能力强,导致DOX的释放速率低于PNIPAM60-b-PLGA20载药胶束。两种聚合物胶束均可实现DOX缓慢释放,有一定的潜在应用价值。
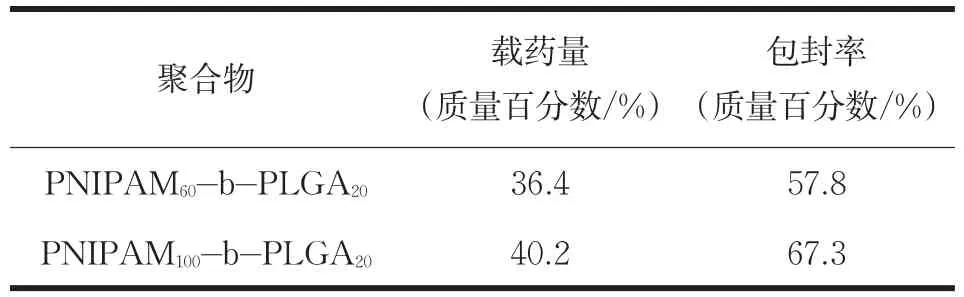
表2 聚合物胶束的载药性能

图9 37℃聚合物载药胶束在pH=7.4的PBS缓冲溶液中的累计释放曲线
3 结论
以二碳酸二叔丁酯、乙醇胺、溴异丁酰溴等为原料制备新型多功能引发剂,采用ATRP法与NCA开环聚合法成功制备聚合物PNIPAM100-b-PLGA20与PNIPAM60-b-PLGA20。两组聚合物的LCST与人体体温相接近,并且在温度高于其LCST时可以自组装成粒径在100 nm以下的球状胶束。两组聚合物胶束均成功负载阿霉素,载药量约为40%,包封率约为60%,缓慢释放长达72 h,是潜在的纳米药物载体。
