5’-尿嘧啶核苷酸与锌离子相互作用研究
2019-11-22卿琳华童群义
卿琳华 童群义
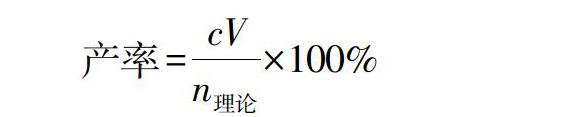
摘要 [目的]研究尿苷酸与锌离子之间的相互作用,为研究尿苷酸在生物体内的作用方式及配合物的潜在应用提供理论基础。[方法]利用傅里叶红外光谱、共聚焦拉曼光谱来研究尿苷酸与锌离子之间的配位方式,并以尿苷酸锌产率为指标来探讨不同条件对它们相互作用的影响。[结果]不同条件对尿苷酸与锌离子相互作用的影响程度不同;红外光谱中尿苷酸锌的磷酸基团峰位置明显向高频移动,且C—O伸缩振动峰出现轻微的频移;拉曼图谱中,尿苷酸锌的羰基伸缩振动峰出现明显裂分现象,且峰的强度变弱。[结论] pH和配合时间对尿苷酸锌产率的影响明显,而温度对其影响较小。锌离子可以与尿苷酸的磷酸基团发生配位作用,并与碱基上的一个羰基氧原子发生相互作用。
关键词 尿苷酸锌;配位方式;红外光谱;拉曼光谱
中图分类号 TS201文献标识码 A
文章编号 0517-6611(2019)20-0179-03
doi:10.3969/j.issn.0517-6611.2019.20.048
開放科学(资源服务)标识码(OSID):
The Interaction between Uridine 5 Monophosphate and Zinc Ions
QING Lin hua, TONG Qun yi
(Jiangnan University,Wuxi,Jiangsu 214122)
Abstract [Objective]The interaction between UMP and zinc ions was studied, aiming to provide a theoretical basis for the mode of UMP in biological body and potential application of complexes. [Method]The interaction between UMP and zinc ions was studied by infrared spectroscopy and Raman spectroscopy, and the influences of different conditions on them were investigated, taking the yield of UMP Zn as target. [Result]Different conditions had different effects on the interaction between UMP and zinc ions. The obvious shifting to higher frequencies of stretching vibration of phosphate group and the slight shifting of C-O can be observed in infrared spectrum data. In Raman spectrum of UMP Zn, the stretching vibration of C-O was split clearly and its intensity became weaker. [Conclusion]The yield of UMP Zn could be influenced greatly by pH and reaction time, but temperature had a little effect on the yield. Zinc ion can coordinate with phosphate group of UMP and interact with a carbonyl oxygen atom on the base.
Key words UMP Zn;Coordination mode;Infrared spectrum;Raman spectrum
5-尿嘧啶核苷酸(uridine 5-monophosphate,UMP,简称尿苷酸)是核苷酸的一种,由尿嘧啶碱基、核糖和磷酸基团组成。尿苷酸在生物体内起着极其重要的作用,可参与肝解毒物质葡萄糖醛酸的生物合成,在医学领域中可用于治疗肝炎、改善冠心病等症状,且尿苷酸及其衍生物对生物体内的免疫调节和代谢调控起到尤为重要的作用[1-2]。作为食品添加剂,包括尿苷酸在内的核苷酸已被允许添加到婴幼儿奶粉当中,可满足婴幼儿对核苷酸的需要,起到维持免疫系统功能、促进肠道成熟等作用[3]。在饲料添加剂领域,核苷酸的复配使用可发挥出促进血液循环和新陈代谢、促进动物生长发育、减少酮体脂肪、增强免疫力等功效[4-5]。
锌元素是生物体必需的微量元素,可直接参与核酸的合成、细胞分化和增殖等生化过程,更是300多种酶和功能蛋白的重要组成部分,在维持蛋白质的结构和功能方面发挥重要作用。缺锌会导致生长迟缓、味觉异常、免疫力降低、嗜睡等病症的发生[6],而体内锌含量过多可能会导致肠胃炎、胰腺受损、免疫力降低,甚至贫血。
生物体内的核苷酸通常与金属离子结合而参与到生物活动过程中[7],且核苷酸的磷酸基团、戊糖部分或者杂环碱基上的氮原子和氧原子均是金属离子可能的结合位点[8-10],对金属和核苷酸的研究对于理解金属与核酸相互作用以及核苷酸的生物学意义十分重要。笔者主要利用红外和拉曼
光谱来分析尿苷酸与锌离子之间的配合方式,并探讨不同条件对尿苷酸与锌离子相互作用的影响,以期为研究尿苷酸在生物体内的作用方式及配合物的潜在应用提供理论基础。
1 材料与方法
1.1 材料
1.1.1 原材料。5-尿苷酸、5-尿苷酸二钠,由杭州美亚药业股份有限公司提供。
1.1.2
主要试剂。无水氯化锌,江苏博美达生命科学有限公司;氢氧化钠、盐酸、乙二胺四乙酸二钠(EDTA)、二甲酚橙、无水乙醇、冰乙酸、乙酸钠、溴化钾,均购于国药集团化学试剂有限公司。
1.1.3
主要仪器。HH-2k8恒温水浴锅(巩义市予华仪器有限公司);R205B旋转蒸发器(上海申顺科技有限公司);RJ-LD-50G低速离心机(无锡市瑞江分析仪器有限公司);RT-10加热磁力搅拌器(广州仪科实验室技术有限公司);SHZ-95B循环水真空泵(巩义市予华仪器有限公司);EL20实验室pH计(梅特勒-托利多仪器(上海)有限公司);AB104-N电子分析天平(梅特勒-托利多仪器(上海)有限公司);DZF真空干燥箱(上海科恒实业发展有限公司);IS10傅里叶红外光谱仪(美国Nicolet公司);LabRAM HR Evolution显微共聚焦拉曼光譜仪(法国HORIBAI Jobin Yvon S.A.S.公司);TGA2热重分析仪(梅特勒-托利多仪器有限公司)。
1.2 方法
1.2.1
尿苷酸与锌离子配合过程的影响因素研究。
1.2.1.1
配合反应过程。称取一定量的5-尿苷酸二钠,用去离子水溶解,调pH,再加入相同物质的量的氯化锌,恒温搅拌反应一段时间,再将溶液转移到蒸馏瓶中进行旋转蒸发浓缩,取浓缩液加入10倍体积左右的无水乙醇浸提,析出白色固体,静置,低速离心、过滤,收集沉淀,分别用去离子水和乙醇洗涤,干燥即得1∶1型配合产物尿苷酸锌(UMP-Zn)。
1.2.1.2
影响因素研究。分别设置不同的pH(2.0、2.5、3.0、3.5、4.0、4.5)、温度(20、40、60、80 ℃)和配合时间(15、30、45、60、75、90、120 min),以尿苷酸锌的产率为指标,探讨不同条件对尿苷酸与锌离子相互作用的影响。
1.2.2
尿苷酸锌产率的测定。水溶液中尿苷酸与锌离子作用一段时间后,取一定体积的反应液加乙醇进行浸提,静置析出沉淀,离心分离,醇洗沉淀2~3次。将沉淀转移至锥形瓶中,加入30 mL去离子水和15 mL乙酸-乙酸钠缓冲溶液(pH 5.5),再滴加2滴二甲酚橙指示剂(2 g/L),溶液呈紫红色,用0.01 mol/L的EDTA溶液滴定,溶液颜色变为亮黄色即为终点,记录消耗的EDTA体积,计算尿苷酸锌配合物的实际生成量,平行重复3次试验。
尿苷酸锌的理论生成量由尿苷酸和锌离子的投入量计算得到,按下式计算产率:
产率=cVn理论×100%
式中,c为EDTA溶液的浓度(mol/L);V为消耗的EDTA体积(L);n理论为尿苷酸锌的理论生成量(mol)。
1.2.3
尿苷酸锌固体的锌含量测定。精确称取尿苷酸锌固体,置于250 mL锥形瓶中,测定方法同“1.2.2”,记录消耗的EDTA体积,测定尿苷酸锌固体的锌含量,平行重复3次试验,锌含量计算公式为:
锌的质量分数=cMVm×100%
式中,c为EDTA溶液的浓度(mol/L);m为尿苷酸锌固体质量(g);M为锌的摩尔质量(g/mol);V为消耗的EDTA体积(L)。
1.2.4 尿苷酸与锌离子配合方式的光谱研究。
1.2.4.1
傅里叶红外光谱分析。用溴化钾(KBr)压片法分别测定400~4 000 cm-1内尿苷酸和尿苷酸锌固体的红外光谱。
1.2.4.2 共聚焦拉曼光谱分析。分别测定尿苷酸和尿苷酸锌固体的拉曼光谱,测定条件为激发波长532 nm,光栅刻线600线/mm,扫描范围200~2 000 cm- 光谱信号采集积分时间5 s,共焦孔径150 μm,50倍长焦距镜头。
1.2.5 热重分析。称取3 mg左右的尿苷酸锌固体,置于瓷坩埚中,测定失重曲线,测定条件为温度30~600 ℃,升温速率为10 ℃/min,氮气保护。
2 结果与分析
2.1 尿苷酸与锌离子相互作用的影响因素研究
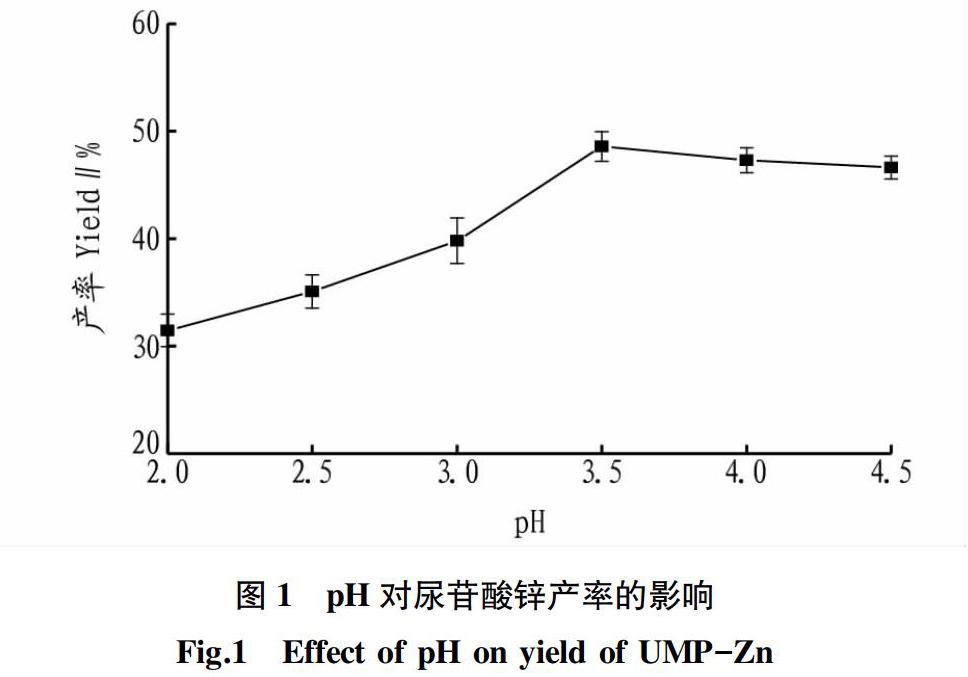
2.1.1 pH。在不同pH溶液中尿苷酸的解离程度不同,因此试验过程中酸度对配合反应的影响很大。pH较低时,体系中的氢离子会与金属离子争夺供电基团;pH较高时,体系中的氢氧根离子会与核苷酸配体争夺金属离子,这都会影响配合反应的进行。探究pH对配合反应的影响非常重要。由图1可知,当pH在2.0~3.5时,随着pH的升高,配合物产率逐渐增加,说明尿苷酸与锌离子的相互作用随着pH的升高而增强;当pH为 3.5时产率最大,为48.58%;而pH>3.5之后,配合物产率呈现逐渐降低的趋势,这可能是pH影响尿苷酸的解离造成的。
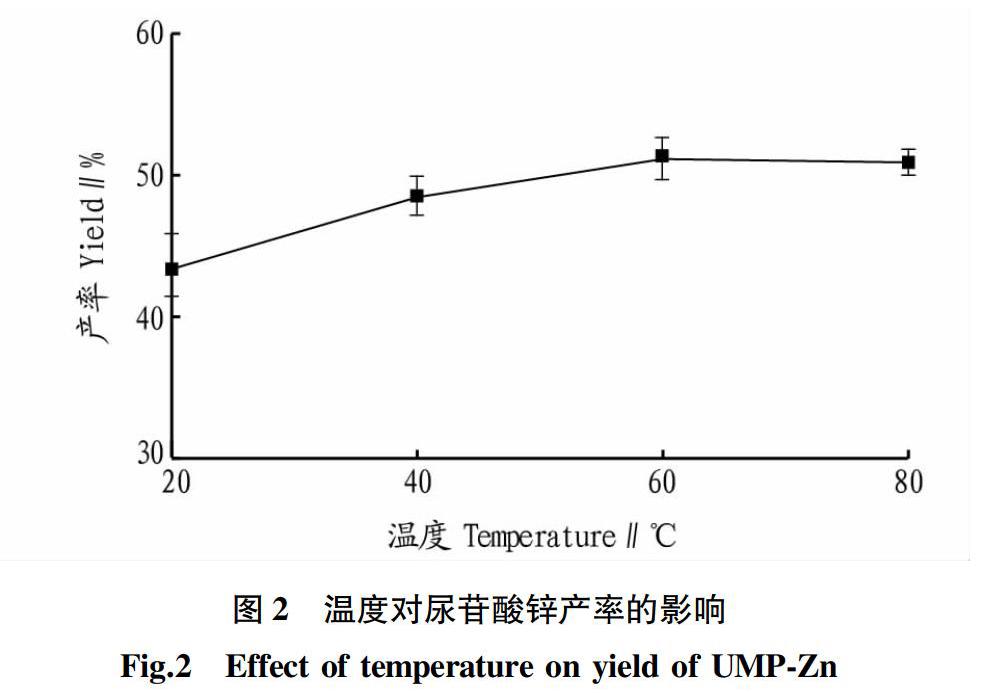
2.1.2 温度。在化学反应中,温度也会影响反应的进行程度。由于尿苷酸与锌离子之间的配合反应为吸热反应,所以温度的升高一般会促进配合反应的进行。由图2可知,尿苷酸与锌离子的配合反应在常温下即可发生,20 ℃时配合物产率为43.65%。当温度在20~60 ℃内,随着温度的升高,配合物产率增大,说明尿苷酸与锌离子之间的相互作用增强。而当温度升高至80 ℃时,配合物产率略有降低,这可能因为较高的温度会对尿苷酸分子的结构造成一定程度的破坏,使得配合物产率无增加趋势。
2.1.3
配合时间。尿苷酸与锌离子配合时间的长短直接关系到配位反应是否完全。由图3可知,随着配合时间的增加,尿苷酸锌的产率先呈现增加趋势后基本持平。在15 min时配合物产率为44.27%,说明尿苷酸与锌离子之间的配合反应较快。在15~60 min内,尿苷酸锌的产率逐渐增大,60 min时产率达51.12%(增加6.85百分点)。此后,继续增加配合反应时间,配合物产率基本不变。
2.2 尿苷酸锌的锌含量和结晶水的含量测定
尿苷酸锌的热重曲线如图4所示,尿苷酸锌的锌含量和结晶水含量分别为15.36%和8.61%。在尿苷酸锌的热重曲线中,存在2个失重平台。第1个失重平台的温度在110 ℃,失去的是结晶水;在第2个失重平台中,尿苷酸锌质量呈现快速下降的趋势,这是因为尿苷酸锌发生了热分解。
2.3 尿苷酸与锌离子相互作用的光谱研究
傅里叶红外光谱仪和拉曼光谱仪具有精度高、速度快、分辨率高等优点,它们都是用于分析物质结构的重要仪器,两者相辅相成,联用时可以更好地分析分子的振动状态,反映出物质分子结构的信息。尿苷酸分子在配位前后,其振动光谱会出现一定程度的改变,出现峰的频移、强度改变等现象。可以通过比较配位前后尿苷酸和尿苷酸锌配合物的红外、拉曼光谱信息来研究尿苷酸与锌离子的相互作用。尿苷酸和尿苷酸锌配合物的红外、拉曼光谱图分别如图5、6所示。
红外光谱是通过官能团的振动信息来分析物质结构的一种常用方法。与尿苷酸的红外图谱(图5a)相比,在尿苷酸锌配合物的红外光谱图中(图5b),尿苷酸分子的主要特征峰均被保留下来,说明在配合物中尿苷酸分子的结构没有发生明显变化。由于核糖C—O的伸缩振动峰和磷酸基团反对称伸缩振动峰由原来的1 124、1 085 cm-1高频移至1 174、1 100 cm-1;且磷酸基团的对称伸缩峰也由原来的980、936 cm-1高频移至1 017、992 cm-1。磷酸基团的高频移动表明锌离子与磷酸基团发生了配位作用,产生诱导效应[11-12],使得磷酸基团的电子云密度增加。此外,羰基伸缩振动峰出现轻微的变化,峰位置往高频方向稍稍移动,位于1 693、1 670 cm- 且出现肩峰,这可能是因为氢键作用或者锌离子与尿苷酸碱基发生相互作用。
红外和拉曼光谱图通常能够互补,这是因为两者振动产生的机理不同。由于磷酸基团的极性较强,在拉曼图谱中的峰强度很弱。在尿苷酸的拉曼谱图中(图6a),主要有3个较强的吸收峰,791 cm-1处的峰归属于尿嘧啶环平面内呼吸振动,位于1 360 cm-1处的峰为C—N键的平面内伸缩振动和C—H键的平面内摇摆振动,位于1 676 cm-1处的峰为碱基上羰基的伸缩振动峰[13-14]。此外,987 cm-1和1 406 cm-1处的峰归属为C—N、C—C键的伸缩振动峰和N—H、C—H的弯曲振动峰[15]。在尿苷酸锌的拉曼图谱中(图6b),主要峰位置仍被保留下来,峰位置无明显变化。而羰基伸缩振动峰出现裂分现象,分别位于1 657、1 678 cm- 且强度稍稍变弱,這可能是因为锌离子和尿苷酸碱基上的1个羰基氧原子之间发生了相互作用,导致2个羰基的电子云密度不同。
3 结论与讨论
(1)探讨了尿苷酸与锌离子配合过程中,不同条件对尿苷酸与锌离子相互作用的影响,pH、温度和配合时间对其产率的影响程度不同。pH和配合时间对尿苷酸锌产率的影响明显,而温度对其影响不明显。
(2)结合红外光谱和拉曼光谱来分析尿苷酸与锌离子之间的配合方式,发现尿苷酸锌的磷酸基团伸缩振动峰向高频移动,且羰基伸缩振动峰发生裂分,这是因为锌离子与磷酸基团发生了配位作用,并与尿苷酸碱基上的一个羰基氧原子发生相互作用。
参考文献
[1] CONNOLLY G P,DULEY J A.Uridine and its nucleotides:Biological actions,therapeutic potentials[J].Trends in pharmacological sciences,1999,20(5):218-225.
[2] DO CARMO G M,DE S M F,BALDISSERA M D,et al.Nucleotide and nucleoside involvement in immunomodulation in experimental Chagas disease[J].Molecular and cellular biochemistry,2018,447(1/2):203-208.
[3] TSUJINAKA T,KISHIBUCHI M,IIJIMA S,et al.Nucleotides and intestine[J].Jpen J Parenter Enteral Nutr,1999,23(S5):74-77.
[4] 蓝汉冰,曹俊明,李国立,等.饲料中添加不同类型核苷酸对凡纳滨对虾生长性能的影响[J].现代渔业信息,2009,24(6):3-5.
[5] 杨玉芬,周世业,乔建国.外源5-尿苷酸对断奶仔猪生长性能及抗氧化能力的影响[J].西北农林科技大学学报(自然科学版),2009,37(5):49-52,58.
[6] 井明艳,孙建义,赵树盛,等.微量元素锌的营养学研究进展[J].饲料工业,2004(10):20-24.
[7] ZHOU P,SHI R F,YAO J F,et al.Supramolecular self assembly of nucleotide-metal coordination complexes:From simple molecules to nanomaterials[J].Coordination chemistry reviews,2015,292:107-143.
[8] FIOL J J,TERRN A,MORENO V.Chromium(III)interactions with nucleotides[J].Inorganica chimica acta,1984,83(2):69-73.
[9] FIOL J J,TERRN A,MULET D,et al.Some new derivatives of Co(III)with uracil,uridine and pyrimidine nucleotides[J].Cheminform,1987,135(3):197-202.
[10] 郭攀娟.核苷酸与金属离子配位作用的理论研究[D].长春:吉林大学,2011.
[11] FIOL J J,TERRN A,MORENO V.Some new derivatives of Cr(III)with uracil,uridine and 5 UMP[J].Polyhedron,1986,5(5):1125-1130.
[12] FIOL J J,TERRON A,MORENO V.Some new derivatives of Ni(II)with uracil,uridine and nucleotides[J].Inorganica chimica acta,1986,125(3):159-166.
[13] 吴国祯.拉曼谱学——峰强中的信息[M].北京:科学出版社,2007.
[14] 吴雷,李菲,金周雨,等.基于密度泛函理论方法的核酸碱基拉曼光谱研究[J].生物化学与生物物理进展,2016,43(3):281-290.
[15] TUSBOI M.5 infrared and raman spectroscopy[J].Basic principles in nucleic acid chemistry,1974,1:399-452.
