壳聚糖/盐酸小檗碱缓释微球的制备
2019-11-21林欣雨李瑶琦
林欣雨,李瑶琦,周 瑾,罗 超
(绍兴文理学院元培学院,浙江 绍兴312000)
微球是指药物分散或被吸附在高分子、聚合物基质中而形成的微粒分散体系,可提高稳定性,降低刺激性,控制释放,并具有被动靶向性,是现代药物传递系统的主要载体形式之一[1]。目前,制备微球的方法主要有相转变法[2]、乳化交联法[3]、喷雾干燥法[4]、膜乳化法等,其中膜乳化法以无机微孔膜(SPG)为介质,利用膜微孔分离和毛细管作用原理,通过在膜一侧施加压力使分散溶液透过膜孔,以微小液滴的形式分散在与其不相溶的溶液中而形成乳液[5],从而交联固化形成微球,该方法反应条件温和,操作简便,易于规模化生产,重复性好。
壳聚糖是自然界存储量仅次于纤维素的天然高分子多糖,由虾、蟹等甲壳动物外壳的甲壳素脱乙酰化而得[6],具有良好的生物相容性、生物可降解性、生物粘附性,是组织工程材料和药物缓控释载体材料的主要基质成分[7-8],可制成微球[3]、纳米粒[9]、水凝胶[10]、微凝胶[11]等多种不同特性的材料。壳聚糖微球可通过包覆[4]、吸 附[3]、共聚[12]等多种手段负载药物,并具有理想的缓控释性能、黏膜粘附性,可提高药物在体液环境中的稳定性和生物利用度。本实验采用SPG 膜乳化法制备壳聚糖/盐酸小檗碱缓释微球,并优化制备工艺,表征理化特性,研究缓释性能,以期为相关研究提供依据。
1 材料
壳聚糖(脱乙酰度95%,分子量1.2×105,浙江澳兴生物技术有限公司);盐酸小檗碱原料药(含有量>98%,郑州丰冠化工产品有限公司);盐酸小檗碱对照品(江苏永健医药科技有限公司,批号200351-161107);司盘-80(上海萨恩化学技术有限公司)。戊二醛(东京仁成工业株式会社)。乙腈为色谱纯;其余试剂均为分析纯。
Waters e2695-2489型高效液相色谱仪(美国Waters 公司);Nicolet 740型红外光谱仪(美国Thermo 公司);X’Pert PRO 型X 射线衍射仪(荷兰PNAlytical 公司);JSM-6360LV 型扫描电子显微镜(日本电子株式会社);FD-1 A-50型冷冻干燥机(北京博医康实验仪器有限公司);高效手动膜乳化器(日本SPG Technology 公司)。
2 方法与结果
2.1 微球制备 将1 g 壳聚糖溶于50 mL 2%醋酸中,配制成2%溶液,在一定温度下将200 mg 盐酸小檗碱溶于其中,持续搅拌一定时间,作为水相,并以10倍体积液体石蜡-环己烷(7 ∶5)混合液为油相,2%司盘-80为乳化剂。在相同温度下,通过50 μm SPG 膜乳化器将水相压入到油相中,形成W/O 型乳液,再加入一定量戊二醛交联1 h,离心收集微球,分别用乙醇、纯水洗涤,真空冷冻干燥,即得。
2.2 含有量测定
2.2.1 色谱条件 SunFire C18色谱柱(4.6 mm×250 mm,5 μm);流动相乙腈-0.5% 磷酸(30 ∶70,三乙胺调pH 至3);体积流量1.0 mL/min;柱温30 ℃;检测波长345 nm;进样量20 μL。
2.2.2 线性关系考察 精密称取盐酸小檗碱对照品10 mg,蒸馏水溶解并定容于100 mL 棕色量瓶中,配制成0.1 g/L,蒸馏水进一步稀释至1.0、2.0、5.0、10.0、15.0、20.0 mg/L,在“2.1.1”项色谱条件下进样测定。以峰面积积分值(Y)对溶液质量浓度(X)进行回归,得方程为Y=6 139.2X-3 897.2(R2=0.999 9),在1~20 mg/L范围内线性关系良好。
2.2.3 精密度试验 1.0、10.0、20.0 mg/L 盐酸小檗碱对照品溶液在“2.2.1”项色谱条件下进样测定,在同1 d 内重复6次,测得盐酸小檗碱峰面积RSD 分别为1.1%、2.0%、1.2%,表明仪器精密度良好。
2.2.4 稳定性试验 10.0 mg/L 盐酸小檗碱对照品溶液于0、2、4、6、8、12、24 h 在“2.2.1”项色谱条件下进样测定,测得盐酸小檗碱峰面积RSD 为1.1%,表明溶液在24 h 内稳定性良好。
2.2.5 加样回收率试验 配制含盐酸小檗碱9.6、9.3、9.7、10.5、10.6、10.2 mg/L 的载药微球溶出样品溶液10 mL,加入对照品溶液(含10.0 mg/L盐酸小檗碱)10 mL,在“2.2.1”项色谱条件下进样测定,测得平均加样回收率为99.12%,RSD为1.53%。
2.2.6 专属性考察 制备盐酸小檗碱对照品溶液、盐酸小檗碱原料药溶液、空白壳聚糖微球浸出液、载药壳聚糖微球浸出液(释放度检测样品),在“2.2.1”项色谱条件下进样测定,色谱图见图1。由图可知,载体材料对盐酸小檗碱检测没有影响,该方法专属性良好。
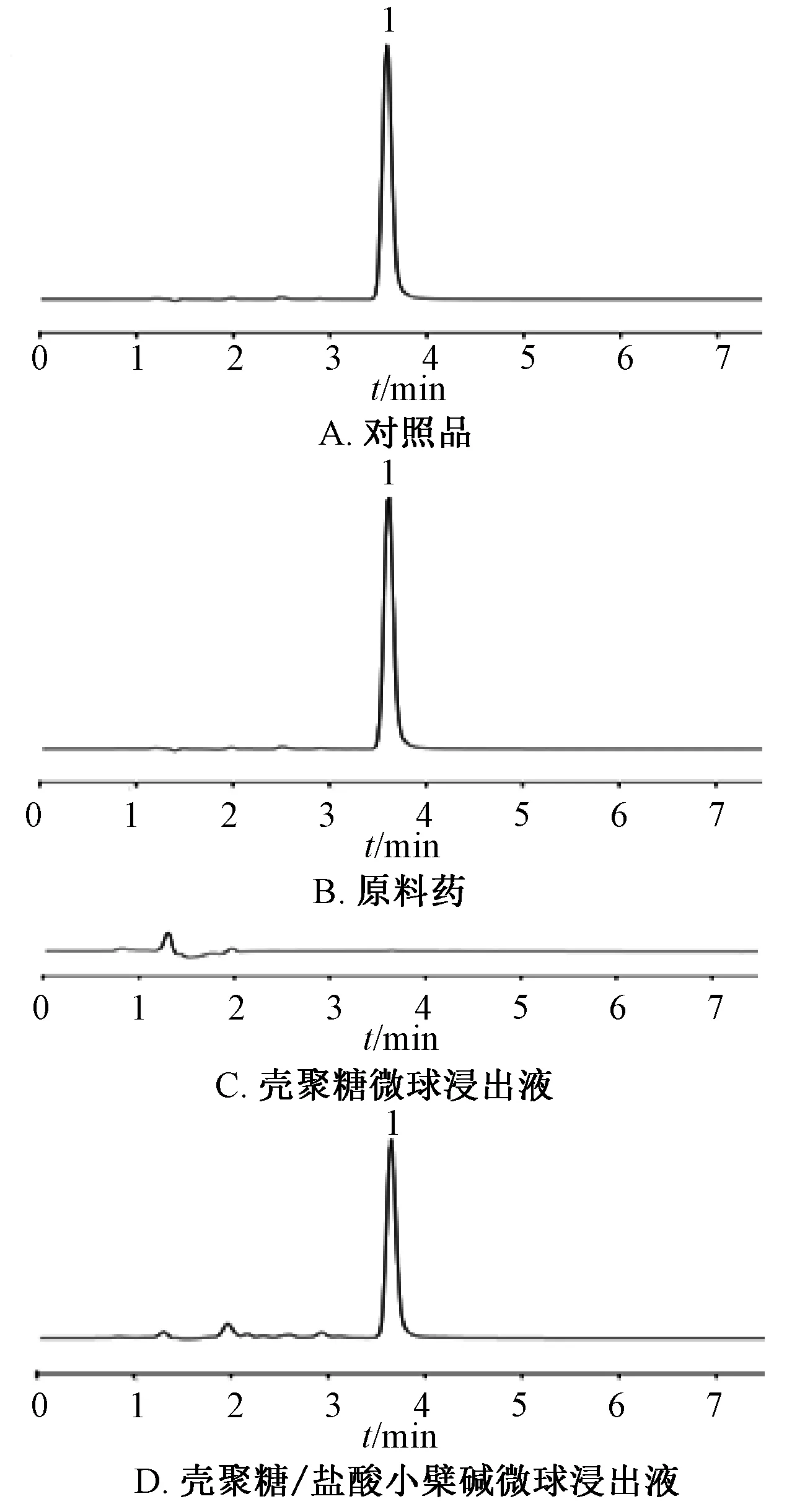
图1 盐酸小檗碱HPLC 色谱图Fig.1 HPLC chromatograms of berberberine hydrochloride
2.3 包封率、载药量测定 取适量载药微球加到甲醇中,密封超声1 h,10 000 r/min 离心30 min以使盐酸小檗碱全部溶出,上清液加甲醇定容到100 mL,在“2.2.1”项色谱条件下进样测定,按下式计算载药量、包封率。

2.4 制备工艺优化[13]根据预实验(单因素试验)结果,选择对载药微球制备影响较大的交联剂用量(X1)、混合搅拌时间(X2)、体系温度(X3)作为影响因素,包封率(Y)作为评价指标,星点设计-效应面法进行优化,结果见表1。再通过Design-Expert 8.0.6.1软件进行拟合,得到回归方程为方差分析见表2。
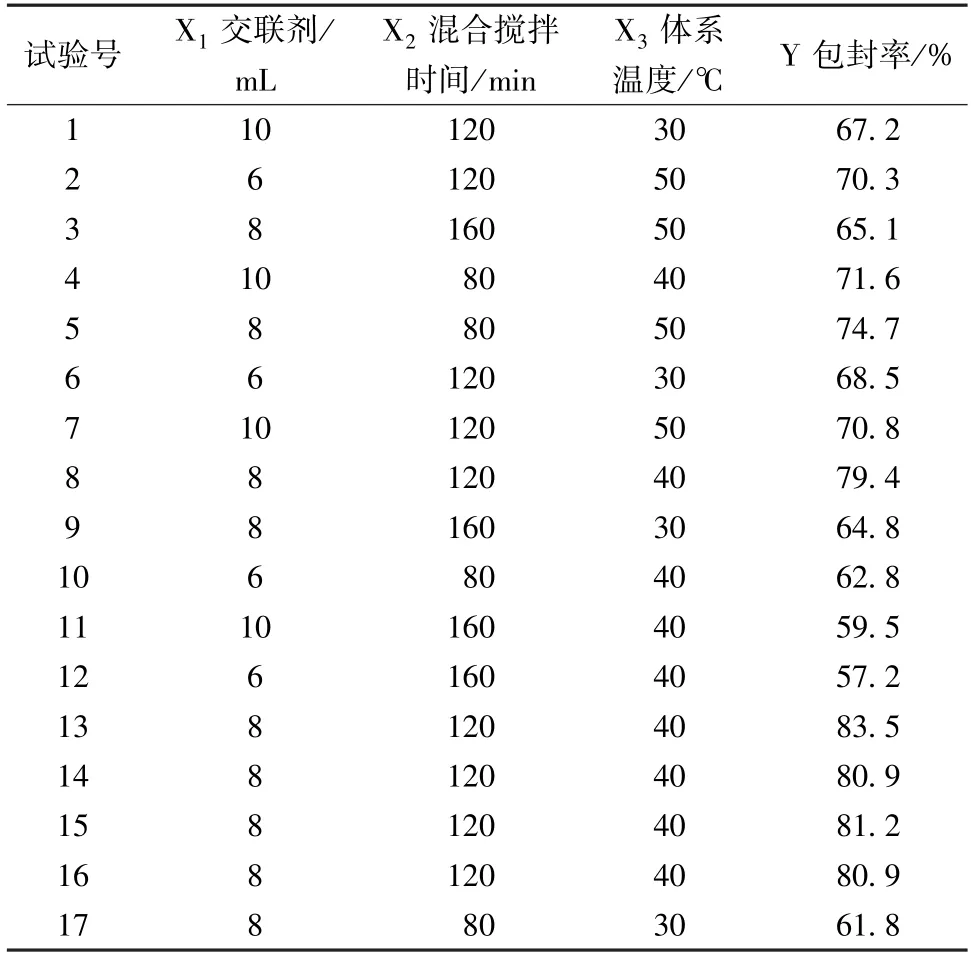
表1 试验设计与结果Tab.1 Design and results of tests
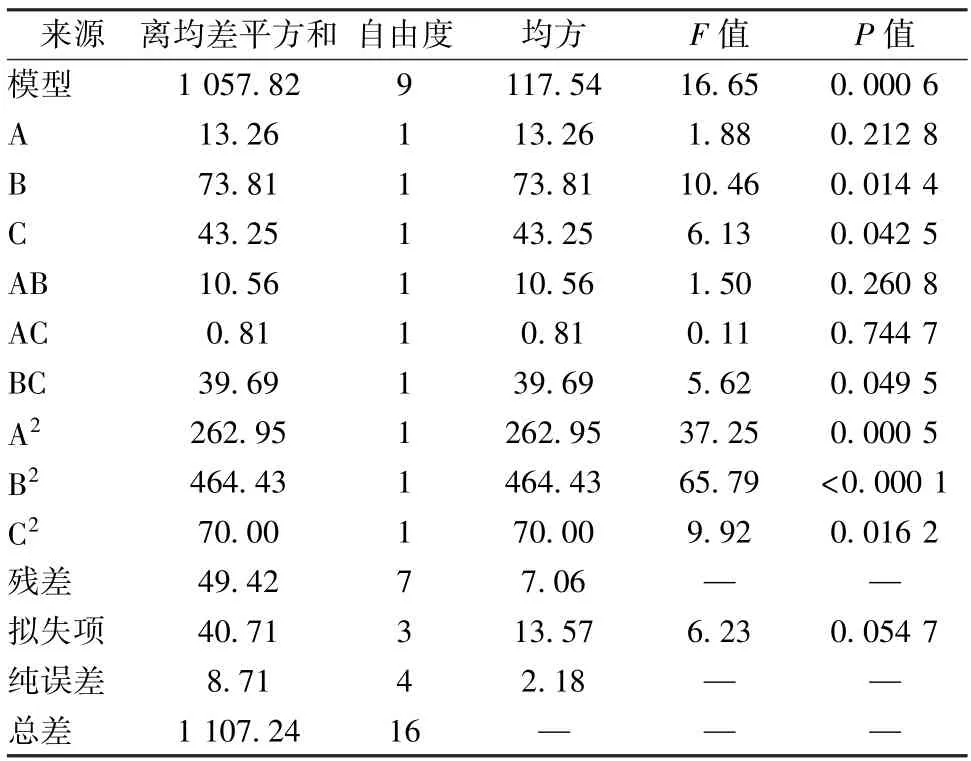
表2 方差分析Tab.2 Analysis of variance
由表2可知,模型P=0.000 6<0.05,表明其稳定可靠;复相关系数R2=0.955 4,表明模型拟合度良好,能准确预测实际情况;校正决定系数=0.898 0,表明模型能解释89.80% 响应值的变化;各因素失拟项P>0.05,表明拟合方程准确性良好;各因素影响程度依次为X2>X3>X1,X2、X3、X2X3、有显著影响(P<0.05)。
响应面分析见图2。通过Design-Expert 8.0.6.1软件,得到最优工艺为交联剂用量8.23 mL,混合搅拌时间111.63 min,体系温度43.72 ℃,包封率82.00%,考虑到实际可操作性,将其修正为交联剂用量8 mL,混合搅拌时间112 min,体系温度44 ℃。

图2 各因素响应面图Fig.2 Respone surface plots for various factors
然后,按照优化工艺进行3批验证试验,结果见表3,可知包封率与预测值82.00%相当(相对误差1.67%),表明工艺稳定可行,模型预测性良好。
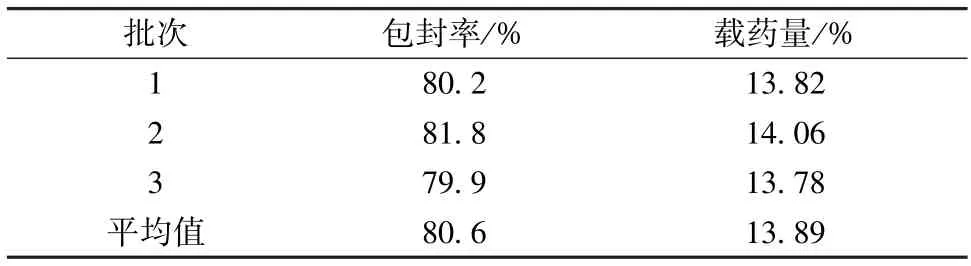
表3 验证试验结果(n=3)Tab.3 Results of verification tests(n=3)
2.5 微球表征
2.5.1 扫描电子显微镜(SEM)取适量微球均匀铺在粘有导电胶的铜块表面,喷金处理后进行观察,结果见图3。由图可知,微球呈规则球形,表面较光滑,大部分粒径在50 μm 左右。

图3 微球SEM 图Fig.3 SEM images for microspheres
2.5.2 傅立叶变换红外光谱(FT-IR)KBr 将盐酸小檗碱、壳聚糖微球、载药微球、物理混合物分别压片,在4 000~400 cm-1处测定红外光谱,结果见图4。由图可知,盐酸小檗碱1 623、1 503 cm-1附近是芳环骨架振动带[14];壳聚糖微球除了壳聚糖特征峰(如3 400 cm-1的O-H 和N-H 伸缩振动峰,1 573 cm-1的 N-H 面内弯 曲振动 峰,1 046 cm-1的C-O 伸缩振动峰)[15]外,还有因戊二醛交联而引入的C-H 伸缩振动峰2 941 cm-1(-CH3)和2 865 cm-1(-CH2);物理混合物可见明显的盐酸小檗碱、壳聚糖微球特征峰叠加;载药微粒除了608 cm-1处有盐酸小檗碱特征峰外,其余特征峰明显减弱,表明微球实现了壳聚糖对盐酸小檗碱的包覆,使后者较好地分散在微球内部。
2.5.3 X 射线衍射分析(XRD)图5显示,盐酸小檗碱在18.29°、25.83°、28.64°,35.42°处有尖锐、狭窄的衍射峰,显示出典型晶体结构[14];壳聚糖微球只在17°附近有1个较宽的特征峰;载药微球除了26°附近有1个较弱的盐酸小檗碱特征峰外,其余均被壳聚糖微球特征图谱掩盖;物理混合物可见明显的盐酸小檗碱、壳聚糖微球特征峰叠加,表明微球较好地包覆了盐酸小檗碱。
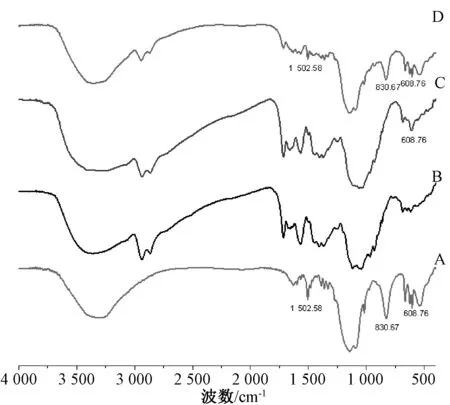
图4 样品FT-IR 图Fig.4 FT-IR spectra for samples
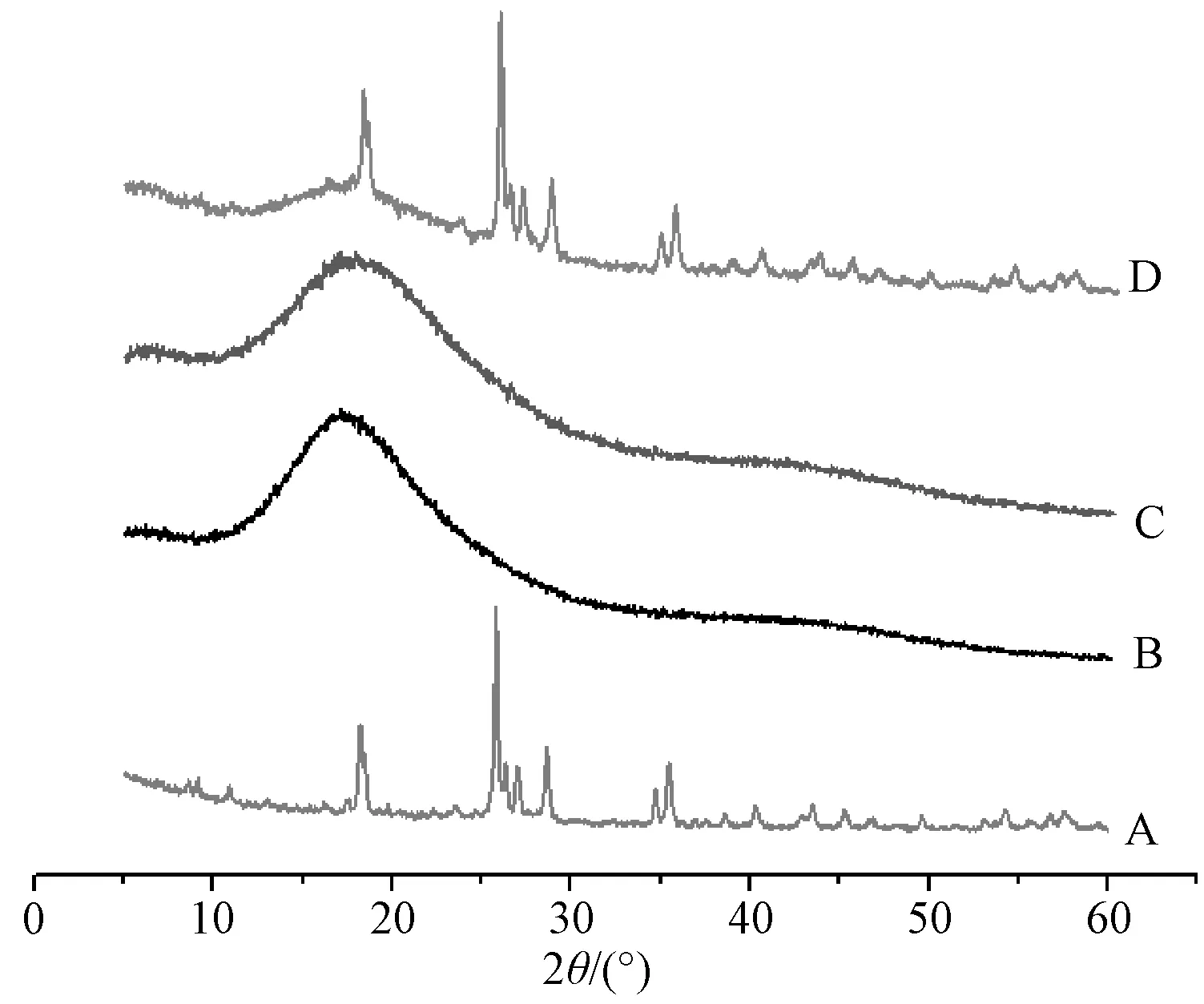
图5 样品XRD 图Fig.5 XRD patterns for samples
2.6 体外释放行为考察 以0.1 mol/L 盐酸(pH=1.2)、磷酸盐缓冲液(pH=7.4)为溶出介质,取相当于盐酸小檗碱质量100 mg 的载药微球,分散于5 mL 溶出介质后装入透析袋内(截留分子量10 000 Da),置于95 mL 相同溶出介质中,(37± 0.5)℃恒温水浴振荡(100 r/min),于0.5、1、2、4、6、8、10、12、24 h 各取样2 mL,并补充相同体积空白介质,0.22 μm 微孔滤膜过滤,在“2.2.1”项色谱条件下进样测定,计算累积释放率Q,公式为其中W为盐酸小檗碱投入量,Cn为第n个取样点溶液质量浓度,Ci为第n-1个取样点溶液质量浓度,V为溶出介质总体积,Vi为取样体积。结果见图6。
由图可知,微球在2种释放介质中显示出良好的缓释性能,其中在0.1 mol/L 盐酸(pH=1.2)中释放更慢,24 h 内累积释放率仅为77.8%,而在磷酸盐缓冲液(pH=7.4)中达85.7%。同时,均未出现明显突释现象,0.5 h 内释放率分别为4.8%、5.3%。
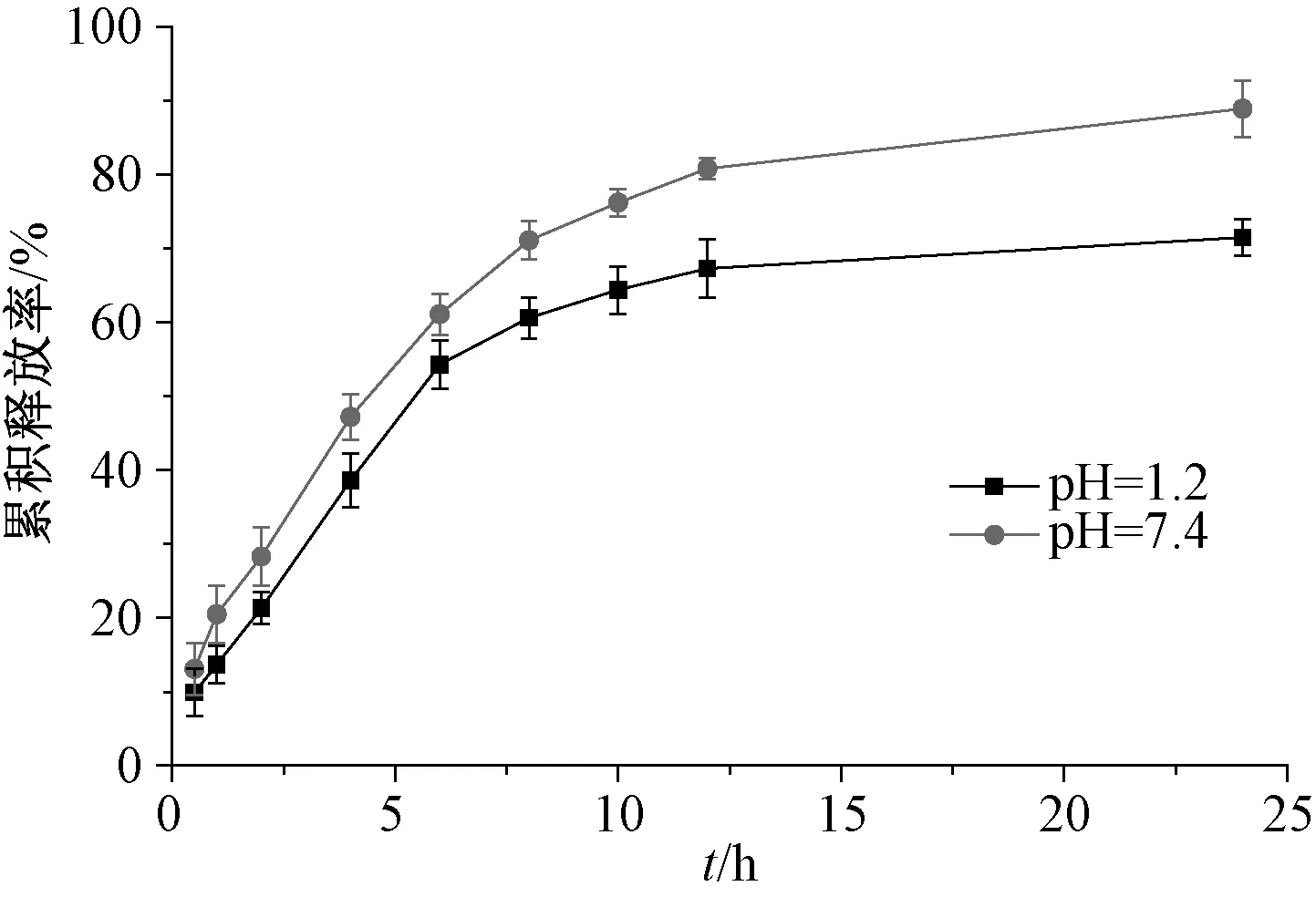
图6 微球体外释药曲线Fig.6 In vitro drug release curves for microspheres
2.7 释放动力学模型拟合 将微球体外释放数据分别以零级、一级、Higuchi、Ritger-Peppas 模型进行拟合[16],结果见表4。由表可知,微球在2种释放介质中均与Peppas 模型拟合度最高,n分别为0.789 2、0.778 9,属于non-Fickian 扩散[17]。
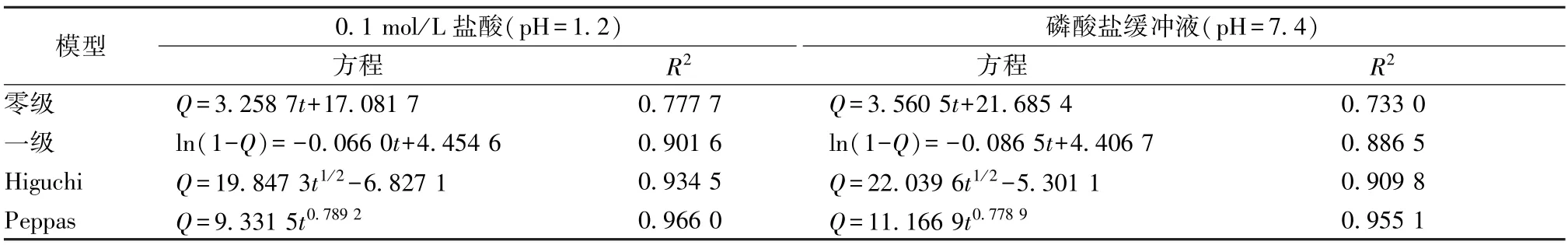
表4 微球模型拟合结果Tab.4 Results of model fitting of microspheres
3 讨论
中药单体活性成分的开发与利用是中医药走向现代化、国际化的重要基础,近几十年来青蒿素、小檗碱、穿心莲内酯、川芎嗪等一大批中药活性单体成分已成为临床一线用药,并受到国际学界高度关注[18]。然而,稳定性差、溶解度低等问题一直困扰着大部分中药单体活性成分的开发利用,如丹参酮ⅡA 在水中的溶解度仅为2.8 ng/mL,半衰期仅为1~2 h[19],虽然纳米粒、脂质体、微球等现代制剂技术可在一定程度上克服这些困扰[20],但稳定性、溶解度问题依然突出。
生物碱是一类含氮的碱性有机化合物,是中药单体活性成分的重要组成部分,小檗碱、阿托品、茶碱、毛果芸香碱等已广泛应用与临床[21]。但大多数生物碱几乎不溶或难溶于水,导致其很难与亲水性基质的水溶液共混制备药物载体,只能以毒性相对较高的疏水性基质或价格较高的两亲性基质作为载体。
壳聚糖是一种廉价易得、性能优越的亲水性药物缓控释载体基质材料,其分子中含有游离氨基,在酸性溶液中易成盐,呈阳离子性质,在酸性环境中的溶解度高于在中性环境中[22],与生物碱的溶解特性相似,常用稀盐酸或稀醋酸作为溶剂,其酸性溶液可促进生物碱溶解,有利于后者与其共混制备各类药物载体。SPG 膜乳化技术制备壳聚糖微球技术成熟,操作简便,制备条件温和,无需高温高压,不会破坏药物成分,而且载药量高,易于规模化生产。
本实验发现,壳聚糖/盐酸小檗碱缓释微球的最优制备工艺为交联剂用量8 mL,混合搅拌时间112 min,体系温度44 ℃,包封率80.6%,载药量13.89%;微球在体外模拟胃液(pH=1.2)、肠液(pH=7.4)中都具有良好的缓释性能,持续释药时间超过24 h,释放均符合Peppas 模型和non-Fickian 扩散。由此可知,该微球可提高生物碱类成分在体液环境中的稳定性,并能减缓血药浓度波动,降低给药频率,提高生物利用度,为相关缓控释制剂研发提供实验依据。
