13X分子筛/凹凸棒土颗粒型复合材料吸附Zn2+的研究
2019-11-20徐积昀范先媛
刘 红,徐积昀,殷 萌,范先媛
(1. 武汉科技大学资源与环境工程学院,湖北 武汉,430081;2. 武汉科技大学冶金矿产资源高效利用与造块湖北省重点实验室,湖北 武汉,430081)
锌是一种储量较为丰富的重金属资源,广泛应用于金属加工、机械制造、镀锌工业、电池工业等众多领域[1],随着相关产业的快速发展,含锌废水的排放量也日益增加,而锌一旦进入环境后很难被生物降解,其中大多数参与食物链循环,并最终在生物体内积累,破坏生物体正常生理代谢活动,危害人体健康[2],因此含锌废水的有效治理一直是世界环保领域的重大研究课题。当前处理含重金属废水的方法主要有化学沉淀、电解、反渗透、吸附、离子交换以及电渗析等[3-4],其中,离子交换法和吸附法常用来对重金属浓度较低或经过中和沉淀的废水进行深度处理,离子交换法具有出水水质好、工艺简单等优点,但其实施成本较高,离子交换树脂需经预处理且易老化、易产生二次污染[5]。吸附法能耗低且操作简单,常以活性炭为吸附材料,而活性炭虽然对有机物吸附效果良好,其再生工艺却相当复杂且费用昂贵,对重金属离子的吸附能力也较弱,在此类吸附材料再生过程中还存在重金属回收困难等问题[6-7],因此,亟待研发吸附容量高且使用成本低的新型重金属吸附材料。
具有规则孔道结构的13X分子筛是一种人工合成硅铝酸盐晶体材料,其比表面积大、吸附性能强,并且骨架结构中含有带负电荷的铝氧四面体单元,通过静电引力可有效吸附去除水中的重金属离子污染物[8],但工业合成的13X分子筛为粉末状,直接作为吸附剂吸附重金属后难以从水中分离,从而产生大量含重金属的污泥,造成二次污染,所吸附重金属也不能得到有效回收,有鉴于此,本文以13X分子筛及天然黏土矿物凹凸棒土为原料,制备出吸附容量大且易与水分离的13X分子筛/凹凸棒土颗粒型复合材料,并对其微观形貌、晶相结构和比表面积等进行了表征,重点考察了复合材料煅烧温度对其吸附性能的影响,测试了复合材料对Zn2+的去除效果并分析了相应的吸附机理。
1 材料与方法
1.1 原料与试剂
200目13X分子筛,上海久宙化学品有限公司;200目凹凸棒土,安徽省明美矿物化工有限公司;羧甲基纤维素钠(CMC-Na),国药集团化学试剂有限公司;硝酸锌Zn(NO3)2·6H2O及硝酸(HNO3)均为分析纯,西陇化工股份有限公司。
1.2 样品的制备
将一定量的CMC-Na粉末溶于一定体积的去离子水中,经磁力搅拌后制得CMC-Na质量占比为0.7%的均匀溶液。按质量比6∶4称取13X分子筛和凹凸棒土,缓慢加入适量上述溶液,混合搅拌均匀后挤压成条状,置于105 ℃烘箱内烘干后破碎,借助20目及40目标准分样筛筛分出粒径为0.45~0.90 mm的颗粒,置于马弗炉中分别在不同温度条件下煅烧2 h,从而制得颗粒状13X分子筛/凹凸棒土复合材料。
1.3 样品的表征
在YHKC-3A型自动颗粒强度测定仪上测量样品颗粒强度,采用Tecnai G2 F30型透射电镜(TEM)及Nova 400 Nano型场发射扫描电镜(SEM)观察样品的显微组织,并结合能谱仪(EDS)对其微区成分进行分析,利用X’Pert Pro MPD型X射线衍射仪(XRD)对样品的物相组成及结构进行分析,使用ASAP 2020型比表面积分析仪测定样品的BET比表面积、孔体积、孔径分布等参数,借助VERTEX 70型傅里叶变换红外光谱仪(FTIR)表征样品表面官能团。
1.4 吸附实验
在室温下,使用Zn(NO3)2·6H2O配制一定Zn2+质量浓度的含Zn2+溶液,调节其pH值至5.5,取300 mL该溶液置于容量为500 mL的烧杯中,加入0.3 g所制复合材料,以200 r/min的转速搅拌一定时间后静置沉淀60 min,取其上清液,经0.45 μm的微孔滤膜过滤后,加1% HNO3酸化,采用novAA 350型全自动火焰原子吸收光谱仪测定其中的Zn2+浓度,则复合材料对Zn2+的平衡吸附量qe为
(1)
式中:C0和Ct分别为含Zn2+溶液中Zn2+的初始浓度及吸附时间为t时的浓度,mg·L-1;V为溶液体积,L;m为复合材料的质量,g。
2 结果与讨论
2.1 煅烧温度对复合材料吸附性能的影响
分别在300、400、500、550、600、700、800 ℃等不同温度条件下煅烧所制复合材料颗粒的抗压强度测试结果如表1所示。由表1可见,所制复合材料颗粒的抗压强度随着煅烧温度的升高而增大,且高温下增幅更大。

表1 不同煅烧温度下所制复合材料的抗压强度
在室温条件下,使用未煅烧及不同煅烧温度条件下所制复合材料分别处理Zn2+初始质量浓度为100 mg·L-1的溶液1 h,结果如图1所示。由图1可见,随着煅烧温度的升高,所制复合材料对Zn2+的吸附量呈不断减小趋势,当煅烧温度不高于550 ℃时,所制复合材料对Zn2+的吸附量相差不大;当煅烧温度超过550 ℃时,所制复合材料对Zn2+的吸附量迅速减小,尤其煅烧温度为800 ℃时所制复合材料对Zn2+的吸附量仅为5.23 mg·g-1。结合图2所示相关样品的SEM照片可知,在煅烧温度不高于550 ℃的条件下,所制复合材料由于脱去了其中的吸附水、沸石水及部分结晶水,使得内部孔体积增大,同时无序堆积的凹凸棒土针棒状晶束紧密地附着在13X分子筛表面(图2(a)),此时复合材料吸附能力较强,而煅烧温度过高会造成复合材料中大部分结晶水和结构羟基水脱除、内部孔道塌陷以及纤维束堆积[9](图2(b)),以至于分子筛结构被破坏,从而导致复合材料吸附能力下降。综合上述测试结果,选择煅烧温度为550 ℃时可兼顾复合材料的抗压强度及吸附性能。
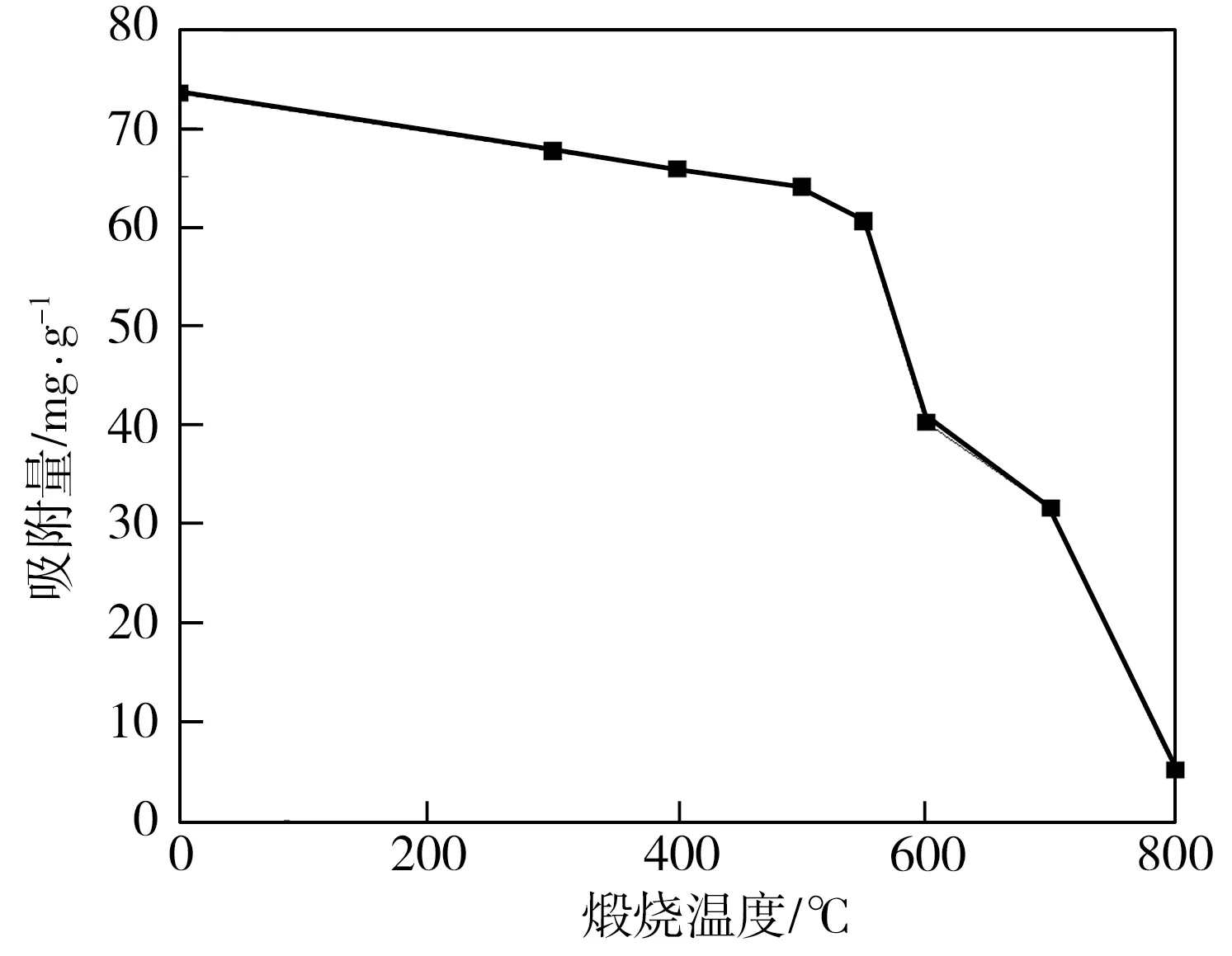
图1 不同煅烧温度下所制复合材料对Zn2+的去除效果
Fig.1 Removal effect of Zn2+by composites prepared at different calcination temperatures

(a)550 ℃煅烧

(b)700 ℃煅烧
2.2 样品的晶相结构及比表面积
13X分子筛、凹凸棒土、未煅烧及550 ℃煅烧所制复合材料的XRD测试结果如图3所示。由图3可见, 13X分子筛在2θ介于5°~40°之间出现多个尖锐的衍射峰,表明其结晶度较高,而凹凸棒土的结晶度相对较低,仅在2θ为8.2°、26.7°和31.0°处出现了较为明显的衍射峰,且峰强度较低,其中2θ为8.2°处的峰对应凹凸棒土的特征衍射峰,2θ为26.7°处的峰对应石英杂质的特征峰[10]。因为13X分子筛在2θ为26.7°和31.0°处也存在衍射峰,所以复合材料在相应位置的衍射峰应为13X分子筛与凹凸棒土的衍射峰叠加而成。此外,经550 ℃煅烧所制复合材料在2θ为8.2°处没有出现衍射峰,这是因凹凸棒土内部晶相经高温煅烧时被破坏所致[11]。13X分子筛的所有衍射峰在复合材料的XRD图谱中均有出现,只是峰强度有所降低,这应归因于复合材料中13X分子筛质量占比较低。由于复合材料中13X分子筛的晶相结构未遭破坏,因此仍能发挥其对重金属的良好吸附作用。

图3 样品的XRD图谱
图4为13X分子筛、凹凸棒土及550 ℃煅烧所制复合材料的N2吸/脱附等温线及孔径分布曲线,样品比表面积与孔结构参数测试结果如表2所示。由图4可见,粉末13X分子筛的N2吸/脱附等温线属于典型的Ⅰ型曲线[12],孔径分布主要集中在0~2 nm之间,表明13X分子筛属于微孔材料。凹凸棒土的N2吸/脱附等温线属于Ⅳ型曲线[12],且出现了滞后环,孔径主要分布在2~50 nm之间,故凹凸棒土属于介孔材料。从复合材料的孔径分布曲线可以看出,该材料既保留了分子筛的微孔和凹凸棒土的介孔,还存在一些因制备过程中二次成孔而形成的大孔,从而呈现出微孔-介孔-大孔兼具的多级孔道结构,这种多级孔道结构有利于重金属离子快速扩散至吸附点位。由表2可见, 13X分子筛比表面积高达712.70 m2·g-1,凹凸棒土的比表面积为121.52 m2·g-1,以二者为原料所制复合材料比表面积为442.95 m2·g-1,表明复合材料仍有足够大的比表面积提供吸附点位。同时注意到,复合材料的孔体积相比13X分子筛及凹凸棒土略大,这可能是因为煅烧使材料失去了表面吸附水和化学吸附水,导致其孔径增大所致。
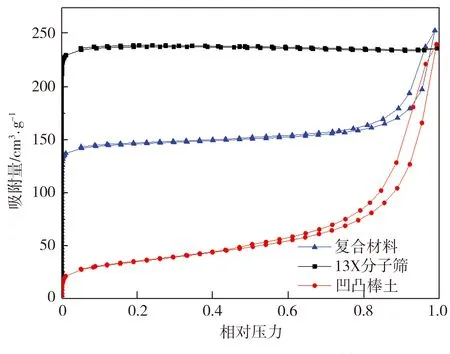
(a)N2吸/脱附等温线

(b)孔径分布曲线
Fig.4 N2absorption-desorption isotherms and pore size distribution curves of samples

表2 样品比表面积与孔结构参数
2.3 吸附动力学
分别向Zn2+初始浓度为20、50、100 mg·L-1的含Zn2+溶液中投加550 ℃煅烧所制复合材料,复合材料对Zn2+的吸附量随Zn2+初始浓度及吸附时间变化的规律如图5所示。由图5可见,在吸附反应初期,复合材料对Zn2+的吸附量增速较快,随着反应时间的延长,吸附量仍在增加但增幅逐渐变缓直至达到吸附平衡,之后再无明显变化;当吸附时间相同时,复合材料对Zn2+的吸附量随Zn2+初始浓度的增加而增大。该试验结果通过拟一级动力学和拟二级动力学进行拟合,拟一级动力学模型表达式为
ln(qe-qt)=lnqe-K1t
(2)
拟二级动力学模型表达式为
(3)
式(2)~式(3)中:t为吸附时间,min;qt为t时刻的吸附量,mg·g-1;K1为拟一级动力学速率常数,min-1;K2为拟二级动力学速率常数,g·mg-1·min-1。相关拟合参数见表3。从表3可知,在不同的Zn2+初始浓度条件下,拟二级动力学的相关系数R2均比拟一级动力学相应值R1更接近于1,表明拟二级动力学模型可以用于描述复合材料对溶液中Zn2+的吸附过程。
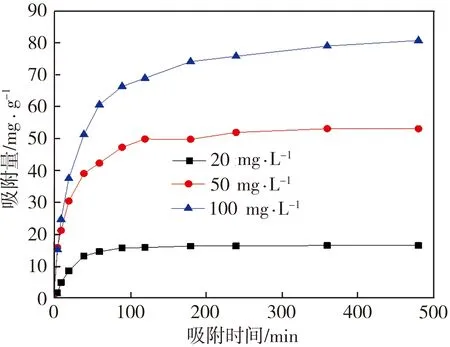
图5 吸附动力学曲线
为确定吸附过程中的扩散机制,采用Weber-Morris模型拟合试验结果,其方程表达式为
qt=Kidt0.5+C
(4)
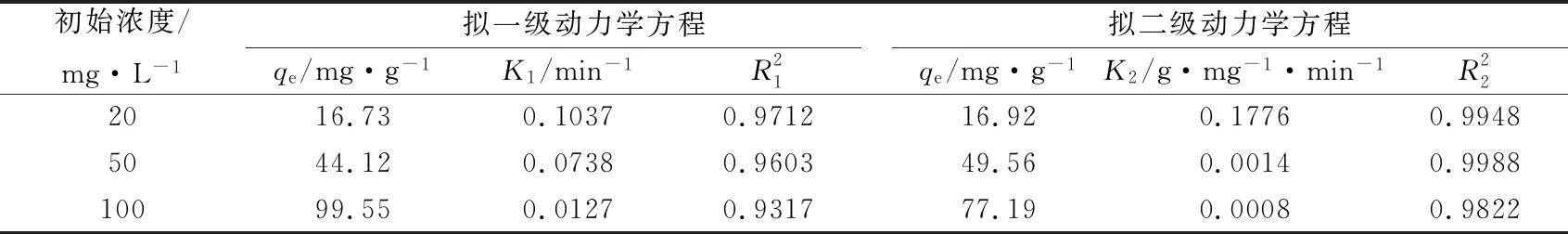
表3 吸附动力学参数
式(4)中:Kid为颗粒内扩散速率系数,mg·(g·min0.5)-1;C为与边界层厚度有关的常数,mg·g-1。Kid数值大小与内扩散速率成正比,数值越大表明吸附质越易在吸附剂内部扩散。拟合曲线及相关参数分别见图6及表4,表4中Rn为相关系数。从图6中可以看出,不同Zn2+初始浓度条件下的拟合曲线均可分为2个阶段,第1阶段直线斜率较大,吸附速率最快,主要为Zn2+由溶液至吸附剂表面的物质传递过程,阻力较小;第2阶段为吸附剂的颗粒内扩散阶段,此时吸附剂表面吸附基本完成,开始进入吸附剂内表面吸附,边界层阻力增大,吸附速率逐渐减小。此外,结合表4可知,qt与t0.5线性关系良好,但拟合曲线不经过原点,表明颗粒内扩散为主要的速控因素,但吸附速率同时还受颗粒外扩散的影响。

图6 Weber-Morris模型拟合曲线

表4 Weber-Morris模型拟合参数
2.4 等温吸附
图7为550 ℃煅烧所制复合材料对Zn2+的等温吸附曲线,分别采用Langmuir和Freundlich模型对其进行线性拟合,相关参数如表5所示,其中qmax为理论最大吸附量,KL为Langmuir方程常数,RT为相关系数,KF和n为Freundlich方程常数。由表5可见,基于Langmuir模型拟合的相关系数RT更接近1,远高于Freundlich模型相应值,这表明复合材料对Zn2+的吸附属于单层吸附且吸附剂表面均匀。由Langmuir模型计算得出550 ℃煅烧所制复合材料吸附Zn2+的饱和吸附量为99.01 mg·g-1。
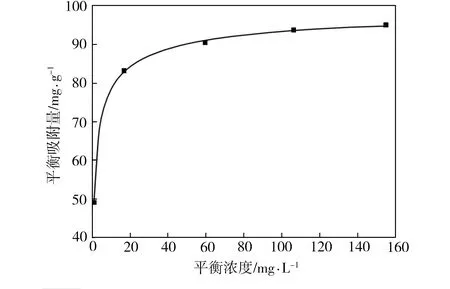
图7 等温吸附曲线
2.5 复合材料吸附Zn2+的机理
复合材料的主要成分是13X分子筛,其晶体结构中存在大量Na+离子,这些Na+可与溶液中的Zn2+发生离子交换。图8所示为550 ℃煅烧所制复合材料吸附水中Zn2+后单个晶粒的TEM照片及元素面扫描分析结果。由图8可见,复合材料吸附Zn2+之后,除少部分Na+未被交换外,其余Na+位置已被Zn2+占据。复合材料吸附Zn2+前后的扫描电镜背散射电子像及其中几种主要元素的EDS分析结果见图9。从图9中可以看出,吸附Zn2+后的复合材料表面覆盖着少许含有金属成分的团絮状物,EDS分析表明其中的锌含量达7.67%。
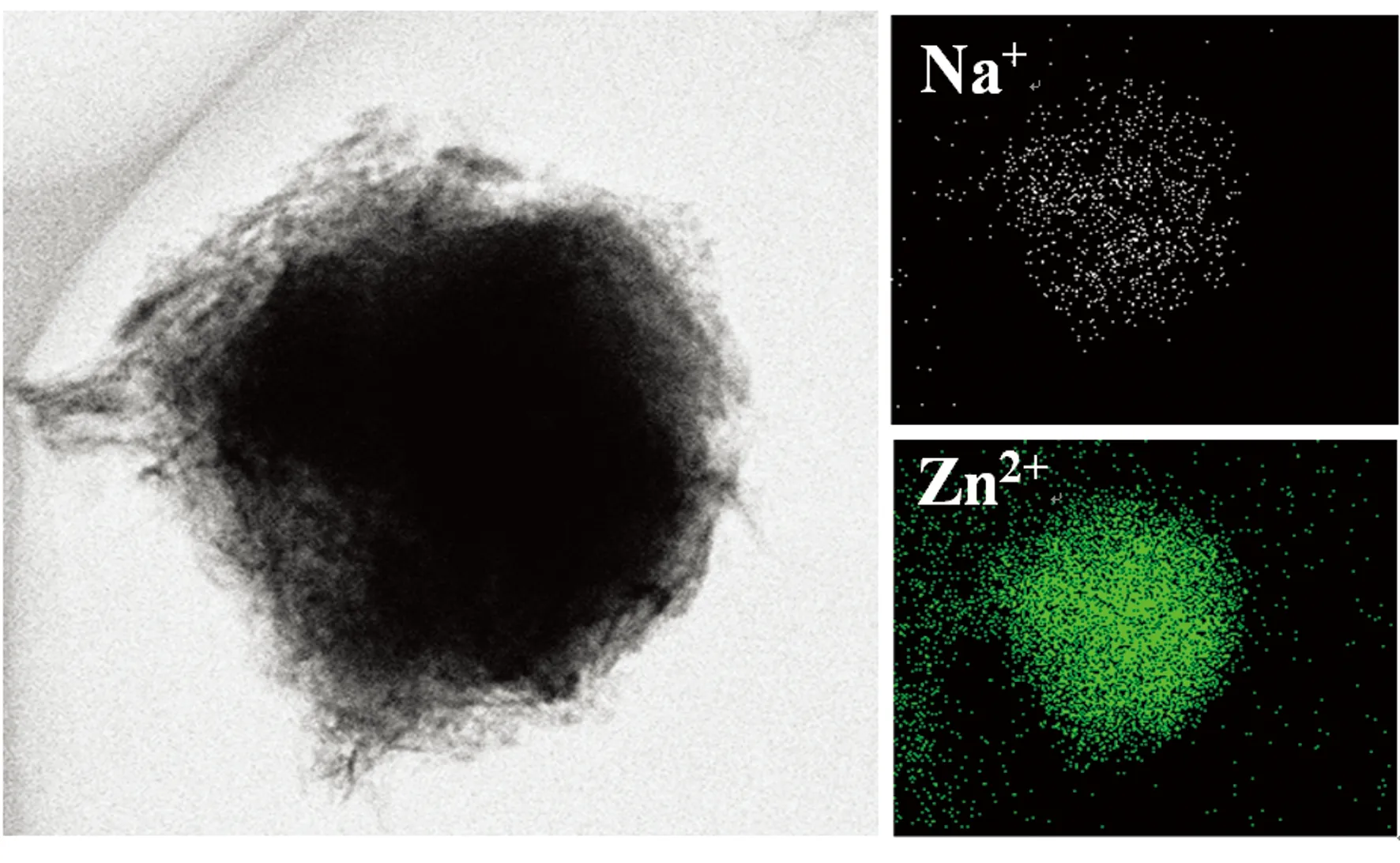
图8 TEM照片及元素分布
分别向Zn2+初始浓度不同的含Zn2+溶液中加入550 ℃煅烧所制复合材料,测定吸附平衡时溶液中的Na+和Zn2+浓度,复合材料中被交换的Na+与溶液中被吸附的Zn2+摩尔比计算结果如表6所示。从表6中可看到,在Zn2+初始浓度不同的情况下,被交换的Na+与被吸附的Zn2+摩尔比均为1.60左右,低于理论值2.00,表明复合材料实际吸附的Zn2+量高于理论值,因此除离子交换外,还有其它机制在复合材料吸附Zn2+的过程中发挥了作用。

(a)吸附前

(b)吸附后
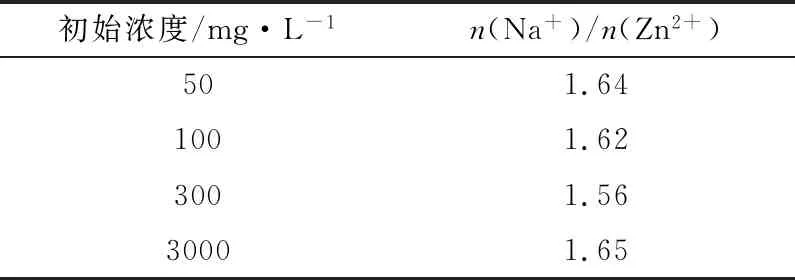
初始浓度/mg·L-1n(Na+)/n(Zn2+)501.641001.623001.5630001.65
550 ℃煅烧所制复合材料在吸附Zn2+前后的FTIR图谱如图10所示。由图10可见,吸附Zn2+后的复合材料在576 cm-1和1382 cm-1处出现的吸收峰为Zn(OH)2的羟基桥联振动峰,表明溶液中有部分Zn2+是以Zn(OH)2沉淀的方式被去除的。这是因为13X分子筛呈碱性,而凹凸棒土经高温煅烧后也会生成CaO、MgO等碱性氧化物,所以当Zn2+由于静电吸引作用到达复合材料表面时,就会在表面附近区域与材料解离出的OH-反应,生成Zn(OH)2沉淀沉积下来。因此,本研究所制复合材料去除溶液中Zn2+是离子交换和化学沉淀共同作用的结果。
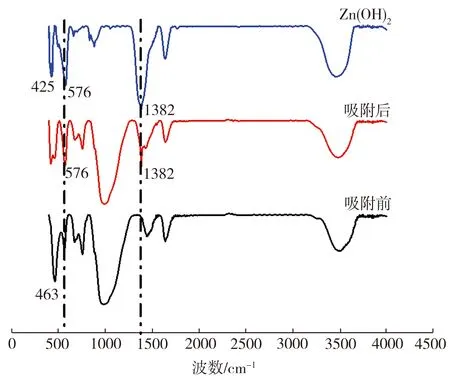
图10 吸附Zn2+前后的复合材料FTIR图谱
Fig.10 FTIR patterns of composite before and after adsorption of Zn2+
3 结论
(1)复合材料适宜的煅烧温度为550℃,所制复合材料具有微孔-介孔-大孔多级孔道,比表面积高达442.95 m2·g-1,孔体积为0.39 cm3·g-1。
(2)复合材料对Zn2+的吸附过程符合拟二级动力学,等温吸附实验数据符合Langmuir模型,最大吸附量为99.01 mg·g-1,吸附速率的主要控制步骤为颗粒内扩散机制。
(3)复合材料去除溶液中的Zn2+是离子交换和化学沉淀共同作用的结果。
