多指标正交设计优化黄芪半仿生提取工艺的研究
2019-11-14陈自泓黄可儿
陈自泓, 黄可儿
(1.广州中医药大学第一临床医学院,广东广州 510405;2.广州白云山星珠药业有限公司,广东广州510931;3.东莞广州中医药大学中医药数理工程研究院,广东东莞 523808)
黄芪为豆科植物蒙古黄芪Astragalus membranaceus(Fisch.)Bge var.mongholicus(Bge.)Hsiao或膜荚黄芪Astragalus membranaceus(Fisch.)Bge.的干燥根。其性甘,微温,归脾、肺经,具有补气升阳、固表止汗、利水消肿、生津养血、行滞通痹、托毒排脓、敛疮生肌的功效[1]。传统水提法对黄芪有效成分的获得率存在一定的局限性。而半仿生提取(SBE)法的提取过程模仿药物口服给药后在胃肠道中的运动、分解、吸收的过程,采用选定pH的模拟胃肠液,依次连续提取,得到中药材中目标成分含量高的活性混合物,既重视单体成分,又注重中药混合物成分的整体作用,能尽量多地保留有效成分,更符合中药在体内代谢和发挥药效作用的过程[2,3]。本研究以黄芪总多糖提取率、总皂苷提取率、提取收率作为综合评判指标,采用正交实验优选半仿生提取法模拟胃肠液的工艺条件,并与传统水提法进行比较,以期为黄芪多糖工业化生产提供理论数据,现将研究结果报道如下。
1 材料与方法
1.1药物与试剂黄芪经广州中医药大学中药鉴定研究室张丹雁教授鉴定为蒙古黄芪Astragalus membranaceus(Fisch.)Bge var.mongholicus(Bge.)Hsiao的干燥根。将黄芪切小段,60℃低温干燥,粉碎过80目筛,备用。D-无水葡萄糖对照品(批号:201707)、黄芪甲苷对照品(批号:201717),均为中国药品生物制品检定所产品;氯化钠(批号:20190105)、磷酸二氢钾(批号:20130901-1)、浓硫酸(批号:20190303)、氢氧化钠(批号:20190228)、浓盐酸(批号:20120106-1)、苯酚(批号:20100902-1)、95%乙醇(批号:20190301)、正丁醇(批号:20190202)、三氯甲烷(批号:20190301)均为广州化学试剂厂产品。
1.2仪器TC-15恒温电热表(海宁市华星仪器厂);SHA-B恒温震荡器(常州澳华仪器有限公司);TG16-WS台式高速离心机(湖南湘仪实验室仪器开发有限公司);LXJ-IIB低速离心机(上海安宁科学仪器厂);XHDLSB-1D/2D低温冷却循环泵(上海霄汉实业发展有限公司);METTLER TOLEDO XP26电子天平、BS 224S(万分之一)电子天平[赛多利斯科学仪器(北京)有限公司];Varian CARY-1E紫外可见分光光度计、电热恒温水浴锅(北京市永光明医疗仪器有限公司)。
1.3模拟胃液、模拟肠液的配制[4]模拟胃液配制:蒸馏水中加入2.0 g氯化钠和7 mL盐酸,再加入适量蒸馏水定容至1 L。模拟肠液配制:6.8 g磷酸二氢钾溶于250 mL蒸馏水中,再加入0.2 mol/L氢氧化钠溶液77 mL和500 mL蒸馏水,用0.2 mol/L氢氧化钠溶液或0.2 mol/L盐酸溶液调节pH为(6.8±0.1),加蒸馏水定容至1 L。
1.4方法
1.4.1 正交设计L9(34)试验设计 为保障试验的重复性与可比性,在黄芪药材前处理的工艺、模拟胃液、模拟肠液、过滤等条件相同的前提下,使用L9(34)正交设计表,确定了考察的主要因素及水平,见表1。
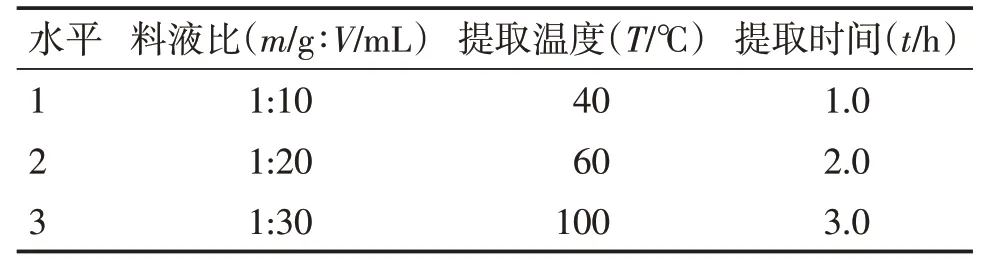
表1 模拟胃液和肠液正交设计的水平设置表Table 1 The orthogonaldesign table for the stimulated gastric and intestinal juice
1.4.2 供试液的制备 精密称取蒙古黄芪粉末4.0 g,溶解于模拟胃液和肠液中,按照表1的参数提取,分别得到模拟肠液及模拟肠液提取液。过滤,取续滤液30 mL,备用。
1.4.3 水提取法的样品溶液制备[5]取黄芪粉末2.0 g,精密称定,加水16 mL,100℃水浴1.5 h,提取3次。过滤,合并滤液,取续滤液30 mL,备用。
1.4.4 总多糖含量测定 以D-葡萄糖为对照品,采用苯酚—硫酸法显色,在检测波长490 nm处测定吸光度[4]。以吸光度Y为纵坐标、以D-葡萄糖浓度X[ρ/(mg·mL-1)]为横坐标,绘制标准曲线。回归方程为Y=14.469 0X-0.020 8,r=0.999 4。结果表明在0.01~0.075 mg/mL范围内线性关系良好。精密量取模拟胃液及模拟肠液供试液2.0 mL,置25 mL量瓶中,按上述方法显色,并于490 nm波长处测定吸收度,根据标准曲线计算总多糖含量。
1.4.5 总皂苷的含量测定[6]以黄芪甲苷为对照品,采用香草醛—硫酸法显示,在检测波长450 nm处测定吸光度。以吸光度Y为纵坐标、以总皂苷浓度X[ρ/(mg·mL-1)]为横坐标,绘制标准曲线。回归方程为Y=13.163 0X+0.086 5,r=0.997 7。结果表明在0.005~0.045 mg/mL范围内线性关系良好。精密量取模拟胃液和模拟肠液供试品1 mL,以甲醇稀释至适合的浓度后,按上述方法显色,于450 nm处测定吸收度,根据标准曲线测定总皂苷含量。
1.4.6 提取收率的测定 精密量取模拟胃液及模拟肠液样品溶液各10 mL,置已烘干恒质量的蒸发皿中,水浴蒸干,于105℃烘3 h,置干燥器内冷却40 min,迅速精密称质量并计算,以干固物百分比(%)计算提取收率。提取收率=(M2-M1)/[M样×(1-水分%)]×稀释位数×100%。M2指有样品的蒸发皿干燥恒质量后的质量(g);M1指蒸发皿恒质量后质量(g);M样指药材粉末样品的质量(g)。
1.4.7 数据分析 采用Microsoft office Excel 2000软件进行数据分析,实验数据进行直观分析、方差分析和加权分析,根据自由度v1=1,v2=4,查F界值表,F>7.71,P<0.05。设计总多糖提取率(w/%)、总皂苷提取率(w/%)、提取收率(w/%)按照30%、30%、40%进行加权分析。
2 结果
2.1在模拟胃液条件下应用L9(34)正交设计考察黄芪总多糖提取率、总皂苷提取率和提取收率
2.1.1 直观分析和方差分析 综合模拟胃液条件下黄芪总多糖提取率的直观分析和方差分析结果见表2、表3。直观分析结果显示,总多糖提取率的最佳工艺为A3B3C3,其中提取温度起主要作用,差异有统计学意义(P<0.01)。方差分析结果显示,对优化提取工艺的贡献度(F值)由大到小依次是提取温度(22.6)>料液比(3.85)>提取时间(0.10)。
综合模拟胃液条件下黄芪总皂苷提取率的直观分析和方差分析结果见表2、表4。直观分析结果显示,总皂苷提取率的最佳工艺为A3B3C3,其中料液比和提取温度起主要作用,差异均有统计学意义(P<0.05)。方差分析结果显示,对优化提取工艺的贡献度(F值)由大到小依次是提取温度(17.5)>料液比(16.0)>提取时间(0.3)。
综合模拟胃液条件下黄芪提取收率的直观分析和方差分析结果见表2、表5。直观分析结果显示,提取收率的最佳工艺为A3B3C3,其中料液比和提取温度起主要作用,差异均有统计学意义(P<0.05)。方差分析结果显示,对优化提取工艺的贡献度(F值)由大到小依次是提取温度(42.1)>料液比(17.0)>提取时间(3.46)。
2.1.2 贡献度加权分析 贡献度加权分析结果显示,加权后贡献度由大到小依次是提取温度(28.9)>料液比(12.8)>提取时间(1.5)。其中:料液比和提取温度起主要作用,差异均有统计学意义(P<0.05);提取时间作用次之,差异无统计学意义(P>0.05)。见表6。
2.2在模拟肠液条件下应用L9(34)正交设计考察黄芪总多糖提取率、总皂苷提取率和提取收率
2.2.1 直观分析和方差分析 综合模拟肠液条件下黄芪总多糖提取率的直观分析和方差分析结果见表7、表8。直观分析结果显示,总多糖提取率的最佳工艺为A3B3C2,其中料液比和提取温度起主要作用,差异有统计学意义(P<0.05)。方差分析结果显示,对优化提取工艺的贡献度(F值)由大到小依次是料液比(72.0)>提取温度(16.5)>提取时间(6.0)。
综合模拟肠液条件下黄芪总皂苷提取率的直观分析和方差分析结果见表7、表9。直观分析结果显示,总皂苷提取率的最佳工艺为A2B3C1,其中提取温度起主要作用,但差异无统计学意义(P>0.05)。方差分析结果显示,对优化提取工艺贡献度(F值)由大到小依次是提取温度(5.28)>提取时间(4.0)>料液比(1.0)。
综合模拟肠液条件下黄芪提取收率的直观分析和方差分析结果见表7、表10。直观分析结果显示,提取收率的最佳工艺为A3B3C3,其中料液比和提取温度起主要作用,差异均有统计学意义(P<0.05)。方差分析结果显示,对优化提取工艺贡献度(F值)由大到小依次是料液比(69.3)>提取温度(15.6)>提取时间(2.4)。
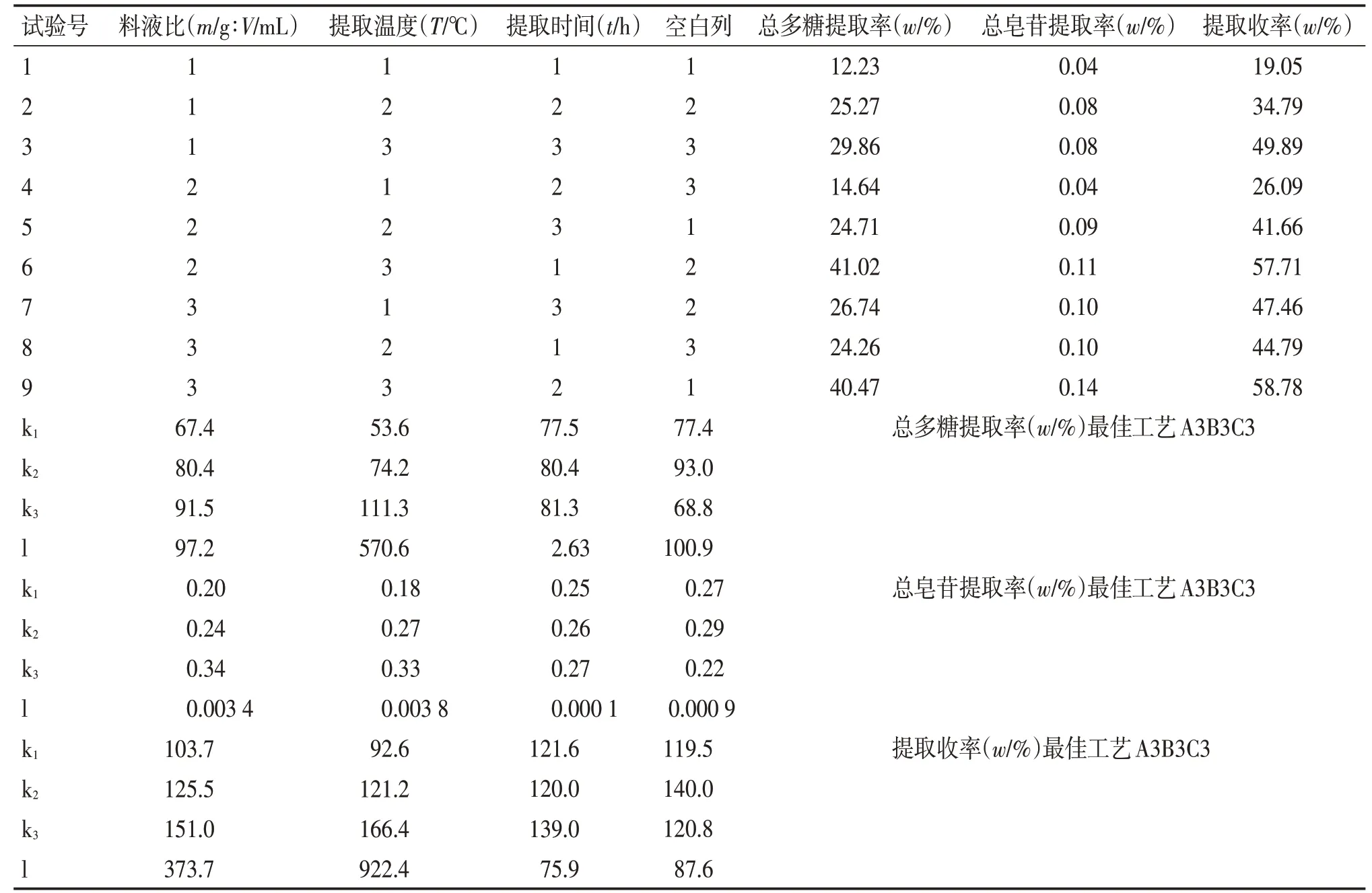
表2 在模拟胃液条件下L9(34)正交设计直观分析表Table 2 The intuitive analysis results of L9(34)orthogonaldesign under the simulated gastric juice conditions

表3 在模拟胃液条件下黄芪总多糖提取率(w/%)的方差分析表Table 3 The variance analysis results of extraction rate of totalpolysaccharide from Radix Astragali(w/%)under the simulated gastric juice conditions
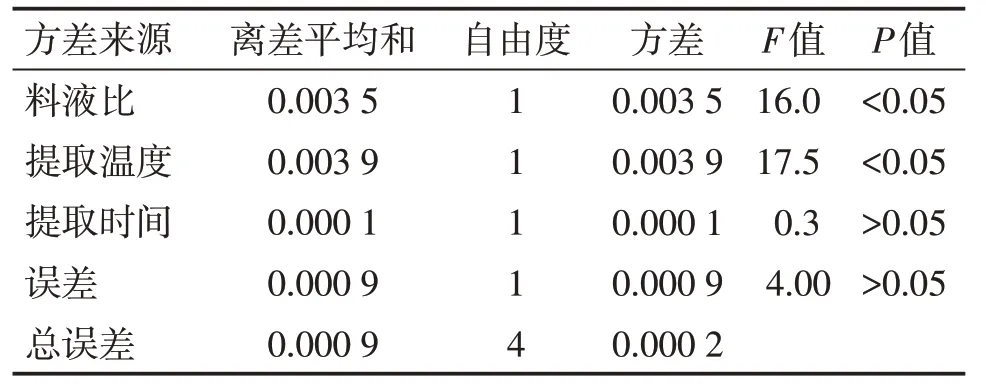
表4 在模拟胃液条件下黄芪总皂苷提取率(w/%)的方差分析表Table 4 The variance analysis results of extraction rate of totalsaponins from Radix Astragali(w/%)under the simulated gastric juice conditions
2.2.2 贡献度加权分析 贡献度加权分析结果显示,加权后贡献度由大到小依次是料液比(49.6)>提取温度(12.8)>提取时间(4.0)。其中:料液比、提取温度起主要作用,差异有统计学意义(P<0.05);提取时间作用次之,差异无统计学意义(P>0.05)。见表11。
2.3半仿生提取法与传统水提法的比较实验结果显示,半仿生提取法总多糖含量、提取收率较水提法显著升高,差异有统计学意义(P<0.01)。
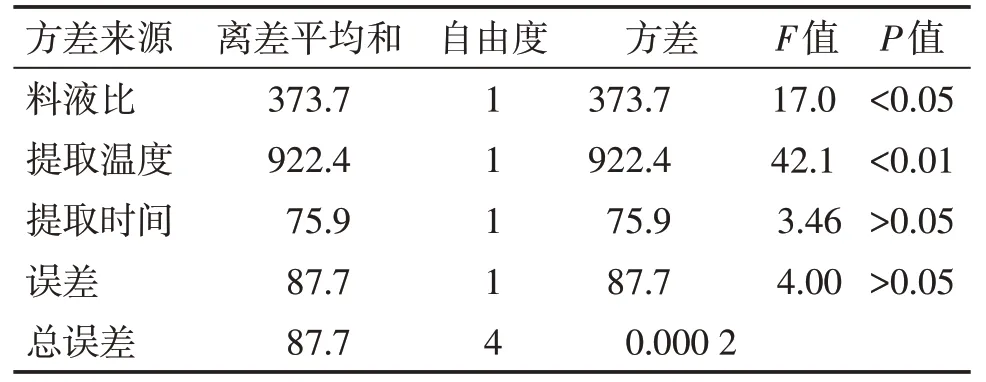
表5 在模拟胃液条件下黄芪提取收率(w/%)的方差分析表Table 5 The variance analysis results of extraction yield of Radix Astragali(w/%)under the simulated gastric juice conditions
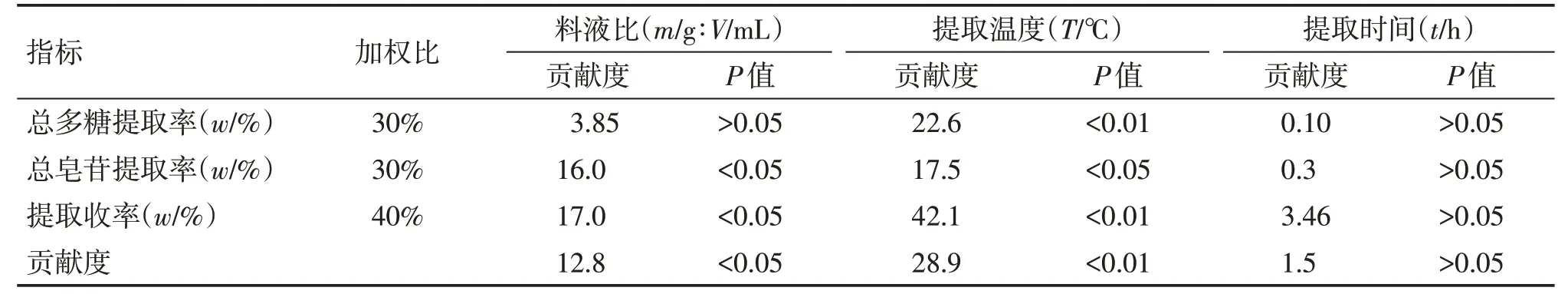
表6 在模拟胃液条件下三因素贡献度的加权分析Table 6 The weighted analysis results of three factor contribution under the simulated gastric juice conditions

表7 在模拟肠液条件下黄芪提取工艺L9(34)正交设计的直观分析表Table 7 The intuitive analysis results of L9(34)orthogonal design under the simulated intestinaljuice conditions
3 讨论
半仿生提取法以一种或几种有效成分、总提取物等作为指标,用选定pH的酸性水、中性水和碱性水依次连续提取,可充分发挥混合物成分的综合作用特点,又有利于单体成分控制制剂质量。料液比、提取温度、提取时间等都对半仿生提取法的提取效果具有一定影响。正交设计法是利用正交表的“均匀分布、整齐可比”的特点使每次实验的因素和水平得到合理的安排,从而通过对实验结果的分析获得较全面的信息,找出各因素的主次地位[7]。本研究采用L9(34)正交设计表对半仿生提取法的影响因素(料液比、提取温度、提取时间)进行工艺优化研究,对总多糖提取率、总皂苷提取率、提取收率等多指标进行综合分析以优化半仿生的提取工艺。
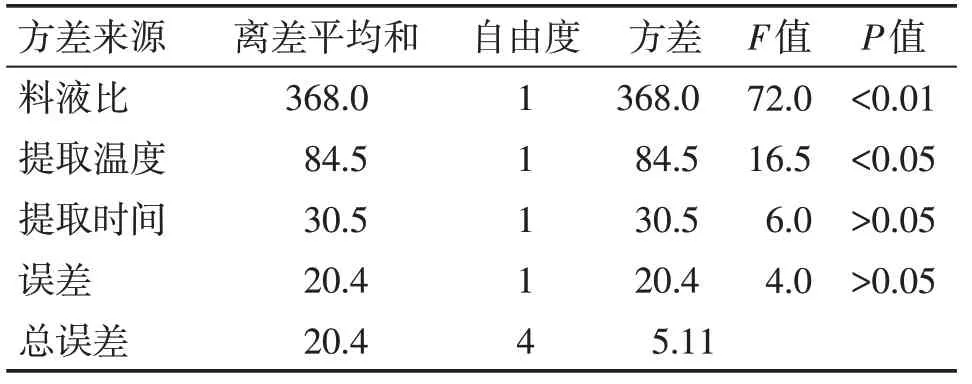
表8 在模拟肠液条件下黄芪总多糖提取率(w/%)的方差分析表Table 8 The variance analysis results of extraction rate of totalpolysaccharide from Radix Astragali(w/%)under the simulated intestinaljuice conditions

表9 在模拟肠液条件下黄芪总皂苷提取率(w/%)的方差分析表Table 9 The variance analysis results of extraction rate of totalsaponins from Radix Astragali(w/%)under the simulated intestinaljuice conditions

表10 在模拟肠液条件下黄芪提取收率(w/%)的方差分析表Table 10 The variance analysis results of extraction yield of Radix Astragali(w/%)under the simulated intestinaljuice conditions
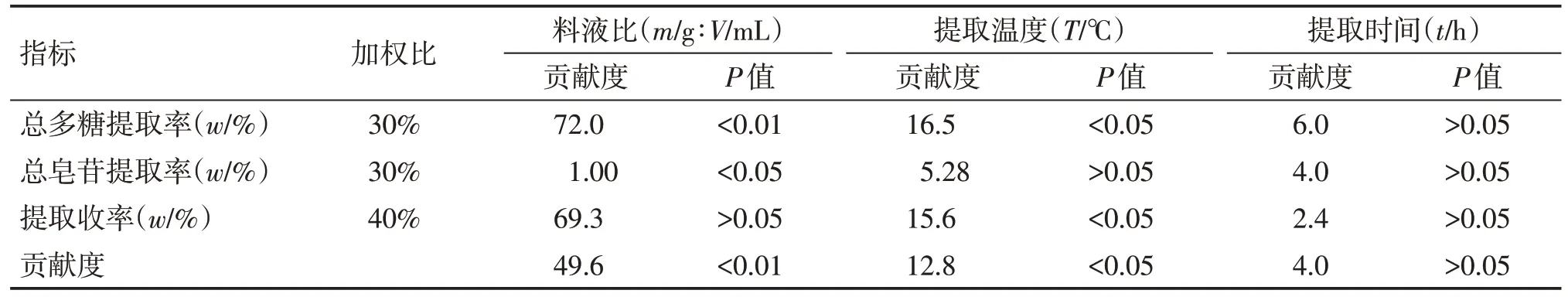
表11 在模拟肠液条件下三因素贡献度的加权分析Table 11 The weighted analysis results of three factor contribution under the simulated intestinal juice conditions
表12 半仿生提取法与传统水提法总多糖含量、总皂苷含量以及提取收率比较Table 12 Comparison of total polysaccharide content,totalsaponin content and extraction yield between semi-bionic extraction method and water extraction method (s)
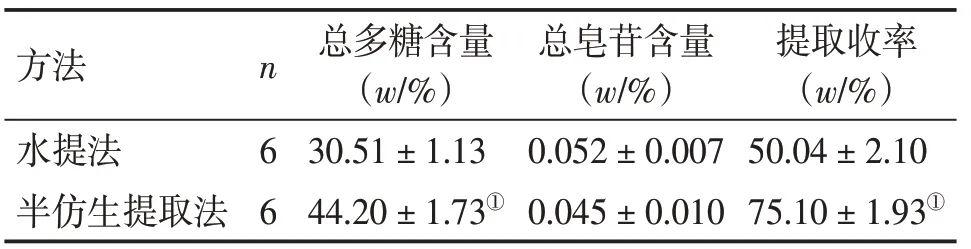
表12 半仿生提取法与传统水提法总多糖含量、总皂苷含量以及提取收率比较Table 12 Comparison of total polysaccharide content,totalsaponin content and extraction yield between semi-bionic extraction method and water extraction method (s)
①P<0.01,与水提法比较
方法水提法半仿生提取法提取收率(w/%)50.04±2.10 75.10±1.93①n 6 6总多糖含量(w/%)30.51±1.13 44.20±1.73①总皂苷含量(w/%)0.052±0.007 0.045±0.010
本研究结果显示:以黄芪总多糖提取率(w/%)、总皂苷提取率(w/%)、提取收率(w/%)作为指标,在模拟胃液提取条件下,加权后贡献度由大到小依次是提取温度(28.9)>料液比(12.8)>提取时间(1.5)。其中:料液比和提取温度起主要作用,差异均有统计学意义(P<0.05);提取时间作用次之,差异无统计学意义(P>0.05)。在模拟肠液提取条件下,加权后贡献度由大到小依次是料液比(49.6)>提取温度(12.8)>提取时间(4.0)。其中:料液比和提取温度起主要作用,差异均有统计学意义(P<0.05);提取时间作用次之,差异无统计学意义(P>0.05)。
综合以上研究结果得出,提取时间对黄芪总多糖提取率、总皂苷提取率、提取收率等3个指标的影响均不大,从经济效益的角度出发,可以考虑料液比为1∶30,提取温度为100℃,提取时间为1 h。半仿生提取法优选工艺黄芪总多糖提取率、提取收率等2个指标明显优于传统水提法,差异有统计学意义(P<0.01)。
半仿生提取法与传统水提法的区别主要在于提取溶剂。半仿生提取法使用酸性溶剂或碱性溶剂进行提取,目前工业产业化已有使用耐酸耐碱的提取设备如搪瓷提取罐对中药有效成分进行酸提或碱提,因此半仿生提取法产业化已具备技术可行性。另外,从经济效益角度分析,半仿生提取法的黄芪总多糖总提取率及得率均优于传统水提法,采用半仿生提取法提取黄芪总多糖可在一定程度上降低原材料成本。
