EMA/FDA药物安全信息
2019-11-13
影像诊断与介入放射学 2019年5期

——欧洲药品管理局(EMA)决定限制线性钆对比剂的使用
·脑部钆沉积现象已通过质谱和脑组织信号增强得到确认
·体外研究和非临床研究均显示,线性钆对比剂中的钆从配体分子游离的倾向远远大于大环状钆对比剂
·在欧盟范围内,撤销静脉用线性对比剂钆双胺、钆弗塞胺,以及钆喷酸葡胺静脉剂型的上市许可
·由于钆塞酸二钠,钆贝葡胺的部分肝代谢,这两种静脉用线性钆对比剂可继续用于肝脏扫描
·由于用药剂量很小,钆喷酸葡胺的关节内剂型可继续使用
·经审核后的所有大环状钆对比剂(钆特酸葡胺、钆布醇、钆特醇)均可继续使用
——美国食品和药物管理局(FDA)警告需要添加钆沉积警告信息
·FDA 要求钆对比剂药品说明中就钆沉积的问题对卫生健康专业人员与患者提出警示, 并通过更新病人用药指南、要求病人在用药前阅读教育信息等措施尽可能减少这一问题带来的影响。
·钆沉积高风险人群包括终身需多次使用GBCAs 的患者、孕妇、儿童和炎症性疾病患者。
·与大环状钆对比剂相比,线性钆对比剂会导致更多、持续时间更长的钆沉积。
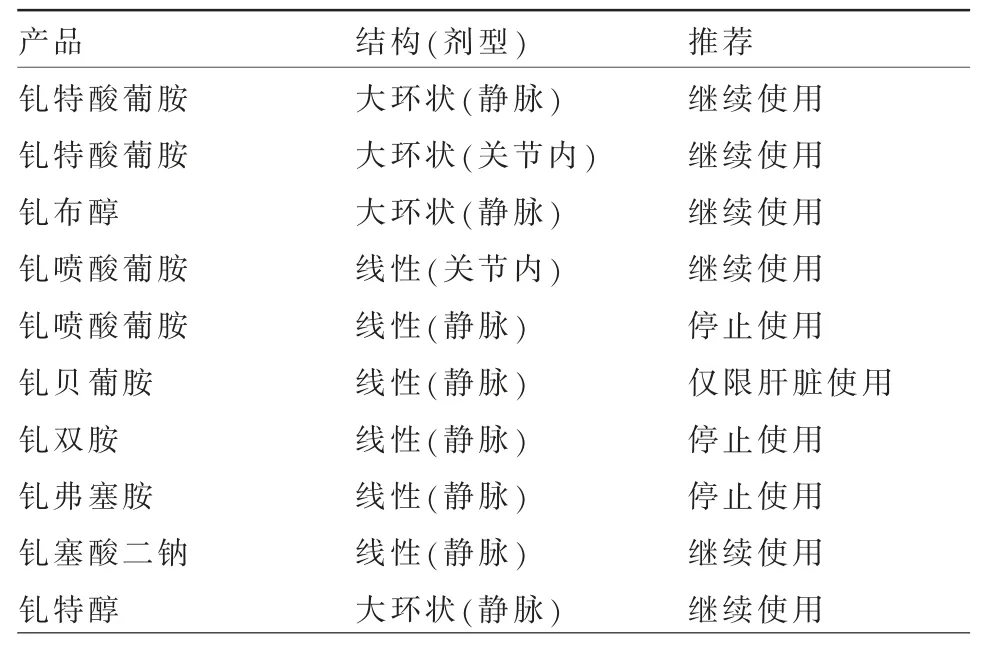
EMA 的建议

FDA 对不同类型钆对比剂的评价
1.http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/referrals/Gadolinium containing_contrast_agents/human_referral_prac_000056.jsp&mid=WC0b01ac05805c516f
2.https://www.fda.gov/Drugs/DrugSafety/ucm559007.htm