活性炭吸附ADN过程的动力学与热力学
2019-11-11潘永飞汪营磊刘卫孝赵宝东
潘永飞,汪营磊,刘卫孝,赵宝东,陈 斌
(西安近代化学研究所,陕西 西安 710065)
引 言
二硝酰胺铵(ADN)是一种新型高能氧化剂,可作为炸药和固体推进剂的氧化剂[1-3]。与高氯酸铵(AP)、硝酸铵(AN)相比,ADN具有能量特性高、特征信号低和绿色环保等优点,被认为是下一代推进剂的候选氧化剂之一,广泛应用于高能、无烟、低特征信号的固体火箭推进剂[4-8]。
目前,关于ADN分离纯化方面的动力学与热力学研究鲜有报道,本研究采用活性炭吸附法对ADN分离纯化进行了动力学与热力学分析,通过不同温度下的静态吸附实验,研究了活性炭吸附ADN的动力学和热力学特征,分别利用准一级动力学模型、准二级动力学模型和颗粒内扩散模型考察了ADN的吸附动力学,并利用Langmuir和Freundlich吸附等温模型对ADN的吸附热力学行为进行了描述,该研究可为ADN分离纯化工艺优化研究提供理论依据。
1 实 验
1.1 试剂与仪器
活性炭(根据不同比表面积选取3种:AC、BC、CC),工业品,上海兴长活性炭有限公司;二硝酰胺铵(ADN),纯度≥99.8%,西安近代化学研究所;硝酸铵(AN),分析纯,斯百全化学(上海)有限公司;硫酸铵(AS),分析纯,广州卡芬生物科技有限公司。
LC-10A高效液相色谱仪、AY-120精密电子天平,日本岛津公司;UV-1800型紫外可见分光光度计,上海仪电科学仪器股份有限公司;色谱柱,Phenomenex Gemini C-18 (250mm×4.6mm×5μm)。
1.2 标准溶液制备
用电子天平准确称取50.0mg ADN标准品,精确至0.0001g,用2.0mL 蒸馏水溶解,并定容至5.0mL容量瓶中,冷冻保存。分别取0.5、1.0mL上述标准溶液至1.0 、10.0mL容量瓶中,用蒸馏水定容,混匀后配制成质量浓度为1000、5000、10000mg/L的系列标准溶液;分别取1000mg/L的标准溶液10、50、100、500 μL至1.0mL的容量瓶中,用蒸馏水定容。混匀后配置成质量浓度为10、50、100、500mg/L的系列标准溶液。
用电子天平准确称取50.0mg AN标准品,精确至 0.0001g,用2.0mL 蒸馏水溶解,并定容至5.0mL容量瓶中,冷冻保存。分别取100、500、800μL上述标准溶液至1.0mL容量瓶中,用蒸馏水定容至1mL,混匀后配制成质量浓度为1000、5000、8000、10000mg/L的系列标准溶液;再准确量取1000mg/L ADN标准溶液100μL用蒸馏水定容至1.0mL容量瓶中,制成100mg/L标准溶液。
1.3 试验方法
由于硝酸铵是ADN合成过程中的副产物,也是ADN的分解产物,通过实验建立了利用反向高效液相色谱法测定ADN母液中ADN与AN含量的分析方法。对以上标准品溶液分别取0.5mL,进行HPLC分析,进样1μL,按上述色谱条件进行HPLC分析,以峰面积Y对质量浓度X进行线性回归,分别绘制ADN、AN标准曲线,然后利用标准曲线计算ADN溶液中ADN和AN的质量浓度。
色谱条件:Phenomenex Gemini C-18色谱柱(250mm×4.6mm×5μm),流动相为A(0.1%三氟乙酸-水溶液)-B(甲醇),柱温为30℃,流速为1mL/min,进样量为1μL,ADN和AN的检测波长分别为280nm和230nm。
1.4 吸附量的测定
取100mL烧杯3个,每个烧杯中均加入稀释10倍的10mL ADN母液,质量浓度为3015.53mg/L,取5mL活性炭(质量约为1.74g),加入已备好的ADN母液中,室温下充分搅拌10min。随后静置使其充分吸附,并开始计时,在充分吸附后的10、20、30、60、90、120min,分别取烧杯中ADN母液进行HPLC分析,分析方法同样为上述色谱方法,进样量1μL,利用标准曲线法计算其中ADN质量浓度,按下式计算3种活性炭的吸附量和吸附率:
(1)
(2)
(3)
式中:qt为t时刻的吸附量,mg/g;qe为平衡吸附量,mg/g;c0为吸附前溶液的质量浓度,mg/mL;ct为吸附t时刻溶液的质量浓度,mg/mL;ce为吸附平衡时溶液的质量浓度,mg/mL;VL为溶液的体积,mL;m为活性炭质量,g;Yt为t时刻的吸附率,%。
1.5 吸附动力学测定
准确称取5mL(1.74g)活性炭于100mL烧杯中,加入稀释10倍的10mL ADN母液,质量浓度为3015.53mg/L,恒温下充分搅拌,随后静置使其充分吸附,定时取样,检测ADN质量浓度的变化,计算吸附量,重复3次求平均值。
1.6 吸附热力学测定
取100mL烧杯5个,分别加入ADN母液、稀释2倍的ADN母液、稀释5倍的ADN母液、稀释10倍的10mLADN母液(编号分别为ADN母液、ADN/2、ADN/5、ADN/10),母液质量浓度为30155.3mg/L,取活性炭5mL(1.74g),分别加入已备好的ADN母液中,分别在常温(28℃)、40℃和50℃下充分搅拌。随后静置使其充分吸附,并开始计时。在充分吸附后的10、20、30、60、90、120min,分别取烧杯中ADN母液进行HPLC分析,利用标准曲线法计算其中ADN的质量浓度,重复3次求平均值。
2 结果与讨论
2.1 标准曲线的建立
对上述标准品溶液分别取0.5mL,进行高效液相色谱(HPLC)分析,进样1μL。以峰面积Y对质量浓度X进行线性回归,分析获得:
ADN标准曲线:Y=84.17997+1.75319X,R2=0.99984;
AN标准曲线:Y=129.51554+0.46575X,R2=0.99941。
回归方程的系数接近于1,表明实验条件及选定质量浓度范围内,紫外检测器对ADN和AN的响应值与质量浓度线性关系良好。
2.2 活性炭的筛选
根据活性炭的特性及前期经验,选取3种活性炭(依次编号为AC、BC、CC)进行了静态吸附和解析实验。结果显示活性炭AC、BC、CC的平衡吸附量分别为12.61、11.28、10.98mg/g,吸附率分别为72.78%、65.07%、63.37%,吸附能力大小顺序为:AC>BC>CC。根据吸附实验结果对比分析可知,AC活性炭对ADN的分离纯化最为适宜。
2.3 吸附动力学研究
2.3.1 活性炭对ADN吸附能力的微观解释
为了从微观层面揭示活性炭对ADN吸附能力的差异,对所用的3种活性炭分别进行BET分析。3种活性炭样品的比表面积和孔尺寸分布通过自动化N2吸附仪在77.3K进行测定,样品在测试前经过150℃脱气11h。N2吸附—脱附等温线及孔径(d)分布曲线见图1。

图1 3种活性炭N2吸附—脱附等温线及孔径分布曲线Fig.1 N2 adsorption—desorption isotherms and poresize distribution curves of three kinds of activated carbons
由图1可以看出,3种活性炭的吸附等温线在p/p0<0.05时,吸附量有一个明显的增加,之后上升较慢,在p/p0>0.2后几乎成水平,这是典型的微孔材料吸附特征。从BJH孔径分布图也可以看出,3种活性炭的孔径均为微孔,几乎没有介孔。
比表面积、孔的体积分布及孔的尺寸分布分别采用不同方法、在不同的相对压力(p/p0)下测定吸附体积(Va)获得。孔体积(Vp)是在p/p0等于0.998的条件下通过测定气体的吸附体积(Va)获得,分析结果见表1。
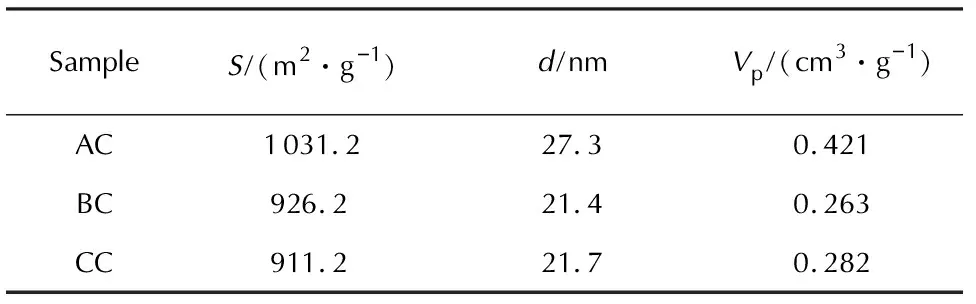
表1 3种活性炭的BET分析结果
注:S为比表面积;d为平均孔径;Vp为孔体积。
从表1可知,活性炭AC具有最大的比表面积、平均孔径与孔体积;活性炭BC的比表面积比CC略大,平均孔径和孔体积两者差别不大。一般而言,比表面积越大,吸附能力越大。因此,活性炭AC的吸附能力最大,这与静态吸附实验结果一致。
2.3.2 ADN在活性炭上的吸附动力学曲线
在25~40℃温度内,分别采用准一级吸附动力学模型、准二级吸附动力学模型和颗粒内扩散模型分析3种活性炭对ADN的吸附过程。
(1)准一级吸附动力学模型(Lagergren模型,用于液固吸附时最为常见):

(3)
式中:qt为t时刻的吸附量,mg/g;qe为平衡吸附量,mg/g;k为吸附速率常数。
分离变量,积分变换得:
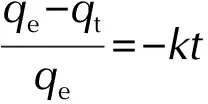
(4)
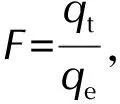
(5)
通过准一级吸附动力学模型分析3种活性炭对ADN的吸附过程,其动力学模型参数见表2,吸附量随时间的变化以及拟合结果见图2。

表2 3种活性炭吸附速率常数
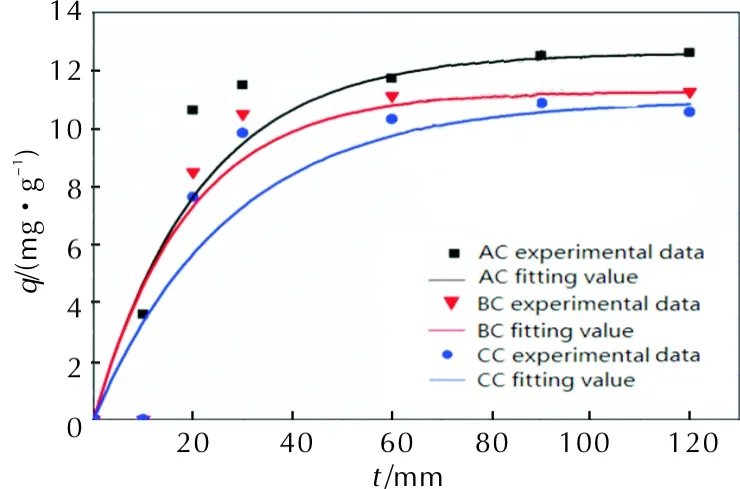
图2 3种活性炭模拟吸附动力学曲线Fig.2 Simulated adsorption kinetic curves of three kinds of activated carbons
从表2和图2可以看出,ln(1-F)与t的线性关系较差,准一级吸附动力学模型不能很好地反应3种活性炭对ADN的吸附过程。
(2)准二级吸附动力学模型(假定吸附速率受化学吸附机理控制,这种化学吸附涉及到吸附剂与吸附质之间的电子公用或电子转移):
(6)
式中:qt为t时刻的吸附量,mg/g;qe为平衡吸附量,mg/g;k为吸附速率常数。
采用准二级吸附动力学模型对实验数据进行拟合,拟合结果见表3和图3。

表3 3种活性炭在准二级吸附动力学模型中的吸附速率常数
注:C为截距;q为平衡吸附量。
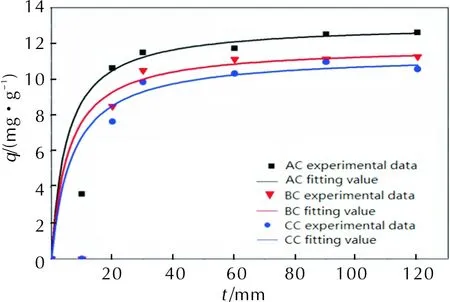
图3 3种活性炭在准二级吸附动力学模型中的模拟吸附动力学曲线Fig.3 Simulated adsorption kinetic curves of three kinds of activated carbons in quasi-secondary adsorption kinetics model
从表3和图3可以看出,t/qt与t线性关系较好,准二级吸附动力学模型能较好地反应3种活性炭对ADN的吸附过程。
(3)颗粒内扩散模型(Weber and Morris模型)
颗粒内扩散模型常用来描述吸附质与吸附剂之间的作用机理,采用粒子扩散模型对可能存在的粒子内扩散进行探讨,初始粒子内扩散速率通过方程进行线性拟合,拟合曲线提供了一种多重线性关系,表明有两个或更多的阶段发生。其数学表达式为:
qt=kipt1/2+C
(7)
式中:kip为粒子内扩散速率常数;C为截距。
采用颗粒内扩散模型对实验数据行进拟合,拟合结果如表4和图4所示。

表4 3种活性炭在颗粒内扩散模型中的吸附速率常数

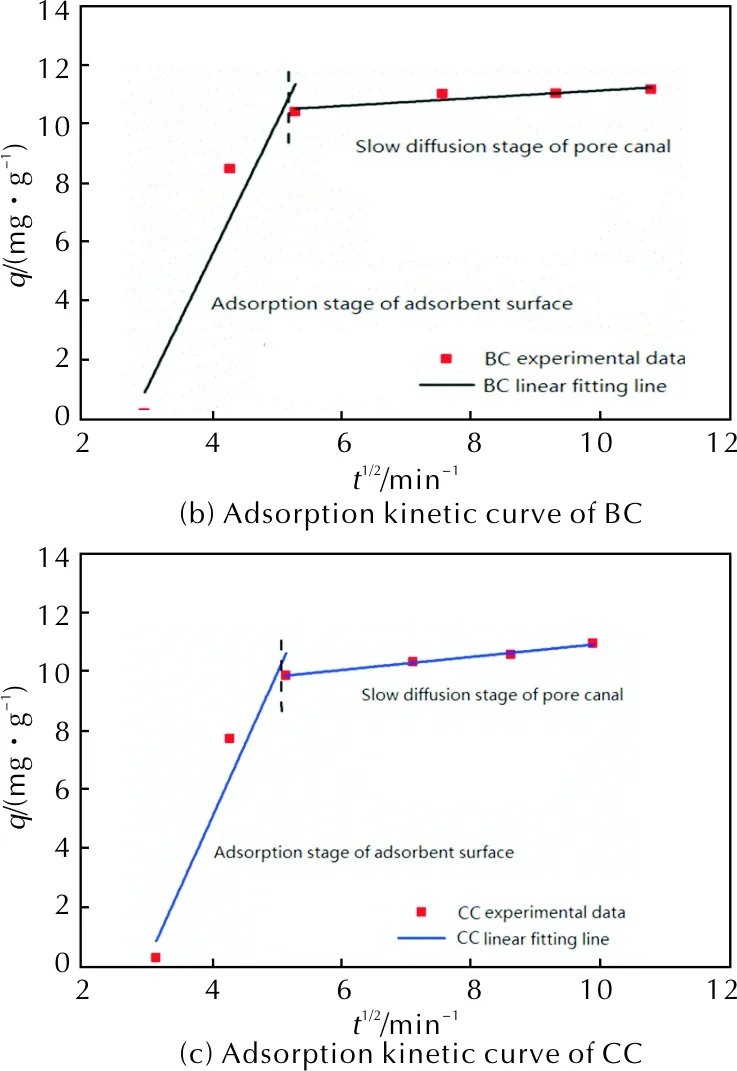
图4 3种活性炭在颗粒内扩散模型中的吸附动力学曲线Fig.4 Adsorption kinetic curves of three kinds of activated carbons in intra-particle diffusion model
从表4和图4可以看出,颗粒内扩散模型不能很好地反应3种活性炭对ADN的吸附过程。采用粒子内扩散模型进行拟合,两条拟合曲线都不经过原点,说明内扩散不是控制吸附过程的唯一步骤;对于活性炭AC,前20min以表面吸附为主,20min以后以颗粒内扩散为主;对于活性炭BC和CC,前30min以表面吸附为主,30min以后以颗粒内扩散为主。
通过以上准一级吸附动力学模型、准二级吸附动力学模型和颗粒内扩散模型的模拟结果可知,准二级吸附动力学模型能较好地描述3种活性炭对ADN的吸附过程(R2>0.99)。在吸附前期,吸附速率相对较大,随着吸附的进行,吸附速率逐渐降低,吸附过程可以分成3个阶段:(1)0~30min,吸附量迅速增大,说明活性炭上有大量的吸附位点;(2)30~80min,吸附量增长变缓并逐渐接近平衡;(3)80~120min,吸附已达到平衡,此后,溶液中的AND质量浓度和吸附量基本不变。前20min由于ADN与活性炭表面充分接触,ADN迅速被活性炭孔径吸附,当大部分的孔径被ADN分子占据后,分子间的排斥力使ADN难于被吸附,需要较长的时间才达到吸附平衡。
2.4 吸附热力学研究
2.4.1 吸附等温线
活性炭对不同质量浓度和不同温度下的ADN的吸附行为可以用吸附等温线来描述。实验中测定了28、40、50℃下AC活性炭对ADN的吸附等温线,结果见图5。
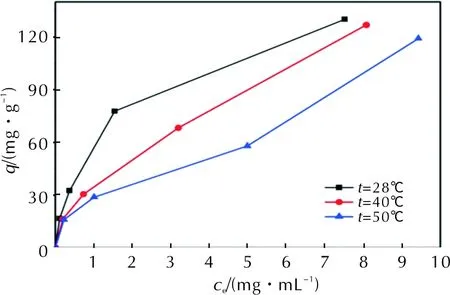
图5 活性炭AC对ADN的吸附等温线Fig.5 Adsorption isotherm of ADN on activated carbon AC
由图5可知,活性炭AC的平衡吸附量随着AND质量浓度的增加而增加,同时在28~50℃范围内吸附量随着温度的升高而降低。
2.4.2 吸附等温方程
当吸附剂在液相中进行吸附时,实质上是溶剂与被吸附组分对吸附剂的竞争,当溶剂的吸附作用可以忽略时,则吸附体系可以按单组分吸附来处理。Langmuir和Freundlich吸附等温线模型是吸附分离研究中最常用的2种吸附等温线模型[11]。其中,Langmuir模型是基于吸附剂的表面只能发生单分子层吸附的假设提出的,其液相吸附表达式为:
This room is twice as large as that one. 这个房间是那个房间的两倍大。
(8)
式中:qm为饱和吸附量,mg/g;qe为平衡吸附量,mg/g;KL为Langmuir等温方程常数;ce为吸附平衡时溶液的质量浓度,mg/mL。
Freundlich模型描述的也是单分子层吸附,但这种模型考虑了实际固体表面的非均一性,吸附剂表面覆盖程度的不同对吸附热的影响,提供了一种单组分吸附平衡的经验描述:
lgqe=lgKF+(1/n)lgce
(9)
式中:qe为平衡吸附量,mg/g;KF、n为Freundlich等温方程常数;ce为吸附平衡时溶液的质量浓度,mg/mL。
分别采用Freundlich和Langmuir等温吸附方程对28、40和50℃温度下的吸附平衡实验数据进行拟合,结果如图6所示。拟合得到Langmuir和Freundlich等温吸附方程的相关参数如表5所示。

表5 不同温度下的吸附等温方程
由图6和表5可知,用Freundlich方程能较好地描述活性炭AC在溶液中对ADN的吸附过程,说明ADN在活性炭AC上的吸附是单分子层吸附,但活性炭的表面不均匀,所以不能用Langmuir方程描述吸附过程。Freundlich方程中的n值是吸附剂表面非理想性的指标,Freundlich方程模拟的活性炭AC吸附等温线如图7所示。一般情况下,1/n在0.1~0.5之间,吸附较易发生;1/n在0.5~1之间,吸附较难发生;1/n大于1,吸附几乎无法发生。通过Freundlich方程拟合可以看出,在28℃和40℃下,活性炭AC拟合的1/n均小于0.5,说明40℃以下,活性炭AC是ADN的良好吸附剂;当吸附温度达到50℃时,1/n大于0.5,活性炭AC的吸附能力下降,所以吸附操作应维持在40℃以下。
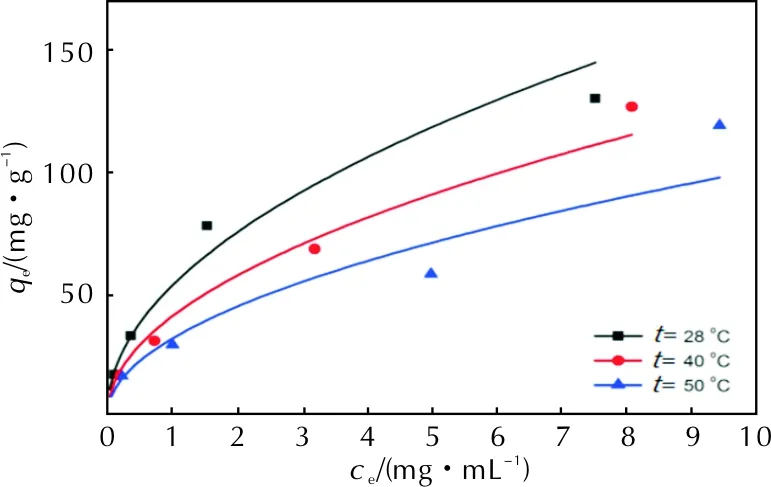
图7 Freundlich方程模拟活性炭AC的吸附等温线Fig.7 Simulated adsorption isotherms of activated carbon AC by using Freundlich equation
2.4.3 吸附热力学参数
吸附焓变与吸附量有密切关系,当吸附量固定在一个定值时,所推导出的焓变称为等量吸附焓变。吸附过程的吸附焓变△H、自由能变△G、熵变△S可按下述公式计算[15-16]:
(10)
ΔS=(ΔH-ΔG)/T
(11)
(12)
根据公式(10),以lnCe对1/T作图,见图8。根据直线斜率求得△H,然后分别由公式(11)和(12)计算得△S和△G,计算结果见表6。
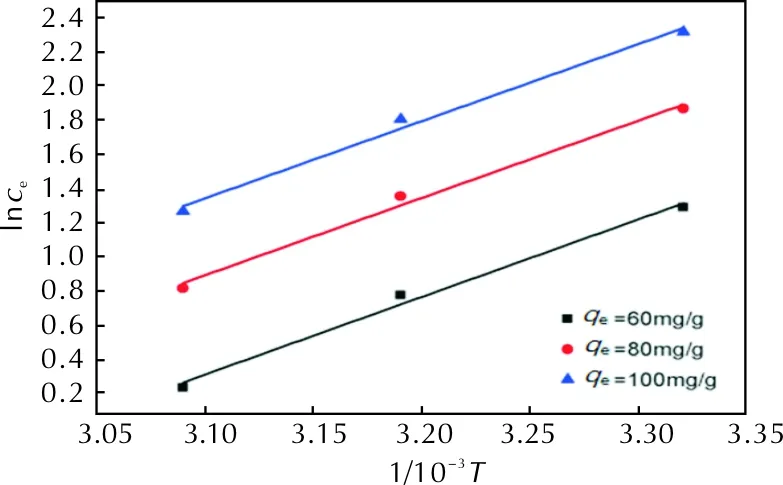
图8 ADN在活性炭AC上的等量吸附焓变Fig.8 Determination of equivalent adsorption enthalpy change of ADN on activated carbon AC
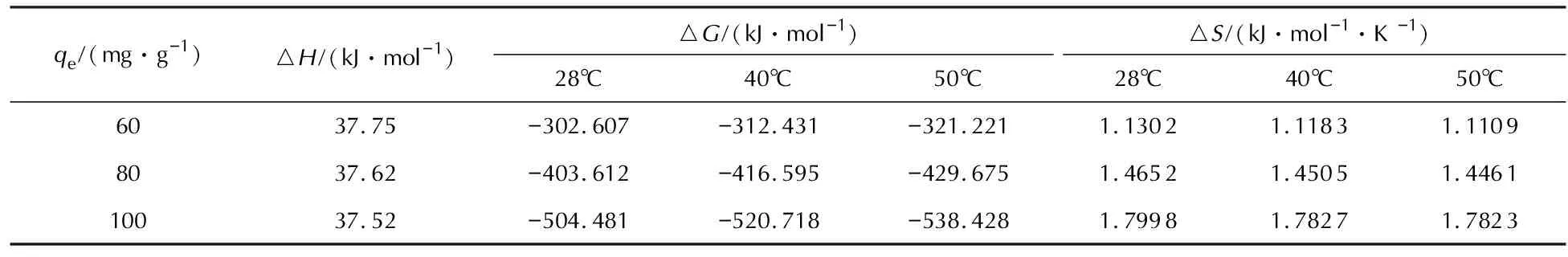
表6 ADN在活性炭AC上吸附过程的热力学参数
从表6可以看出,ADN在活性炭AC上的吸附吉布斯自由能△G均为负值,而吸附熵变△S均为正值,这表明吸附过程可自发进行。不同吸附量下的吸附焓变△H均大于零,表明ADN在活性炭AC上的吸附为吸热过程。所以,整个吸附过程不是一个完全的物理吸附过程,而是在物理吸附的同时伴有少量的化学吸附过程。ADN是离子化合物,同时活性炭表面残存一定的离子,所以发生化学吸附是活性炭表面与ADN分子共同作用的结果。
3 结 论
(1)通过实验,建立了利用反向高效液相色谱法测定ADN母液中ADN与AN含量的分析方法。以峰面积Y对质量浓度X进行线性回归,分别获得了ADN的标准曲线方程:Y=84.17997+1.75319X,R2=0.99984;AN的标准曲线方程:Y=129.51554+0.46575X,R2=0.99941。
(2)静态吸附试验结果显示,活性炭AC、BC、CC的平衡吸附量分别为:12.61、11.28、10.98 mg/g,吸附率分别为:72.78%、65.07%、63.37%,吸附能力大小顺序为:AC>BC>CC。实验表明,活性炭AC用于分离纯化ADN效果最好。
(3)ADN在3种活性炭上的吸附过程符合准二级吸附动力学模型;动力学研究表明,活性炭AC的吸附能力最大,这与静态吸附实验结果一致。
(4)活性炭AC在溶液中对ADN的吸附过程属单分子层吸附;通过Freundlich方程拟合可以看出,活性炭AC是ADN的良好吸附剂。此吸附过程中△G<0,△S>0,吸附过程可自发进行;吸附过程中△H>0,表明是一个吸热过程。
