泽漆部分化学成分研究
2019-11-07赵杰吴繁荣李宁葛金芳陈飞虎
赵杰,吴繁荣,李宁,葛金芳,陈飞虎
泽漆(Euphorbia helioscopia L.)是大戟科大戟属一年生或两年生草本植物。味辛、苦,性微寒,春季、夏季均可采集,全草晒干后入药[1],功能主治为行水消肿;化痰止咳;解毒杀虫。多年来,国内外研究者对泽漆的化学成分,临床应用和药理作用进行了一系列的研究,揭示该植物主要含有二萜酯类,黄酮类,三萜类,甾醇等化学成分,且研究表明泽漆具有抗肿瘤,抑菌杀虫,止咳平喘,抗银屑病等作用[2-3]。为了阐明其抗银屑病的药效物质基础,本研究对2014年7月至2015年10月泽漆提取物的化学成分进行了系统的分离,并观察得到的单体化合物对角质形成细胞HaCaT的增殖抑制作用,及对细胞分泌白介素1(interleukin-1,IL-1)和IL-6的影响,为进一步开发泽漆提供科学依据。
1 材料与方法
1.1 药材泽漆于夏季6月采自河南省巩义县,经安徽医科大学药学院中药学教研室张群林教授鉴定为大戟科大戟属泽漆Euphorbia helioscopia L。
1.2 仪器与试剂AM-300、400,DRX-500型核磁共振光谱仪(瑞士Bruker公司,四甲基硅烷作为内标);Sephadex LH-20(瑞典GEHealthcare Bio-Sciences公司);MCI小孔树脂(日本 Mitsubishi Chemical公司);十八烷基键和硅胶(octadecylsilyl,ODS,日本Fujisilysia Chemical公司);硅胶(青岛海洋化工厂);薄层色谱GF254硅胶板板(烟台江友硅胶开发有限公司);氘代试剂(美国Sigma-aldrich公司);胎牛血清(杭州四季青生物工程材料有限公司);DMEM高糖培养基(美国Hyclone);CCK-8试剂盒(上海贝博生物);Elisa试剂盒(美国R&D公司)。
1.3 方法
1.3.1提取分离 取泽漆阴干药材15 kg,倒入提取罐,加90%的乙醇溶液80 L,蒸汽加热至60℃,在该温度条件下浸泡24 h,浸泡液经旋转蒸发仪蒸干溶剂,得到总提物浸膏,并重复提取4次。合并四次所得总提物浸膏1.14 kg。加水混悬后,依次用石油醚、氯仿、乙酸乙酯、正丁醇进行萃取,萃取液浓缩至干,得到石油醚部位(Fra),氯仿部位(Frb),乙酸乙酯部位(Frc)和正丁醇部位(Frd)。石油醚部位Fra(120 g)经硅胶柱色谱(石油醚-乙酸乙酯50∶1~0∶1)梯度洗脱得到8个部分,Fra-1~Fra-8。Fra-6经中低压柱色谱(石油醚-丙酮15∶1)得到6个部分,Fra-6-1~Fra-6-6,Fra-6-1经中低压柱色谱、反复硅胶柱色谱,重结晶得到化合物4(19 mg);Fra-6-2经Sephadex LH-20、反复硅胶柱色谱,得到化合物6(22 mg)。Fra-7经中低压柱色谱(石油醚-乙酸乙酯5∶1)得到5个部分,Fra-7-1~Fra-7-5,其中Fra-7-2经Sephadex LH-20(石油醚-氯仿-甲醇5∶5∶1)、反复硅胶柱层析,最后经Sephadex LH-20(纯乙醇)纯化得一对同分异构体2/3(12 mg)。氯仿部位Frb(250 g)经硅胶柱色谱(石油醚-丙酮60∶1~0∶1)梯度洗脱得到9个部分,Frb-1~Frb-9。Frb-3经硅胶柱(石油醚-乙酸乙酯15∶1~0∶1)得到6个部分,Frb-3-1~Frb-3-6,其中Frb-3-4经反复硅胶柱色谱进一步分离纯化,最后经过Sephadex LH-20(纯乙醇)纯化,得到化合物1(8 mg)。Frb-3-6经Sephadex LH-20(纯乙醇)得到4个部分,Frb-3-6-1~Frb-3-6-4,其中Frb-3-6-4采用硅胶柱色谱(石油醚-丙酮8∶1)分离,再经过Sephadex LH-20(纯乙醇)纯化得到化合物5(19 mg)。
1.3.2CCK-8法检测细胞增殖抑制作用 取对数期的HaCaT细胞以4×103个/孔的细胞密度接种于96孔板中,边缘孔用PBS填充,空白对照组加入等体积的培养基不接种细胞,置于37℃、5%CO2培养箱中孵育24 h后,空白对照组加等体积的培养基,药物组加入等体积不同浓度的药物(药物终浓度为12.5、25、50、100、200 µmol/L),置于37 ℃、5%CO2培养箱中孵育24 h后,吸弃培养基,药物组加入等体积不同浓度的药物,空白对照组加等体积的培养基,置于37℃、5%CO2培养箱中继续孵育24 h后每孔加入10µL CCK-8,置于37 ℃、5%CO2培养箱中孵育3 h后,震荡数分钟后用酶标仪测定450 nm处各孔的吸光度值。
1.3.3Elisa法检测IL-1、IL-6含量 取对数期的Ha-CaT细胞,以1×104个/孔的细胞密度接种于96孔板中,空白对照组加入等体积的培养基不接种细胞,置于37℃、5%CO2培养箱中孵育12 h,待细胞贴壁后,加入10 ng/mL TNF-α溶液刺激,继续培养12 h后,药物组加入等体积不同浓度的药物(药物终浓度为6.25、12.5、25、50、100 µmol/L)其中槲皮素作为阳性对照组。培养24 h后,吸取各孔上清液,4℃、3 000 r/min离心10 min,取上清液,按照Elisa试剂盒说明操作。
2 结果
2.1 结构鉴定化合物1:无色针状结晶,溶于氯仿,分子式为C29H50O2。1H-NMR(600 MHz,CDCl3)δ 5.60(d,J=4.9 Hz,1H,H-6),3.85(s,1H,H-7),3.58(m,1H,H-3),0.99(s,3H,H-19),0.93(d,J=6.5 Hz,3H,H-21),0.84(m,9H,H-26,27,29),0.68(s,3H,H-18)。13C-NMR(151 MHz,CDCl3)δ 146.38(C-5),123.98(C-6),71.49(C-3),65.52(C-7),55.83(C-17),49.55(C-14),45.95(C-24),42.39(C-9),42.28(C-13),42.13(C-4),39.30(C-12),37.64(C-8),37.53(C-10),37.14(C-1),36.25(C-20),34.04(C-22),31.49(C-2),29.24(C-25),28.43(C-16),26.02(C-23),24.45(C-15),23.19(C-28),20.84(C-11),19.95(C-26),19.16(C-27),18.95(C-21),18.40(C-19),12.14(C-29)11.78(C-18)。1H-NMR和13C-NMR数据与文献[4]报道一致,确定该化合物为豆甾-5-烯-3β,7α-二醇。
化合物2:白色粉末,溶于氯仿,分子式为C30H50O2。1HNMR(600MHz,CDCl3)δ 4.92(d,J=6.7Hz,1H,H-26a),4.83(s,1H,H-26b),4.01(t,J=6.3Hz,1H,H-24),3.27(m,1H,H-3),1.72(s,3H,H-27),0.96(s,3H,H-18),0.87(m,6H,H-21,28),0.80(s,3H,H-30),0.54(d,J=3.4Hz,1H,H-19β),0.32(d,J=3.8Hz,1H,H-19α)。13C-NMR(151MHz,CDCl3)δ 147.88(C-25),111.57(C-26),111.05(C-23),78.97(C-3),76.89(C-24),52.29(C-17),48.93(C-14),48.12(C-8),47.22(C-5),45.39(C-13),40.61(C-4),36.07(C-11),36.04(C-20),35.68(C-12),33.00(C-15),32.09(C-1),32.01(C-22),30.49(C-2),30.04(C-19),28.27(C-7),26.58(C-16),26.18(C-10),26.14(C-11),25.57(C-30),21.25(C-6),20.10(C-9),19.45(C-28),18.45(C-18),17.73(C-17),14.15(C-29)。1H-NMR和13C-NMR数据与文献[5]报道一致,确定该化合物为24R-环阿屯-25-烯-3β,24-二醇。
化合物3:白色粉末,溶于氯仿,分子式为C30H50O2。1H-NMR(600MHz,CDCl3)δ 4.92(d,J=6.7Hz,1H,H-26a),4.83(s,1H,H-26b),4.01(t,J=6.3Hz,1H,H-24),3.27(m,1H,H-3),1.72(s,3H,H-27),0.96(s,3H,H-18),0.87(m,6H,H-21,28),0.80(s,3H,H-30),0.54(d,J=3.4Hz,1H,H-19β),0.32(d,J=3.8Hz,1H,H-19α)。13C-NMR(151MHz,CDCl3)δ 147.57(C-25),111.57(C-26),111.05(C-23),78.97(C-3),76.49(C-24),52.29(C-17),48.93(C-14),48.12(C-8),47.22(C-5),45.39(C-13),40.61(C-4),36.07(C-11),36.04(C-20),35.68(C-12),33.00(C-15),32.01(C-1),31.74(C-22),30.49(C-2),29.84(C-19),28.22(C-7),26.58(C-16),26.18(C-10),26.14(C-11),25.57(C-30),21.25(C-6),20.10(C-9),19.45(C-28),18.44(C-18),17.32(C-17),14.15(C-29)。1H-NMR和13C-NMR数据与文献[5]报道一致,确定该化合物为24S-环阿屯-25-烯-3β,24-二醇,与化合物2互为差向异构体。
化合物4:白色粉末,溶于甲醇,分子式为C20H34O5。1H-NMR(600 MHz,CD3OD)δ 3.48(d,J=11.4 Hz,1H,H-17a),3.34(d,J=11.6 Hz,1H,H-17b),3.15(dd,J=11.3,4.4 Hz,1H,H-3),0.99(s,3H,H-20),0.96(s,3H,H-18),0.78(s,3H,H-19);13CNMR(151 MHz,CD3OD)δ 79.84(C-3),75.14(C-16),69.61(C-17),56.91(C-5),53.42(C-15),53.19(C-9),40.81(C-7),39.85(C-4),38.94(C-1),38.59(C-8),33.82(C-10),33.10(C-12),28.70(C-18),28.49(C-2),27.59(C-14),24.41(C-13),24.17(C-11),19.60(C-6),16.24(C-19),14.58(C-20)。1H-NMR和13C-NMR数据与文献[6]报道一致,确定该化合物为阿替生烷-3β,16α,17-三醇。
化合物5:白色结晶,溶于甲醇,分子式为C21H32O5。1H-NMR(600 MHz,CD3OD)δ 6.64(d,J=11.6 Hz,1H,H-7),6.06(d,J=11.0 Hz,1H,H-14),3.98(dd,J=10.9,2.8 Hz,1H,H-12),3.79(dd,J=6.4,3.2 Hz,1H,H-3),2.57(m,1H,H-1a),2.29(dd,J=10.7,3.0 Hz,1H,H-11a),2.13(m,2H,H-1b,H-8),2.00(s,3H,H-16),1.76(s,3H,H-20),1.69(dd,J=24.6,12.6 Hz,1H,H-11b),1.47(m,3H,H-17),1.18(d,J=9.0 Hz,3H,H-21),1.09(s,3H,H-19),1.04(d,J=6.4 Hz,3H,H-18);13C-NMR(151 MHz,CD3OD)δ 197.00(C-2),171.73(C-15),148.08(C-7),145.91(C-13),133.47(C-6),121.85(C-14),97.03(C-4),82.48(C-3),75.96(C-12),42.05(C-1),41.70(C-8),37.32(C-11),32.37(C-5),30.71(C-10),29.19(C-21),25.73(C-9),21.60(C-16),19.13(C-17),18.58(C-18),16.76(C-19),12.34(C-20)。1H-NMR 和13CNMR数据与文献[7]报道一致,确定该化合物为3,12-dihydroxy-clerodan-13E-en-15-oic acid。
化合物6:白色结晶,溶于氯仿,分子式为C20H18O5。1H-NMR(400 MHz,CDCl3)δ 5.90(d,J=1.2 Hz,1H,H-7),5.78(d,J=1.8 Hz,1H,H-1),4.26(s,1H,H-3),4.11(dd,J=11.7,1.7 Hz,1H,H-8),3.91(s,1H),3.60(s,1H,H-5),2.46(m,1H,H-11),2.24(ddd,J=15.6,8.4,2.6 Hz,1H,H-12a),1.84(d,J=1.34 Hz,3H,H-19),1.76(m,1H,H-12b),1.24(s,3H,H-17),1.05(s,3H,H-16),0.95(m,4H,H-14,H-18),0.69(m,1H,H-13);13C-NMR(101 MHz,CDCl3)δ 207.93(C-9),139.64(C-2),136.39(C-6),129.58(C-1),122.29(C-7),83.42(C-4),79.97(C-3),73.82(C-5),72.99(C-10),64.22(C-20),44.12(C-8),38.42(C-11),31.27(C-12),28.69(C-16),23.91(C-15),23.63(C-13),23.07(C-14),17.98(C-18),15.80(C-19),15.70(C-17)。1H-NMR和13C-NMR数据与文献[8]报道一致,确定该化合物为巨大戟醇。
2.2 化合物对HaCaT增殖的影响利用CCK-8法检测分离得到的单体化合物对角质形成细胞HaCaT增殖的影响,比较各化合物的半数抑制浓度(half maximal inhibitory concentration,IC50)值,以维A酸作为阳性对照药。结果显示,化合物1,4,5,6均有一定的抑制HaCaT细胞增殖的能力(表1),但均较阳性药维A酸(52.67µmol/L)弱,其他化合物的增殖抑制作用不明显。
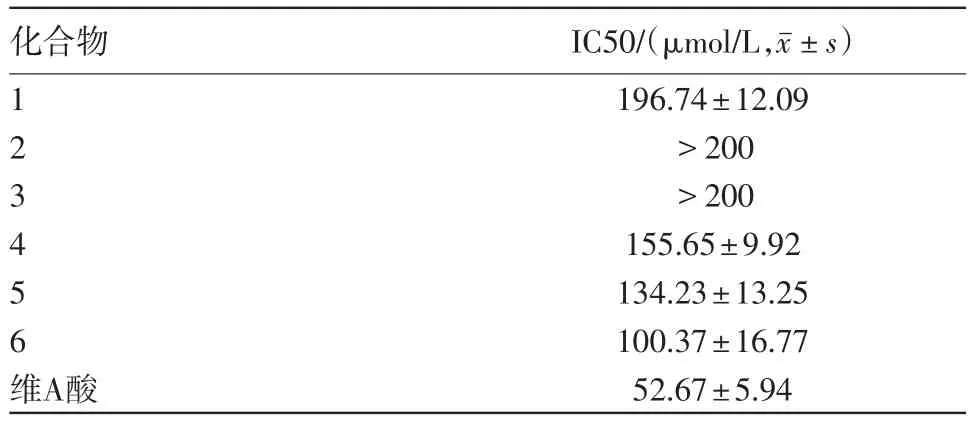
表1 单体化合物对HaCaT细胞的抑制效应的IC50(n=3)
2.3 化合物对TNF-α刺激的HaCaT细胞分泌细胞因子的影响在细胞增殖抑制实验的基础上进行化合物抗炎活性筛选,采用Elisa法测定TNF-α(10ng/mL)刺激的HaCaT细胞上清中IL-1和IL-6的含量,以槲皮素作为阳性对照药。结果显示,化合物对TNF-α刺激的HaCaT细胞IL-1分泌量差异无统计学意义,但能在一定程度上减少IL-6的分泌(表2)。
表2单体化合物对TNF-α刺激的HaCaT细胞生成IL-1和IL-6生成的抑制作用/(ng/L,±s,n=3)
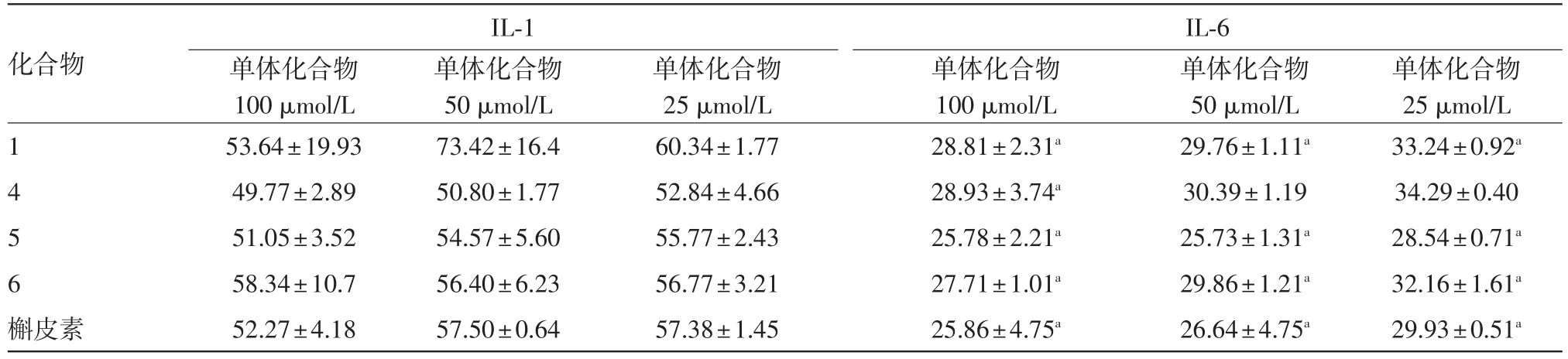
表2单体化合物对TNF-α刺激的HaCaT细胞生成IL-1和IL-6生成的抑制作用/(ng/L,±s,n=3)
注:与模型组(IL-1:61.36±2.58,IL-6:35.81±1.19)比较,aP<0.05
IL-1 IL-6化合物1 4 5 6槲皮素单体化合物25µmol/L 33.24±0.92a 34.29±0.40 28.54±0.71a 32.16±1.61a 29.93±0.51a单体化合物100µmol/L 53.64±19.93 49.77±2.89 51.05±3.52 58.34±10.7 52.27±4.18单体化合物50µmol/L 73.42±16.4 50.80±1.77 54.57±5.60 56.40±6.23 57.50±0.64单体化合物25µmol/L 60.34±1.77 52.84±4.66 55.77±2.43 56.77±3.21 57.38±1.45单体化合物100µmol/L 28.81±2.31a 28.93±3.74a 25.78±2.21a 27.71±1.01a 25.86±4.75a单体化合物50µmol/L 29.76±1.11a 30.39±1.19 25.73±1.31a 29.86±1.21a 26.64±4.75a
3 讨论
银屑病是一种常见的慢性炎症性皮肤疾病,主要是由环境因素、免疫因素、遗传因素等相互作用所致[9],其确切的病因和发病机制仍未完全阐明。局部浸润的炎细胞和表皮角质形成细胞通过分泌的细胞因子,在银屑病发生过程中起重要作用[10],参与银屑病炎症反应的细胞因子主要有有IL-1β,IL-6,IL-21,IL-23,TNF-α,IFN-γ以及一些转录因子如RORγt,RORɑ,Stat3[11-13],细胞因子间相互作用,促表皮角质形成细胞的异常增殖,和炎症细胞的转移。研究表明IL-1和IL-6与银屑病患者的患病程度密切相关,患者的皮损处和血浆的IL-1和IL-6的水平都较正常人高,且血浆IL-1和IL-6的水平不仅可以反映炎症的情况,可以作为治疗反应的一个指标[14-16]。可见IL-1和IL-6的水平在银屑病的病程中的重要作用。本实验中用TNF-α刺激人表皮角质形成细胞,诱导其发生异常增殖和分泌炎性细胞因子增多,模拟了银屑病的体外模型。利用此体外模型我们进行泽漆单体化合物对角质形成细胞异常增殖的抑制作用进行了实验,结果表明,泽漆中的众多的化学成分对角质形成细胞异常增殖都有一定的抑制作用,且部分化学成分可减少炎性细胞因子IL-6的分泌,具有不同程度的抗银屑病作用。
然而,泽漆的化学成分尚未完全阐明,因此还需进一步的分离和筛选,得到一些活性更好的化合物,为明确泽漆抗银屑病药效提供物质基础。
