2019年全国I卷理综化学实验综合题特点分析及教学启示
2019-11-07福建省厦门市翔安第一中学361101洪兹田罗德炳陈女婷
福建省厦门市翔安第一中学(361101) 洪兹田 罗德炳 陈女婷
分析近3年的全国I卷理综化学实验题,不难发现这3年的实验综合题的考查不尽相同。从考查类型看,2017年考查以凯氏定氮法为背景的定量测定实验,2018 年考查以醋酸亚铬制备为背景的物质制备类实验题,2019年则考查硫酸铁铵制备为背景的物质制备类实验题。从呈现形式看,2017年、2018 年以实验装置图形式呈现,而2019年则以工艺流程的形式呈现。分析2019年流程式的物质制备实验题的命题特点,提出对今后此类实验复习教学的若干启示:整体规划设计实验教学,促进“物质制备实验”的学习进阶;掌握一般范式和建构思维模型,实现分析问题模型化;掌握审题四部曲和答题五关键,实现解决问题方法化的目的。
1 试题分析
1.1 原题呈现
硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如图1所示。
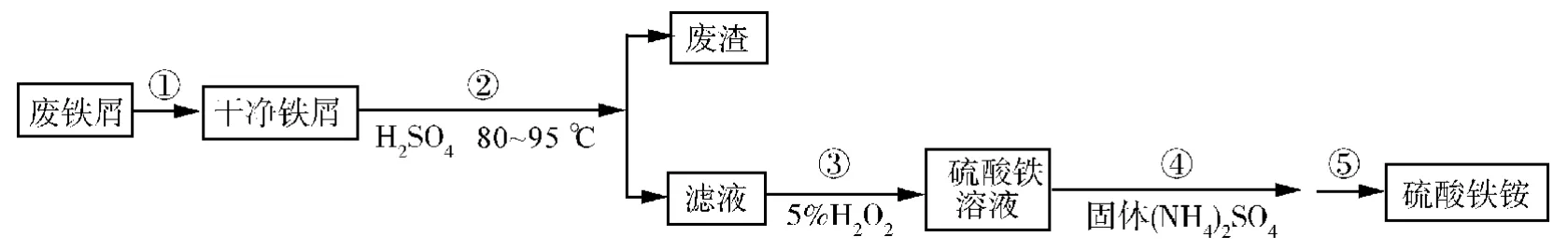
图1 制备流程图
回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是______。
(2)步骤②需要加热的目的是______,温度保持80~95 ℃,采用的合适加热方式是______。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为____(填标号)。

(3)步骤③中选用足量的 H2O2,理由是______。分批加入H2O2,同时为了______,溶液要保持pH 值小于0.5。
(4)步骤⑤的具体实验操作有______,经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为_____________。
1.2 分析与解答
流程型实验题包括3种类型:操作流程型、物质转化流程型、综合流程型。本题属于物质转化流程型实验题。
(1)热的纯碱溶液有利于促进CO2-3的水解,导致溶液碱性增强,油脂在碱性条件下会发生水解(称为“皂化反应”)。工业上常用热的纯碱溶液清洗去除废铁屑表面的油污。因此,答案为:碱煮水洗。
(2)温度升高,反应速率加快,故加热的目的是为了加快反应速率。为保持温度恒定为80~95 ℃且低于水的沸点(100 ℃),可采用水浴加热方式。铁屑中含少量硫化物,硫化物与硫酸反应生成少量有剧毒的H2S 气体。H2S 在水中的溶解度不大(常温下1∶2.6),但易与NaOH 溶液反应。因此,选用NaOH 溶液作为吸收剂,同时选用倒扣漏斗作为防倒吸装置,故合适装置为C。因此,答案为:加快反应速率;热水浴;C。
(3)滤液成分中有FeSO4,加入H2O2可将Fe2+氧化为Fe3+,且H2O2的还原产物为H2O(2Fe2++H2O2+2H+=2Fe3++2H2O),不引入新杂质。因为H2O2本身易分解,故在加入时需分批加入。使Fe3+产生沉淀的溶液pH 值为1.5~3.7,pH 值越大Fe3+越易水解生成Fe(OH)3沉淀,溶液保持pH<0.5 的目的是防止Fe3+水解。因此,答案为:将Fe2+全部氧化为Fe3+,不引入新杂质;防止Fe3+水解。
(4)为了除去可溶性的硫酸铵等,需要经过的步骤为:加热浓缩、冷却结晶、过滤(洗涤)。因此,答案为:加热浓缩、冷却结晶、过滤(洗涤)。

2 命题特点
2.1 重视基础性,考查必备知识和关键能力
试题考查难度适中,多数设问为实验必备知识和关键能力在具体实验情境中的应用。例如,本题的设问落脚点主要集中在以下几点。
(1)反应条件的控制。例如,试题第(2)问中考查保持温度为80~95 ℃采用的加热方式。
(2)元素化合物知识的应用。例如,试题第(2)问中考查H2S 气体的尾气净化处理的装置选择(涉及H2S与NaOH 溶液反应);试题第(3)问中考查Fe2+转化为Fe3+的过程中,选用足量的H2O2的理由(涉及陌生氧化还原反应的产物分析)。
(3)实验装置的选择。例如,试题第(2)问中考查H2S气体的尾气吸收和防倒吸装置。
(4)化学反应原理的应用。例如,试题第(1)问中考查去除废铁屑表面油污的方法;试题第(2)问中考查步骤②加热的目的;试题第(3)问中考查控制溶液pH<0.5的目的。
(5)物质分离提纯的方法与操作。例如,试题第(4)问中考查分离提纯硫酸铁铵晶体的方法。
(6)目标产物的分析与研究。例如,试题第(5)问中考查利用热重法计算确定物质组成。
2.2 提供流程信息,考查信息获取和加工能力
采用流程图形式简约明了地介绍制备实验的完整过程,实现对学生获取信息、吸收和整合信息能力的考查。例如,学生通过对“废铁屑制备硫酸铁铵”流程图信息的获取和加工,获得如下主要信息。
(1)实验步骤:铁屑预处理→硫酸亚铁制备→硫酸铁制备→硫酸铁铵制备→浓缩结晶。
(2)主要发生的反应如下。步骤①:油脂在碱性条件下的水解反应;步骤②:Fe+H2SO4=FeSO4+H2↑,FeS+H2SO4=FeSO4+H2S↑,Fe2O3+H2SO4=Fe2(SO4)3+H2O,Fe2(SO4)3+Fe=3FeSO4;步骤③:2Fe2++2H++H2O2=2Fe3++H2O;步 骤④⑤:Fe2(SO4)3+(NH4)2SO4+2xH2O=2[NH4Fe(SO4)2·xH2O]。
2.3 注意原型启发,考查类比迁移能力
高考考查的实验多数是课本实验或所学知识的改造和升级。遇到陌生实验仪器、原理、方法、操作等问题,应尽可能与所掌握的实验必备知识与关键能力进行类比迁移。例如,步骤②中产生的H2中混有H2S气体,考虑安全必须对H2S气体进行净化处理。H2S气体的处理可类比氨气的尾气处理方式。氨气用水(或稀硫酸)吸收,同时要注意防止倒吸。但考虑到H2S 气体在水中的溶解度不大,不能用水吸收,而应用碱液(如NaOH 溶液)吸收。又如,温度保持80~95 ℃采用的加热方式,可类比乙酸乙酯的水解实验中采用水浴加热控温在70~80 ℃等操作。
2.4 融入新技术手段,考查定量分析方法和定量思维
考查制备原理、实验过程和突出新技术手段应用的同时,也涉及测定物质组成的定量分析方法和定量思维的考查。例如,本题在考查利用废铁屑来制备硫酸铁铵的过程中,也涉及了利用热重分析法测定物质分子式的方法的考查。测定物质组成的方法有:测量气体体积法、沉淀法、滴定法、热重分析法等。前3种定量测定方法在中学教材中涉及较多,而“热重分析”这一方法虽然在往年的全国卷中也曾涉及,但在中学阶段学生必修和选修教材却较少涉及。因此,本题的考查有利于引导中学教师关注和适度拓展大学教材中涉及并且基础教育阶段学生可理解的定量分析方法。
3 教学启示
3.1 整体规划设计实验教学,促进“物质制备实验”的学习进阶
严格贯彻落实普通高中化学课程标准 (2017版)规定的学生必做实验。学生能做的实验教师不代替,教师演示能做的实验视频不代替。有条件的学校可开展开放实验室活动。
高一、高二阶段围绕物质的制备、物质的分离与提纯等方面选择真实的、有意义、引发学生兴趣的基础实验活动,引导学生认识解决此类实验任务的一般思路和常用方法。对于 “物质的制备”可选择硫酸亚铁铵的制备、侯氏制碱法制备碳酸钠等典型实验,帮助学生掌握物质制备实验的一般流程:根据目标产品→确定反应原理及选择原料→设计反应途径→设计反应→控制反应条件→分离提纯产品。对于 “物质的分离与提纯”,可选择海带中碘元素的分离和检验、粗盐的提纯等典型实验,帮助学生建立分离与提纯的原则、物理方法和化学方法的思维模型。通过基础实验探究,引导学生掌握必要的实验操作技能,改变在实验中注重动手但缺少思考的现状。高三复习阶段可以选择高考考题中经典的物质制备类 (特别是流程式)的探究题作为学生分组实验素材,促进学生动手能力和高阶思维能力的提升,同时进一步发展学生解决综合实验问题的能力。
3.2 掌握一般范式和建构思维模型,实现分析问题模型化
(1)物质制备实验和工艺流程题的一般范式见图2。

图2 物质制备实验的一般范式
(2)物质制备实验的思维模型见图3。
3.3 指导审题四部曲和答题五关键,实现解决问题方法化
3.3.1 审题四部曲
化工流程式实验题,应将流程路线、理论知识和试题设问有机结合。审题四部曲如下:
(1)明确原料和产品(包括副产物),即箭头进出方向。
(2)依据流程图分析反应原理,分析原料转化为产品的流程中每一步操作进行的反应和加入的辅助试剂的作用。

图3 工艺流程一般范式
(3)分析除目标物质外产生的副产物 (或杂质),该副产物是否要除去及如何除去。
(4)分析为了确保目标产物的纯度和产率应采取的措施。
3.3.2 答题五关键
(1)原料预处理的考查关键。常考查:研磨的目的、灼烧 (煅烧)的目的、搅拌的目的、酸(碱、水)浸的目的、提高浸出率的措施等。
(2)反应条件控制的考查关键。反应流程中选择的试剂、温度控制、pH 控制、反应体系压强控制、分离提纯手段可从热力学、动力学、物质特性、绿色化学思想 (废物处理、物料循环利用与环境保护)、工程思维等多维视角进行综合分析。
(3)产品分离提纯的考查关键。分离提纯方法的表达应准确,以下分离提纯方法容易混淆,应准确区分。例如,蒸发与蒸馏、分馏;蒸发结晶与冷却结晶、重结晶;趁热过滤与普通过滤、抽滤;萃取与分液等。另外,判断沉淀剂过量、洗涤沉淀、检验沉淀、洗涤干净、溶液结晶的方法表达也应规范。
(4)工程思维的考查关键。关注常考化工术语(如煅烧、研磨、浸泡、雾化)的含义,理解经济因素 (如物料价格、能耗)在实际生产中的重要意义,考虑苛刻条件 (如高温高压)带来的设备复杂性。
(5)定量计算的考查关键。物质制备类实验常穿插定量计算。例如,考查利用测量气体体积法、沉淀法、滴定法、热重分析法等测定物质组成或纯度计算。也常涉及多步反应一步计算。元素守恒与电子转移守恒是流程图中定量计算的核心。应加强针对性专题训练和策略指导,克服学生的畏难情绪。
