高荧光强度金银合金簇的合成及其对Hg2+的检测
2019-11-05张诗琪许惠凤周鑫悦王丽丽陈婷婷余丽双
张诗琪, 许惠凤, 周鑫悦, 王丽丽, 陈婷婷, 胡 筱, 余丽双*
(1.福建中医药大学药学院,福建福州 350122;2.福建省中西医结合老年性疾病重点实验室,福建福州 350122;3.福建中医药大学中西医结合研究院,福建福州 350122)
汞是污染最为普遍、毒性最强的重金属,对人体健康造成了极大危害[1]。传统的Hg2+检测方法如电感耦合等离子体发射光谱法、原子荧光法、火焰原子吸收光谱法等[2 - 4]已在实际检测中得到很好的应用。此外,采用诸如荧光分析[5]、电化学传感[6]等技术进行Hg2+的快检方法也得到广泛报道,这些方法在一定程度上实现了对Hg2+的快速灵敏检测。即便如此,继续寻找高效快速的分析方法仍然是研究者在Hg2+检测中一直努力的方向。
近年来,金属纳米簇的研究受到人们的广泛关注。所谓纳米簇,通常指由几个到几十个原子构成的相对稳定的纳米结构。这种纳米簇的尺寸通常小于2 nm,接近于电子的费米波长,这赋予其非常独特的理化特性,如离散的能级和强荧光活性等[7 - 9]。金属纳米簇这些特性使其能够作为理想化的纳米材料用于生物医药及环境科学等领域的研究[9 - 10]。其中,贵金属簇(Au、Ag、Pd和Pt)具有高的比表面积、丰富的表面原子以及显著的荧光响应等特点,常常作为一类新型的荧光探针[8 - 9,11]。相比单一金属簇,双金属合金簇能够通过控制原子在金属簇中的分布以获得额外的自由度。同时,合成的合金簇具有更优异的光电活性,Zhang等[11]发现在Pb簇表面引入Au原子能显著提高其葡萄糖氧化的活性。另有报道表明,在Au纳米簇(AuNCs)中引入Ag能更有效地增强其荧光[12],并且这些具有强荧光响应的合金簇也能够用于金属离子的检测。Jin课题组合成了硫醇类包覆的AuNCs,实验发现Ag+能明显引起该金簇荧光强度的增强,从而可以实现对Ag+检测[13]。而采用不同模板合成的Au/AgNCs也能够对Cr3+、Cr6+、As3+等重金属离子进行定量检测[14 - 15]。
截止目前,已有多种生物分子比如蛋白质、多肽和寡核苷酸[16 - 19]等被用作合成金属纳米簇的模板,以增强其光稳定性并减小纳米簇的聚沉。本研究以牛血清白蛋白(Bovine Serum Albumin,BSA)为模板合成了具有强荧光响应的金银纳米簇(BSA-Au/AgNCs),并以此为荧光探针来构建检测Hg2+的方法。该方法对Hg2+的响应范围为2~30 nmol/L,检测限达到0.6 nmol/L。同时,该方法对Hg2+有良好的特异性,可以对实际水样中汞的含量进行测定。
1 实验部分
1.1 仪器与试剂
FS5型荧光光谱仪(英国,Edinburgh公司);AVATAR360型傅立叶变换红外光谱仪(美国,Nicolet公司);TECNAI G2F20型高分辨率透射电子显微镜(美国,FEI公司);QL-866型振荡器(江苏海门其林贝尔仪器制造有限公司);KQ520DB型超声波清洗器(昆山市超声仪器有限公司)。
牛血清白蛋白(BSA)、HAuCl4·3H2O购自美国Sigma-Aldrich公司;NaOH、Na2HPO4·12H2O,NaH2PO4·12H2O、AgNO3、Hg(NO3)2等购自国药集团化学试剂有限公司;其余试剂均为分析纯。水为去离子水。
1.2 实验方法
1.2.1 BSA-Au/AgNCs的合成所有用于合成BSA-Au/AgNCs的玻璃器皿事先都先用王水浸泡4 h,然后用乙醇漂洗,最后用水冲洗干净。合成方法参考文献方法[18]。将5.0 mL 50 mg/mL BSA溶液和4.0 mL 1.0×10-2mol/L HAuCl4溶液混合,接着加入1.0 mL不同浓度的AgNO3溶液,室温振荡10 min,立即加入1.0 mL 1.0×10-3mol/L NaOH溶液,在37 ℃下反应12 h。将反应液先使用30 000 MW的滤膜处理,4 ℃下3 000 r/min离心15 min,去除未反应的BSA。再使用水对其透析48 h(每6 h换一次水),以除去未反应的HAuCl4和NaOH。最后将得到的BSA-Au/AgNCs溶液4 ℃放置以备用。取1 mL溶液冻干后称重,计算得到最终BSA-Au/AgNCs母液的浓度为3.4 mg/mL。
1.2.2 Hg2+的荧光检测取100 μL上述BSA-Au/AgNCs溶液,加900 μL浓度为2.0×10-2mol/L磷酸盐缓冲液(PBS,pH=7.0),得到浓度为0.34 mg/mL的BSA-Au/AgNCs溶液。分别移取1 μL不同浓度的Hg2+溶液加入到1 mL上述BSA-Au/AgNCs溶液中,进行荧光测定。
2 结果与讨论
2.1 BSA-Au/AgNCs的合成及表征
图1A为BSA-Au/AgNCs在激发波长280 nm处的荧光光谱图,由图可见最大发射波长为625 nm。这些荧光特征与文献报道的基本一致[19],表明实验已经成功合成了BSA-Au/AgNCs。日光下制备的BSA-Au/AgNCs呈棕黄色(如图1A插图a),而在365 nm的紫外灯下显示出很强的橘红色荧光,如图1插图b所示。
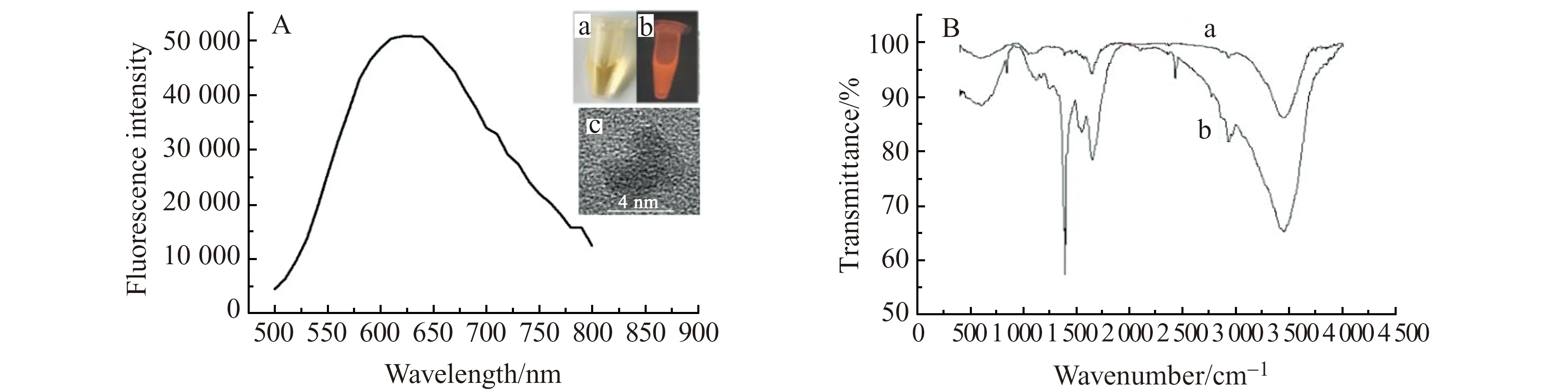
图1 BSA-Au/AgNCs的荧光光谱(A)和红外光谱(B)图Fig.1 Fluorescence spectra(A) and IR spectra(B) of BSA-Au/AgNCsInset a in Fig.A:Image of BSA-Au/AgNCs under the daylight lamp; Inset b:Image of BSA-Au/AgNCs under 365 nm UV light;Inset c:HRTEM image of BSA-Au/AgNCs.
利用高分辨透射电镜(HRTEM)研究了合成的BSA-Au/AgNCs的尺寸。如图1插图c所示,可以观察到合成的BSA-Au/AgNCs尺寸约4 nm,表明BSA-Au/AgNCs具有高度结晶的结构。利用红外光谱表征了BSA-Au/AgNCs的结构信息,结果如图1B所示。其中曲线a为BSA-Au/AgNCs的红外谱,曲线b为BSA的红外光谱。与BSA的红外光谱相比,BSA-Au/AgNCs的红外光谱在1 654 cm-1的特征吸收峰有较为明显的减弱,这表明反应后蛋白质的α螺旋结构减少了,蛋白质的二级结构发生了改变,同时在蛋白质中巯基与Au、Ag形成共价键。
2.2 BSA-Au/AgNCs对Hg2+的荧光响应
考察了Hg2+存在时BSA-Au/AgNCs为荧光探针荧光信号变化情况,结果如图2所示。从图中可以看出,本实验合成的BSA-Au/AgNCs在625 nm处显示出很强的荧光(曲线a),而随着Hg2+的加入,BSA-Au/AgNCs的荧光信号强度显著降低(曲线b)。图2的插图是在365 nm紫外灯下,在不同条件下的BSA-Au/AgNCs的荧光图。在紫外灯下,单纯的BSA-Au/AgNCs呈现出明亮的橙红色(插图a),而加入Hg2+后,明亮的橙红色几乎完全褪去,而显示出微弱的蓝光(插图b)。这一结果表明,Hg2+可有效地猝灭BSA-Au/AgNCs的荧光。其原因可能是Hg2+与BSA-Au/AgNCs表面的Au+之间存在着高特异性的Hg2+-Au+噬金属效应(Metallophilic Interactions),导致BSA-Au/AgNCs的荧光猝灭。所谓的噬金属效应[19]是指一些闭壳层金属(Closed-shell Metal)原子或离子间存在着的高亲和性作用力,如Cu+(3d10)与Ag+(4d10)或Hg2+(5d10)与Au+(5d10)。这些闭壳层金属间强的相互作用力能够实现某些金属离子的特异性检测。
2.3 实验条件的优化
2.3.1 Au和Ag配比的选择固定BSA的用量,调整HAuCl4和AgNO3的比例,分别合成不同Au、Ag比例的合金簇,并考察不同比例的Au、Ag合金簇的荧光光谱。如图3所示,当Au∶Ag=3∶1时,得到的合金簇的荧光强度最强(曲线b)。因此,实验选择Au、Ag比例为3∶1合成BSA-Au/AgNCs。

图2 加入Hg2+前(a)、后(b)BSA-Au/AgNCs的荧光光谱和紫外灯下图片Fig.2 Fluorescence spectra and image under UV light of BSA-Au/AgNCs without (a) and with (b) Hg2+a.in the absence of Hg2+;b.in the presence of 3.0×10-8 mol/L Hg2+.

图3 不同Au、Ag比例BSA-Au/AgNCs的荧光光谱Fig.3 Fluorescence spectra of BSA-Au/AgNCs with different molar ratiosa.Au∶Ag=4∶1;b.Au∶Ag=3∶1;c.Au∶Ag=2∶1;d.Au∶Ag=1∶1;e.Au∶Ag=0.5∶1.
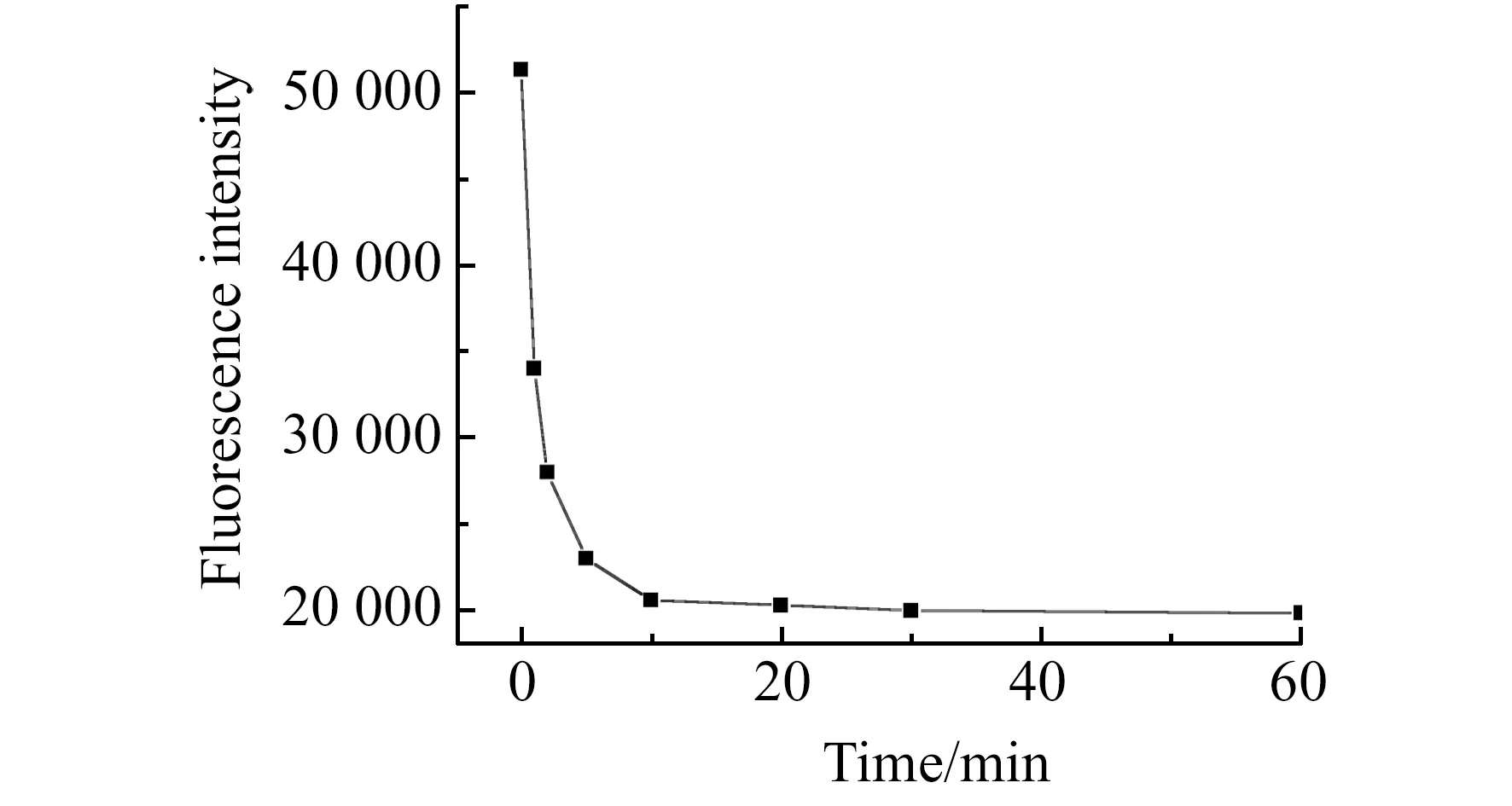
图4 Hg2+和BSA-Au/AgNCs(Au∶Ag=3∶1)反应的动力学曲线Fig.4 The dynamics curve between BSA-Au/AgNCs(Au∶Ag=3∶1) and Hg2+The final concentration of Hg2+ and BSA-Au/AgNCs are 2.0×10-8 mol/L and 0.34 mg/mL in 0.02 mmol/L PBS buffer(pH=7.0),respectively.
2.3.2 反应时间的选择反应时间对检测结果有很大影响。实验考察了Hg2+对BSA-Au/AgNCs荧光响应的情况。从图4中可以看出,随着反应时间的延长,荧光强度逐渐降低,当反应10 min后,荧光降低趋于缓慢,因此在后续实验中,所有反应时间均设为10 min.
2.4 线性方程及检测限
按照上述优化条件,实验研究了不同浓度Hg2+对BSA-Au/AgNCs荧光强度的影响。从图5A中可以看出,随着Hg2+浓度的增加,荧光强度逐渐降低。同时发现Hg2+的浓度在一定范围内时(2~30 nmol/L),荧光强度与Hg2+浓度有着良好的线性关系,如图5B所示,回归方程为:y=-1224.2x(nmol/L)+47319.6,相关系数R2为0.9928,方法的检测限(S/N=3)为0.6 nmol/L。3次平行实验得到结果的相对标准偏差(RSD)为3.6%,方法具有稳定性。

图5 (A)不同浓度Hg2+条件下BSA-Au/AgNCs的荧光光谱;(B)荧光强度与Hg2+浓度的线性关系曲线Fig.5 (A) Fluorescence spectra of BSA-Au/AgNCs in the presence of different concentrations of Hg2+;(B) The relationship curve of the fluorescence intensity with Hg2+ concentrationscHg2+ (a-f):0,2,5,12,20,30 nmol/L.

图6 不同金属离子的响应信号变化图Fig.6 Signal changes responding to different metal ionsNote:The concentration of Hg2+ was 1.2×10-8 mol/L and those of other ions were 1.2×10-7 mol/L.
2.5 干扰实验
选用一些常见的无机离子Cu2+、Mn2+、Pb2+、Mg2+、Zn2+、Ba2+和Cd2+等作为干扰离子。实验结果用荧光的改变量ΔF来表示,定义ΔF=F0-F,其中F0为初始荧光值,F为加入相应离子后的荧光值。从图6中可以看出,同样条件下,Hg2+对BSA-Au/AgNCs的荧光具有显著猝灭作用,而其他金属对其则没有明显作用。由此可见,基于BSA-Au/AgNCs的荧光检测方法对Hg2+具有良好的选择性识别能力。
2.6 实际水样中Hg2+的检测
实验中所用的水样均采自闽江,在检测前静置过夜,并通过滤膜(0.22 mm)过滤掉不溶物。利用所建立方法在此水样中进行Hg2+的检测,结果并没有检测到信号变化,其原因可能是河水中Hg2+的含量低于该方法的检测限。在水样中加入已知浓度的Hg2+标准溶液进行加标回收实验,检测结果如表1所示,其回收率在90.1%~107.2%范围内。

表1 河水样品中Hg2+的检测
3 结论
本文以BSA为模板,以HAuCl4和AgNO3为原料,合成了一种高荧光强度的Au、Ag合金簇BSA-Au/AgNCs。实验发现,由于Hg2+与BSA-Au/AgNCs表面的Au+存在的高特异性的噬金属效应,因而能显著猝灭合金簇的荧光信号。本研究进一步以该BSA-Au/AgNCs为荧光探针,开发了一种快速检测Hg2+的方法。该检测方法操作简单,快速,灵敏度较高,不需复杂仪器;同时,合成的合金簇绿色环保。
