基于层层自组装技术与季铵盐类抗菌剂接枝制备表面抗菌涂层的研究*
2019-10-30周俊涛潘艳周超邓林红
周俊涛,潘艳,周超,邓林红△
(1. 常州大学材料科学与工程学院,江苏常州 213164;2. 常州大学生物医学工程与健康科学研究院,江苏常州 213164)
1 引 言
生物医用材料在临床应用中,由于细菌的粘附与增殖,会在患者体内引起严重的细菌感染,甚至威胁到患者的生命安全[1-3]。因此,一般需要对生物医用材料表面进行修饰,使其具有抗菌功能。近几年,层层自组装技术由于工艺简单,厚度可控,适用于结构复杂的表面等优点而广泛应用于生物医用材料的表面修饰[4]。该技术通过静电力的作用将带有异种电荷的聚电解质链交替沉积在基底材料表面来制备多功能涂层,如,Li等[5]通过层层自组装技术将聚(2-乙基-2-恶唑啉)和聚丙烯酸交替沉积,制备出一种结构稳定的自组装涂层。该涂层具有超亲水表面,通过空间排斥来阻断细菌的初始粘附,但因不具备直接杀灭细菌的功能,故抗菌性能一般。
为提高抗菌性能,使涂层表面具有杀菌功能很有必要。目前,实现表面杀菌的方法可以分为两类。释放杀菌:表面包裹抗菌剂,在外界刺激作用下,释放抗菌剂,杀死材料表面及附近细菌[6-7]。但是,抗菌聚合物释放完后就失去了表面抗菌的作用。接触杀菌:表面接枝带有正电荷的物质,如Ag+,Mg2+等重金属离子,通过表面电荷作用杀灭材料表面粘附的细菌[1, 8-9]。虽然重金属离子可以杀菌,但会对人体的正常生理组织造成伤害。因此,在自组装涂层表面接枝生物相容性较好的抗菌聚合物成为人们研究的热点。在前期工作中,采用辅助活化还原原子转移自由基聚合(SARA ATRP)的方法获得了一种生物相容性好且杀菌效率高的季铵盐类抗菌聚合物,其合成路线简单,催化剂用量少,反应条件温和[10],但尚未有研究将该抗菌聚合物接枝到自组装抗菌涂层中并考察其表面的抗菌性能。
因此,本研究首先通过层层自组装技术制备表面抗细菌粘附的涂层,再通过“巯基-烯”点击反应(Thiol-ene Click Reaction),将末端为巯基修饰而且有杀菌性能的季铵盐类抗菌聚合物接枝到含氧降冰片烯结构的涂层中,使涂层表面具有抗细菌粘附以及长效杀菌的功能。实验表明,该表面抗菌涂层不仅拥有较好的生物相容性,而且大幅度提高其表面的抗菌性能。
2 实验部分
2.1 材料与仪器
聚乙烯亚胺(PEI, Mw 10 000), 聚丙烯酸(PAA,Mw 100 000), 多巴胺盐酸盐(Dopamine Hydrochloride,98%), 3-马来酰亚胺基丙酸(3-Maleimidopropionic Acid, 97%), 糠胺(2-Furfurylamine,99%), 三(羟甲基)氨基甲烷盐酸盐(Tris·HCl,99%), 1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC,99%), N-羟基琥珀酰亚胺(NHS, 99%), 2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮(IRGACURE 2959, 98%), DL-二硫苏糖醇(DTT,99%),上海阿拉丁生化科技股份有限公司;MH培养基,美国索莱宝公司;胰蛋白胨,赛默飞世尔科技;酵母粉,OXOID;琼脂粉,上海润捷化学试剂有限公司;DEME高糖和胰蛋白酶,赛默飞世尔科技;盐酸(HCl,37%), 浓硫酸(H2SO4,98%), 双氧水(H2O2,30%), 无水乙醇(C2H5OH),氯化钠(NaCl),氯化钾(KCl),氢氧化钠(NaOH),碳酸氢钠(NaHCO3), 磷酸氢二钠(Na2HPO4), 磷酸二氢钾(KH2PO4), 二氯甲烷(CH2Cl2), 四氢呋喃(THF),N,N-二甲基甲酰胺(DMF),无水甲醇(CH3OH,分析纯),国药集团化学试剂有限公司。
冷冻干燥机,2.5 L, Freezone公司;pH计,PB-10,Sartorius公司;倒置式显微镜,Primo Vert,德国-卡尔蔡司;超净工作台,VS-1300L-U,AIRTECH公司;核磁共振波普仪,AVANCEⅡ 500 M,德国布鲁克;傅里叶红外光谱仪,Nicolet A vatar 370,Thermo Fisher;水接触角测试仪。
2.2 聚阳离子电解质的合成
在圆底烧瓶中加入PEI (1 g,0.0233 mol),用50 mL 1X PBS溶液将其溶解,再加入NHS (2.68 g,0.0233 mol)、EDC (4.46 g,0.0233 mol),在37 ℃水浴下搅拌活化6 h,转速为360 rpm,接着加入3-Maleimidopropionic Acid (3.93 g,0.0233 mol),继续搅拌48 h。待反应结束后,透析24 h,以除去未反应的小分子物质。通过冷冻干燥得到絮状物PEI-M。反应方程式见图1(a)。
2.3 聚阴离子电解质的合成
在圆底烧瓶中加入PAA (1 g,0.0139 mol),用50 mL 1X PBS溶液将其溶解,再加入NHS (1.6 g,0.0139 mol)、EDC (2.66 g,0.0139 mol),在37 ℃水浴下搅拌活化6 h,转速为360 rpm,接着加入2-Furfurylamine (1.35 g, 0.0139 mol),继续搅拌48 h。待反应结束后,透析24 h,以除去未反应的小分子物质。通过冷冻干燥得到絮状物PAA-F。反应方程式见图1(b)。
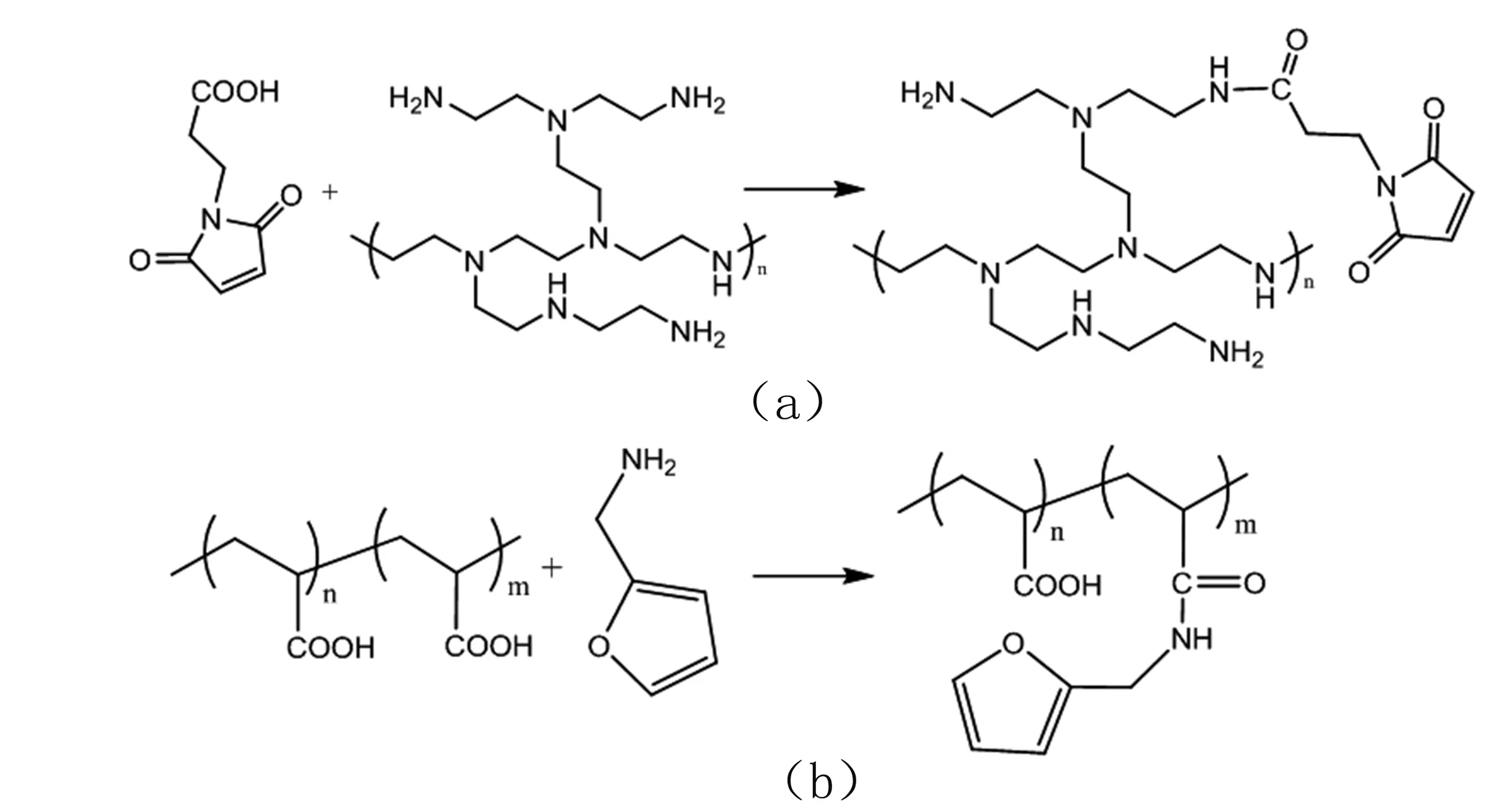
图1 (a).PEI-M的合成;(b).PAA-F的合成Fig.1 (a).Synthesis of PEI-M;(b).Synthesis of PAA-F
2.4 基材表面处理
将1 cm×1 cm的不锈钢片分别用去离子水、乙醇超声清洗5 min,并用氮气吹干。通过浸入食人鱼溶液(H2SO4(95~97%):H2O2(30%)= 7:3)中浸泡40 min使表面富羟基化,用去离子水清洗,氮气吹干。将Dopa溶于50 mM Tris-HCl (PH= 8.5)中,浓度为4 mg / mL,将不锈钢片浸入溶液中,37℃水浴,高速搅拌反应24 h,取出基板,用去离子水冲洗,氮气吹干。获得SS-PDA样品。
2.5 PEI-M/PAA-F的层层自组装
将PEI-M和PAA-F分别用去离子水溶解,浓度为1 mg/mL。然后将SS-PDA连续浸入PEI-M溶液和PAA-F溶液中10 min,获得一个PEI-M/PAA-F双层,重复10次后获得SS-PDA-(PEI-M/ PAA-F)10样品,简写为SS-PDA-L。将该样品浸入去离子水中,37℃下进行Diels-Alder反应2 h,以获得含氧降冰片烯结构。
2.6 抗菌聚合物的制备以及涂层接枝抗菌剂
制备含有双硫键的抗菌聚合物聚(3-丙烯酰胺丙基)三甲基氯化铵(PAMPTMA)[10]。接着将PAMPTMA(Mn = 27 000 g/mol,1 g,0.037 mmol)聚合物溶于50 mL THF中,通氮气30 min后将DTT(0.077 g,0.5 mmol)加入Schlenk管中。将混合物在氮气流保护下在50℃下搅拌24 h。将得到的AMPTMA-SH透析3 d,通过冷冻干燥分离产物(产率为95%)。
称取50 mg产物,用去离子水配置浓度为3 mg/mL的溶液,再加入一定量的紫外光引发剂(IRGACURE 2959)。将表面沉积了多层聚电解质涂层的不锈钢片浸入其中,在紫外光下(波长365 nm)照射15 min,将抗菌剂接枝在涂层表面,使不锈钢表面获得抗菌性能。获得SS-PDA-L-AMPTMA样品。反应方程式见图2。
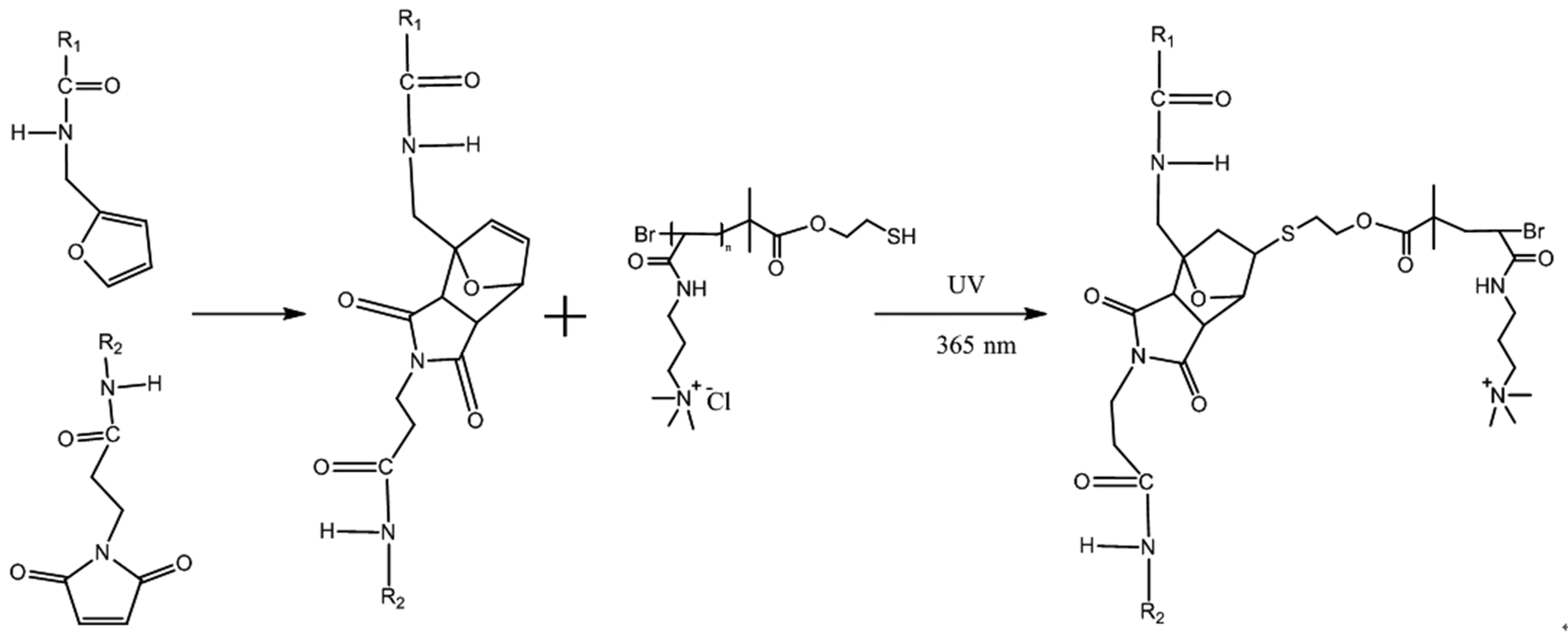
图2点击化学:Diels-Alder及硫醇-烯加成反应;R1:PAA, R2:PEI
Fig.2Click chemistry: Diels-Alder reaction and thiol-ene reaction;R1:PAA, R2:PEI
2.7 细胞毒性测试
将4种样品(SS、SS-PDA、SS-PDA-L、SS-PDA-L-AMPTMA)浸入1X PBS溶液中24 h后,分别收集浸提液备用。取3~5代的成骨细胞,用胰酶将细胞从培养瓶壁上消化下来,用DMEM高糖培养液将细胞悬液的浓度调至5×104cell/ mL。然后在96孔板中,每孔加入细胞悬液100 μL以及4种样品的浸提液100 μL,以1X PBS为空白对照。在细胞培养箱(37℃,5% CO2)中培养24 h使细胞贴壁,然后加入20 μL 的MTT溶液,培养4 h后将孔板中的液体除尽,接着每孔加入150 μL的 DMSO,振荡10 min后,使用紫外分光光度计测量每孔的OD值。细胞存活率见式(1):
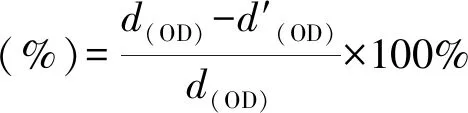
(1)
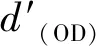
2.8 抗菌性能测试
将4种样品(SS、SS-PDA、SS-PDA-L、SS-PDA-L-AMPTMA)置于24孔板中紫外杀菌30 min。每孔中加入1 mL浓度为107CFU/ mL的S.aureus细菌悬液,放入37℃恒温培养箱分别培养1、3、5 d,将不锈钢片取出用无菌水轻轻冲洗3次,然后放入装有10 mL无菌水的离心管中超声30 min,接着吸1 mL液体加入到另一个装有9 mL无菌水的离心管中进行稀释,重复M次。从M个试管中分别吸取100 μL液体置于MH固体培养基上进行涂平板,取3个平行样。将平板置于生化培养箱(37℃,5% CO2)中培养24 h,统计菌落的个数N。E.coli的抗菌性能的测试方法同上。细菌浓度的计算见式(2);以SS为对照组,抗菌率的计算见式(3):
细菌浓度(CFU/mL)=N×10M+2
(2)
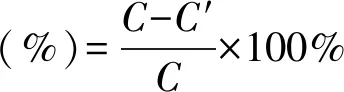
(3)
式中,C为对照样细菌浓度;C′为不同样品的细菌浓度。
3 结果与讨论
3.1 聚合物的结构表征
通过红外光谱图3(a)中可以看到,与PEI相比,PEI-M在波数为3 480 cm-1处出现了N-H键的特征吸收峰;2 800 cm-1处为不饱和C-H键的特征吸收峰;在1 715 cm-1处出现了碳碳双键的特征吸收峰;在1 637 cm-1处出现了C=O键的特征吸收峰;波数为1 175 cm-1处是脂肪环中C-N键的特征吸收峰;波数为768 cm-1处出现了五元环的特征吸收峰。核磁氢谱图3(b)中,δ=5.0为位于a处的C-H,δ=5.9为位于b处的-CH2-,δ=6.25为位于c处的N-H,与结构式中氢位置相对应。
通过红外图谱图3(c)可以看到,与PAA相比,PAA-F在波数为3 500 cm-1处出现了N-H的特征吸收峰;在波数为1 715 cm-1处,碳碳双键的特征吸收峰增强;1 637 cm-1处出现了C=O的特征吸收峰;波数为1 250 cm-1处脂肪环中C-N键的特征吸收峰也增强。核磁氢谱图3(d)中,δ=3.0为位于b处的-CH2,δ=5.5~6.7为位于c、d、e处的C-H,δ=7.4~8.0为位于a处的N-H,与结构式中各氢的位置相对应。
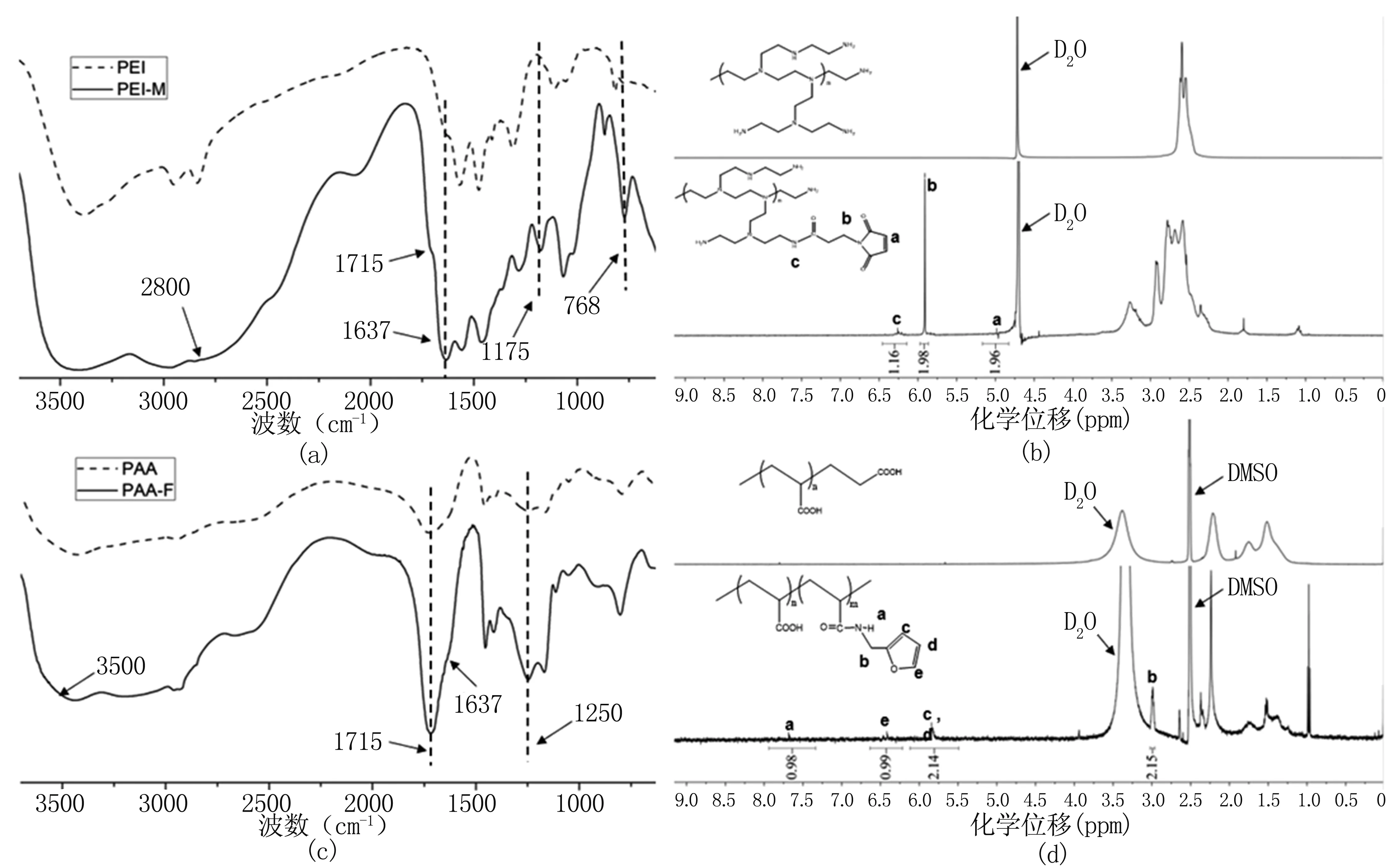
图3(a).PEI和PEI-M的红外光谱图;(b).PEI和PEI-M的核磁氢谱图;(c).PAA和PAA-F的红外光谱图;(d)PAA和PAA-F的核磁氢谱图
Fig.3(a).FT-IR of PEI and PEI-M;(b).1HNMR of PEI and PEI-M;(c).FT-IR of PAA and PAA-F;(d).1HNMR of PAA and PAA-F
3.2 层层自组装以及接枝抗菌剂的过程
由图4(a)可以看出,PEI-M和PAA-F的亲水性不同使得涂层表面水接触角角度在(6.3°±0.8°)~(28.7°±1.4°);从图4(b)中观察到多层膜的厚度在9层后,随着层数的增加而近似线性增加,表明沉积过程稳定。以上数据证明PEI-M和PAA

图4P(EI-M)/P(AA-F)涂层随聚电解质层数增加的关系图(a).水接触角;(b).膜厚-F在基材表面成功进行了层层自组装。
Fig.4Graph of P(EI-M)/ P(AA-F) coating with increasing number of layers(a).Water contact angle;(b).Thickness
由图5可以看到,涂层表面接枝了抗菌剂后,在1 715 cm-1处C=C的特征吸收峰减弱,而在1 093 cm-1处出现了C-S的特征吸收峰,说明表面抗菌剂成功接枝在涂层表面。
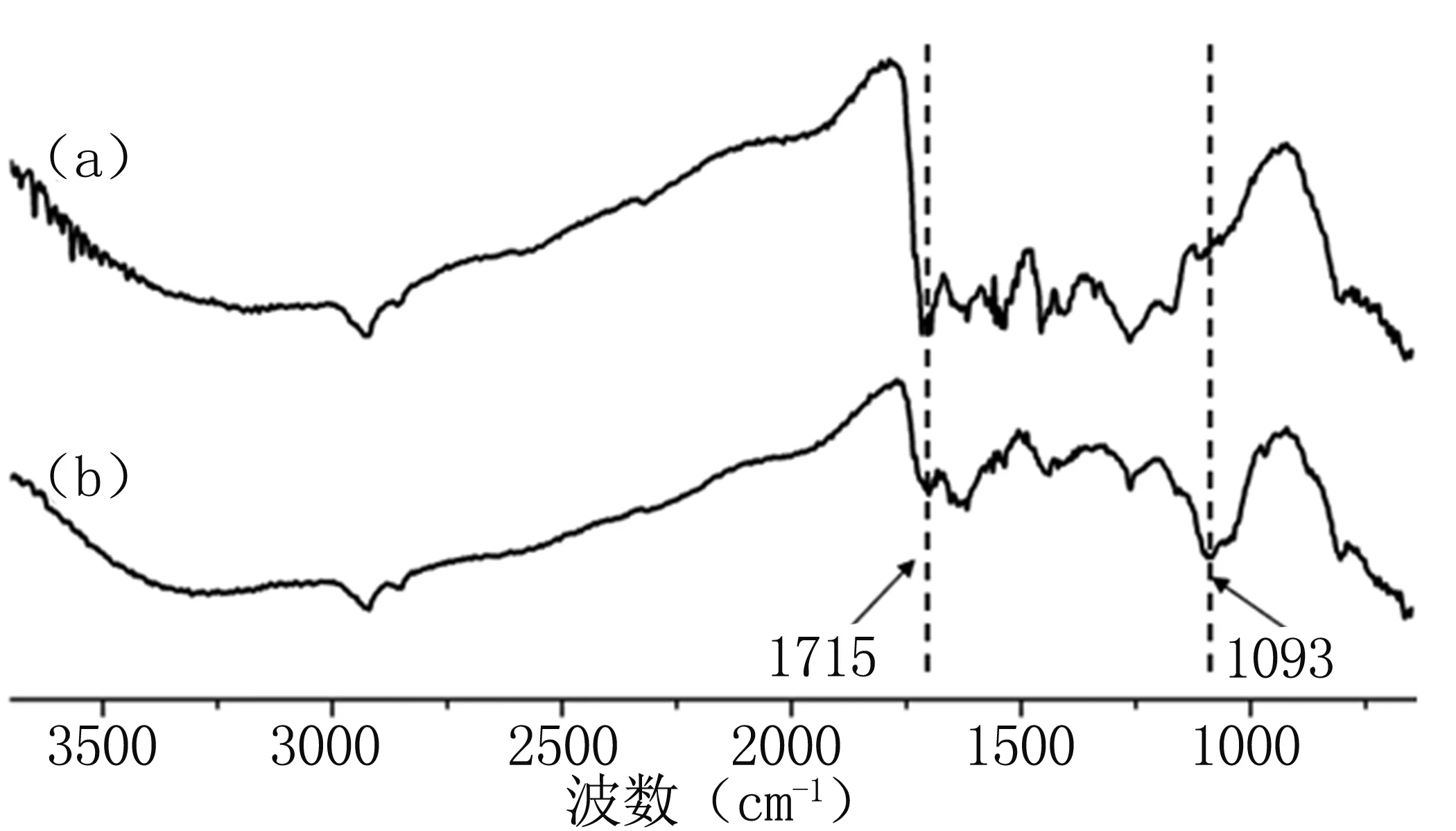
图5 (a).SS-PDA-L的ATR-FTIR图谱;(b).SS-PDA-L-AMPTMA的ATR-FTIR图谱
Fig.5(a).ATR-FTIR of SS-PDA-L;(b).ATR-FTIR of SS-PDA-L-AMPTMA
3.3 涂层细胞毒性测试
由图6可以看出,4种样品对细胞均表现为无毒。SS-PDA-L由于涂层最外层为生物相容性较好的PAA聚电解质,细胞存活率较高,为105.5%;接枝了抗菌剂以后,细胞存活率提高到109.4%,说明将抗菌聚合物接枝到该涂层可以有效降低抗菌剂本身的生物毒性。
3.4 涂层的抗菌性能
为了研究各个涂层表面的抗菌性能,分别采用S.aureus和E.coli进行1、3、5 d的测试。为保持细菌的活性,没有除去培养基,使该实验处于细菌持续繁殖和抗菌剂持续杀菌的动态过程。以SS为对照组,从表1中我们可以看出,SS-PDA由于DOPA具有生物粘性,使得表面更容易粘附细菌,所以细菌浓度高于SS组,抗菌率一直为负;SS-PDA-L虽然表面没有接枝抗菌剂,但凭借表面的超亲水性,使得细菌无法轻易粘附在表面,随着实验天数的增加,涂层表面抗菌率变化不大,因为涂层表面只能抗细菌粘附,且已经达到饱和状态;SS-PDA-L-AMPTMA的抗菌率最高,一方面利用表面的低表面能来抗细菌粘附,另一方面利用接枝的抗菌剂将粘附的细菌杀死,对S.aureus的抗菌率平均在90%,对E.coli的抗菌率则趋于99%,抗菌效果明显。
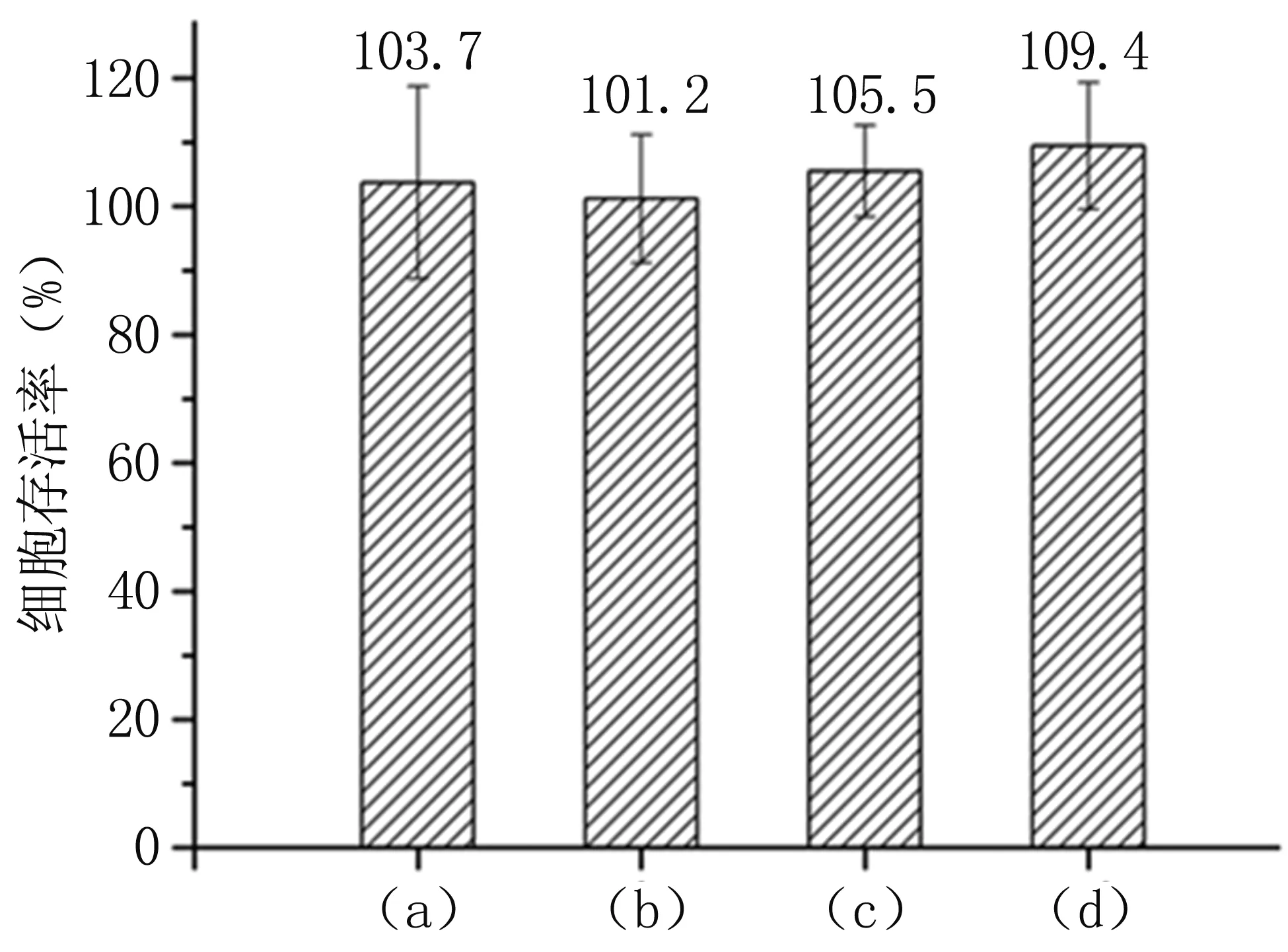
图6 样品的细胞存活率(a).SS;(b).SS-PDA;(c).SS-PDA-L; (d).SS-PDA-L-AMPTMAFig.6 Cell viability (a).SS;(b).SS-PDA; (c).SS-PDA-L;(d).SS-PDA-L-AMPTMA表1 抗菌性能测试Table 1 Antibacterial performance test

细菌种类实验天数(d)抗菌率(%)SS-PDASS-PDA-LSS-PDA-L-AMPTMA1-88.442.990.6S.aureus3-98.958.485.45-37.144.397.41-6.79299.1E.coli3-23.33598.65-10.668.598
4 结论
本研究以PEI和PAA为原料,分别在聚合物链上接枝马来酰亚胺丙酸和糠胺小分子,再利用层层自组装技术在不锈钢基材表面沉积表面抗细菌粘附涂层,最后通过“巯基-烯”点击反应在涂层表面接枝季铵盐类抗菌剂,使自组装涂层具有表面杀菌的能力。通过1HNMR、FT-IR、QCM以及水接触角测试来表征所制备的聚合物结构。并以S.aureus、E.coli为对象进行抗菌测试,结果表明,通过层层自组装技术制备的涂层在接枝抗菌聚合物后,既能抵抗细菌的粘附又杀死材料表面的细菌,抗菌性能得到大幅度提高,而且能持久杀灭细菌,在生物医用材料表面抗菌功能化方面具有良好的应用前景。
