固相萃取-气相色谱法和全二维气相色谱法测定食品接触用纸制品中饱和烃矿物油的迁移量
2019-10-29钱沙沙张玉萍纪晗旭吴肖肖
钱沙沙,杨 洋,张玉萍,庄 棪,纪晗旭,李 宁,吴肖肖,张 驰*
(南京市产品质量监督检验院,江苏 南京 210019)
烃类矿物油(mineral oil hydrocarbons,MOH)是一类极其复杂的烃类混合物,其碳原子数一般在10~50之间,主要包括由直链、支链和环状烷烃组成的饱和烃类矿物油(mineral oil saturated hydrocarbons,MOSH)及由烷基化聚芳烃化合物组成的芳香烃类矿物油(mineral oil aromatic hydrocarbons,MOAH)[1-2]。纸和纸制品中的矿物油主要来源于回收纸制品中的油墨、连接料溶剂和脱模剂[3]。鉴于MOAH潜在的致癌性,其迁移导致的食品安全风险受到广泛重视[4-5]。近年来,随着MOSH新的毒理学数据及危害性不断被披露,联合国粮食与农业组织、世界卫生组织食品添加剂联合专家委员会、德国联邦风险评估研究所也相继规定了MOSH的迁移限量[6-8]。在我国,优恪检测等机构也相继报道了多款奶粉及食用油产品受到MOSH污染的测评报告,引起社会公众的广泛关注[9]。食品接触用纸和纸制品中MOSH的污染情况也十分普遍,消费者长期摄入受到污染的食品,体内的矿物油含量会大量累积,从而造成严重的健康隐患[10]。印刷回收纸中MOSH含量会明显提高,最高可达3 800 mg/kg[11]。在政府开展的食品接触用纸制品风险监测中,MOSH也是重要的监测指标之一,其检出率往往达到20%以上。
纸制品及其迁移液中MOSH的检测是食品安全检测中的难点技术之一[12-13]。目前,国内已有的检测标准方法采用皂化法或荧光法检测矿物油,未能对MOSH和MOAH进行有效分离[14-15]。刘亮等[16]采用气相色谱-质谱法检测矿物油,但是由于矿物油结构信息不足、没有共同的离子碎片也无法有效地分别定量MOSH和MOAH;李克亚等[17-18]将浸泡法、超声波和微波辅助提取3 种提取方法进行对比,用气相色谱法对食品纸包装材料中的矿物油MOSH含量进行了测定,但是检测步骤相对复杂。在2016年的国家级监测中,采用固相萃取-气相色谱法进行样品中MOSH含量和迁移量的检测,实验室在完成监测任务的同时,也出现了部分样品分离效果不佳和检测灵敏度不足的问题。同时,固相萃取-气相色谱法检测步骤繁琐,对操作人员要求较高,容易造成目标物的损失[17,19-21]。国外有高效液相色谱-气相联用法分离检测MOSH和MOAH的报道,它通过液相色谱与气相色谱的接口技术实现在线净化、富集,有效提高了矿物油的分离,但是仪器价格昂贵,较难普及[22]。
全二维气相色谱是利用化合物沸点和极性的不同,进行二次分离,能够对普通气相色谱无法解决的碳混合物进行有效地分离定量[23]。最新研究表明,在相同分析时间和检测限条件下,全二维的峰容量可达到普通一维色谱的10 倍[24]。但是利用全二维气相色谱法检测食品接触用纸制品中MOSH还鲜少被使用。
本研究完善了国内常用的固相萃取-气相色谱法检测,同时建立并优化了全二维气相色谱法,应用固相萃取-气相色谱法和全二维气相色谱法分别对食品接触用纸制品中MOSH的迁移量的检测技术进行方法学比较,并分别对实际样品进行检测,验证方法的实用价值。
1 材料与方法
1.1 材料与试剂
MOSH(纯度≥99%),MOAH标准母液(EPA方法610混合多环芳烃PAHs 16 种化合物混合标准溶液,质量浓度均约为2 000 mg/L),矿物油保留时间检测标准溶液(C7~C40正构烷烃混合标准溶液,质量浓度均1 000 mg/L),双环已烷(bicyclohexyl,Cycy)(CAS号:92-51-3,纯度≥99.5%),胆甾烷(cholestane,Cho)(CAS号:481-21-0,纯度≥99%),1-甲基萘(1-methylnaphthalene,1-MN)(CAS:90-12-0,纯度≥98%),1,3,5-三叔丁基苯(1,3,5-tri-tertbutylbenzene,TBB)(CAS号:1460-02-2,纯度≥98%),十八烷基苯(octadecylbenzene,C18-B)(CAS号:4445-07-2,纯度≥95%);己基苯(1-phenylhexane,C6-B)(CAS号:1077-16-3,纯度≥90%);正己烷、二氯甲烷、异辛烷、乙醇(均为色谱纯);0.3%硝酸银硅胶柱。所有上述标准品均为德国Dr. Ehrenstorfer公司生产,所有标准品和试剂耗材均购自上海安谱实验科技股份有限公司。
1.2 仪器与设备
7890B气相色谱仪(火焰离子化检测器) 安捷伦科技有限公司;固态热调制器(SSM1800/HV系列调制柱及Canvas 1.0.12.6雪景科技数据处理软件) 雪景电子科技(上海)有限公司;BSA224S电子天平 德国赛多利斯公司;SA8旋涡振荡器 比比科技有限公司;TS-18823氮吹仪 赛默飞科技有限公司。
1.3 方法
1.3.1 溶液的配制
正己烷-二氯甲烷混合洗脱溶液:分别量取正己烷80 mL,二氯甲烷20 mL,混合均匀,配成正己烷-二氯甲烷(8∶2,V/V)洗脱溶液。
混合内标中间溶液:准确称取10 mg(精确至0.01 mg)各内标物(Cycy、Cho、TBB、1-MN用于固相萃取-气相色谱法;Cycy、Cho、TBB、1-MN、C18-B、C6-B用于全二维气相色谱法),用正己烷溶解,定容至100 mL刻度。充分摇匀,混合内标中间溶液终质量浓度应为100 mg/L。
MOSH标准中间溶液:准确移取适量的石蜡油标准储备溶液,用正己烷定容至刻度,充分摇匀,配成400 mg/L的标准中间溶液,MOSH标准曲线点各质量浓度分别为10、20、50、100、200 mg/L。
MOAH标准中间溶液:准确移取MOAH标准母液至容量瓶中,用正己烷稀释定容,充分摇匀,配成20 mg/L的MOAH标准中间溶液。
C7~C40正构烷烃混合标准溶液:准确移取C7~C40正构烷烃混合标准溶液于容量瓶中,用正己烷稀释定容至刻度,充分摇匀,配成20 mg/L。
1.3.2 色谱条件
固相萃取-气相色谱法:色谱柱:CD-5HT石英毛细管柱(30 m×0.25 mm,0.1 µm);升温程序:初始温度50 ℃,以2.5 ℃/min升至60 ℃,然后以22 ℃/min升至280 ℃,再以30 ℃/min升至325 ℃,保持11 min;进样口温度275 ℃;火焰离子化检测器温度340 ℃;载气:氮气;柱流量1.5 mL/min;进样体积1 µL;进样方式:不分流。
全二维气相色谱法:一维色谱色谱柱:DB-5HT(30 m×0.25 mm,0.1 µm);二维色谱色谱柱:DB-17MS(0.7 m×0.18 mm,0.18 µm);调制柱:初始温度50 ℃保持3 min,以13 ℃/min升至310 ℃,保持15 min;进样口:280 ℃,不分流进样;进样量:1 µL;检测器温度:320 ℃;梯度流速:1.5 mL/min保持13 min,以0.1 mL/min升至2.6 mL/min,保持6 min;调制器出口端升温程序:50 ℃保持3 min,以13 ℃/min升温至310 ℃保持15 min;调制器进口端温度程序: 50 ℃保持6.85 min,以13 ℃/min升温至260 ℃保持7 min。
1.3.3 样品迁移实验
依照GB 31604.1—2015《食品接触材料及制品迁移试验通则》[25]预期接触油脂及表面含油脂食品的冰淇淋筒、淋膜纸杯、吸油纸、烘焙纸、烧烤纸,选择异辛烷替代油酯类食品模拟物,迁移温度为70 ℃,迁移时间为2 h;预期接触含酒精类食品的纸制品,选择50%的乙醇溶液为模拟液,迁移温度为40 ℃,迁移时间为2 h;样品面积和模拟液体积的浸泡规则依照GB 5009.156—2016《食品接触材料及制品迁移试验预处理方法通则》[26]进行。
1.3.4 样品前处理
固相萃取-气相色谱法:加入6 mL正己烷活化平衡柱,在加载样品前,应始终保持硝酸银硅胶固相萃取小柱湿润,防止干涸。准确移取10 mL迁移液,加入60 µL混合内标中间溶液,混匀,室温下氮吹浓缩至约1 mL,全部转移至小柱上,用10 mL玻璃浓缩管开始收集矿物油MOSH部分,分两次共加6.0 mL正己烷洗脱MOSH部分,当第2次正己烷流至上玻璃纤维滤膜时,关闭阀门,更换成大的玻璃浓缩管,收集矿物油MOAH部分,分两次共加15.0 mL正己烷-二氯甲烷混合洗脱液,洗脱矿物油MOAH部分。将收集的矿物油MOSH部分和MOAH部分氮吹浓缩至约1 mL,防止吹干,最后用正己烷定容至1.0 mL,供进样测定。
全二维气相色谱法:准确移取25 mL迁移液于具塞玻璃管中,加入60 µL混合内标中间溶液和5 mL蒸馏水,10 mL正己烷,涡旋振荡,待溶液分层,取上清液,室温下氮吹至尽干,最后用正己烷定容至1.0 mL,供进样测定。
2 结果与分析
2.1 标准溶液色谱检测结果
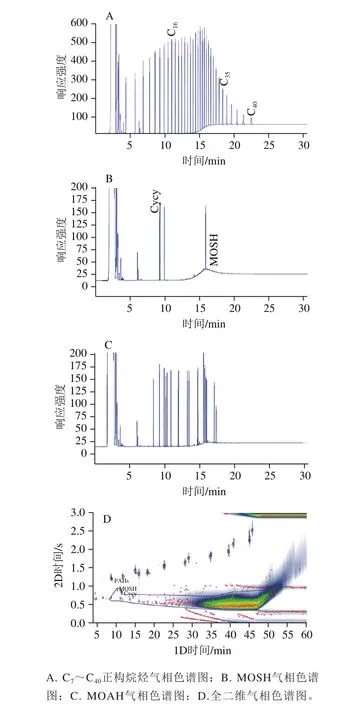
图1 标准溶液色谱图Fig. 1 Chromatograms of standards
在开展食品接触用纸制品中矿物油的分析之前,使用C7~C40正构烷烃混合标准工作溶液确定气相色谱分析条件以及确定矿物油的保留时间。从图1A可以看出,C7~C40正构烷烃标准品保留时间为6.00~23.00 min,完成整个色谱的分析时间为17 min,目标物MOSH(C16~C35)的保留时间为11.00~19.00 min,由于目标物的馏程较宽,沸点差距大,因此采用不分流进样。权衡分离效果和溶剂效应,选择1.3.2节部分所述的程序升温条件。
从图1B可以看出,MOSH是一个类似“驼峰”的宽峰[27],保留时间为11.00~19.00 min,和使用保留时间检查标准溶液C7~C40正构烷烃得到的保留时间结果一致。从图1C可以看出,MOAH标准品的保留时间为8.00~17.00 min,与MOSH在保留时间11.00~19.00 min有部分重合。因此,如果样品中同时存在MOSH和MOAH,采用常规气相色谱法无法将两者分开,更无法定量,需要通过一定的前处理步骤,才可以实现常规气相色谱上MOSH的有效分离。
在全二维气相色谱上,分别按照上述色谱条件,对100 mg/L的MOSH标准溶液、5 mg/L的C18-B、C6-B、Cho、TBB、Cycy、1-MN的6 种内标混标溶液、4 mg/L的C7~C40正构烷烃标准溶液,50 mg/L MOSH、50 mg/L MOAH进行进样。由图1D可见,MOSH被6 种内标物质和C7~C40正构烷烃所形成的轮廓包围,形成雾状条带,在全二维上清晰地与MOAH分开。因此,在全二维气相色谱法上,将样品迁移液简单浓缩后进样,即可实现MOSH的检测。
2.2 MOSH的分离与检测结果
采用硝酸银硅胶萃取小柱进行样品的前处理。在迁移液中,加入Cycy、Cho、1-MN和TBB四种内标液。由于MOSH和MOAH先后流出,通常采用Cho和TBB作为定位标记物,用于标示MOSH和MOAH的分离情况[28]。Cycy和Cho在MOSH部分,Cycy为定量内标;1-MN和TBB在MOAH部分,1-MN为定量内标。固相萃取后,样品的MOSH的气相色谱图见图2A,图中仅出现了标记物Cho,未出现MOAH的标记物TBB,说明MOSH得到有效分离[28];根据MOSH标准溶液的气相色谱图(图1B),MOSH的保留时间在11.00~19.00 min。图2A中,在11.00~19.00 min出现了明显的色谱峰,判断为MOSH。进一步的加标实验也表明此“驼峰”为MOSH。因此固相萃取-气相色谱法实现了样品中MOSH的有效分离,可实现分开定量。
在全二维气相色谱上,对样品浸泡得到的迁移液浓缩定容后直接进样,并依次点选内标物质的上边沿和下边界物质的下边沿,由软件自动连接成闭合区域,建立了MOSH的积分区域[29]。由图2B可见,内标物质和目标物形成了岛状区域,岛边界是内标物质围成的闭合区域,岛内物就为目标物MOSH,而MOAH在岛之外。表明全二维气相色谱法不需要经过复杂的前处理,就可以实现样品中MOSH的有效分离和定量。
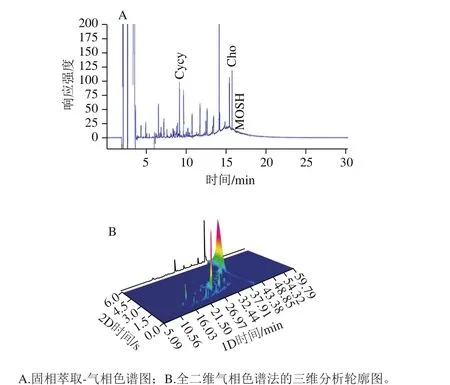
图2 实际样品色谱图Fig. 2 Chromatograms of real samples
2.3 方法标准曲线、检出限、定量限、加标回收率和精密度
在固相萃取-气相色谱中,使用10、20、50、100、200 mg/L标准溶液,方法的线性方程为Y=0.010 7X-0.003 1,R2=0.998 8。根据Moret等[30]提出的固相萃取法-气相色谱检出限和定量限计算方法,得到本方法检出限为5 mg/L,定量限为10 mg/L。在全二维气相色谱法中,使用10、20、50、100、200 mg/L的MOSH标准溶液,方法的线性回归方程为:Y=0.0175X+0.0297,R2=0.990 7,该方法的检出限为1.0 mg/L,定量限为2.5 mg/L。
使用20 mg/L和50 mg/L的MOSH加标溶液,对50%乙醇迁移液进行加标回收和精密度测试。如表1所示,固相萃取-气相色谱法MOSH的回收率为79.2%~88.5%,相对标准偏差为4.3%;全二维气相色谱法的回收率为94.4%~102.4%,相对标准偏差也为4.3%。
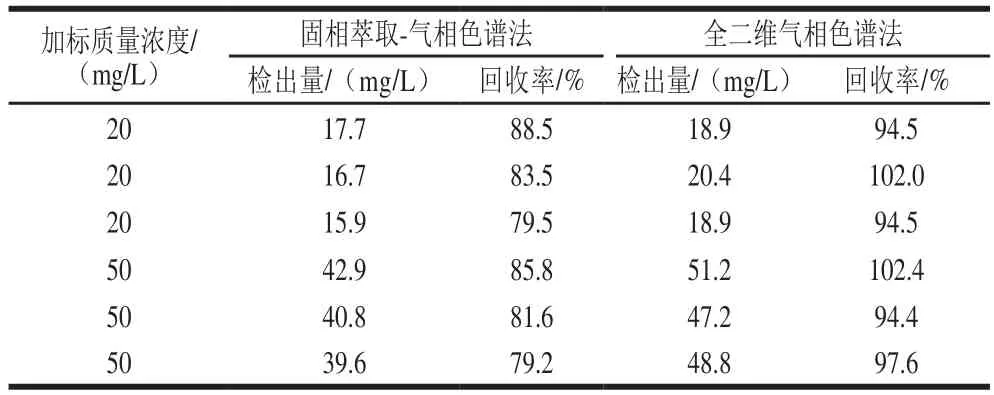
表1 MOSH的方法回收率测试结果Table 1 Recoveries of MOSH from spiked samples
2.4 实际样品的检测结果
分别采用上述两种方法,对从市场上随机抽取的17 批食品接触纸及纸制品中MOSH的迁移量进行检测。所有样品均采用异辛烷模拟液和乙醇模拟液进行迁移实验。结果表明,所有样品的异辛烷迁移液中均未检出MOSH。在乙醇模拟液中,共有7 个样品(3 个防油纸和4 个淋膜纸杯)使用两种方法均检出了MOSH。这7 个样品的固相萃取-气相色谱法和全二维气相色谱法的检出值分别为(38±4.2)mg/L和(42±4.1)mg/L,偏差为8.6%。
值得注意的是,有1 个冰淇淋筒样品,其乙醇模拟液利用固相萃取-气相色谱法未检出MOSH,但是全二维气相色谱法的检测值为4.8 mg/L。这可能是由于固相萃取-气相色谱法前处理复杂,造成目标物的流失导致检出限偏高,而全二维气相色谱法则具有更低的检出限和更好的适用性。从图3A可以看出,使用固相萃取-气相色谱法时,色谱图在11.00~19.00 min未发现MOSH的峰,未检测到MOSH;但是,图3B中全二维气相色谱图中MOSH积分区域出现了明显的目标物雾状条带。
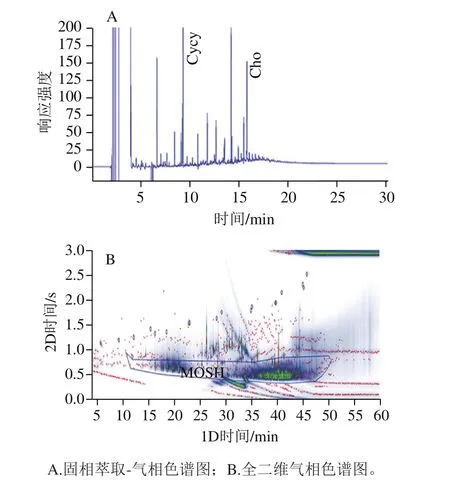
图3 冰淇淋筒样品色谱图Fig. 3 Chromatograms of MOSH from ice cream container
3 结 论
本研究在完善固相萃取-气相色谱法对食品接触用纸制品中MOSH迁移量检测技术的同时,建立并优化了全二维气相色谱法,开展了两种技术的方法学比较,并在实际样品的检测中验证其实用价值。两种方法均能实现迁移液中MOSH的有效分离,均可以有效地检测食品接触材料中的MOSH迁移量。固相萃取-气相色谱法在前处理的过程中采用固相萃取分离MOSH和MOAH,然后用气相色谱进行测试;全二维气相色谱法不需要复杂的固相萃取前处理,对样品浸泡得到的迁移液浓缩定容后就可以直接进样,相较固相萃取-气相色谱法前处理简单,检出限低、回收率高。两种方法的相对标准偏差基本一致。在对实际样品的检测中,全二维气相色谱法具有更广泛的适用性,可对固相萃取-气相色谱法不能检出的样品进行检测与定量。
本研究针对当前食品接触材料检测中的关键问题,开展创新方法开发和验证。采用固相萃取-气相色谱法和全二维气相色谱法对食品接触用纸制品中MOSH检测优化和比较评价,也为新标准的制定提供了重要的方法学基础数据支撑。
