LMNA基因突变与先天性心脏病患者的关系研究
2019-10-26王涵磊林志勇葛捍伟薛继阳楼志凌赵琦峰
林 炜 王涵磊 林志勇 葛捍伟 薛继阳 楼志凌 赵琦峰
先天性心脏病(congenital heart disease,CHD)简称先心病,是一种由多因素导致的疾病,其致病机制十分复杂,致病因素主要是环境因素和基因因素[1]。先天性心脏病是先天性遗传病最常见的类型,发生率约为0.6%~1.2%[2]。大约5%~8%的CHD是由于染色体的异常引起的,其中3%的基因缺陷在一级家庭成员中具有高复发风险[3]。我国的先心病发生率呈逐年上升趋势,每年大约有15万~20万的先心病患儿出生[4]。研究CHD的分子机制,不仅对CHD发生的机制和遗传干预有重要的理论依据作用,而且为探索行之有效的疾病筛查和诊治技术预防CHD的发生提供新的思路。
LMNA基因是编码核纤层蛋白,核纤层蛋白的异常会导致多种疾病的发生,根据临床特征不同,至今被认识的核纤层蛋白病已有10余种,包括Emery-Dreifuss肌营养不良、Hutchinsong-Gilford早衰综合征(Hutchinsong-Gilford progeria syndrome,HGPS)、扩张性心肌病等[5]。LMNA基因突变会引起多种心脏异常,如心肌病、心脏传导异常等,但与先天性心脏发育异常的关系研究未见报道。本研究团队早期发现1例先天性心脏发育异常[室间隔缺损(VSD)+房间隔缺损(ASD)]伴HGPS的患者(图1),早衰综合征是罕见的儿童过早衰老性疾病,研究发现绝大多数HGPS病例的遗传基础是在LMNA基因的第11个外显子中G608G发生了突变[6]。笔者对该患者进行高通量外显子测序和群体比对,发现其致病基因也是LMNA基因,并发现了LMNA基因的新突变c.407A>G,蛋白质水平突变为p.D136G(图2);笔者对具体突变进行分析,发现突变位点高度保守,同时利用多种软件预测都提示该突变为致病突变(图3)。已有报道研究人员利用CRISPR基因编辑技术成功对HGPS突变DNA进行定点编辑及修正[7]。本研究通过分析LMNA基因与先天性心脏病的关系,为未来提早干预并治疗先心病提供可能。
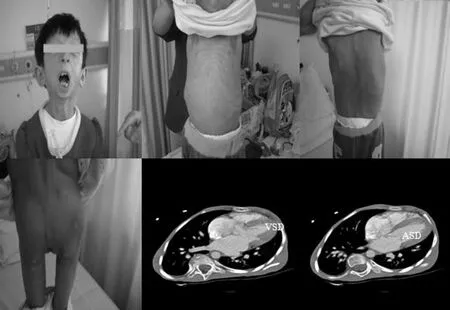
图1 CHD(VSD+ASD)伴HGPS的患儿

图2 新发现的LMNA基因突变

图3 LMNA基因新突变保守性分析及预测
编码核纤层蛋白的LMNA突变可引起一系列表型不同的疾病,本研究拟利用新一代基因测序技术探讨LMNA基因突变与人类先天性心脏发育异常的关系,从基因层面探索CHD患者的遗传学背景,分析LMNA突变在先天性心脏发育异常中的比例与分布情况。
资料与方法
1.一般资料:选取2016~2017年温州医科大学附属第二医院小儿心胸外科所收治的100例CHD患者并随机选取100例种族匹配的例行身体检查的健康儿童作为对照组。CHD组男性62例,女性38例,患儿年龄0.5~14岁,平均年龄2.1±2.7岁。对照组男性60例,女性40例,年龄1~12岁,平均年龄2.4±2.1岁。所有CHD患者均经超声心动图、心电图、胸部X线片及心脏手术确诊,排除综合性先天性心脏病患儿(如Down 综合征、DiGeorge 综合征)。本研究经温州医科大学伦理学委员会批准,且患儿或家属均知情同意并签字。
2.标本采集:患儿均采集空腹外周静脉血4~5ml至EDTA抗凝采血管中,混匀,将标本存放于-80℃冰箱中,待测。
3.制备基因组DNA:用常规饱和酚-氯仿法提取基因组DNA:①将300~400μl血液加入至1ml细胞裂解液中,充分颠倒混匀后,8000r/min离心10min至细胞沉淀较完全;②弃去上清,取1ml细胞裂解液加入,用枪头轻轻吹打使细胞沉淀散开,继续8000r/min离心5min;③重复步骤②直至液体澄清;④弃去上清,分别将STE 300μl、20%SDS 20μl、蛋白酶K(10μg/μl)15μl加入离心管中,充分混匀后置于50℃水浴锅中12h;⑤12h后从水浴锅中取出离心管,取100μl饱和NaCl溶液(6mol/L)加入,轻轻晃动可见白色沉淀析出,继续冰浴10min至沉淀完全析出,4℃环境下5000r/min离心10min;⑥取出上清液至新的离心管中,在通风橱中取等量体积酚/氯仿/异戊醇(25∶24∶1)加入, 5000r/min离心10min,取上清后加入3倍体积冷乙醇,轻轻颠倒摇晃,有白色絮状DNA沉淀析出;⑦4℃环境下5000r/min离心10min,弃去冷乙醇,可见离心管底有块状DNA沉淀,将离心管倒置于滤纸上使水分自然晾干;⑧加入200μl TE Buffer,并利用紫外分光光度计测定所得DNA浓度,4℃冰箱中保存。
4.引物设计LMNA:LMNA基因序列来自GenBank(NC_000001.11)。利用Primier 5.0软件设计1~12号外显子的PCR引物用于扩增目的片段及测序,引物序列见表1。
5.LMNA基因1~12号外显子PCR反应体系:从离心管中根据所测浓度取出模板DNA约20ng,加入正向与反向引物(10pmol/L)各1μl,2×PCR Master Mix(Thermo Fisher Scientific)10μl,补双蒸水至20μl。其中,PCR 的发生条件如下: 预变性环节,温度95℃,时间5min; 变性环节,温度95℃,时间30s; 退火环节,温度范围55℃,时间60s; 延伸环节,温度72℃,时间30s; 终延伸环节,温度72℃,时间5min。共35个循环。

表1 LMNA基因1~12号外显子引物序列
6.基因测序: 将PCR产物回收送杭州擎科梓熙生物技术有限公司,以PCR上游引物为测序引物,用ABI 3730xl 自动测序仪进行测序,使用序列分析软件SnapGene分析测序结果并将所测序列与GenBank 中的已知序列进行比来识别基因变异。
结 果
1.PCR结果:琼脂糖凝胶电泳验证PCR产物并与标准DNA Marker比对,各PCR产物与设计的各片段大小基本符合。
2.DNA测序结果:在CHD患者组中的LMNA基因中均未发现突变。
讨 论
LMNA基因位于1q21.2~q21.3,基因组序列长度56.7kb,其中编码区域长度约为24kb,共编码12个外显子。LMNA基因转录时,10号外显子会发生选择性剪切,此时会有两种不同的mRNAs,分别编译两种不同的蛋白,即prelamin A和lamin C[8]。prelamin A的C末端是“CAAX”模序,经金属蛋白酶Zmpste24、肽链内切酶2、异戊烯半胱氨酸羧基端甲基转移酶作用后转化为lamin A[9]。lamin C和lamin A的N末端有相同的566个氨基酸残基,由LMNA基因编码的这两种主要产物lamin A/C 属于核膜中间丝蛋白,其作用在于维持细胞核膜内层结构和功能,是核膜中主要的骨架蛋白,它在染色质结构和基因组的空间定位中发挥作用并能决定细胞核的大小和形状[10,11]。越来越多的证据表明,在DNA复制、RNA转录、细胞分化和凋亡中lamin A/C也参与并发挥着重要的作用[12]。有许多研究已经明确了LMNA基因的400多种突变,可表达20多种不同的表现型,与心肌病相关位点就多达100多个,导致各种不同类型的心肌病[13]。LMNA基因突变导致的扩张性心肌病特征为心腔大、室壁薄、常伴有心脏传导系统疾病、发病早、预后差[14]。笔者前期发现的1例LMNA基因突变国际上尚无报道,此病例患儿表现为早老症,涉及心血管、骨骼、肌肉及皮肤脂肪等多种系统和组织异常,并无心肌病的表现,但存在CHD(VSD+ASD),关于LMNA基因与CHD的相关性目前国内外尚无研究报道。
本研究分别通过对100例CHD患儿及100例正常体检儿童进行LMNA基因的突变筛查,结果未发现任何突变,LMNA基因突变与CHD患者之间可能无明显相关性。基因在地区、人群、遗传背景中的分布具有不同的特异性,因此要从多地区、多人群、大样本的研究中才能明确某一基因在致病过程中发挥的作用,从根本上解释发病机制。因此,LMNA基因突变是否对CHD具有致病意义尚需要进一步的研究。本研究未发现LMNA基因的致病性突变,笔者认为可能与以下几个因素有关:①前期发现的LMNA基因突变伴有其他心脏、神经、肌肉、脂肪代谢障碍等病变,而本研究中患者具有这些病变的比例较低;②LMNA基因的突变在先天性心脏病中较为罕见,其突变可能并非是导致先天性心脏病的原因;③研究的样本数量还不够大,后续如果有更大的样本量也许能发现LMNA基因的其他致病性突变。
