结核性脑膜炎患者磁共振血管成像异常的危险因素分析
2019-10-23杜训松强光刘张培培
宋 培 杜训松* 陆 松 强光刘 张培培
结核性脑膜炎是肺外结核的常见且严重类型,亦是常见的慢性与亚急性脑膜炎,其病理改变在于脑积水、基底池渗出、脑梗死及肉芽肿等[1]。结核性脑膜炎患者的病死率较高,即便是存活的患者,也有约50%的伴有神经功能缺损[2]。深入探究结核性脑膜炎患者颅内动脉病变,对加深结核性脑膜炎继发脑梗死的认识,及时采取有效措施减少脑梗死的发生和改善患者预后状况具有重要意义。
磁共振血管成像(magnetic resonance angiography,MRA)是近年来临床常用的影像学检查手段之一,其具有安全、简单方便、无需造影剂、无创等临床优势在临床应用较广,对多种脑血管疾病的诊断均具有良好的应用价值[3]。本研究通过回顾性分析的方式,探讨结核性脑膜炎患者发生MRA异常的危险因素。
1 资料与方法
1.1 一般资料
回顾性收集2015年1月至2018年8月安徽省第二人民医院收治的85例结核性脑膜炎患者的临床资料,其中男性51例,女性34例;年龄23~68岁,平均年龄(37.97±9.13)岁;病程12~35 d,平均病程(19.07±3.25)d。根据MRA是否异常,将其分为MRA正常组(48例)和MRA异常组(37例)。患者临床表现为局灶性肢体无力、颅神经损害、意识障碍、癫痫发作等,分析其病情严重程度,影像学检查,是否伴有脑积水、颅底粘连及结核瘤等。本研究经医院伦理委员会批准,且患者及家属知情同意。
1.2 纳入与排除标准
(1)纳入标准:①符合结核性脑膜炎的临床诊断标准[4];②年龄≥18岁;③入院后7 d内接受磁共振成像(magnetic resonance imaging,MRI)常规序列扫描及MRA检查。
(2)排除标准:①伴有糖尿病、高血压、结缔组织疾病、心律失常及其他已知脑血管疾病的危险因素;②伴有脑血管病史;③存在MRI、MRA检查禁忌证;④入院前已接受抗结核治疗,且疗程>1周;⑤临床资料不全。
1.3 仪器设备
采用Signa HDX型3.0T MR扫描仪(美国GE公司)。
1.4 检查方法
采用3.0T MR扫描仪行T1加权像、T2加权像、液体衰减反转恢复序列、T1增强、弥散加权成像及MRA序列检查,分别由神经内科及放射科医师独立阅片,判断患者是否存在脑积水、梗死灶、结核瘤及颅底渗出粘连等情况。
1.5 观察与评价指标
(1)意识障碍。采用格拉斯哥昏迷评分[5]评价患者意识情况,15分表示意识清楚,12~14分为轻度意识障碍,9~11分为中度意识障碍,≤8分为昏迷。
(2)病情严重程度。①1级,无意识障碍,无局灶神经系统体征;②2级,无意识障碍,但出现局灶神经系统体征;③3级,出现意识障碍,局灶神经系统体征[6]。
(3)影像学检查。主要包括胸部影像学等相关检查,MRA异常定义为颅内动脉管腔弥漫性不规则,或颅内动脉局灶性管腔至少50%狭窄和闭塞,单个动脉局部低于50%狭窄判为MRA正常[7]。若读片结果存在意见不一时,则由二者协商后确定。
1.6 统计学方法
2 结果
2.1 患者MRA影像表现
85例患者中人类免疫缺陷病毒(hu man immunodeficiency virus,HIV)均为阴性;MRA异常37例,发生率为43.53%,包括颅内动脉局灶性狭窄或闭塞17例,颅内动脉管腔弥漫性不规则20例。颅内动脉局灶性狭窄或闭塞共35条,其中受累动脉主要为大脑中动脉(18条),MRA异常影像见图1。
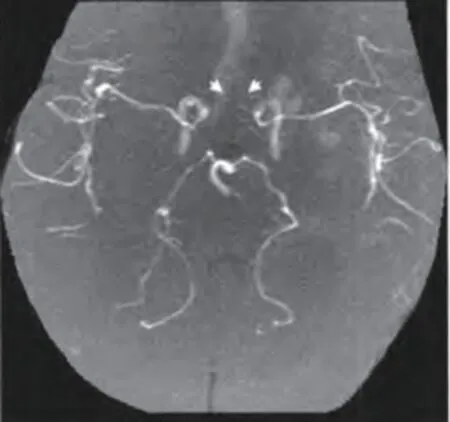
图1 结核性脑膜炎患者MRA异常影像
2.2 两组患者MRA异常单因素分析比较
(1)单因素分析,患者年龄≥60岁、病程≥3周、病情严重程度为3级、脑积水、局灶性肢体无力、颅底粘连、颅神经损害及结核瘤的患者MRA异常率与年龄<60岁、病程<3周、病情严重程度为1~2级、无脑积水及无局灶性肢体无力比较,差异有统计学意义(t=6.05,t=20.11,t=6.11,t=4.92;P<0.05),见表1。
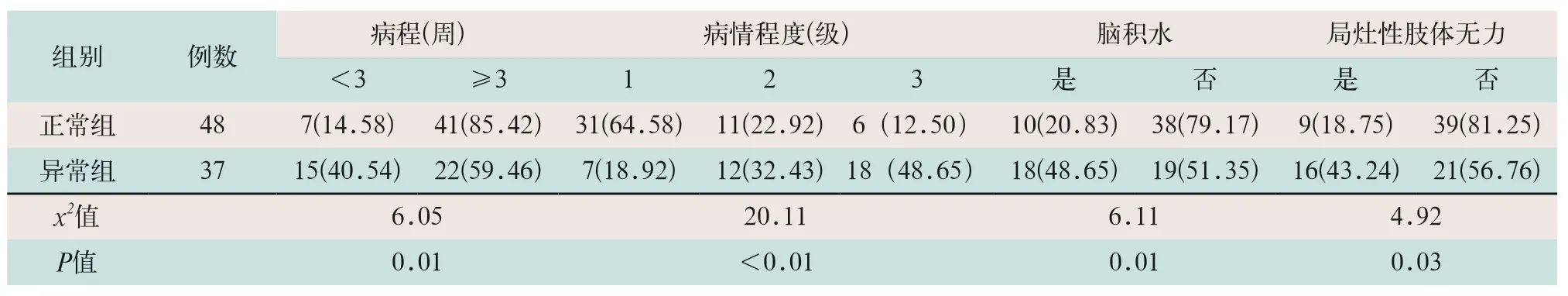
表1 两组患者MRA异常中病情严重程度、脑积水及局灶性肢体无力单因素分析[例(%)]
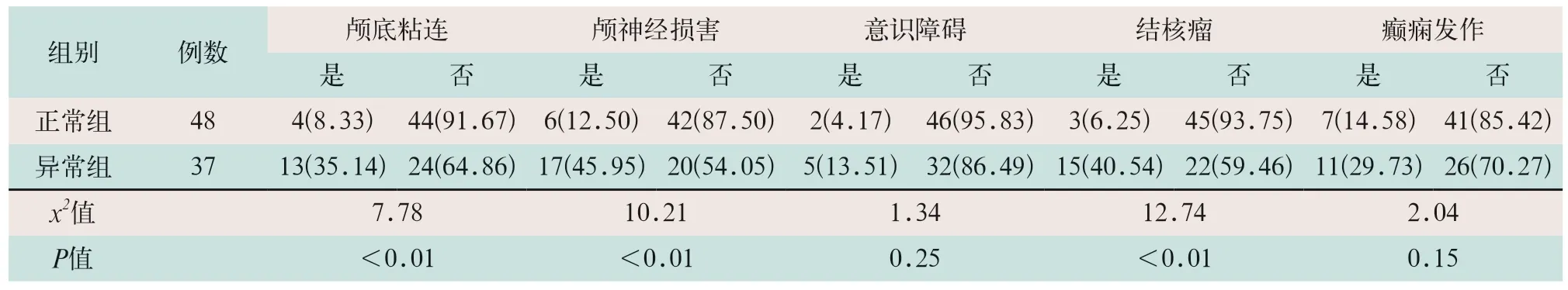
表2 两组患者MRA异常中颅底粘连、颅神经损害、意识障碍、结核瘤及癫痫发作单因素分析[例(%)]
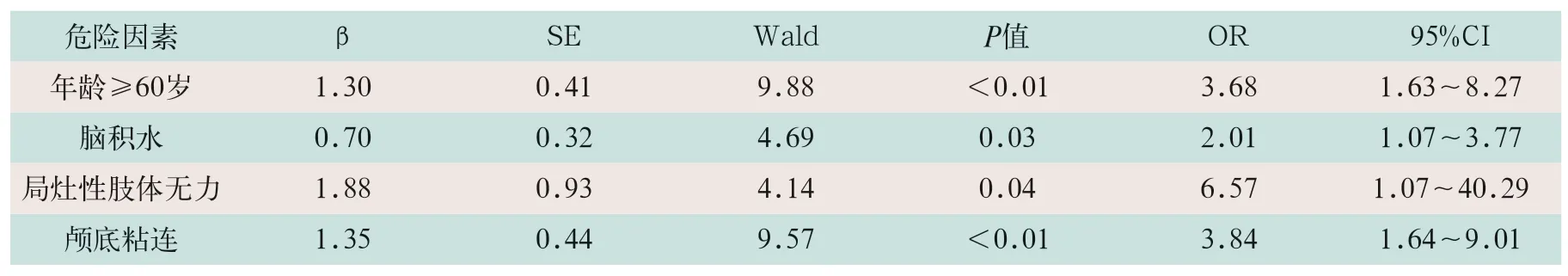
表3 结核性脑膜炎患者MRA异常多因素分析
(2)两组患者无颅底粘连、无颅神经损害及无结核瘤者明显升高,差异有统计学意义(t=7.78,t=10.21,t=12.74;P<0.05);而伴有意识障碍和癫痫发作的患者两组比较,差异无统计学意义(t=1.34,t=2.04;P>0.05),见表2。
2.3 患者MRA异常多因素分析
以单因素分析结果中具有统计学意义的指标为自变量,以MRA是否异常为因变量纳入多因素Logistic回归分析。患者年龄≥60岁、脑积水、局灶性肢体无力及颅底粘连是结核性脑膜炎患者出现MRA异常的独立危险因素,见表3。
3 讨论
在结核性脑膜炎患者中,继发脑梗死的发生率为13%~57%,是患者致残的主要原因[8]。结核性脑膜炎病程早期通常因颅内动脉痉挛而引发脑梗死,但随着病情程度的加重,可继发增殖性动脉内膜病变[9]。结核性脑膜炎导致动脉损害而继发脑梗死在目前仍未得到足够关注和重视,脑膜纤维素性渗出是结核性脑膜炎的主要病理表现,其渗出物主要聚积于前颅窝、视交叉及脚间窝,且可向外侧裂延伸,炎症可蔓延累及走行于其间的动脉[10]。随着结核性脑膜炎病情的进展及病程的延长,颅内动脉特别是颅底动脉可经历炎症—痉挛—收缩—栓塞的过程[11]。
目前,仅有少数研究报道结核性脑膜炎后颅内动脉病变的血管减影造影、MRA及CT血管造影等影像学表现,国内研究有关结核性脑膜炎患者颅内动脉损害MRA表现的报道并不多见[12]。Kalita等[13]研究报道,结核性脑膜炎患者MRA异常率为50%~70%,且以大脑中动脉或颈内动脉颅内段为主要受累动脉。本研究结果显示,85例结核性脑膜炎患者中,MRA异常37例,发生率为43.53%,表明结核性脑膜炎患者出现MRA异常的情况并不少见,应引起临床重视。同时,本研究表明,结核性脑膜炎患者颅内动脉损害容易使前循环受累,且易累及多动脉,如大脑中动脉等,这与结核性脑膜炎患者炎症容易累及颅底部使得Willis环邻近的动脉受累的观点相符[14]。
本研究经单因素分析结果发现,年龄≥60岁、病程≥3周、病情严重程度为3级、脑积水、局灶性肢体无力、颅底粘连、颅神经损害及结核瘤的结核性脑膜炎患者MRA异常率较年龄<60岁、病程<3周、病情严重程度为1~2级、无脑积水、无局灶性肢体无力、无颅底粘连、无颅神经损害及无结核瘤者明显升高。进一步行多因素Logistic回归分析发现,年龄≥60岁、脑积水、局灶性肢体无力及颅底粘连是结核性脑膜炎患者出现MRA异常的独立危险因素,其结果表明,年龄≥60岁的结核性脑膜炎患者MRA异常率明显高于年龄<60岁者,这与年龄是诱发多种脑血管疾病的影响因素[15]的观点相符,提示随着结核性脑膜炎患者年龄的增长,其发生颅内动脉损害的风险性亦会随之升高,最终可诱发脑梗死。发生脑积水时,血流速度明显减缓,因脑室变形而压迫颅内动脉,这可能是导致颅内动脉形态异常的主要原因。然而,脑积水的发生与颅内动脉损害的发生机制是否一致,目前仍无定论,有待日后深入探究。
本研究发现,局灶性肢体无力亦是结核性脑膜炎患者出现MRA异常的独立危险因素。脊髓损害、颅内结核瘤使得脑组织受损及脑梗死是结核性脑膜炎患者发生局灶性肢体无力的主要原因[16]。而本研究表明,颅内动脉病变引发脑梗死是患者肢体无力的主要原因。本研究结果显示,颅底粘连是结核性脑膜炎患者出现MRA异常的影响因素,而颅底炎性渗出是引发颅底大动脉病变的重要原因之一,因此结核性脑膜炎患者MRA异常的发生也与颅底渗出粘连密切相关。
结核性脑膜炎患者MRA异常率较高,其与年龄增长、脑积水、局灶性肢体无力及颅底粘连等因素密切相关,提示临床中可通过患者年龄、是否存在肢体无力症状及影像学检查是否存在颅底渗出粘连、脑积水等情况,可早期预测患者颅内动脉损害的可能性,有助于早期评估患者病情程度,及时干预和处理以改善患者预后。
