新月弯孢霉CICC40301 催化4-烯-3-酮甾体化合物羟基化反应产物的鉴定
2019-10-23李慧杰郭文丽王正祥刘晓光
李慧杰,李 明,金 鹏,郭文丽,王 雪,王正祥,刘晓光
(1.天津科技大学生物工程学院,天津 300457;2.天津科技大学化工与材料学院,天津 300457)
甾体化合物具有广泛的药理和生理活性,在抗炎、抗肿瘤、调节性功能和生育控制等方面具有极其重要的作用[1-2].天然的甾体化合物往往药理活性较低,在甾体药物的特定位点引入羟基可以显著提高其药理与生理活性[3-4].甾体化合物结构复杂且含有多个非对称中心,用化学合成法在甾体化合物的关键位点引入氧原子非常困难,涉及多步复杂的保护和去保护反应,如在黄体酮的C11α-羟基引入羟基需要9 步化学反应,而利用黑根霉(Rhizopus nigricans)转化可以一步完成C11α-羟化反应生成C11α-羟基黄体酮,得率达到85%[5].由于微生物转化具有特异性强、效率高、污染低等优点,已广泛应用于甾体药物羟基化修饰[6-8].
目前已报道的具有甾体转化活性的微生物多达1 500 种,但成功应用于工业生产的菌株并不多[4,6].进一步研究开发工业生产菌种对于改进甾体生物转化效率和拓宽微生物催化在甾体工业中的应用范围具有重要意义.丝状真菌新月弯孢霉(Curvularia lunata)在工业上用于C11β 羟化Reichstein S 化合物(RS),生产具有抗炎活性的氢化可的松[9].C17α-羟基孕酮是合成氢化可的松、泼尼松龙、地塞米松等多种甾体药物的一个关键中间体[10],而C14α-羟基4AD 是合成抗肿瘤化合物C14α-羟基-3,6,17 三酮的关键前体[11].作者在研究新月弯孢霉的甾体底物转化的过程中发现新月弯孢霉菌株CICC40301 不能转化RS,但对孕酮、睾酮、雄甾-4-烯-3,17-二酮(4AD)都有明显的转化活性,通过HPLC、1H NMR、13C NMR 方法确认其相应的主要转化产物为C17α-羟基孕酮、C15-羟基睾酮和C14α-羟基4AD.
1 材料与方法
1.1 材料
1.1.1 菌株
新月弯孢霉(Curvularia lunata)CICC40301 为本实验室保存菌株.
1.1.2 试剂
甲醇、石油醚、二氯甲烷、氯仿、丙酮、乙酸乙酯、乙腈,二甲基亚砜-d6(DMSO-d6),国药集团化学试剂有限公司;薄层层析硅胶板,烟台德信生物科技有限公司.
1.1.3 甾体化合物
孕酮、睾酮和雄甾-4-烯-3,17-二酮(4AD)均由北京紫竹药业有限公司提供.
1.1.4 培养基
PDA 培养基(g/L):土豆200,葡萄糖20,琼脂粉20,115 ℃灭菌 20 min.
YPD 培养基(g/L):蛋白胨 20,酵母粉 10,葡萄糖20,115 ℃灭菌20 min.
1.2 方法
1.2.1 新月弯孢霉的培养及孢子悬浮液的制备
将新月弯孢霉CICC40301 孢子接种于PDA 斜面培养基,28 ℃恒温培养2~4 d.待孢子成熟后,将长有新月弯孢霉孢子的PDA 斜面用无菌水洗下分生孢子,血球计数板计数,再用无菌水调节孢子悬液至浓度为107mL-1,备用.
1.2.2 新月弯孢霉CICC40301 菌丝的培养
吸取1 mL 浓度为107mL-1的孢子悬液接入50 mL 的 YPD 液体培养基中,放入恒温摇床180 r/min、28 ℃培养至36 h.
1.2.3 底物的转化
将新月弯孢霉培养36 h 后,将甾体底物孕酮、睾酮和4AD 通过球磨机研磨,使其颗粒直径为10~15µm.投入甾体底物使其终质量浓度为2 g/L,并添加 1%的 N,N-二甲基酰胺(DMF)作为助溶剂,28 ℃、180 r/min 振荡培养48 h 后取样.
1.2.4 高效液相色谱检测分析
取甾体底物孕酮、睾酮和4AD 及其对应的转化产物样品加入到1.5 mL EP 管中,加入600µL 80%乙腈完全溶解后,经0.22µm 膜过滤至液相小瓶中,备用.
色谱条件:色谱柱为C18 柱(4.6 mm×250 mm,5µm),乙腈-水(体积比为80∶20)为流动相,流量0.8 mL/min,柱温25 ℃,进样量10µL,采用紫外检测器,检测波长240 nm.本方法中所用乙腈为色谱纯,水为去离子水经过滤超声处理.
1.2.5 核磁共振检测分析
样品处理:取100 mL 底物发酵液中的30 mL 于50 mL 离心管,用6 mL 乙酸乙酯萃取,剧烈震荡,使其与发酵液充分混合,12 000 r/min 离心5 min,分别萃取3 次,合并有机相.
产物制备:取有机相在层析板上点样.在展开前用展开剂饱和层析缸30 min.将点有样品的硅胶板放入装有展开剂的层析缸中加盖、密封,待展开剂前沿快到顶端时,取出点样板后烘干.采用紫外检测仪观察层析斑点的颜色和大小.孕酮转化产物的展开剂为V(氯仿)∶V(丙酮)∶V(乙酸乙酯)=5.5∶3.5∶1;4AD、睾酮转化产物的展开剂为V(二氯甲烷)∶V(石油醚)∶V(甲醇)∶V(水)=385∶60∶30∶2.
通过刮板得到产物,加二氯甲烷和甲醇混合液(二氯甲烷与甲醇体积比为5∶1)10 mL 溶解,混匀.将得到的溶液加入到50 mL 的圆底烧瓶中,旋转蒸发除去二氯甲烷和甲醇得到产物,之后向产物中加入DMSO 将其溶解,将溶解的溶液加入到核磁管中进行检测分析.
核磁共振条件:1H NMR、13C NMR 谱分别用400 MHz 和101 MHz 记录,布鲁克Ascend 400 系列核磁共振仪使用DMSO-d6作为溶剂.
2 结果与分析
2.1 新月弯孢霉孕酮转化产物的分析
2.1.1 孕酮转化产物HPLC 分析
通过刮板分离得到转化产物,HPLC 分析(图1)显示,孕酮底物出峰时间为6.760 min,孕酮两种转化产物的出峰时间分别为3.032 min 和3.686 min,其中一种孕酮转化产物纯化之后的出峰时间为3.029 min,并且其转化率为22.2%.
2.1.2 孕酮转化产物表征
1H NMR(400,MHz,DMSO-d6)δ5.623(s,1H,C-4H),4.011(s,1H,OH),0.657(s,3H,H-18),1.139(s,3H,H-19).13C NMR(101,MHz,DMSO-d6)δ 210.37(C-20),198.54(C-3),171.63(C-5),123.40(C-4),83.60(C-17),59.57(C-14),48.15(C-9),46.26(C-13),38.64(C-10),38.30(C-12),35.80(C-8),34.12(C-1),32.35(C-2),32.30(C-6),31.62(C-7),30.83(C-21),27.44(C-15),21.52(C-16),20.31(C-11),17.17(C-19),17.17(C-18).
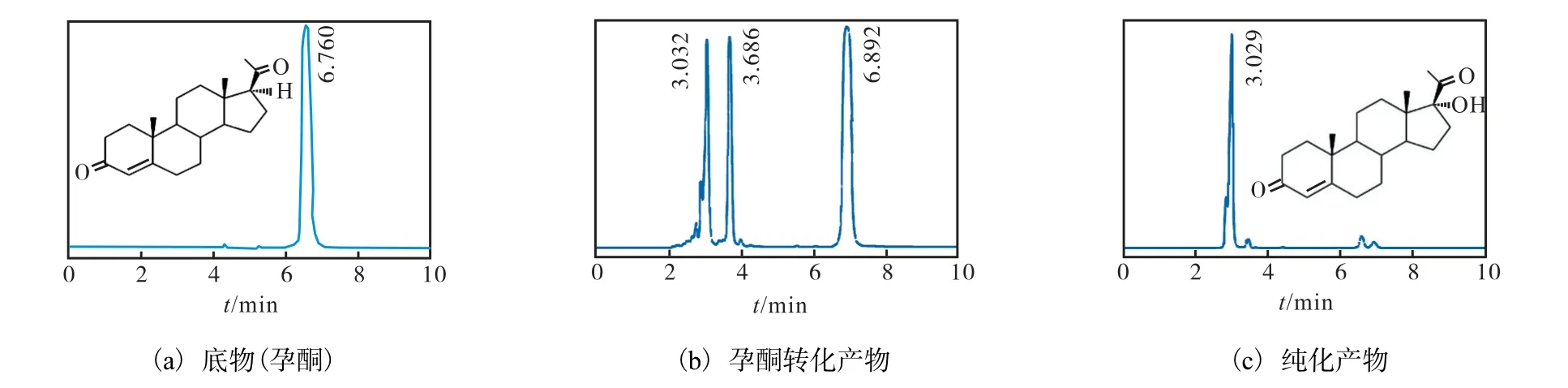
图1 新月弯孢霉CICC40301孕酮转化产物的HPLC分析Fig.1 HPLC analysis of the progesterone transformation product catalyzed by Curvularia lunata CICC40301
2.1.3 孕酮转化产物确认
根据孕酮转化产物的1H NMR、13C NMR 结果,碳谱中C17 的化学位移从孕酮的63.23 变为83.60,后者与文献报道C17-羟基孕酮的碳谱数据一致[12],氢谱的特征峰(H4=5.623,H18=0.657,H19=1.139)的化学位移值与文献报道C17-羟基孕酮的氢谱数据基本一致[13],鉴于孕酮母核的C17α-H 被OH 取代,故产物确认为C17α-羟基孕酮.
2.2 新月弯孢霉雄甾-4-烯-3,17-二酮(4AD)转化产物的分析
2.2.1 雄甾-4-烯-3,17-二酮(4AD)转化产物HPLC分析通过刮板分离得到转化产物,HPLC 分析(图2)显示,4 AD 底物出峰时间为4.434 min,4 AD 两种转化产物的出峰时间分别为2.781 min 和3.059 min,其中一种 4 AD 转化产物纯化后的出峰时间为3.059 min,并且其转化率为45.1%.
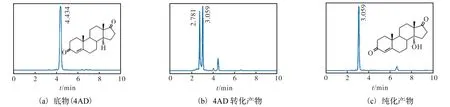
图2 新月弯孢霉CICC40301 4AD转化产物的HPLC分析Fig.2 HPLC analysis of the 4AD transformation product catalyzed by Curvularia lunata CICC40301
2.2.2 雄甾-4-烯-3,17-二酮(4AD)转化产物表征
1H NMR(400,MHz,DMSO-d6)δ5.641(s,1H,C-4H),4.304(s,1H,OH),0.921(s,3H,H-18),1.150(s,3H,H-19).13C NMR(101 MHz,DMSOd6)δ218.03(C-17),197.98(C-3),170.82(C-5),123.02(C-4),78.93(C-14),52.09(C-13),46.41(C-9),38.20(C-10),37.35(C-12),35.27(C-1),33.62(C-2),32.78(C-6),31.63(C-7),28.89(C-8),25.43(C-15),24.51(C-16),18.82(C-11),17.12(C-19),16.82(C-18).
2.2.3 4AD 转化产物确认
根据4AD 转化产物的 1 H NMR、13C NMR 结果,碳谱中C14 的化学位移从4AD 的51.67 变为78.93,后者与文献报道C14-羟基4AD 的碳谱数据一致[12],氢谱的特征峰(H4=5.641,H18=0.921,H19=1.150)的化学位移值与文献报道 C14-羟基4AD 的氢谱数据基本一致[13],鉴于4AD 母核的C14α-H 被OH 取代,故产物确认为C14α-4AD.
2.3 新月弯孢霉睾酮转化产物的分析
2.3.1 睾酮转化产物HPLC 分析
通过刮板分离得到转化产物,HPLC 分析(图3)显示,睾酮底物出峰时间为4.007 min,睾酮转化产物的出峰时间为2.772 min,纯化的睾酮转化产物出峰时间为2.890 min,并且其转化率为88.2%.
2.3.2 睾酮转化产物表征
1H NMR(400,MHz,DMSO-d6)δ5.609(s,1H,CH4),4.240(d,1H,J=5.2 Hz,OH),4.227(m,1H,H-15),0.759(s,3H,H-18),1.143(s,3H,H-19).13C NMR(101 MHz,DMSO-d6)δ198.56(C-3),171.91(C-5),123.32(C-4),81.74(C-17),77.32(C-15),46.99(C-9),46.79(C-14),39.07(C-13),38.75(C-10),35.83(C-1),34.15(C-2),32.37(C-6),32.03(C-7),29.84(C-8),28.86(C-12),26.53(C-16),19.98(C-11),17.21(C-19),15.33(C-18).
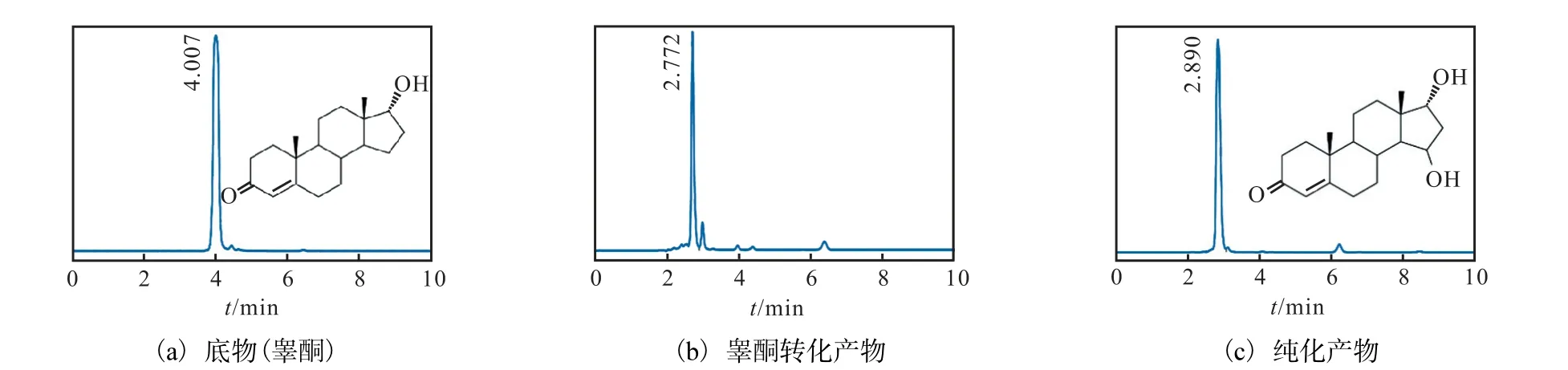
图3 新月弯孢霉CICC40301睾酮转化产物的HPLC 分析Fig.3 HPLC analysis of the testosterone transformation product catalyzed by Curvularia lunata CICC40301
2.3.3 睾酮转化产物确认
根据睾酮转化产物的1H NMR、13C NMR 结果,碳谱中C15 的化学位移从睾酮的27.43 变为77.32,与文献报道C15-羟基睾酮的碳谱数据一致[12],氢谱的特征峰(H4=5.609,H18=0.759,H19=1.143)的化学位移值与文献报道的C15-羟基睾酮氢谱数据基本一致[13],故产物确认为C15-羟基睾酮.
3 结 论
新月弯孢霉(Curvularia lunata)CICC40301 能够转化甾体底物孕酮、雄甾-4-烯-3,17-二酮和睾酮,利用高效液相色谱(HPLC)和核磁共振方法分析鉴定了相应的主要转化产物,结果为:C17α-羟基孕酮、C14α-羟基4AD、C15-羟基睾酮.转化产物C17α-羟基孕酮是用于合成氢化可的松等多种甾体药物的重要中间体,C14α-羟基4AD 是合成抗肿瘤化合物C14α-羟基-3,6,17 三酮的关键前体.
