关于申办方临床研究是否采用外包模式的一些浅见
2019-10-21王茂
王茂

临床研究是药物研发流程中至关重要的环节,虽然722以来,国内临床研究的设计和实施水平在不断提高,但是临床质量的把控一直是临床研究中最让申办方头痛和费心的事情。针对不同的临床研究类型,风险的出现和把控的难度往往跟临床的规模不一定呈正相关性。BE试验虽然周期短,但风险点集中在试验前期,血样采集过程中一旦发生偏差几乎无法补救,对整体试验结果影响巨大;大临床风险集中度却较为分散,如果入组前期发现问题,还有一定程度的纠偏可能。
那么针对不同规模类型的临床研究,申办方往往容易觉得像BE试验这样周期短的临床研究项目,完全可以由自己的团队来完成相关研究。事实上,确实在项目实施的前期,很多申办方都面临采用自建团队或者委外合作模式的选择。本文就以BE临床试验研究为例,对两种模式进行一个初步的对比讨论,以期抛砖引玉,帮助各申办方做出理性的决策。
首先自建团队的申办方至少需要近30人的配置,配置的部门人员包括但不仅僅只有部门总监或经理、医学经理、项目经理、监查员若干(查医院、查检测机构、查数据统计分析单位的监查员专业要求各不同)、质控稽查人员、药物警戒人员(医学背景)、数据管理和统计分析人员。这种模式已经接近国内小型CRO的人员规模。目前国内仅有一部分申办方在采用此模式,该模式单看运行成本相对委外模式肯定要高出不少,但是适合项目较多,能够分摊运营成本的公司,好处是对临床项目的风险把控能力强,但对该模式下申办方部门的管理要求也相对较高。
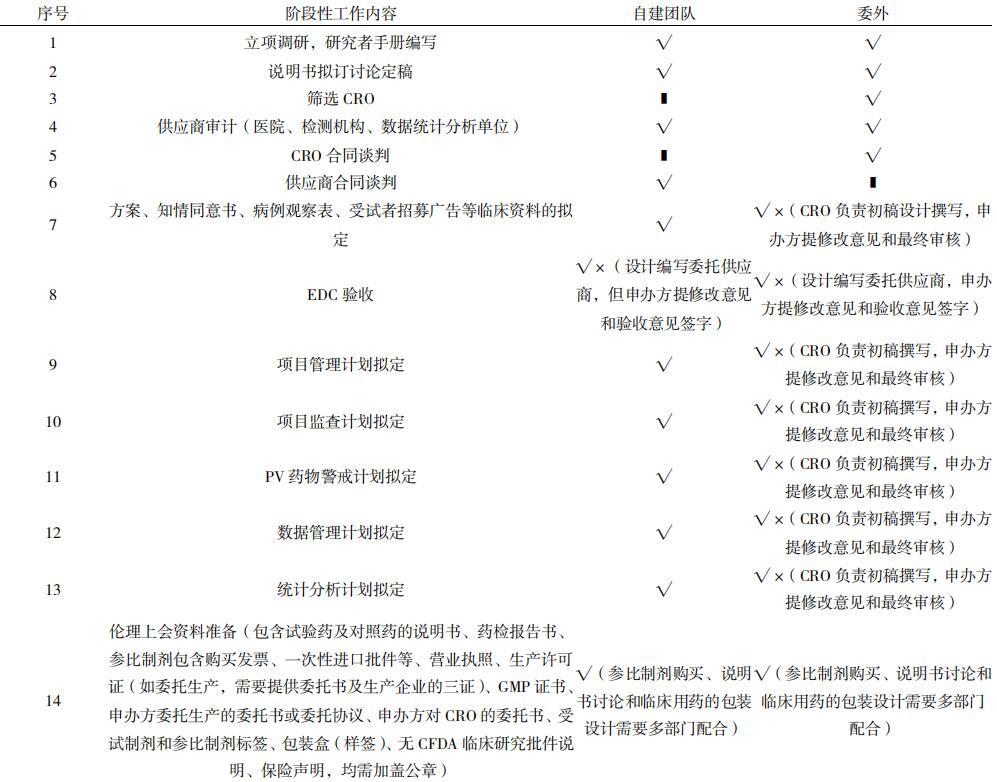
对于委外模式,是否申办方的人员配置和工作量就会少很多,切看下面的工作清单对比表,以BE试验为例,√表示要开展此项工作,∕表示不负责此项工作开展,√×表示部分开展此项工作。
由上表可以发现,实际对于申办方而言,委外和自建团队执行的差别主要还是工作量前期和后期会有一些差异,过程中都必须委托外部资源(医院、检测机构、统计单位)开展工作,因此对于申办方来讲,临床试验研究就是一个协调外部资源开展的系统性工作。
综上所述,申办方对临床研究是否采用外包模式的考虑,还是要从自身人员配置和项目的数量,以及外部资源的整合上去综合考虑。无论是否委外,过程监管和所配置人员自身素质、从业经验是至关重要的,审核把关的最终责任仍然是申办方的。以上仅是一点粗浅的观点,分析也不够全面,还请大家多多给予探讨和建议。
