以知识结构化复习发展学科核心素养
2019-10-21蓝伟华
蓝伟华
【摘要】 以知识结构化复习为抓手,开展高三化学有效复习的教学,要求重视知识形成,知识由繁杂变成简化概括,培养“微观探析”素养,强化知识应用,发展“模型认知”。再基于“模型认知”,创设情境训练,优化学生思维品质,培养综合分析能力和创新意识。
【关键词】 知识结构化 学科核心素养 原电池
【中图分类号】 G633.7 【文献标识码】 A 【文章编号】 1992-7711(2019)05-118-02
知识结构化是把所学的知识要素按其相互作用、相互联系的方式和秩序组合起来,使知识由繁杂变成简化概括。作为一线教师,要使学生对知识的体系和结构产生形象化的感觉和认识,便于学习记忆。我选择了在高三化学复习教学中,以“新课标”为指导,探索促进知识结构化的高三化学复习,发展学生“宏观辨识与微观探析”“证据推理与模型认知”等学科核心素养,突显学科本质和育人价值。下面结合高三“原电池”复习谈谈自己的教学实践,为高三进行有效化学复习教学提供参考与借鉴。
一、重视知识形成,培养“微观探析”的素养
利用铜—锌双液原电池的复习,从能量转换和氧化还原反应的视角,对原电池工作原理进行分析,具体理清:构成要素、电极判断、电子流向、阴阳离子迁移、电极反应。
建立学习模型,把原电池的工作原理和形成要素,归纳概括为:“1234”,即一个概念、二个电极、三种流向、四个条件。引导学生理解原电池的概念和氧化还原反应的关系。二个电极判断:负极是失电子,化合价升高,发生氧化反应;正极是得电子,化合价降低,发生还原反应。三个流向:即电子流向:电子从负极流出,沿导线流入正极;电流方向:正极到负极;离子移动方向:阳离子→正极,阴离子→负极。四个原电池的构成要素:两个导体电极、电解质溶液、形成闭合电路、还有自发的氧化还原反应。
整个教学过程从看得见的电极到微观的电子流向和离子移动,按照原电池知识的逻辑关系进行知识整合,知识的形成过程往往就是一个相对完整的创造过程,蕴含着探讨问题、解决问题的思想和方法。从电子、离子水平认识原电池原理,培养学生微观探析素养。
二、强化知识应用,发展“模型认知”素养
学生理解了原电池的工作原理,从新能源的大力发展,促使各种新型化学电池的涌现,设计新的问题,如特斯拉电动汽车使用的磷酸铁锂电池,电池使用含Li+的导电固体为电解质,电池反应为:FePO4+LiLiFePO4
问题:(1)从所给的方程式和图形中能够获取哪些信息?
(2)请分析磷酸铁锂电池的放电原理:电极判断、电子流向、阴阳离子迁移、电极反应式等。
使学生回归到原电池的基本规律、原理,积极体验并建构学科知识,在知识积累的过程中提升学生信息获取、逻辑思维能力,培养“模型认知”的核心素养。
三、设计燃料电池,培养创新意识
通过问题进行实验和探究活动,如制作一个简单的燃料电池,需画出装置(包括电极、电解质溶液并标明电极反应物、电子流动方向)写出电极反应方程式。学生思考交流、设计方案,展示作品,评价优缺点。
在此基础上又提出问题:二甲醚(CH3OCH3)直接燃料电池具有启动快、能量密度高、效率好等优点,若电解质为碱性,二甲醚直接燃料电池的负极反应式如何书写?若电解质为酸性,二甲醚直接燃料电池的负极反应式如何书写?考查学生书写陌生情境的電极反应式的能力。
当学生遇到困难时,帮助总结“四据四定”,即据元素化合价变化定得失电子数目;据反应介质定物质变化后的存在形式;据电荷守恒定补H+或者OH-,的位置和系数;据原子守恒定其余物质及系数。引导学生学习新知识,训练运用已有知识和方法综合分析化学过程,培养了学生思维的全面性和严密性。
四、基于模型认知,优化思维品质
复习中进一步追问:以甲烷燃料电池为例来分析在不同的环境下电极反应式的书写方法,总结出思维模型。
1.酸性条件
总反应式:CH4+2O2===CO2+2H2O ①
正极反应式:O2+4H++4e-===2H2O②
①②×2,得负极反应式: 。
2.碱性条件
总反应式:CH4+2O2+2NaOH===Na2CO3+3H2O①
正极反应式:O2+2H2O+4e-===4OH- ②
①②×2,得负极反应式: 。
3.小结燃料电池电极反应式的书写模型。
根据燃料电池的特点,一般在正极上发生还原反应的物质都是O2,我们只要熟记以下四种情况:
(1)酸性电解液:O2+4H++4e-===2H2O
(2)碱性电解液:O2+2H2O+4e-===4OH-
(3)固体电解质(高温下能传导O2-):O2+4e-===2O2-
(4)熔融碳酸盐(如:熔融K2CO3):O2+2CO2+4e-===2CO32-
再根据电池总反应式和正极反应式写出电池的负极反应式:
负极反应式=总反应式-正极反应式,注意在将两个反应式相减时,要约去正极的反应物O2。
整个教学过程,运用化学模型解释化学现象的本质和规律,培养模型认知的核心素养。
五、创设情境训练,培养综合分析能力
近几年高考中对电化学内容的考查,逐渐倾向于以新型电池为真实情境,考查学生运用所学电化学原理。创设情境,引导学生关注生活,用真实客观存在的教学情境,训练学生运用所学知识解决实际问题。如(1)铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O==Fe(OH)2+2Ni(OH)2
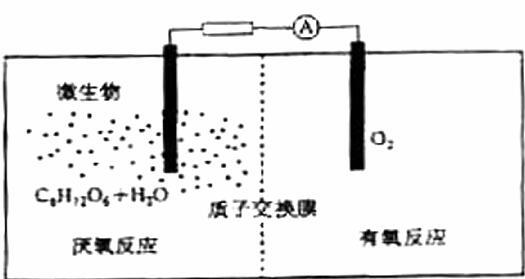
(2)微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。
(3)银制器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可进行如下处理:在银质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去。
用教学情境设计训练题,引导学生思考交流,对原有知识的回顾和新知识体系的教学有机融为一体,充分发挥教师主导和学生的主体作用,有利于提高学生的综合能力。
总之,教学不能离开知识,但不能止于知识。高考坚持知识、能力和素养的有机统一,彰显素质教育鲜明的导向。
[ 参 考 文 献 ]
[1]教育部.普通高中化学课程标准(2017年版)[S].北京:人民教育出版社,2018.
[2]张青杨.张括志.掌控电能绿色出行——基于培育学科核心素养的“电化学”复习教学设计[J].中学化学教学参考.2018(1-2).15-17.
[3]杨向东.以科学探究为例看素养与知识的关系[J].基础教育课程2018(2):89.
