HPLC法测定复方感冒灵流膏中7种成分的含量
2019-10-19李柯陈丹李军侯茜戚建中李若存
李柯 陈丹 李军 侯茜 戚建中 李若存

[摘要] 目的 建立同時测定复方感冒灵流膏中7种成分含量的高效液相色谱法。 方法 采用Kromasil C18色谱柱(4.6 mm×250 mm,5 μm),以乙腈-0.4%磷酸水溶液(梯度洗脱)为流动相,流速为1.0 mL/min,检测波长327 nm,柱温为30℃。 结果 新绿原酸、绿原酸、隐绿原酸、异绿原酸C、异绿原酸B、异绿原酸A、蒙花苷质量浓度分别在5.681~113.62 μg/mL(r = 0.9996)、6.42~128.4 μg/mL(r = 0.9995)、6.806~136.12 μg/mL(r = 0.9996)、3.924~78.48 μg/mL(r = 0.9996)、4.863~97.26 μg/mL(r = 0.9994)、2.273~45.46 μg/mL(r = 0.9991)、43.08~861.6 μg/mL(r = 0.9993)范围内与峰面积呈良好的线性关系;平均加样回收率(n = 6)分别为97.79%、98.24%、96.92%、97.84%、99.23%、99.00%、100.04%。 结论 所建立的高效液相色谱法能为复方感冒灵流膏的质量控制提供依据。
[关键词] 复方感冒灵流膏;高效液相色谱法;新绿原酸;绿原酸;隐绿原酸;异绿原酸C;异绿原酸B;异绿原酸A;蒙花苷;质量控制
[中图分类号] R286.0 [文献标识码] A [文章编号] 1673-7210(2019)10(a)-0035-05
Quantitative determination of seven components of Fufang Ganmaoling Fluid Extract by HPLC
LI Ke1 CHEN Dan2 LI Jun3 HOU Xi1 QI Jianzhong3 LI Ruocun1
1.Hu′nan Academy of Chinese Medicine, Hu′nan Province, Changsha 410013, China; 2.Xiangtan Medicine & Health Vocational College, Hu′nan Province, Xiangtan 411104, China; 3.Huarun Sanjiu (Chenzhou) Pharmaceutical Co., Ltd., Hu′nan Province, Chenzhou 423000, China
[Abstract] Objective To establish simultaneous determination of 7 components in Fufang Ganmaoling Fluid Extract method by high performance liquid chromatography. Methods Kromasil C18 column(4.6 mm×250 mm, 5 μm) column was used as the column, acetonitrile- 0.4% phosphoric acid solution was used as the mobile phase of the gradient elute, with the detection wavelength of 327 nm and the flow rate of 1.0 mL/min. The colomn temperature maintained at 30℃. Results The neochlorogenic acid, chlorogenic acid, cryptochlorogenic acid, 4,5-dicaffeoylquinic acid, 3,4-dicaffeoylquinic acid, 3,5-dicaffeoylquinic acid, in the range of 5.681-113.62 μg/mL (r = 0.9996), 6.42-128.4 μg/mL (r = 0.9995), 6.806-136.12 μg/mL (r = 0.9996), 3.924-78.48 μg/mL (r = 0.9996), 4.863-97.26 μg/mL (r = 0.9994), 2.273-45.46 μg/mL (r = 0.9991), 43.08-861.6 μg/mL (r = 0.9993) showed good linear relationship with the peak area. The average recovery rates (n = 6) of the seven components were 97.79%, 98.24%, 96.92%, 97.84%, 99.23%, 99.00% and 100.04% respectively. Conclusion The method could be used for the comprehensive quality control of Fufang Ganmaoling Fluid Extract.
[Key words] Fufang Ganmaoling Fluid Extract; High performance liquid chromatography; Neochlorogenic acid; Chlorogenic acid; Cryptochlorogenic acid; 4,5-dicaffeoylquinic acid; 3,4-dicaffeoylquinic acid; 3,5-dicaffeoylquinic acid; Buddleoside; Quality control
复方感冒灵颗粒由山银花、五指柑等6味中药和对乙酰氨基酚等3种西药制成,功能为辛凉解表,清热解毒,临床用于风热感冒及温病之发热,微恶风寒,头身痛,口干而渴,鼻塞涕浊,咽喉红肿疼痛,咳嗽,痰黄粘稠。本品疗效确切,市场需求量大,國内有多家企业生产。现有标准均未对中药流膏与成品建立定性定量指标,不能有效控制产品质量,成为制约复方感冒灵颗粒产业发展亟待解决的问题[1]。流膏为连接中药饮片与成品的桥梁,其质量与成品质量的均一性,疗效的一致性密切相关。目前,关于复方感冒灵流膏质量控制方法的研究未见报道,在前期建立流膏(中间体)指纹图谱的基础上[2-3],本试验建立了HPLC法同时测定复方感冒灵流膏中新绿原酸、绿原酸、隐绿原酸、异绿原酸A、异绿原酸B、异绿原酸C[4-7]、蒙花苷[8-9]7种有效成分含量的方法,为复方感冒灵颗粒流膏(中间体)及成品的质量控制与评价提供依据。
1 仪器与试药
1.1 仪器
高效液相色谱仪(2695型,美国Waters;LC-20A型,日本岛津)。紫外检测器(SPD-20A型,日本岛津)。电子分析天平(XS205,瑞士Mettler Toledo,十万分之一)。超声波清洗器(KQ800-KDE,昆山市超声仪器有限公司)。
1.2 试药
复方感冒灵流膏由华润三九(郴州)制药有限公司提供,共取10批,批号分别为Z1701104、Z1701105、Z1701106、Z1701107、Z1701108、Z1701109、Z1701110、Z1701111、Z1701112、Z1701113,分别编号为S1~S10。蒙花苷对照品(批号:111528-201710,含量以96.6%计)、绿原酸对照品(批号:110753-201716,含量以99.3%计)购自中国食品药品检定研究院。新绿原酸对照品(批号:MUST-18031001,含量以99.67%计)、隐绿原酸对照品(批号:MUST-18032403,含量以99.07%计)、异绿原酸A对照品(批号:MUST-18032601,含量以98.82%计)、异绿原酸B对照品(批号:MUST-18031602,含量以99.05%计)、异绿原酸C对照品(批号:MUST-18031603,含量以99.84%计)均购自成都曼思特生物科技有限公司。乙腈为色谱纯(购自Tedia公司),甲醇、乙醇均为分析纯(长沙市汇虹化玻仪器设备有限公司),水为纯净水。
2 方法与结果
2.1 复方感冒灵流膏的制备
称取山银花104 g、五指柑415 g、野菊花310 g、三叉苦520 g、南板蓝根310 g、岗梅835 g,加水煎煮2次,煎液合并浓缩至适量,加乙醇沉淀,滤过,滤液浓缩成流膏。
2.2 色谱条件
色谱柱:Kromasil C18柱(250 mm × 4.6 mm,5 μm);流动相:乙腈(A)-0.4%的磷酸水溶液(B),梯度洗脱:0~20 min A:3%→15%,B:97%→85%;20~45 min A:15%→24%,B:85%→76%;45~55 min A:24%→35%,B:76%→65%;55~60 min A:35%→3%,B:65%→97%;60~65 min A:3%,B:97%。检测波长:327 nm;柱温:30℃;流速:1.0 mL/min;进样量10 μL。
2.3 溶液的制备
2.3.1 对照品溶液 精密称取7种对照品各适量,加50%甲醇制成浓度分别为绿原酸0.6420 mg/mL、新绿原酸0.5681 mg/mL、隐绿原酸0.6806 mg/mL、异绿原酸A 0.2273 mg/mL、异绿原酸B 0.4863 mg/mL、异绿原酸C 0.3924 mg/mL、蒙花苷4.3080 mg/mL的混合对照品溶液。再精密量取上述混合对照品溶液1 mL,置10 mL容量瓶中,加50%甲醇稀释至刻度,得到浓度分别为绿原酸64.20 μg/mL、新绿原酸56.81 μg/mL、隐绿原酸68.06 μg/mL、异绿原酸A 22.73 μg/mL、异绿原酸B 48.63 μg/mL、异绿原酸C 39.24 μg/mL、蒙花苷430.80 μg/mL的混合对照品溶液。
2.3.2 供试品溶液 称取复方感冒灵流膏1.0 g,精密称定,置150 mL锥形瓶中,加50%甲醇约50 mL,称重,超声处理(功率250 W,频率50 kHz)30 min,冷却,重新称重,用50%甲醇补足失重,摇匀,滤过,即得。
2.3.3 空白对照溶液 按复方感冒灵流膏处方和制备工艺制备缺野菊花的空白样品及缺山银花、野菊花、五指柑及岗梅的空白样品,并按“2.3.2”项下方法分别制成缺野菊花和缺山银花、野菊花、五指柑及岗梅的空白对照溶液。
2.4 方法学考察
2.4.1专属性试验 分别精密吸取混合对照品溶液、供试品溶液(S1)与空白溶液各10 μL,按“2.2”项下色谱条件,测定,即得。见图1。
2.4.2 线性关系考察 精密吸取“2.3.1”项下混合对照品溶液0.1、0.5、1.0、1.5、2.0 mL,各置10 mL容量瓶中,分别加50%甲醇稀释至刻度,摇匀,即得一系列浓度的对照品溶液。按“2.2”项下色谱条件,测定,记录峰面积。以对照品的质量浓度(μg/mL)为横坐标、峰面积为纵坐标,进行线性回归方程计算,结果见表1。
2.4.3 精密度试验 取混合对照品溶液,按“2.2”项下色谱条件,连续进样测定6次,以新绿原酸、绿原酸、隐绿原酸、异绿原酸C、异绿原酸B、异绿原酸A、蒙花苷峰面积计,RSD分别为1.52%、1.28%、1.67%、1.36%、1.12%、1.80%、2.66%,表明仪器精密度良好。
2.4.4 稳定性试验 取供试品溶液(S1),分别于放置0、2、4、8、12、24 h,按“2.2”项下色谱条件,测定,以新绿原酸、绿原酸、隐绿原酸、异绿原酸C、异绿原酸B、异绿原酸A、蒙花苷峰面积计,RSD分别为1.25%、1.32%、1.64%、1.77%、1.51%、1.68%、1.94%,表明供试品溶液在24 h内保持稳定。
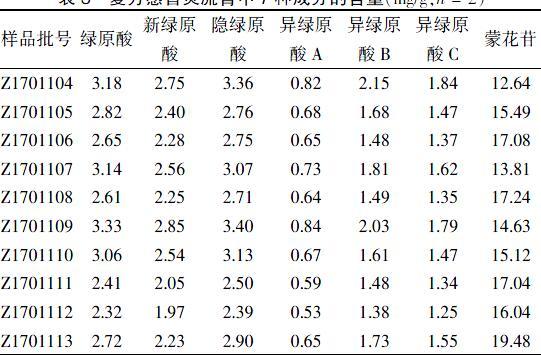
2.4.5 重复性试验 取同一批样品(S1)适量,按“2.3.2”项下方法制备6份供试品溶液,按“2.2”项下色谱条件测定记录峰面积。新绿原酸、绿原酸、隐绿原酸、异绿原酸C、异绿原酸B、异绿原酸A、蒙花苷含量平均值分别为2.75、3.18、3.36、1.84、2.15、0.82、12.64 mg/g,RSD分别为1.99%、1.67%、2.28%、2.09%、2.64%、2.41%、2.50%,表明本方法重复性良好。
2.4.6 重现性试验 取同一批样品(S1)适量,按“2.3.2”项下方法制备6份供试品溶液,采用高效液相色谱仪,紫外检测器,按“2.2”项下色谱条件测定,记录峰面积。新绿原酸、绿原酸、隐绿原酸、异绿原酸C、异绿原酸B、异绿原酸A、蒙花苷含量平均值分別为2.66、3.32、3.50、1.81、2.31、0.89、12.92 mg/g,RSD分别为1.82%、1.35%、2.06%、1.99%、2.72%、2.17%、2.32%,表明本方法中间精密度良好。
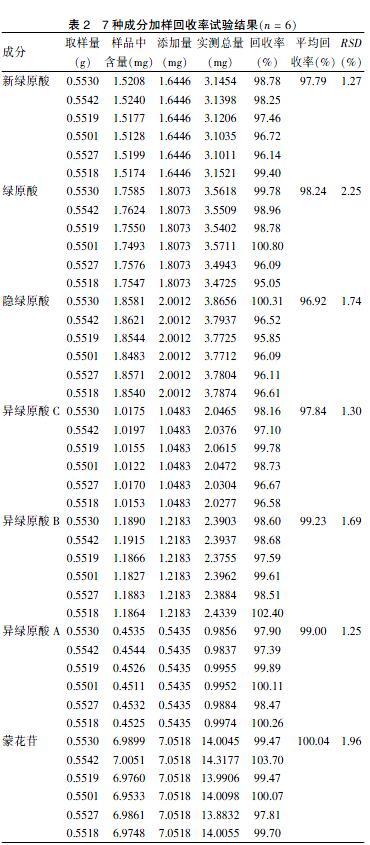
2.4.7 加样回收率试验 精密称取同一批已知含量样品(S1)6份,分别加入与供试液中新绿原酸、绿原酸、隐绿原酸、异绿原酸C、异绿原酸B、异绿原酸A、蒙花苷约成1∶1对照品量,按“2.3.2”项下方法制备供试品溶液,再按“2.2”项下色谱条件进样,测定,计算样品含量,并计算加样回收率。见表2。
2.5 样品含量测定
取10批复方感冒灵流膏,分别按“2.3.2”项下方法制备供试品溶液,再按“2.2”项下色谱条件测定样品中新绿原酸、绿原酸、隐绿原酸、异绿原酸C、异绿原酸B、异绿原酸A、蒙花苷含量。见表3。
3 讨论
前期通过HPLC-Q-TOF-MS/MS对复方感冒灵流膏指纹图谱中的主要色谱峰进行了结构鉴定,明确了流膏中的主要成分为绿原酸、新绿原酸、隐绿原酸、异绿原酸A、异绿原酸B、异绿原酸C及蒙花苷[3,10-19],因此,本试验选择上述7种成分作为流膏测定的指标性成分。鉴于绿原酸、新绿原酸、隐绿原酸、异绿原酸A、异绿原酸B、异绿原酸C为方中山银花、岗梅、五指柑、野菊花的共有成分,蒙花苷为野菊花的特有成分,因此在设计阴性对照时,制备了缺山银花、岗梅、五指柑、野菊花四味药材的阴性样品及缺野菊花的阴性样品。
本试验用二极管阵列检测器全波长扫描,各有机酸的最大吸收波长为(327±2)nm[20],蒙花苷的最大吸收波长为334 nm[20],分别采用327 nm与334 nm对7种成分进行含量测定,结果两波长下测定的含量相差无异,但327 nm有机酸类的峰面积值均较大,因此选择327 nm作为检测波长。
研究表明,绿原酸、新绿原酸、隐绿原酸、异绿原酸A、异绿原酸B、异绿原酸C有抗菌、抗炎、抗病毒、抗氧化、护肝作用[10-21],蒙花苷有抗菌、抗氧化、护肝及抗血管炎症损伤的作用[22-23],这些成分均源自于本方中的山银花、岗梅、五指柑、野菊花。本试验首次建立了同时测定复方感冒灵颗粒流膏中蒙花苷、绿原酸、新绿原酸、隐绿原酸、异绿原酸A、异绿原酸B、异绿原酸C的HPLC分析方法,该法灵敏度高,重复性好,结果可靠,操作简单易行,为该产品的中间体健立了一个全面有效的质量控制方法。
[参考文献]
[1] 国家药典委员会.国家食品药品监督管理局复方感冒灵颗粒(复方感冒灵茶)标准[S].编号ZGB2017-38.2017.
[2] 陈海刚,龚小兵,符国成,等.复方感冒灵流膏化学成分标准指纹图谱及构建方法、应用:中国,ZL201510888682. 9[P].2018-4-24.
[3] 符国成,龚小兵,陈海刚,等.复方感冒灵流膏的HPLC指纹图谱研究[J].国际药学研究杂志,2018,45(6):460-464.
[4] 罗艳,杨柳,涂晓琴,等.高效液相色谱法同时测定灰毡毛忍冬中7种有机酸的含量[J].中南药学,2018,16(9):1283-1286.
[5] 刘敏彦,高淑丽,刘丽华,等.HPLC法同时测定不同产地金银花和山银花中6种有机酸成分[J].中药材,2013, 36(2):196-198.
[6] 孟晓岩,丁勇.高效液相色谱法同时对金银花中5种有效成分的含量测定[J].实用药物与临床,2012,15(2):93-94.
[7] 李淼,王永香,孟谨,等.HPLC法测定金银花中新绿原酸等8种成分的量[J].中草药,2014,45(7):1006-1010.
[8] 郭巧生,房海灵,申海进.不同产地野菊花中绿原酸、咖啡酸和蒙花苷含量[J].中国中药杂志,2010,35(9):1160-1163.
[9] 李婷,区硕俊,王强,等.高效液相色谱法同时测定野菊花中的4种药用成分[J].当代化工,2017,46(3):566-568.
[10] 王亚丹,何轶,戴忠,等.HPLC-MS/MS法同时测定山银花中7个有机酸的含量[J].药物分析杂志,2016,36(6):998-1005.
[11] 张倩,张加余,高凤阳,等.HPLC-DAD法同时测定清开灵注射液中7个酚酸类成分[J].药物分析杂志,2013, 33(1):73-77.
[12] 代晶,罗玲,王佳慧,等.HPLC-UV-ELSD同时测定灰毡毛忍冬中9种成分的含量[J].中药材,2015,38(6):1217-1219.
[13] 罗艳,杨柳,涂晓琴,等.高效液相色谱法同时测定灰毡毛忍冬中7种有机酸的含量[J].中南药学,2018,16(9):1283-1286.
[14] 杜冰曌,杨鑫瑶,冯晓,等.岗梅的化学成分和药理作用研究進展[J].中国中药杂志,2017,42(1):20-28.
[15] 杜冰曌,张和新歌,杨鑫瑶,等.岗梅茎的化学成分研究[J].中国中药杂志,2017,42(21):4154-4158.
[16] 王亚丹,何轶,戴忠,等.HPLC-MS-MS同时测定山银花中10种活性成分的含量[J].中国中药杂志,2016,41(10):1870-1875.
[17] 马斌,宋伟峰,何秋毅,等.高效液相色谱串联质谱分析五指柑水煎液的化学成分[J].中药材,2013,36(1):75-77.
[18] 刘慧妍,沈国滨.一测多评法同时测定野菊花中7种成分[J].中草药,2017,48(10):2012-2017.
[19] 樊高洁,李淑敏,张珊,等.野菊花的质量标准研究[J].中草药,2017,48(19):4073-4076.
[20] 国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2015:221,314.
[21] 薛林萌,赵博贤,陈鑫,等.传统中药萃取物抗神经胶质瘤作用的研究进展[J].医学综述,2018,24(8):1621-1626.
[22] 许韩婷,苏洁,吴亚军,等.蒙花苷对脂多糖诱导的血管内皮细胞炎症损伤的影响[J].中药药理与临床,2016, 32(1):29-32.
[23] 吴亚军,苏洁,黄浦俊,等.蒙花苷对TNF-α 诱导的血管内皮细胞炎症损伤及TLR4/IκBα/NF-κB信号通路的影响[J].中国现代应用药学,2017,34(5):637-643.
(收稿日期:2019-04-19 本文编辑:刘永巧)
