互穿网络型腐植酸保水材料的制备及其性能
2019-10-18张昌辉牛育华任军哲
张昌辉,阮 欢,牛育华,2,宋 洁,任军哲
(1.陕西科技大学 化学与化工学院 教育部轻化工助剂化学与技术重点实验室,陕西 西安 710021;2.陕西农产品加工技术研究院,陕西 西安 710021;3.陕西润中清洁能源有限公司,陕西 咸阳 713600)
0 引言
保水材料属于农业领域新型的化学节水材料[1],具有优良的吸水保水能力,可以作为“微型水库”提高土壤的保水保肥性能,减少土壤无效蒸发,从而稳定土壤结构、改良透气性、防止土壤表层结皮[2,3].同时,保水材料还可以作为肥料的缓释载体,为植物提供所需的营养成分,有效提高种子的发芽率、幼苗的成活率,改善作物品质,同时提高作物产量[4].虽然目前对于保水材料的研究很广泛,但改进其性能、发展其理论、提高其结构和性能的可操作性仍是关键问题.同时,如何改善保水材料的环境友好特性仍然是现在的研究热点.
为了提高保水材料的结构和性能,本研究采用天然高分子腐植酸、聚乙烯醇为原料,制备出低成本、环境友好的互穿网络结构型PVA/PAA/KHA保水材料.腐植酸广泛存在自然界的土壤、湖泊以及硅酸盐类、泥炭、褐煤、风化煤中,具有多种活性官能团及亲水基团,能够提高保水材料的亲水基数量与种类,提高保水材料的性能[5].同时腐植酸还具有改良土壤、吸附土壤重金属离子、刺激作物生长等功效.将腐植酸应用于保水材料中有利于构建“土肥和谐”新关系,也符合现代生产力发展要求[6,7].
聚乙烯醇(PVA)作为保水材料的原料,具有化学性质稳定,机械强度高,无毒副作用、可生物降解,生物相容性好等特点,是一种重要的功能材料.但现有的聚乙烯醇类保水材料溶胀性能较差、不具备pH敏感性和重金属离子络合功能,通过聚丙烯酸、腐植酸的添加可以有效提高聚乙烯醇类保水材料的结构和性能[8].
通过FT-IR、XRD和SEM对保水的结构进行了表征,产物具有良好的吸水性、保水能力,材料本身也实现了“水肥一体化”.通过测定青菜叶片相关的生理活性指标,表明了保水材料可以提高植物品质、抗逆性.因此,制备的互穿网络结构PVA/PAA/KHA保水材料具有良好的应用潜力.
1 实验部分
1.1 试剂与仪器
1.1.1 主要试剂
青菜种子,极速成317;PVA,聚合度1 700+50,天津市天力化学试剂有限公司;腐植酸钾,实验室自制;丙烯酸,纯度>99%,天津市大茂化学试剂厂;氢氧化钠,纯度>96%,天津市大茂化学试剂厂;N,N′ -亚甲基双丙烯酰胺,纯度>99%,天津市大茂化学试剂厂;过硫酸钾,纯度>99%,天津市大茂化学试剂厂.
1.1.2 主要仪器
VECTOR-22型傅里叶变换红外光谱仪,美国Thermo公司;D/max2200PC型X射线多晶衍射分析仪(XRD),德国Bruker AXS公司;S4800 型扫描电镜,日本理学公司;FLB-100型粉碎机,上海兆申科技有限公司.DR5000型紫外可见分光光度计,美国哈希HACH公司.
1.2 PVA/PAA/KHA的制备
PVA/PAA/KHA采用水溶液聚合法制备.称取1 g PVA溶于20 mL蒸馏水中,至于装有冷凝回流管的 250 mL 三口烧瓶中,于90 ℃的温度下完全溶解,得到5%的聚乙烯醇溶液,冷却至室温后加入1 g的腐植酸钾和10 g中和度为65%的丙烯酸,升温至40 ℃,随后缓慢滴加0.25 g引发剂过硫酸钾和0.06 g交联剂N,N′-亚甲基双丙烯酰胺的混合溶液;按程序升温方式30 min/10 ℃,升温至80 ℃,待反应体系粘稠并出现爬杆现象时停止反应.将产品用蒸馏水浸泡洗涤2~3次,洗去未反应的反应物,然后用无水乙醇进行脱水处理,于80 ℃条件下烘干粉碎即得到产品.反应路线如图1所示.
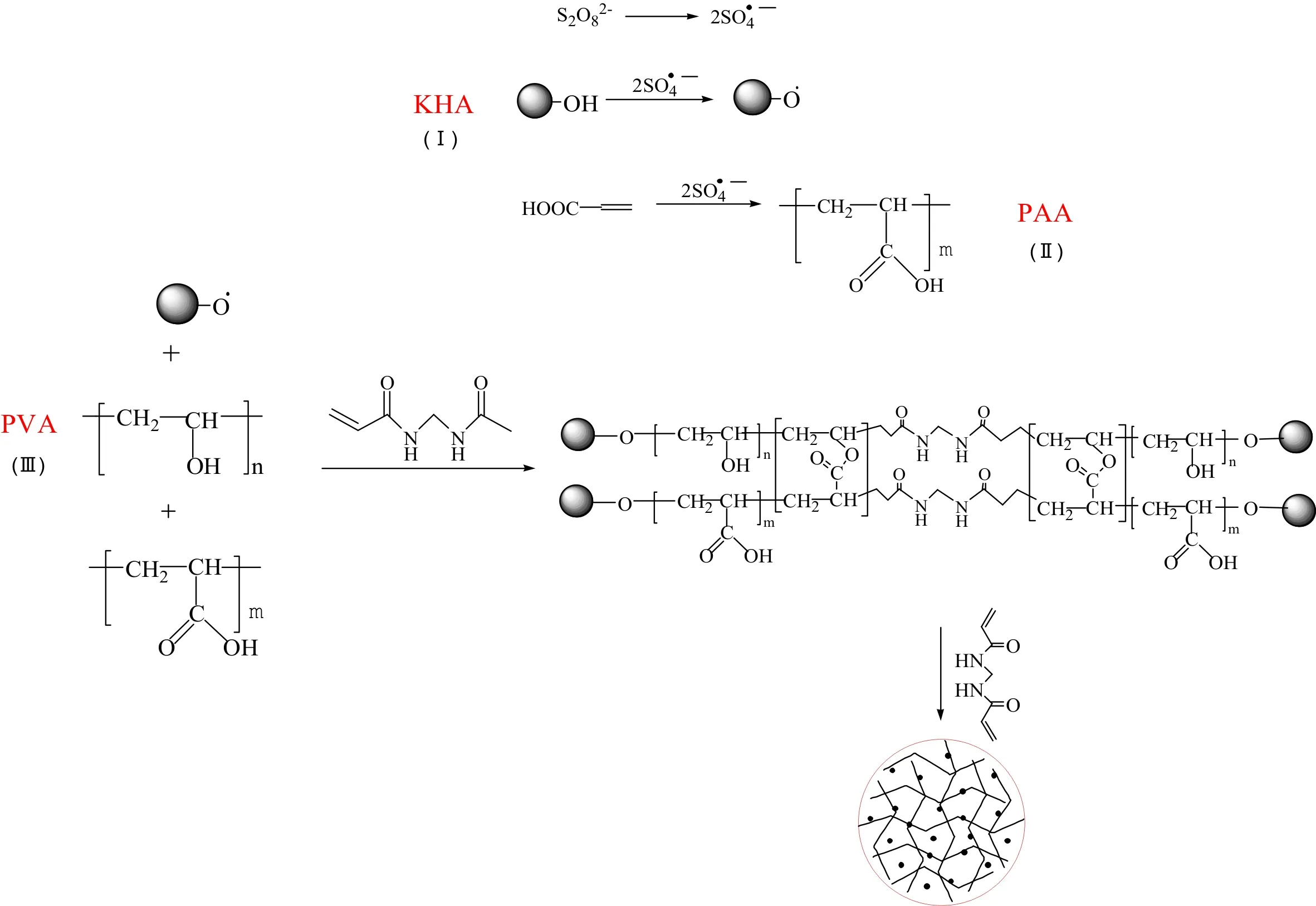
图1 合成材料的反应路线
1.3 室内盆栽青菜实验
将青菜种子播种在盆内,待长出3~4片真叶时,移入营养钵中室内培养.取本地土壤装于直径为10.5 cm、高为7 cm的营养钵内,每钵土220 g,加入不同量的保水材料与土壤混匀配成不同处理样,每种处理样重复四组,并设置空白对照.每7天取一次样,测定叶片中的叶绿素、可溶性蛋白、丙二醛含量,取样周期为28天.
1.4 测试与表征
1.4.1 红外光谱(FT-IR)分析
样品经过KBr压片后,采用VECTOR-22型傅立叶变换红外光谱仪测定产物官能团,测定范围为4 000~500 cm-1.
1.4.2 X-射线衍射(XRD)分析
样品经过充分研磨,采用D/max2200PC型X射线多晶衍射分析仪进行测定,设置参数为:管电压40 kV,管电流40 mA,旋转2θ角:5 °~50 °,步进0.02 °.
1.4.3 扫描电镜(SEM)表征
选取孔隙明显且吸水性较好的保水材料利用扫描电镜观察样品的微观结构,试样镀金厚度约为25 nm,电压为10 kV.
1.4.4 吸水倍率测试
吸水倍率按GB/T 8810-2005测定,计算公式如下:
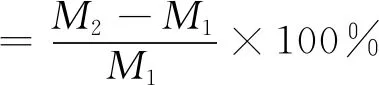
(1)
式(1)中:M1为样品吸水前的质量,g;M2为样品吸水后的质量,g.
1.4.5 保水倍率的测试
保水倍率按GB/T 22905-2008测定,计算公式如下:
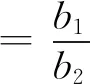
(2)
式(2)中:b1为充分吸水的保水材料的质量,g;b2为该保水材料烘干后的质量,g.
1.4.6 可溶性蛋白质含量测定
采用考马斯亮蓝G-250法,利用蛋白质-染料显色反应,测定595 nm处吸光度值,计算可溶性蛋白含量.
1.4.7 叶绿素含量的测定
根据叶绿体色素提取液对可见光谱的吸收,测定663 nm和645 nm处吸光度值,计算叶片的叶绿素总量.
1.4.8 丙二醛(MDA)含量测定
采用硫代巴比妥酸(TBA)法,即硫代巴比妥酸与丙二醛的显色反应原理,测定532 nm、600 nm和450 nm波长处吸光度值,计算MDA浓度.
2 结果与讨论
2.1 反应条件的考察
2.1.1 聚合温度对保水材料吸水、保水倍率的影响
AA/PVA/KHA质量比为10∶1∶1,AA中和度70 %,KPS用量0.25 g,MBA用量0.06 g,讨论聚合温度对保水材料吸水、保水倍率的影响,如图2所示.
随着聚合温度的增加,产物的吸水倍率、保水倍率都为先增大后减小的趋势,当聚合温度在80 ℃时产物的保水、吸水倍率达到最大值,分别为90.5%和481.3 g/g.自由基聚合反应中,单体间的聚合速率取决于引发剂的分解速率,当引发剂的浓度是恒定时,引发剂的分解速率取决于温度.聚合温度小于80 ℃时,引发剂的分解速率慢,聚合速度慢,此时反应不完全,导致保水、吸水倍率不高;当聚合温度大于80 ℃时,聚合速率过快,单体交联后聚合物的分子量迅速增大,产生暴聚现象,影响产物保水、吸水性能[9].
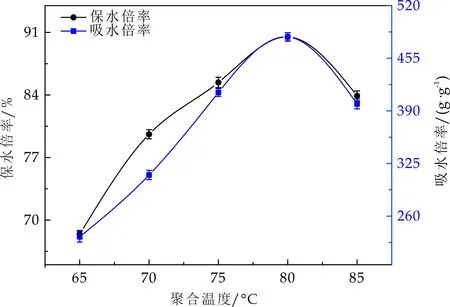
图2 聚合温度对保水材料吸水、保水倍率的影响
2.1.2 AA∶PVA∶KHA用量配比对保水材料吸水、保水倍率的影响
AA中和度70%,KPS用量0.25 g,MBA用量0.06 g,聚合温度80 ℃,讨论AA∶PVA∶KHA用量配比对保水材料吸水、保水倍率的影响,如图3所示.
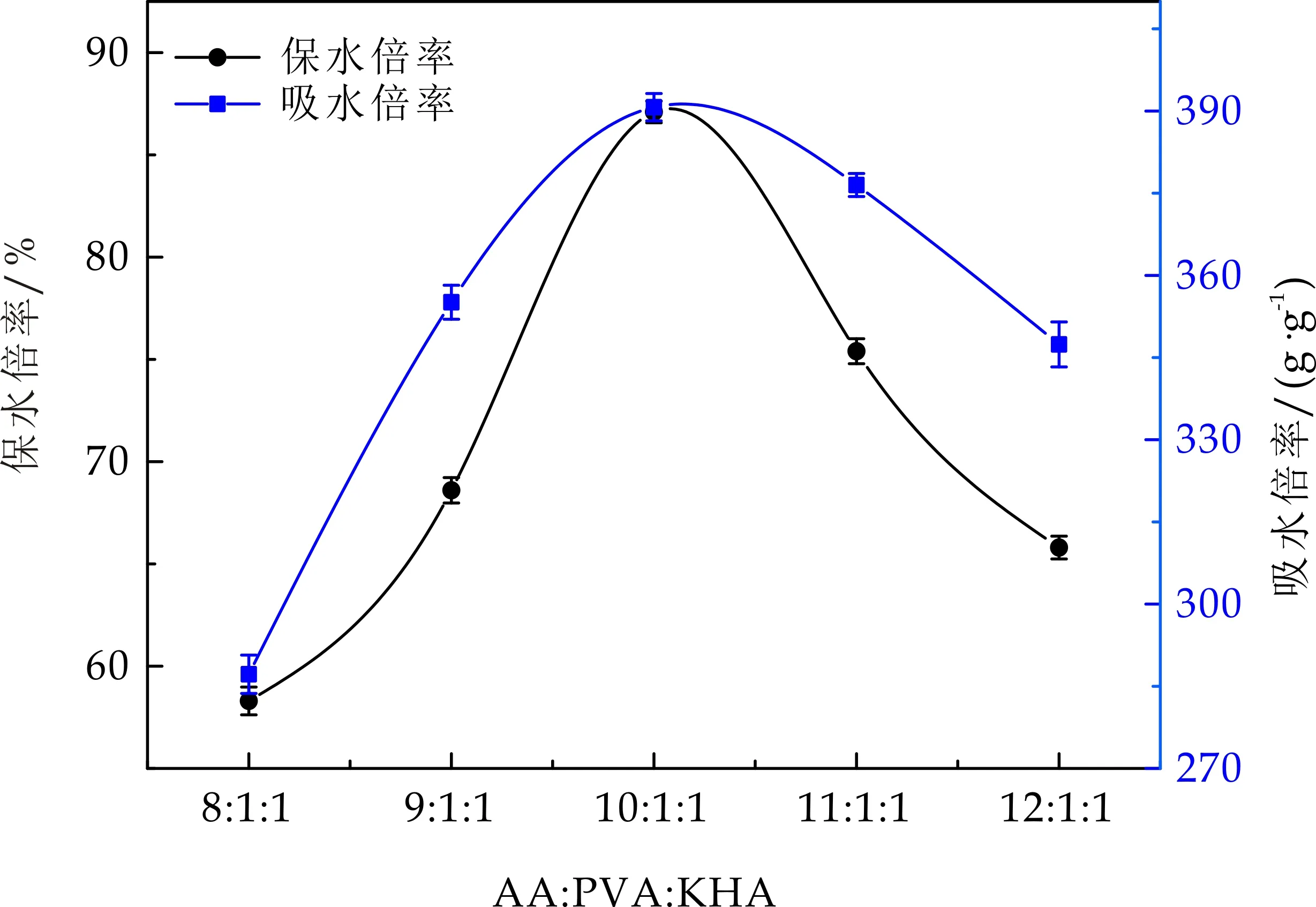
图3 AA∶PVA∶KHA用量配比对保水材料吸水、保水倍率的影响
随着AA∶PVA∶KHA用量配比从8∶1∶1升至10∶1∶1,吸水、保水倍率先增大后减小,在配比为10∶1∶1,聚合产物达到最佳的保水倍率87.1 g/g,吸水倍率90.7 g/g.丙烯酸单体与聚乙烯醇、腐植酸钾配比值直接影响接枝支链分子量的大小,由于交联剂用量不变,所以配比大小又直接影响交联密度的高低,从而影响产物的吸水、保水倍率.
2.1.3 引发剂用量对吸水、保水倍率的影响
AA/PVA/KHA质量比为10∶1∶1,AA中和度70%,聚合温度80 ℃,MBA用量0.06 g,讨论引发剂用量对吸水、保水倍率的影响,如图4所示.
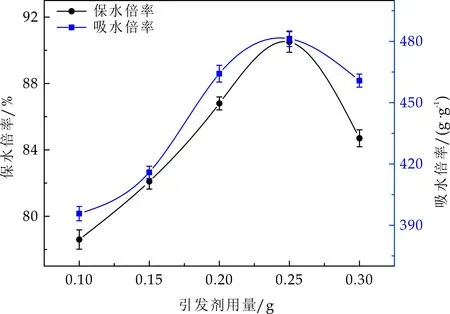
图4 引发剂用量对保水材料吸水、保水倍率的影响
随着引发剂用量的不断增加,产物的吸水倍率和保水倍率都为先增大后减小的趋势,当引发剂用量为0.25 g时,吸水倍率升至最高481.3 g/g,保水倍率达到90.5%.在自由基聚合体系中,引发剂经过加热引发单体产生自由基,增加接枝位点有利于聚合网络的形成[10].当引发剂用量小于0.25 g时,接枝位点少,形成的产物接枝网络不完善,导致产物可溶部分增多,吸水、保水性能降低.而引发剂用量大于0.25 g时,自由基浓度过高,链终止点的数量增多,发生暴聚现象,导致产物吸水、保水性能变差.
2.1.4 交联剂用量对吸水、保水倍率的影响
AA/PVA/KHA质量比为10∶1∶1,AA中和度70%,聚合温度80 ℃,KPS用量0.25 g,讨论交联剂用量对吸水、保水倍率的影响,如图5所示.
随着交联剂用量的不断增加,产物的吸水倍率和保水倍率呈现先增大后减小的趋势,在用量为0.06 g时,吸水倍率升至最高402.7 g/g,保水倍率88.6%.交联剂通过交联作用使分子链相互连结以形成三维网状结构[11].当交联剂的含量低于0.06 g时,由于没有足够的交联点,聚合物网络不能有效地形成,对水分子的束缚能力减小,宏观上表现产物的水溶性较大,因此吸水、保水倍率下降.当交联剂的含量大于0.06 g时,交联密度随之增加,聚合物网络空间紧凑,导致吸水、保水倍率下降.
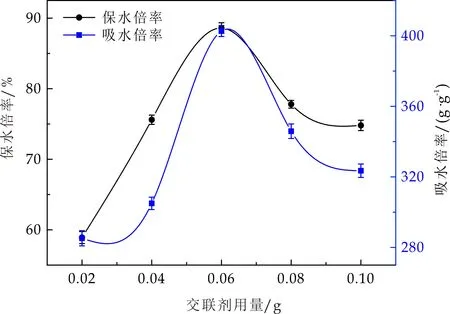
图5 交联剂用量对保水材料吸水、保水倍率的影响
2.1.5 丙烯酸中和度对保水材料吸水、保水倍率的影响
当AA/PVA/KHA质量比为10∶1∶1,KPS用量0.25 g,聚合温度80 ℃,MBA用量0.06 g,讨论丙烯酸中和度对保水材料吸水、保水倍率的影响,如图6所示.
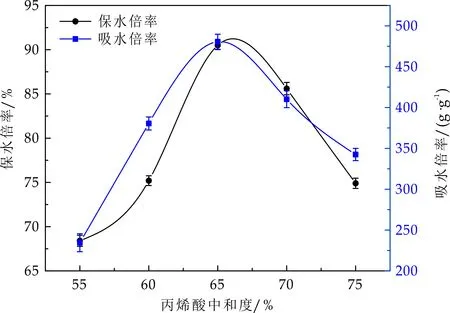
图6 丙烯酸中和度对保水材料吸水、保水倍率的影响
随着丙烯酸中和度的不断增加,产物的吸水倍率和保水倍率呈现先增大后减小的趋势,在中和度为65%时,保水倍率90.5%,吸水倍率升至最高480.6 g/g.丙烯酸中和度较低时,反应体系中-COOH基团浓度较大,聚合反应迅速,不易形成长链和完整的网络结构,所以吸水、保水倍率较低.过高的中和度会导致大量的-COOH转化成-COONa,体系中离子含量增加,相邻的带羧基基团相互排斥,体系交联程度降低,可溶部分增多,网络扩展受到抑制,不利于产物的吸水、保水性能[12].
2.2 FT-IR分析
KHA(a曲线)、PVA(b曲线)、PVA/PAA/KHA(c曲线)的FT-IR光谱如图7所示.在3 650~3 200 cm-1处的宽而强的带是由于-OH伸缩振动;在KHA(a曲线)的红外谱中,1 704 cm-1、1 613 cm-1分别为C=O、芳环中C=C伸缩振动,1 370 cm-1处产生的吸收为-CH3和-CH2及酚羟基的碳氧拉伸的叠加,1 242 cm-1处产生的吸收为羟基的碳氧拉伸及芳基醚和酚的碳氧拉伸,证明了腐植酸具有多种官能团.
在PVA(b曲线)的红外图谱中1 690 cm-1处的吸收属于残留的聚醋酸乙烯酯结构中C=O键的伸缩振动,1 503 cm-1处为-CH2的弯曲振动,1 202 cm-1和931 cm-1处的吸收峰分别为C-O的伸缩振动和全同立构序列特征吸收峰.
PVA/PAA/KHA(c曲线)显示了产物的特征吸收峰.KHA、PAA、PVA 三者发生了氢键缔合作用,所以-OH伸缩振动区(3 365 cm-1)向低波数移动且谱带变宽,1 654 cm-1出现酯的C=O伸缩振动,1 346 cm-1为-COO的对称伸缩振动,PVA(b曲线)的1 202 cm-1(C-O伸缩振动)处的峰值向低波数1 167 cm-1移动,该转变表明在PVA和KHA-g-PAA之间形成氢键.在产物的FT-IR光谱中看不到与PVA全同立构序列相关的特征吸收峰(931 cm-1),这表明PVA在互穿网络结构中处于非晶态.此外,由于交联,KHA特征吸收峰发生了位移且强度减弱.结果证明了PVA/PAA/KHA保水材料的成功制备.
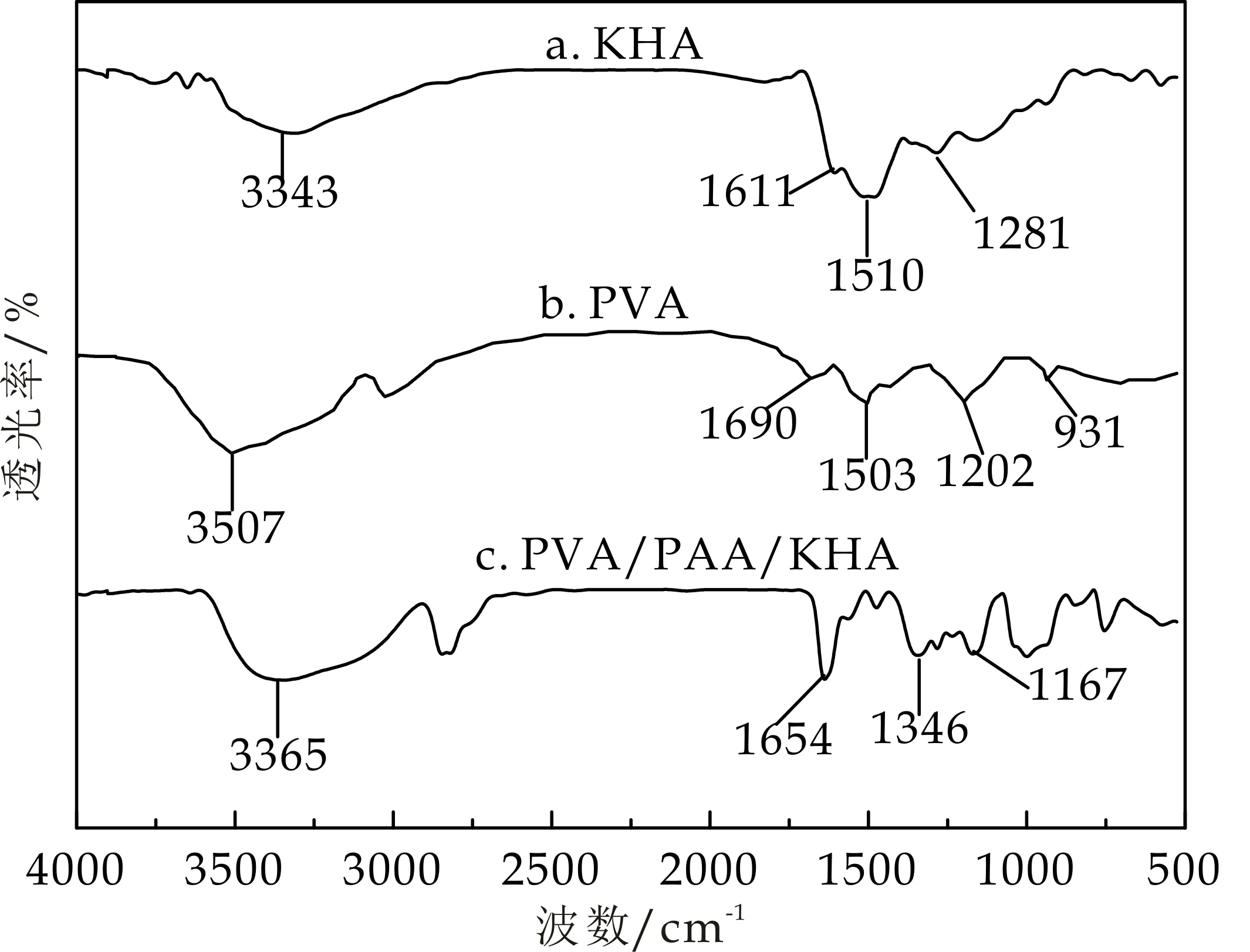
图7 KHA、PVA、PVA/PAA/KHA的红外光谱图
2.3 XRD分析
从图8的XRD谱图可以看出,PVA(a曲线)的XRD 在19.52 °附近产生了特征衍射峰,而PVA/PAA/KHA(b曲线)的 XRD 图中19.52 °附近特征衍射峰强度减弱,说明PVA、PAA、KHA接枝共聚后,破坏了PVA中的结晶结构,从而使其结晶度改善,衍射峰较PVA规整,合成出了新的材料.
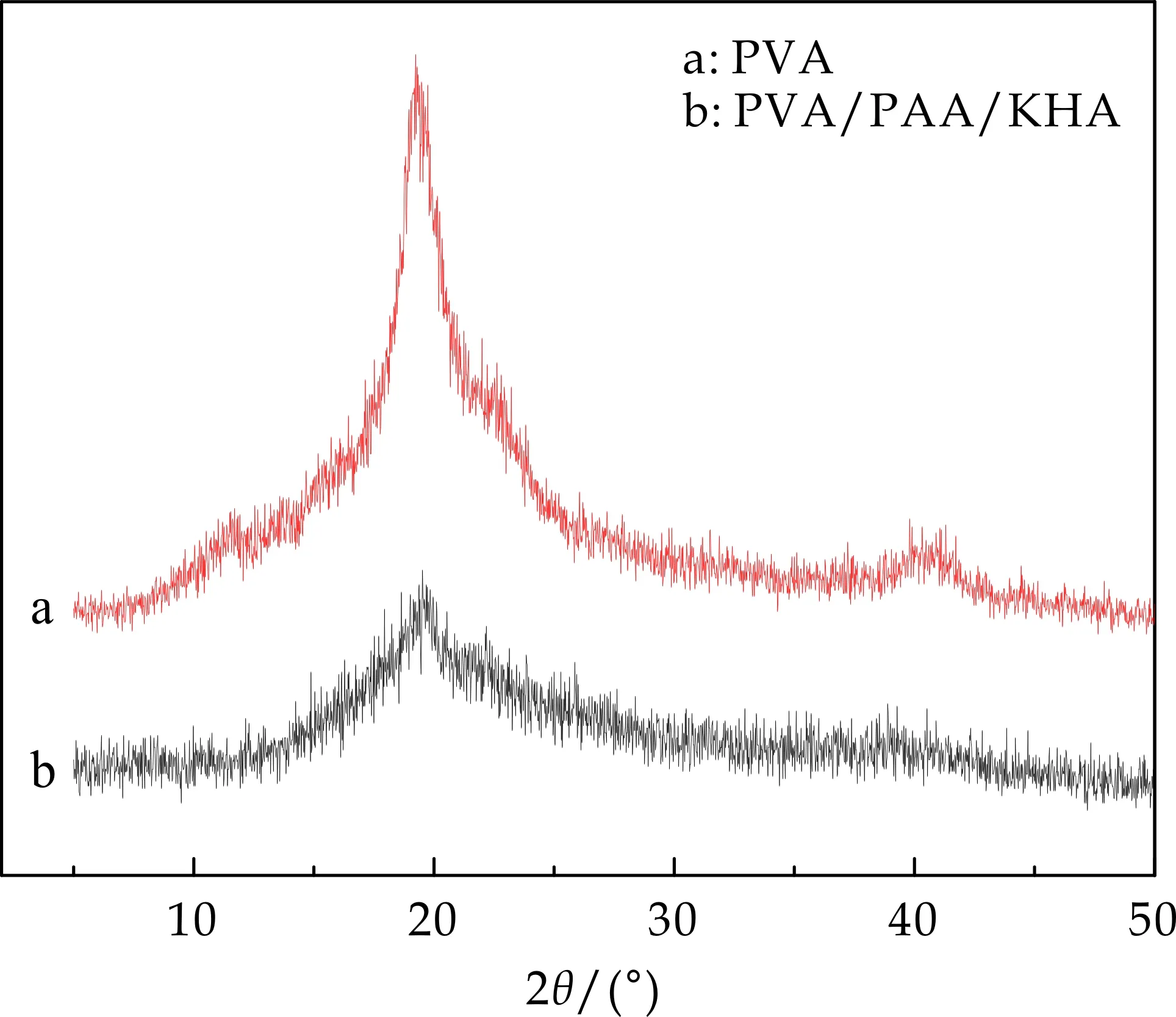
图8 PVA、PVA/PAA/KHA的XRD图
2.4 SEM分析
从图9可以看出,在低倍放大中,材料表面呈现孔状,分布相对均匀;在高倍放大中,孔隙的内部还有小孔,由于 PVA 分子链的定向排列,孔隙之间相互贯通,呈褶皱条纹状.这种互穿网络结构具有较大的比表面积,从而提高了水化过程中亲水性基团对水的利用率.材料溶胀后形成一个个“微型水库”,能够持续供水供肥,延缓了养分的溶出速率,具有比较好的缓释性能.

(a)10 μm

(b)5 μm图9 PVA/PAA/KHA不同放大倍数的SEM照片
2.5 保水材料对青菜叶片生理活性的影响
2.5.1 保水材料对青菜叶片中可溶性蛋白含量的影响
可溶性蛋白是植物体内氮素存在的主要形式,参与各种代谢反应,是植物的渗透调节物质之一,其含量是衡量植物代谢反应强弱和对外界逆境抵抗能力的一个重要指标.如图10所示,不同保水材料添加量处理对青菜中叶绿素含量均有显著影响(p<0.05).随着青菜生长周期变长,叶片可溶性蛋白含量呈先升高、后降低的趋势,且保水材料处理下青菜叶片可溶性蛋白含量均高于对照.第7~14天,青菜叶片中蛋白质含量普遍呈现上升趋势,保水材料处理对青菜叶片可溶性蛋白含量具有促进作用;青菜生长第21天时,当土壤(g):保水材料(g)为500∶1的添加量时,叶片可溶性蛋白含量达到最大值,为18.9 mg/g,其余处理可溶性蛋白含量均有所下降;第28天时青菜叶片中蛋白质含量普遍呈现下降趋势,但保水材料处理与对照差异显著,说明保水材料处理对青菜叶片可溶性蛋白含量的促进作用较为明显,最适宜的保水材料添加为500∶1.
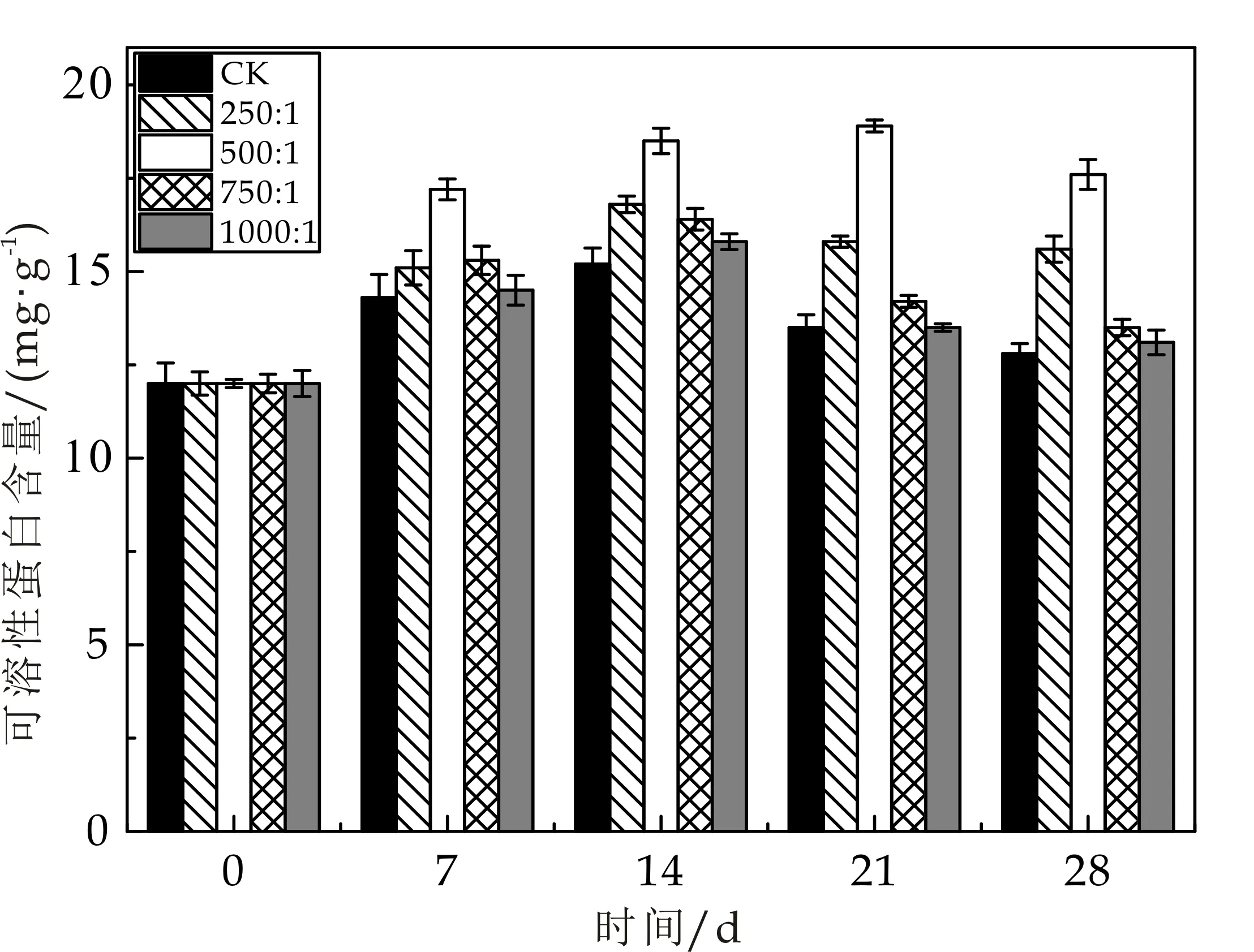
图10 不同比例保水材料对青菜叶片中蛋白质含量的影响
2.5.2 保水材料对青菜叶片中叶绿素a含量的影响
由图11可知,不同保水材料添加量处理对青菜中叶绿素含量均有显著影响(p<0.05),都呈先增大后降低的趋势,但保水材料处理与对照差异显著,其中500∶1处理在第7天时青菜叶绿素含量达到最大值1.28 mg/g.叶绿素含量下降是因为叶绿素在青菜中处于不断更新状态,随着生长周期的延长,不断被叶绿素酶分解,或经光氧化而漂白,引起了叶绿素的分解破坏.保水材料中腐植酸作为重要碳源,可以将有效碳直接作用于植物根部,大大提高CO2吸收转化量,增强叶绿素的光合作用和含量.其次添加保水材料处理能够对肥料养分进行缓慢释放,延长养分释放周期,从而为植物持续输送养分,所以在植物生长后期,青菜中叶绿素含量均大于空白对照.
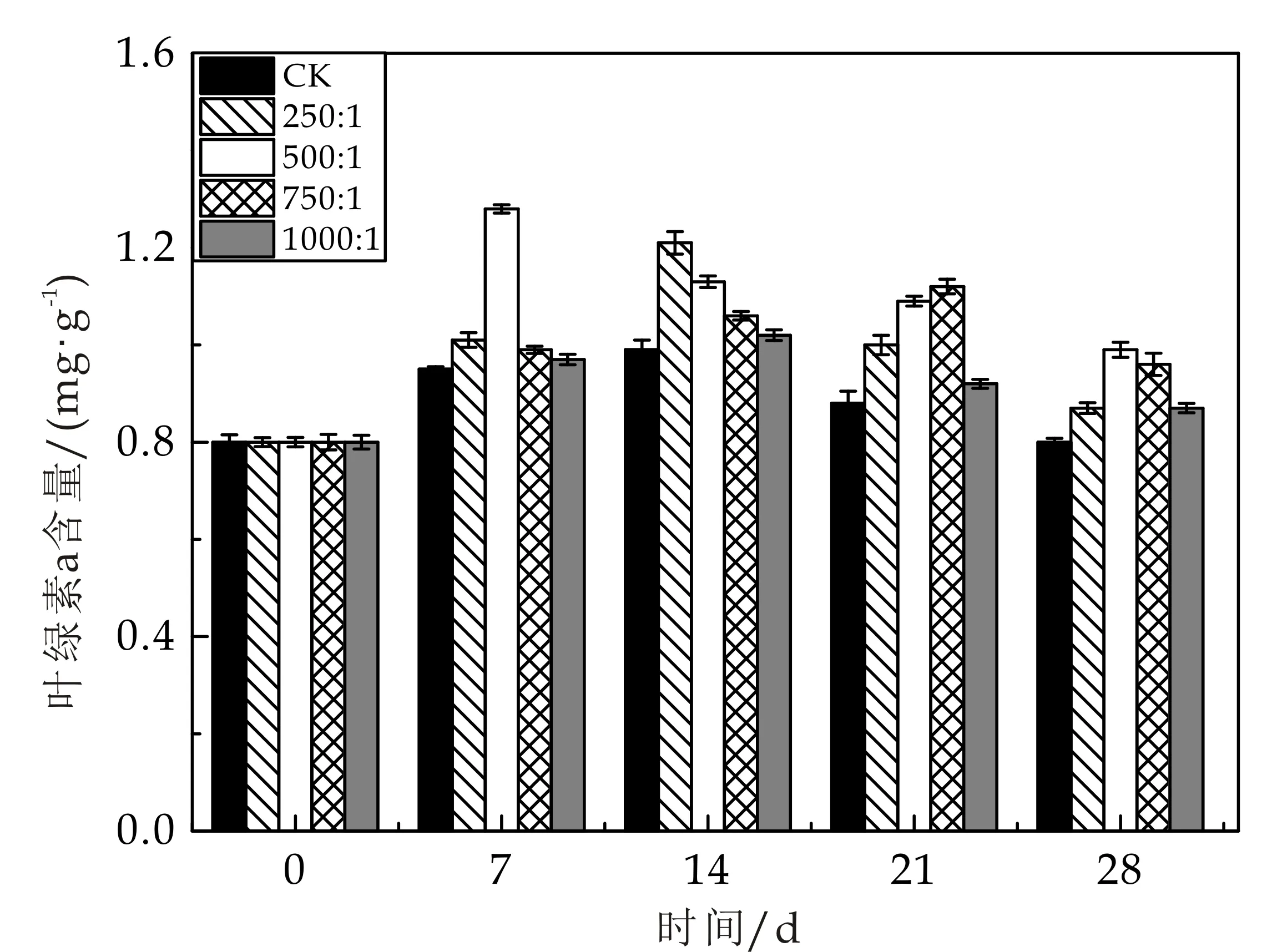
图11 不同比例保水材料对青菜叶片中叶绿素a含量的影响
2.5.3 保水材料对青菜叶片中丙二醛(MDA)含量的影响
植物器官在逆境条件下时,往往发生膜脂过氧化,MDA是其产物之一,MDA含量越高,表明植物体细胞膜损伤越严重.如图12所示,添加保水材料初期,充足的肥效使青菜生长茂盛,膜脂过氧化逐渐降低,MDA含量呈下降趋势;第14天,500∶1处理下,青菜MDA含量达到最低值0.086 mg/g,随着环境的胁迫,MDA含量开始升高,在21~28天CK对照MDA含量上升显著(p<0.05),但保水材料处理依然维持在较低水平(p<0.01),也进一步说明保水材料对青菜细胞代谢平衡起到协调和保护作用,避免了青菜受环境胁迫的伤害.
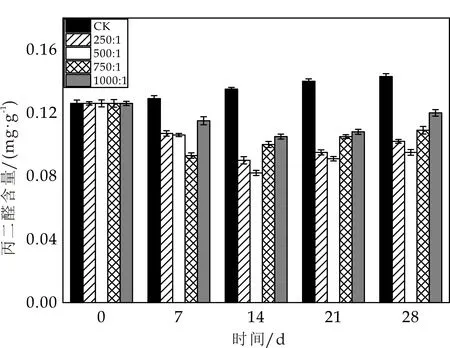
图12 不同比例保水材料对青菜叶片中丙二醛含量的影响
3 结论
通过水溶液聚合法将腐植酸钾、聚乙烯醇、丙烯酸三者接枝共聚,成功合成了成本低廉、绿色环保的互穿网络型腐植酸保水材料PVA/PAA/KHA.最佳工艺条件下保水材料吸蒸馏水能力最高可达481.3 g/g,保水倍率可达90.3%.通过FT-IR、XRD分析表明,PVA、PAA、KHA三者发生了接枝共聚反应,合成出了目标产物,SEM表征结果显示产物有多孔型互穿网络结构.添加量为500∶1时,可溶性蛋白、叶绿素a含量分别高达18.9 mg/g、1.28 mg/g,MDA含量可降至0.086 mg/g,提高了植物品质、抗逆性,将在农、林等领域有潜在的应用价值.
