基于手持技术的二元弱酸盐离子平衡实验设计
2019-10-17龚迪黄香王真真毕建洪合肥师范学院化学与化学工程学院230601
龚迪 黄香 王真真 毕建洪 合肥师范学院 化学与化学工程学院 230601
“二元弱酸盐溶液离子平衡”是高中选修四的内容,涉及水解和电离平衡,是本章的重点内容。“二元弱酸盐溶液离子平衡”知识点是抽象性知识点,对学生思维要求较高,仅利用传统教学方式进行教学的话,学生理解起来有一定的困难,为帮助学生更好的掌握该部分内容,本文利用手持技术实验选取两个实验案例进行实验教学案例设计,以期对教师教学和学生学习提供一定帮助。
一、实验用品及原理
邻苯二甲酸氢钾(potassium acid phthalate)固体,浓盐酸,去离子水, 0.1mol/L、0.5mol/L、1mol/L氢氧化钠和盐酸溶液,数据采集器(LabQuest mini data interface system),pH传感器(pH sensor),计算机及配套软件,磁力搅拌器(magnetic stirring apparatus),两用滴定管。
实验原理:
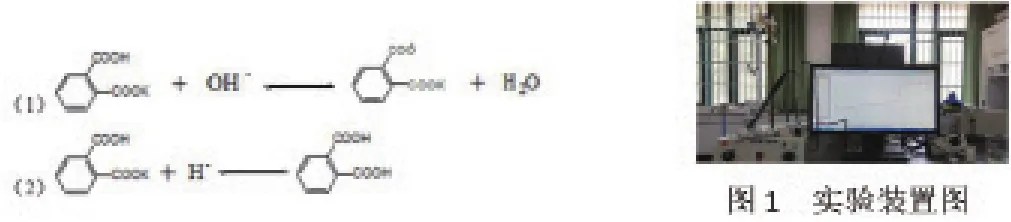
实验装置图同图1。
二、实验过程
1)配制0.05mol/L邻苯二甲酸氢钾溶液,连好装置,打开软件。
2)分别取两份100mL去离子水、邻苯二甲酸氢钾溶液倒入四个烧杯中。
3)将pH传感器依次放入两种溶液中(每次放入前校准传感器),向两用滴定管装满0.1mol/L NaOH,开始滴定时,同时点击软件的启动按钮记录实验数据。
4)步骤同上,盐酸滴定溶液。
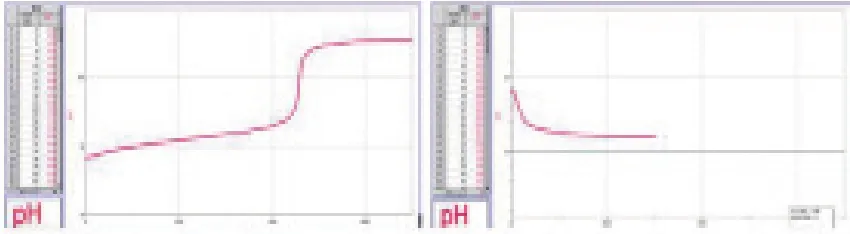
图2 氢氧化钠、盐酸滴定曲线
三、实验数据及分析
实验曲线图如右图2,数据分析:分析滴加碱的一组数据可知,两种等体积的溶液在加入相同量的氢氧化钠后,pH变化显著不同,说明两种溶液对于加入的碱的缓冲效果不同,其中去离子水明显对于加入的氢氧化钠无缓冲能力,而邻苯二甲酸氢钾溶液能有效对加入的氢氧化钠溶液产生缓冲作用,这是因为邻苯二甲酸氢钾溶液能够与碱发生反应。相应的,通过分析滴加酸的一组数据我们得知,加酸时,去离子水溶液的pH呈直线下降,说明其对加入的盐酸溶液无缓冲作用,而邻苯二甲酸氢钾溶液能有效对加入的盐酸溶液产生缓冲作用,而且,通过实验图像以及数据分析可知,邻苯二甲酸氢钾溶液的缓冲能力位于4.6—8.8。
综上,在高中化学知识中,选修四的知识主要是讲述某个化学现象的本质原因、原理是什么,对学生来说具有挑战性,本文中摒除以前的传统教学方式,用时代前沿技术手持技术实验与传统教学方式结合,有效锻炼学生实验能力,掌握前沿技术的操作方法,能够培养出顺应时代需要的人才。
