绵萆薢化学成分研究(II)
2019-10-11邓旭坤余惠凡刘钊舒广文郑燕段欢
邓旭坤,余惠凡,刘钊,舒广文,郑燕,段欢
(1中南民族大学 药学院, 武汉 430074; 2 中南民族大学 学报编辑部, 武汉 430074;3 淮北职业技术学院 医学系,淮北 235000)
绵萆薢为薯蓣科植物绵萆薢(DioscoreaseptemlobaThunb.)的干燥根茎,又名大萆薢、萆薢、硬饭团、金刚等,主要分布在我国浙江、江西、福建、湖南、湖北、广东及广西等地.绵萆薢在湖北省恩施地区也是常用的一种土家药.土家医称之为“穿地龙”、“过山龙”.因其具有利湿去浊、祛风除痹的功效,在临床上常用于淋病白浊、白带过多、湿热疮毒、腰膝痹痛等病症;在慢性前列腺炎、乳糜尿、风湿及类风湿性关节炎等病的治疗多有应用[1].现代研究表明:绵萆薢主要含有甾体类、二芳基庚烷类、木脂素类、有机酸、酯类、多糖、黏液质及鞣质等化学成分,具有抗肿瘤、抗骨质疏松、降尿酸、降血脂、抗真菌、抗心肌缺血及预防动脉粥样硬化等药理作用[2-4].
为了探明其药效物质基础,本课题组对其化学成分进行了系统研究.运用正相和反相硅胶柱色谱、高效液相半制备色谱等分离和纯化方法[5,6],同时配合硅胶薄层层析跟踪分析,从绵萆薢的乙酸乙酯萃取部位分离得到了8个化合物.
1 实验部分
1.1 仪器与材料
核磁共振波谱仪(AM-600 型,德国Bruker);高效液相色谱仪(Ultimate 3000 型,美国Dionex);色谱柱(10 mm × 250 mm,XDB-C18 ,美国Agilent);薄层三用紫外分析仪(ZF-6型,上海嘉鹏).
柱层析硅胶(100~200目、200~300目,青岛海洋化工厂);乙醇、石油醚、二氯甲烷、乙酸乙酯、正丁醇、甲醇(分析纯,天津博迪);乙腈(色谱纯,中国昌泰兴业).
2016年4月上旬,在湖北恩施宣恩县椿木营乡海拔1650~1800 m的山坡路旁密林下和灌丛中采集绵萆薢,经中南民族大学药学院刘新桥副教授鉴定为薯蓣科绵萆薢属植物绵萆薢(D.septemlobaThunb.).药材标本存放于中南民族大学药学院.
1.2 提取与分离
取绵萆薢的干燥根茎10 kg淋洗切片后晒干,粉碎.粗粉置95%和70%乙醇中依次回流提取各3次,每次3 h,过滤,合并滤液,减压浓缩得浸膏,将浸膏用蒸馏水分散后依次用石油醚、二氯甲烷、乙酸乙酯及正丁醇进行萃取后得石油醚萃取部位(5 g)、二氯甲烷部位(22 g)、乙酸乙酯部位(49 g)及正丁醇部位(340 g).取乙酸乙酯部位浓缩物30 g,经正相硅胶柱色谱分离,以二氯甲烷-甲醇梯度洗脱(体积比分别为10∶0,9.5∶0.5,9∶1,8.5∶1.5,8∶2,7∶3,6∶4,5∶5,0∶10),TLC薄层分析合并同类成分得到18个不同组分(Fr.1~Fr.18),Fr.3(4.3 g)经反相硅胶柱(C18)、水-甲醇梯度洗脱(体积比10∶0→0∶10)和半制备高效液相(HPLC)进行分离,得到单体化合物1、2(10,12 mg),同样的方法,Fr.4(2.2 g)分离纯化得到化合物3(9 mg),Fr.9(2.2 g)分离纯化得到化合物4、5(8,9 mg),Fr.11(1.2 g)分离纯化得到化合物6(9 mg),Fr.12(3.2 g)得到化合物7、8(35,21mg).化合物结构式见图1.
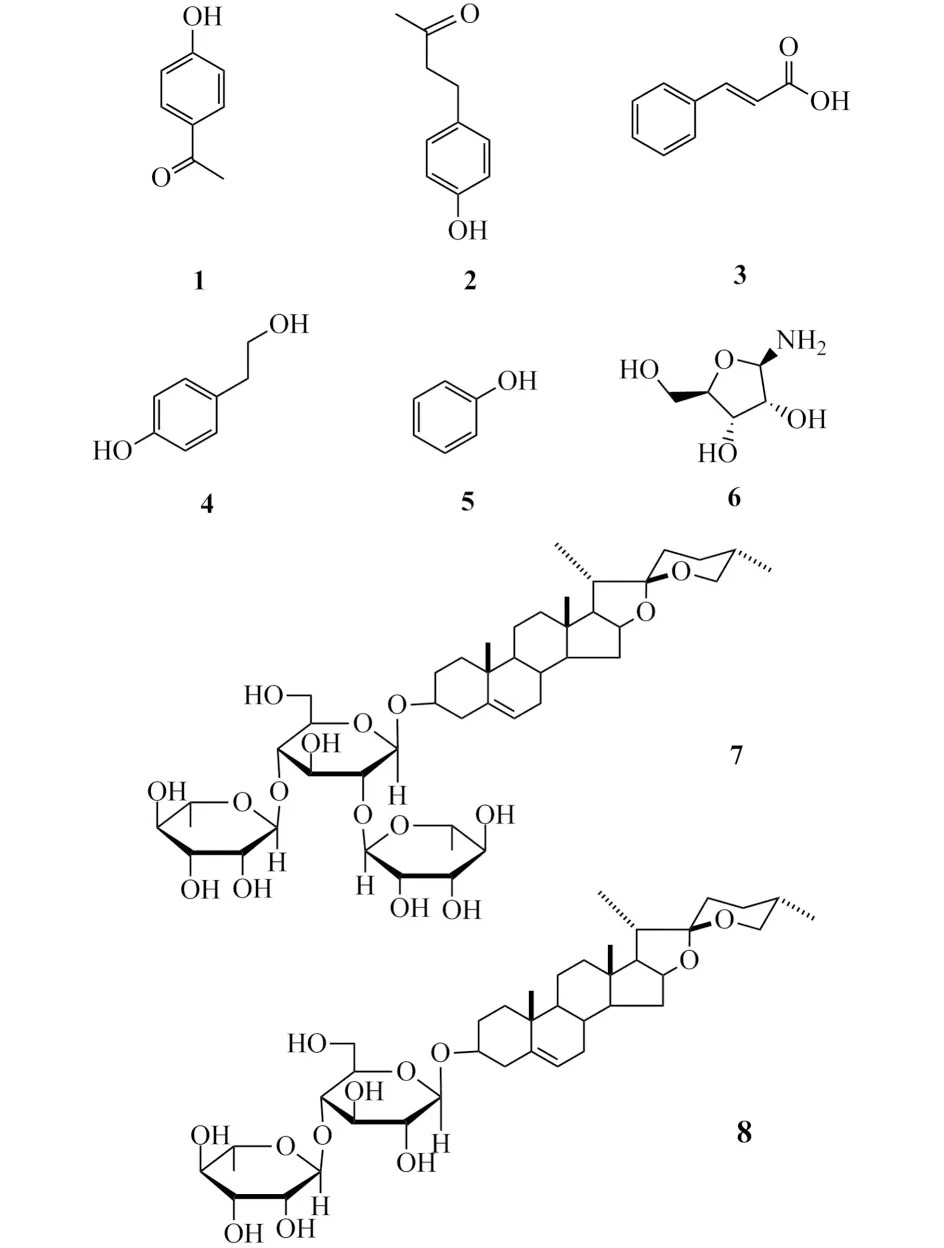
图1 化合物1~8的结构式
2 结构鉴定
化合物1:无色针晶(C8H8O2),1H NMR(600 MHz, MeOD)δ: 7.89(2H, d,J=9.0 Hz, H-2, 6), 6.84(2H, d,J=9.0 Hz, H-3, 5), 2.52(3H, s,J=9.0 Hz, COCH3);13C NMR(150 MHz, MeOD)δ: 199.33(C-7), 164.10(C-1), 132.01(C-2, 6), 129.88(C-4), 116.15(C-3, 5), 26.22(C-8).以上数据与文献[7]基本一致,故鉴定其为对羟基苯乙酮.
化合物2:白色粉末(C10H12O2),1H NMR(600 MHz, MeOD)δ: 6.97(2H, d,J=9.0 Hz, H-2′, 6′), 6.64(2H, d,J=9.0 Hz, H-3′, 5′), 2.70(4H, s, H-3, 4), 2.07(3H, s, H-1);13C NMR(150 MHz, MeOD)δ: 211.40(C-2), 156.65(C-4′), 133.16(C-1′), 130.23(C-2′, 6′), 116.15(C-3′, 5′), 46.26(C-3), 30.02(C-1), 30.01(C-4).以上数据与文献[8]中基本一致,故鉴定其为4-(对羟基苯基)-2-丁酮.
化合物3:无色针状晶体(C9H8O2),1H NMR(600 MHz, MeOD)δ: 7.60(1H, d,J=12.0 Hz, H-3), 7.51(2H, m, H-3′, 5′), 7.31~7.32(3H, m, H-2′, 6′, 4′), 6.40(1H, d,J=12.0 Hz, H-2);13C NMR(150 MHz, MeOD)δ: 170.51(C-1), 146.45(C-3), 135.96(C-1′), 131.56(C-3′, 5′), 130.20(C-2′, 6′), 129.33(C-4′), 119.51(C-2).以上数据与文献[9]报道一致,故鉴定其为桂皮酸.
化合物4:无色片状晶体(C8H10O2),1H NMR(600 MHz, MeOD)δ: 7.01(2H, d,J=8.9 Hz, H-2, 6), 6.63(2H, d,J=8.9 Hz, H-3, 5)2.75(2H, t,J=7.7 Hz, H-1′), 2.44(2H, t,J=7.7 Hz, H-2′);13C NMR(150 MHz, MeOD)δ: 156.61(C-4), 133.41(C-1), 130.21(C-2, 6), 116.11(C-3, 5), 64.38(C-2′), 31.80(C-1′).以上数据与文献[10]报道一致,故鉴定其为对羟基苯乙醇.
化合物5:白色晶体(C6H6O),1H NMR(600 MHz, MeOD)δ: 7.44(1H, m, H-4), 7.36(2H, d,J=8.9 Hz, H-3, 5), 6.74(2H, d,J=8.9 Hz, H-2, 6);13C NMR(150 MHz, MeOD)δ: 160.66(C-1), 130.73(C-3, 5), 127.75(C-2, 6), 116.68(C-4).与苯酚对照品共薄层,Rf值一致故鉴定其为苯酚.
化合物6:白色针状结晶(C7H11N3O4),1H NMR(600 MHz, MeOD)δ: 8.27(1H, s H-4), 8.14(1H, s H-2), 5.91(1H, d,J=6.5 Hz, H-1′), 4.70(1H, t, H-3′), 4.28(1H, dd,J=6.5, 2.5Hz, H-4′), 4.13(1H, d,J=2.5 Hz, H-2′), 3.83(1H, dd,J=2.5, 13.0 Hz, H-5′a), 3.69(1H, dd,J=2.5, 12.5 Hz, H-5′b);13C NMR(150 MHz, MeOD)δ: 153.48(C-2), 142.04(C-4), 91.24(C-1′), 88.19(C-4′), 75.44(C-3′), 72.68(C-2′), 63.48(C-5′).以上数据与文献[11]基本一致,故鉴定其为1-β-D-呋喃核糖基-1H-1,2,4-三氮唑.
化合物7:无色针状结晶(C45H72O16),按文献[12]方法:1%盐酸水解,以标准D-葡萄糖、L-鼠李糖对照,经带蒸发光散射检测器的HPLC分析确定糖部分具有D-葡萄糖、L-鼠李糖,根据端基质子的耦合常数,确定为α-L-吡喃鼠李糖和β-D-吡喃葡萄糖,异核多键碳氢相关谱 (HMBC)谱确定糖的连接位置.1H NMR(600 MHz, MeOD)δ: 5.35(1H, br s, H-6), 5.16(1H, s, rha, H-1″), 4.80(1H, rha, H-1‴), 4.47(1H, d,J=6.5 Hz, glc H-1′), 4.36(1H, m, H-5″), 4.10(1H, m, H-16), 3.35~3.98(糖质子),1.50~2.20(苷元质子)1.21(6H, dd,J=6.5 Hz, H-6″, H-6‴), 1.01(3H, s, H-19), 0.88(3H, d,J=6.5 Hz, H-21), 0.84(3H, s, H-18), 0.80(3H, d,J=6.5 Hz, H-27);13C NMR(150 MHz, MeOD)δ: 141.87(C-5), 122.65(C-6), 110.58(C-22), 82.21(C-16), 79.87(C-3), 63.72(C-17), 57.79(C-14), 51.69(C-9), 42.89(C-20), 41.41(C-13),40.92(C-12), 39.48(C-4), 38.56(C-1), 38.07(C-10), 32.79(C-8), 32.73(C-7), 32.41(C-23), 31.44(C-15), 30.75(C-2), 21.98(C-11), 19.84(C-19), 16.78(C-18), 14.90(C-21); 糖部分: glc: 102.99(C-1′), 79.87(C-4′), 79.30(C-2′), 78.02(C-5′), 76.57(C-3′), 61.90(C-6′); rha: 102.33(C-1″), 73.89(C-4″), 73.70(C-3″), 72.45(C-2″), 70.63(C-5″), 17.98(C-6″); rha: 100.39(C-1‴), 73.80(C-4‴), 72.18(C-3‴), 72.14(C-2‴), 69.77(C-5‴), 17.86(C-6‴).以上数据与文献[12]基本一致,故鉴定其为薯蓣皂苷元-3-O-[α-L-吡喃鼠李糖(1→2)]- [α-L-吡喃鼠李糖(1→4)]-β-D-吡喃葡萄糖.
化合物8:白色粉末状(C39H62O12),按文献[12]方法进行酸水解薄层层析,以标准D-葡萄糖、L-鼠李糖对照,确定糖部分具有β-D-葡萄糖、α-L-鼠李糖.1H NMR(600 MHz, MeOD)δ: 5.34(1H, br s, rha, H-1″), 5.16(1H, br s, H-6), 4.49(1H, d,J=6.5 Hz, H-1′), 4.36(1H, m, H-5″), 4.10(1H, m, H-16), 3.21~3.88(糖质子), 1.52~2.20(苷元质子), 1.20(3H, d,J=6.5 Hz, H-6″), 1.01(3H, s, H-19), 0.93(3H, d,J=6.5 Hz, H-21), 0.77(3H, s, H-18), 0.75(3H, d,J=6.5 Hz, H-27);13C NMR(150 MHz, MeOD)δ: 141.97(C-5), 122.59(C-6), 110.54(C-22), 82.17(C-16), 79.13(C-3), 67.82(C-26), 63.70(C-17), 57.78(C-14), 51.66(C-9), 42.88(C-20), 41.88(C-13), 39.49(C-12), 38.54(C-4), 38.02(C-1), 33.18(C-7), 32.78(C-15), 32.73(C-8), 32.40(C-23), 31.43(C-25), 30.73(C-2), 29.88(C-24), 29.76(C-24), 21.98(C-11), 19.86(C-19), 18.99(C-10),16.81(C-18), 14.81(C-21); 糖部分: glc: 100.48(C-1′), 79.33(C-4′), 78.98(C-5′), 77.67(C-3′), 71.74(C-2′), 62.70(C-6′); rha: 102.15(C-1″), 73.87(C-4″), 72.4(C-3″), 72.17(C-2″),69.72(C-5″),18.6(C-6″).以上数据与文献[13]基本一致,故鉴定其为薯蓣皂苷元-3-O-[α-L-吡喃鼠李糖(1→4)]-β-D-吡喃葡萄糖.
3 结语
通过对绵萆薢乙酸乙酯萃取部位的系统分离,得到了8个化合物,分别鉴定为:对羟基苯乙酮(1)、4-(对羟基苯基)-2-丁酮(2)、肉桂酸(3)、对羟基苯乙醇(4)、苯酚(5)、1-β-D-呋喃核糖基-1H-1,2,4-三氮唑(6)、薯蓣皂苷元-3-O-[α-L-吡喃鼠李糖(1→2)]- [α-L-吡喃鼠李糖(1→4)]-β-D-吡喃葡萄糖(7)、薯蓣皂苷元-3-O-[α-L-吡喃鼠李糖(1→2)]-β-D-吡喃葡萄糖(8).其中化合物1~6为首次从该植物分离得到,且化合物1、4、5、6是首次从该属植物中分离得到,均为常见化合物,其中前5个化合物为酚酸类化合物,化合物6为核苷类化合物,化合物7和8为甾体皂苷类化合物.为绵萆薢的开发和研究工作提供了一定的依据.
致谢:向中南民族大学药学院分析测试中心对样品测试和数据采集的帮助表示诚挚谢意
