沉淀温度对K-CuLaZrO2 催化剂上合成气直接合成异丁醇的影响
2019-10-10武应全解红娟陈建刚
谭 理,武应全,张 涛,解红娟,陈建刚
(1.福州大学 分子催化与原位表征研究所和化学学院,福建 福州 350108;2.中国科学院山西煤炭化学研究所 煤转化国家重点实验室,山西 太原 030001)
低碳醇合成是基础化学工业中的一个重要过程,其产品被广泛用作燃料、辛烷或十六烷增强燃料添加剂和氧化燃料添加剂[1-4]。异丁醇,作为混合醇中的一种,广泛用作溶剂(硝酸纤维素的助溶剂,多种油类、橡胶、天然树脂的溶剂及氯化锂提取剂),也是基本有机化工原料,主要用于生产邻苯二甲酸二异丁酯增塑剂、乙酸异丁酯溶剂,还有少部分用于生产丁酸异丁酯、乳酸异丁酯等[5-7]。此外,异丁醇已于2010年被美国环保署(EPA)批准为汽油添加剂,市场上对异丁醇的需求会逐步增大。
ZrO2催化剂由于其特殊的性质(同时具有酸碱性和氧化还原性)在甲醇合成[8-10]、甲醇氧化重整[11,12]、水煤气变换反应[13]及不同加氢[14]等催化过程中得到了广泛的应用。另外,在ZrO2基催化剂中引入碱金属对其进行改性后,并用于CO加氢反应过程中发现,C2+醇选择性明显提高,尤其是异丁醇[15-21]。
共沉淀法是合成固体复合氧化物的主要方法,具有控制精确、分散度高、相互作用强、制备工艺简单等特点。但是,由于沉淀过程属于非均匀非线性,控制过程复杂,重复性差。近年来,研究人员逐渐认识到,一个优良的催化剂不仅仅是对其进行后处理(煅烧或还原),而应该从沉淀反应开始,其中,沉淀温度是影响沉淀反应过程的重要因素之一。Zheng等[22-24]发现,在适当的沉淀温度下,可获得较高比表面积的ZrO2基催化剂。唐德仁等[25]研究了沉淀温度对CuO/ZnO/Al2O3催化剂前驱体组成及其对水煤气变换反应的催化活性的影响,作者观察到在较高的沉淀温度下形成了CuO-ZnO固溶体,且具有较高的催化活性。Cui等[26]发现,当沉淀温度为70 ℃时,形成了CuO-CeO固溶体,具有良好的还原性能和储氧能力,有利于结构的稳定。Jittiarporn 等[27]在不同的温度下合成了花瓣状MoO3晶体,且发现在最高反应温度(85 ℃)下制备的催化剂具有最佳的光致变色性能。Frei等[28]报道了沉淀和老化温度对Cu/ZnO/ZrO2催化剂体系结构和催化性能的影响,发现沉淀温度对催化剂前驱物组成及晶化过程具有明显的影响,进而影响到催化剂结构和催化性能。
综上所述,在催化剂制备过程中,沉淀温度对催化剂结构、表面性质以及其在反应过程中的催化性能具有非常大的影响。作者前期研究发现,ZrO2基催化剂上具有较好的CO加氢合成异丁醇催化性能[21,29-31],但是以上工作对ZrO2基催化剂的制备参数研究较少。本文采用共沉淀法在不同的沉淀温度(30、60和80 ℃)下制备了三个不同催化剂,并采用BET、XRD、XPS、H2-TPR和FT-IR等对其进行了表征,从催化剂结构特征、元素在催化剂表面的还原性和分布,以及CO在催化剂表面的吸附性能方面研究了沉淀温度对异丁醇合成性能的影响。
1 实验部分
1.1 催化剂的制备
采用共沉淀法制备催化剂。将一定量Cu(NO3)2·3H2O,La(NO3)3·6H2O和ZrO(NO3)2·2H2O(n(Cu)∶n(La)∶n(Zr)= 1∶0.2∶4)溶于350 mL去离子水中,同时将一定量KOH溶于400 mL去离子水中,分别将配制好的盐溶液与碱液同时滴入烧杯中进行共沉淀反应,烧杯中提前加入1 L去离子水。沉淀温度分别控制为30、60和80 ℃。沉淀完成后静置老化3 h,然后抽滤、洗涤至中性。滤饼在100 ℃条件下干燥12 h后再在450 ℃下焙烧4 h。
将上述所得催化剂研磨成粉末,之后分别浸渍2%的K(%)进行改性,KOH为碱金属前驱体,在100 ℃下干燥12 h,然后在450 ℃下焙烧 4 h,压片后破碎至30-40目备用。不同沉淀温度下(30、60和80 ℃)制备的催化剂分别命名为CLZ-30、CLZ-60和CLZ-80。
1.2 催化剂的表征
催化剂XRD谱图在Bruker Rigaku D8型衍射仪上测试,CuKα特征谱线(λ=0.15418 nm)电压40 kV,电流100 mA。
催化剂的比表面积(BET)采用Tristar 3000型物理吸附仪进行测定,(77 K N2吸附)。
H2-TPR在自制装置上进行,称取0.1 g催化剂放于石英管中,在Ar (300 ℃)下进行处理2 h(除去吸附水),之后降温至50 ℃,切换为10%H2/Ar(体积比)的还原气,基线走平后进行程序升温还原(5 ℃/min),TCD检测器。
X射线光电子能谱是在Vg Escalab MK-2型光谱仪上进行测定,AlKα辐射(HT=1486.6 eV,250 W)。
催化剂表面羟基测试在德国Bruker公司生产的Tensor 27型红外光谱仪上进行。研磨细的催化剂粉末装入红外样品池后,在Ar气氛下、350 ℃条件下脱除吸附水1 h后采集光谱,采集前采用KBr作为背景。
吸附态CO红外光谱在以上红外光谱仪上进行。研磨细的催化剂装入样品池,于350 ℃纯氢还原2 h,通Ar吹扫20 min,降温后扫背景,然后通入CO吸附30 min,最后切换成Ar吹扫,间隔5 min测谱。
1.3 催化剂的评价
将5 mL催化剂装入反应器(φ15 mm×480 mm),通入10% H2/N2(体积比)的还原气在常压下对催化剂进行还原,之后切换合成气进行反应,反应条件:H2/CO=2,360 ℃,10 MPa,3000 h-1,产物经冷阱进行分离后收集液体。
气相产物采用GC4000A(炭分子筛柱,TCD检测器)和GC4000A(GDX-403柱,FID检测器)进行分析;液相产物采用GC4000A(GDX-401柱,TCD检测器)和GC-7AG(Chromsorb l01柱,FID检测器)进行分析。
2 结果与讨论
2.1 催化剂组成(ICP)
用电感耦合等离子体(ICP)对不同沉淀温度下制备的催化剂中元素的实际含量进行了测量,如表1所示。由表1可以看出,在催化剂合成过程中,测定的各元素含量与计量比配制的催化剂含量非常接近,表明催化剂组分即使在不同的制备温度下也能很好地完全沉淀。
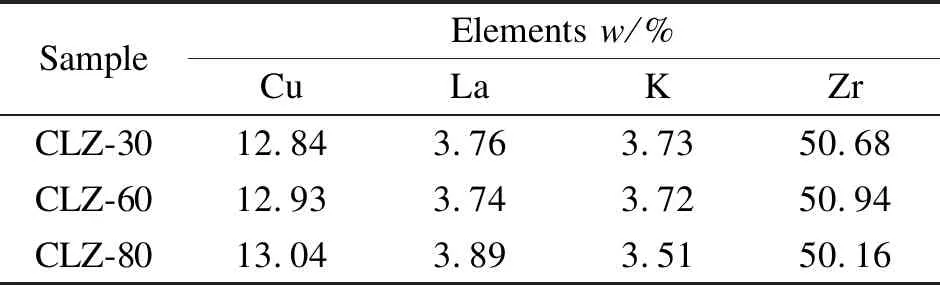
表1 沉淀温度对各组分含量的影响Table 1 Effect of precipitation temperature on content of components
2.2 催化剂的织构参数
表2为催化剂织构参数。由表2可以看出,新鲜样品的平均孔径和孔体积随沉淀温度的升高略有增大,而比表面积有轻微增加趋势,当沉淀温度升高到80 ℃时,CLZ-80比表面积达到122 m2/g。
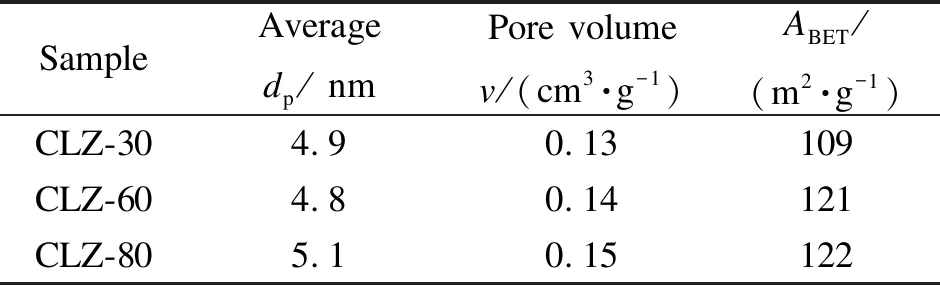
表2 催化剂织构参数Table 2 Texture parameters of different catalysts
2.3 催化剂的XRD表征
在不同沉淀温度下合成的催化剂XRD谱图见图1。在CLZ-30催化剂谱图上~31°处出现一个宽峰,这是无定形氧化锆(am-ZrO2)的特征峰。没有观察到CuO物相的衍射峰,表明铜物种在ZrO2中处于高度分散状态,CuO和ZrO2之间形成了较好的固溶体[32]。当沉淀温度升高到60 ℃时,35.6°和38.8°处出现明显的衍射峰,这是CuO相的特征峰(JCPDS card N.45-0937)[33],此时ZrO2仍以无定形状态存在。随着沉淀温度的进一步升高(80 ℃),归属为CuO的特征峰强度进一步升高,同时,在30.4°、50.7°和60.1°处出现了新的衍射峰,这归因于四方氧化锆(t-ZrO2)的特征峰(JCPDS card N.50-1089)[33]。另外在~31°处仍存在一个宽峰,说明部分ZrO2以t-ZrO2和am-ZrO2形式共存。从图1可以看出,由于La2O3含量低,所有催化剂均未发现La2O3晶体的衍射峰。Cui等[26]研究发现,适当提高沉淀温度(70 ℃)有助于在沉淀初期形成较大的晶体尺寸,大晶粒的存在可以增大孔半径,扩大孔径分布,有利于保持较高的表面积。郑建东等[24]研究了沉淀温度对LaMnAl11O19催化剂的影响,结果表明,低温不利于沉淀结晶。唐德仁等[25]同样发现,在较高的沉淀温度下可以提高催化剂结晶程度。因此,较高的沉淀温度有利于催化剂的高度结晶,较低的沉淀温度下化合物各组分的分散性较好。CuO和ZrO2在较低的沉淀温度(30 ℃)下分散性好,粒径小。
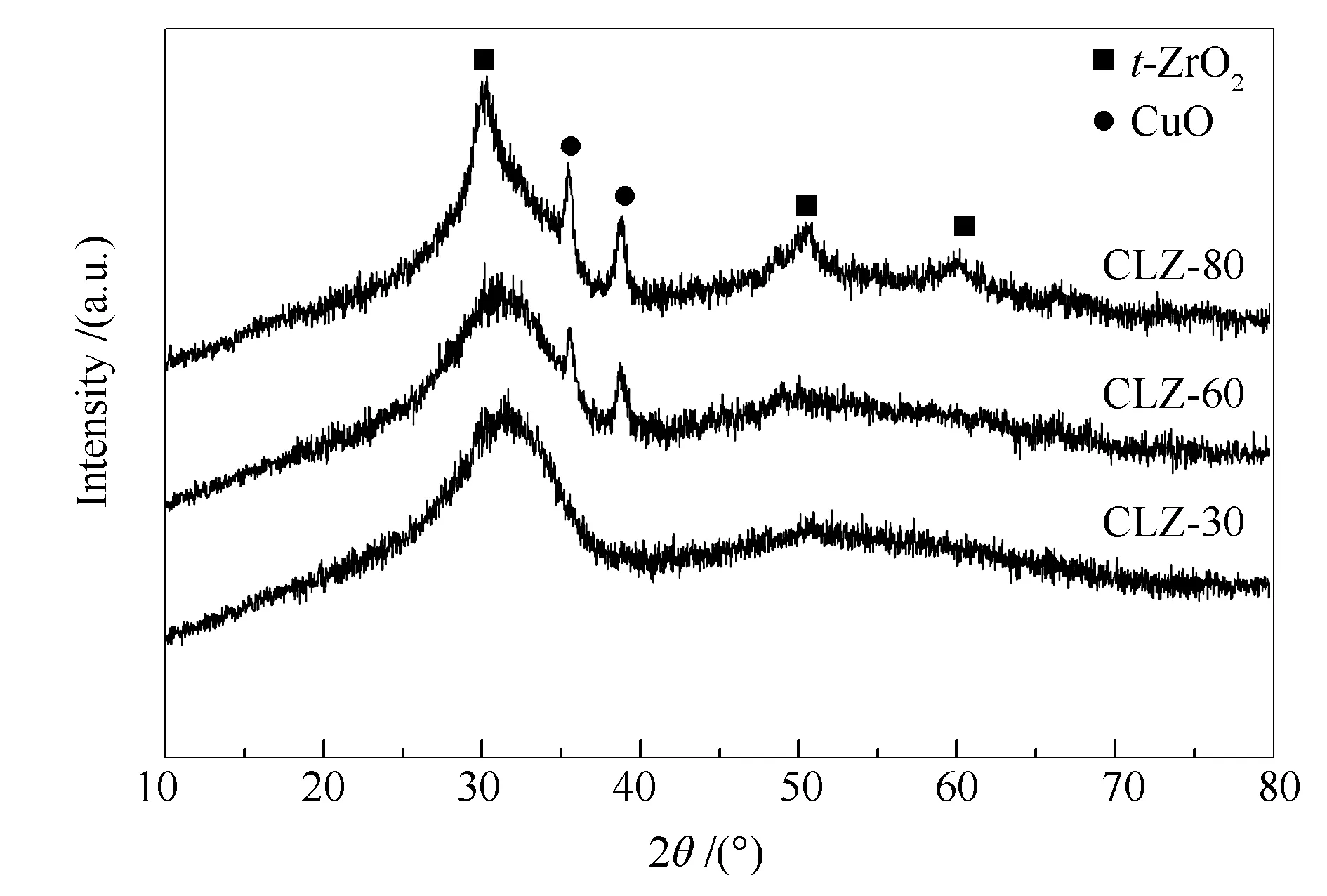
图1 不同沉淀温度下催化剂的XRD谱图Figure 1 XRD patterns of the catalysts precipitated at different temperatures
2.4 催化剂H2-TPR表征
图2为不同沉淀温度下所得催化剂的H2-TPR谱图。从图2可以看出,所有样品都显示出宽的还原峰(150-350 ℃)。在30 ℃沉淀温度下制备的催化剂上(CLZ-30),其还原峰出现在203 ℃附近。随着沉淀温度升高,H2还原峰逐渐向高温移动,当沉淀温度为80 ℃时,峰值转移到最高温度(231 ℃)。通过比较不同沉淀温度下制备的催化剂可以发现,在较低沉淀温度下所制备的催化剂中CuO容易还原。

图2 不同沉淀温度下催化剂的H2-TPR谱图Figure 2 H2-TPR patterns of the catalysts precipitated at different temperatures
2.5 催化剂的XPS分析
图3给出了不同沉淀温度下催化剂的XPS谱图,Cu 2p和Zr 3d的结合能见表1。不同沉淀温度下制备的催化剂上Cu 2p3/2的结合能都在933 eV附近,在高结合能处(940-945 eV)有震激峰出现,说明Cu以Cu2+形式存在。另外,Zr 3d5/2结合能约为182 eV,说明Zr以Zr4+形式存在[30]。表3为Cu 2p3/2和Zr 3d5/2的结合能。从表3中可以看出,Cu 2p3/2和Zr 3d5/2的结合能随着沉淀温度的升高而发生了明显的变化,在30 ℃时,Cu 2p3/2的结合能为934.3 eV,在80 ℃的沉淀温度下结合能为934.0 eV。相反,随着沉淀温度的升高,Zr 3d5/2的结合能明显增加,表明Cu和Zr组分的化学环境随着沉淀温度的变化而变化。这些结果清楚地表明电子转移发生在铜物质和氧化锆之间。此外,不同催化剂表面Cu/Zr比也随着沉淀温度的变化发生了变化(见表3),即铜在氧化锆载体上的分散度发生了变化。由以上结果可知,Cu/Zr比在较高的沉淀温度下达到最大值,表明Cu在较高的沉淀温度下会迁移到催化剂的表面。催化剂表面上更多的Cu含量将导致聚集。这可能是CuO衍射峰出现的原因之一,并且在高沉淀温度下其强度变强。
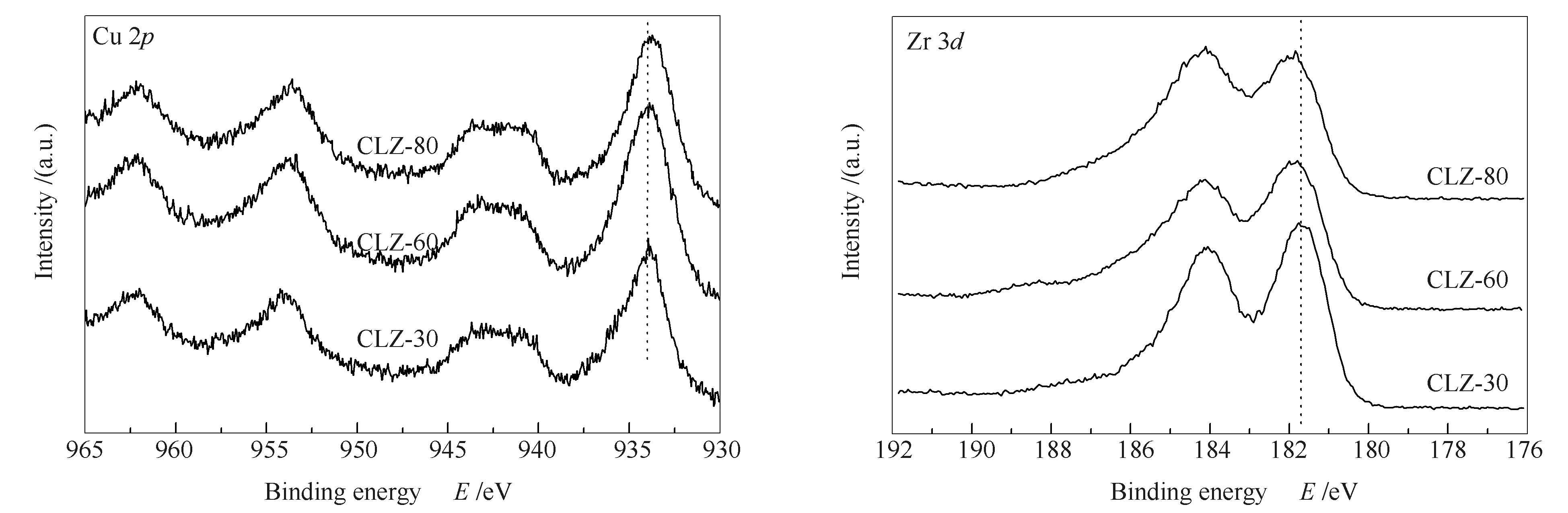
图3 不同沉淀温度下催化剂的Cu 2p和Zr 3d的XPS谱图Figure 3 XPS spectra of Cu 2p and Zr 3d over the catalysts precipitated at different temperatures

表3 Cu 2p3/2和Zr 3d5/2的结合能Table 3 Binding energy values of Cu 2p3/2 and Zr 3d5/2
2.6 催化剂表面羟基
催化剂表面羟基与C1中间体形成有关,例如甲酸盐物种、碳酸氢盐物种或碳酸盐物种等,这些C1中间体主要由催化剂表面羟基与CO或CO2反应形成。因此,采用FT-IR光谱考察不同沉淀温度下催化剂表面羟基分布情况,进而了解催化剂在反应过程中表面C1物种覆盖情况,具体见图4。所有样品在3400 cm-1附近呈现出一个较宽的包峰,可归属为羟基(-OH)的特征峰。另外,在3679 cm-1处含有一个明显的肩峰,为催化剂表面桥式吸附羟基[34,35]。通过对比不同催化剂表面羟基特征强度可以发现,随着沉淀温度的升高,催化剂表面羟基含量逐渐降低。
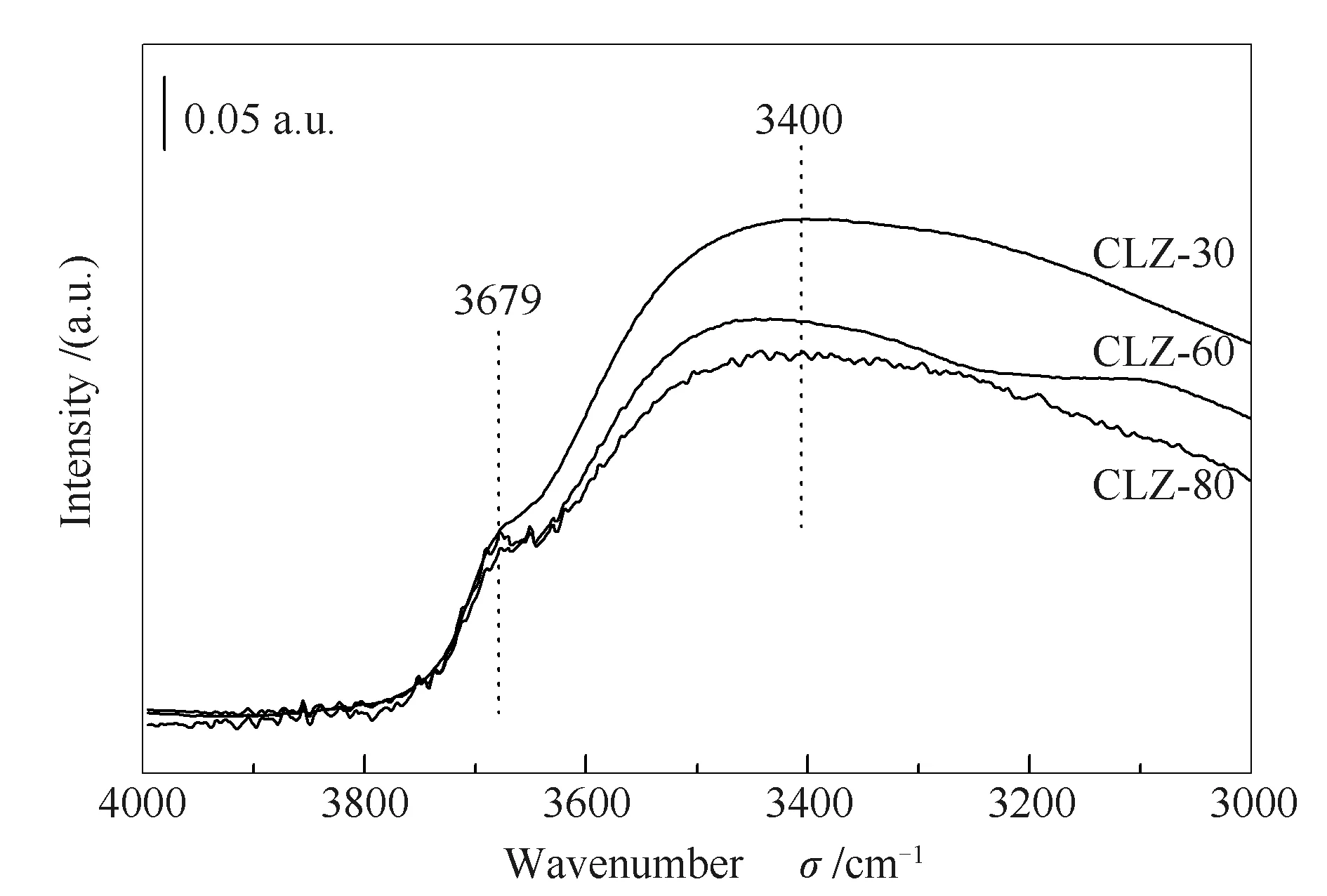
图4 不同沉淀温度下催化剂表面羟基分布Figure 4 Hydroxyl distribution on catalyst surface at different precipitation temperatures
2.7 催化剂的CO吸附
由于不同制备方法所制备的催化剂表面性质不同,为此,本研究采用红外光谱研究了CO分子在不同催化剂表面的吸附和活化性能,具体见图5。从图5可以看出,三种不同的催化剂表面都出现了明显的羧酸盐特征峰(1649、1260 cm-1)[29],但是不同催化剂表面羧酸盐物种特征峰的峰强度明显不同,随着沉淀温度的提高,归属为羧酸盐的特征峰强度逐渐下降,说明催化剂表面羧酸盐物种含量随沉淀温度升高而逐渐减少。
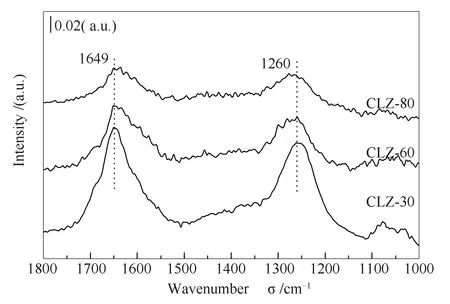
图5 不同沉淀温度下催化剂表面CO吸附红外光谱谱图Figure 5 FT-IR spectra of CO adsorption over catalysts precipitated at different temperatures
2.8 催化剂的催化性能
沉淀温度对催化剂上CO加氢合成异丁醇的催化性能的影响见表4。

表4 不同沉淀温度下催化剂的性能评价Table 4 Catalytic performance of catalysts precipitated at different temperatures
reaction conditions:360 ℃,10.0 MPa,GHSV=3000 h-1,H2/CO=2
从表4可以看出,CLZ-30催化剂上CO转化率为45.70%,随着沉淀温度的升高而逐渐降低,当沉淀温度为80 ℃时,CO转化率降到26.3%。总醇时空收率(STY)随沉淀温度升高略有降低,总醇选择性随沉淀温度变化不大,约为27%。除醇产物外,碳氢化合物和二氧化碳在产品中也具有高选择性,产物中还含有少量DME。在醇类产品中,甲醇和异丁醇是主要产品,其他醇含量不足10%。甲醇的选择性随着沉淀温度升高而增加,并且在CLZ-80催化剂上达到最大值61.6%。相反,异丁醇的选择性随着沉淀温度的升高而降低,并且在CLZ-30催化剂上达到最大值,即38.7%,说明提高沉淀温度后,碳链增长受到抑制,导致C2+醇选择性降低,尤其是异丁醇选择性。
如图3所示,沉淀温度对K-CuLaZrO2催化剂的还原能力影响很大。前人发现,Cu和Zr的相互作用不同会导致不同类型的Cu物种。比较不同样品的H2-TPR谱图,可以得出结论,在较低的沉淀温度下得到的催化剂上CuO物种比较高沉淀温度下的CuO物种容易还原,XRD结果也说明在高温沉淀条件下,CuO颗粒发生聚集长大,还原变得困难,与H2-TPR结果相吻合。在XPS结果中,Cu 2p3/2的电子结合能随着沉淀温度的升高而降低,而Zr 3d5/2的电子结合能则呈现相反的趋势,表明Cu和Zr组分的化学环境在不同的沉淀温度下发生变化。在之前的工作中[21,30]作者发现,CuO和ZrO2之间的强相互作用将导致CuO更容易被还原,当Cu 2p3/2和Zr 3d5/2分别达到最高值和最低值时,CuO和ZrO2之间的相互作用最强。由表3结果可见,随着沉淀温度的升高,CuO和ZrO2之间的相互作用逐渐变弱。
众所周知,在Cu/ZrO2基催化剂上有两个活性中心参与CO2/CO加氢催化过程[38,39]。一个是Cu组分,另一个是所谓的“载体”ZrO2。Cu可用于吸附H2和CO,并通过溢流效应向ZrO2提供原子氢和CO,最后在ZrO2上形成低碳醇。因此,CuO和ZrO2之间的强相互作用有利于C2+醇的形成。基于XRD和H2-TPR以及XPS结果,CuO和ZrO2在室温下均匀分散,相互作用最强。同时,由于两者分散较好,出现了更多的Cu-Zr界面。但是,随着沉淀温度的升高,CuO和ZrO2之间的相互作用变弱,Cu-Zr的界面也同时减少。如表4所示,异丁醇的选择性随着沉淀温度升高而逐渐降低。
由图4可知,与所有样品相比,CLZ-30在催化剂表面上具有更多的-OH基团,羟基与表面C1(CHxO)中间体的形成有关。从图5中可以看出,在CLZ-30催化剂上形成更多的C1中间体(羧酸盐),而这些物种是形成异丁醇的活性C1中间体[40],为此,在CLZ-30催化剂上具有较高的异丁醇选择性(38.7%)。
3 结 论
沉淀温度显著影响着K-CuLaZrO2催化剂的结构、还原性、分散性以及表面CO吸附性能。XRD结果表明,在较低沉淀温度下,CuO和ZrO2相互分散较好,形成了较好的固溶体,随着沉淀温度的升高,CuO和ZrO2的粒径逐渐增大,两者分散性变差。H2-TPR表明,CuO物种在最低的沉淀温度下容易还原,提高沉淀温度以后,CuO和ZrO2相互减弱,CuO较难还原。XPS进一步证实,CuO和ZrO2之间的相互作用随着沉淀温度的升高而减弱。在FT-IR结果中,CLZ-30催化剂表面具有更多的OH基团,并且在CO吸附后形成了大量的C1中间体,提高了表面C1物种覆盖度,促进了碳链增长,明显提高了异丁醇选择性,在CLZ-30催化剂上,异丁醇选择性达到了38.7%。
