姜黄素对类风湿关节炎破骨细胞分化中核因子κB受体活化因子基因及蛋白表达的影响
2019-10-09徐子涵蔡佳宇李婧商玮赵智明蔡辉
徐子涵,蔡佳宇,李婧,商玮,赵智明,蔡辉
骨破坏是类风湿关节炎(rheumatoid arthritis,RA)主要的病理特征之一,往往导致进行性关节损伤和关节功能减退[1]。破骨细胞(osteoclast,OC)的活化是导致RA早期骨丢失的主要机制[2],RA病人全身骨丢失的加重与OC活性增加密不可分[3]。核因子κB受体活化因子(receptor activator for nuclear factor-κB,RANK)是破骨细胞前体细胞(osteoclast precursor cell,OPC)或成熟OC表面的关键跨膜分子,被其配体(RANK ligand,RANKL)激活,导致OC分化过程中特异性基因的表达以及成熟OC骨吸收功能的活化[4-6]。姜黄素(Curcumin)是中药姜黄的主要药效成分,具有抗肿瘤、抗氧化、抗血管生成等多方面药理作用[7]。Chandran等[8]对活动性RA病人进行的临床研究已证实了姜黄素用药的安全性和有效性。本课题组前期在动物实验中发现,姜黄素提高佐剂性关节炎大鼠骨密度水平是通过调节RANKL/OPG(骨保护素)比值实现的[9]。本研究通过建立RA病人OC体外培养体系,探究姜黄素对RA病人OC分化中RANK基因和蛋白表达的影响及其可能机制,为姜黄素应用于RA骨破坏的防治提供依据。

图1 姜黄素对类风湿关节炎病人破骨细胞分化的影响(TRAP染色×200):A为空白对照组;B、C、D分别为姜黄素2.5 μmol/L组、5 μmol/L组、10 μmol/L组
1 资料与方法
1.1一般资料病例为2015年1—12月在东部战区总医院门诊或住院治疗的RA病人12例,年龄(42.3±14.4)岁,符合2010年RA分类标准[10],均处于疾病活动期。排除肝肾功能不全者,患有内分泌系统疾病及肿瘤性疾病者,长期服用抗凝剂、性激素类药物及调节骨代谢药物者。受试者均签署知情同意书,本研究符合《世界医学协会赫尔辛基宣言》相关要求。
1.2材料胎牛血清购于杭州四季青生物工程材料有限公司,RANKL、巨噬细胞集落刺激因子(macrophage colony-stimulating factor,M-CSF)购于美国Pepro Tech公司,人淋巴细胞分离液购于美国Sigma公司,α-MEM培养基购于美国Gibco公司,抗酒石酸酸性磷酸酶(tartrate-resistant acid phosphatase,TRAP)染色试剂盒购于南京建成科技有限公司,实时荧光定量聚合酶链式反应(Real-time PCR)(Master Mix SYBR Green)试剂盒购于日本TOYOBO公司,RANK抗体购于Cell Signaling Technology公司。
1.3方法(1)建立外周血OC培养体系。采集RA病人外周血10 mL,密度梯度离心法分离外周血单个 核 细 胞(peripheral blood mononuclear cell,PBMC),接种于培养皿中(2×106/cm2),培养箱(37℃,5%二氧化碳)内孵育2~3 h获得贴壁细胞,接种于24孔板中(2×105/cm2),用α-MEM培养基配置细胞培养液(100 ng/mL RANKL、50 ng/mL M-CSF及20%胎牛血清),2~3 d换液1次[11]。
(2)姜黄素细胞毒性检测。于96孔板中加入5×105/mL的单核细胞悬液(每孔100 μL),放置于培养箱中24 h,向培养板中加入含药培养基(0、2.5、5、10 μmol/L),每组3个复孔,置于培养箱中孵育24 h、48 h和72 h后,加入CCK-8溶液10 μL,孵育4 h,设空白孔(只含有培养基和CCK-8溶液),对照孔(含有细胞、培养基和CCK-8溶液)。用酶标仪于450 nm波长处测吸光度OD值,进行细胞存活率计算。参照下列公式:细胞存活率(%)=[(含药组OD值-空白孔OD值)/(对照孔OD值-空白孔OD值)]×100%。
(3)分组与给药。设4组:空白对照组(含100 ng/mL RANKL、50 ng/mL M-CSF的α-MEM培养基);姜黄素2.5 μmol/L组、姜黄素5 μmol/L组和姜黄素10 μmol/L组为在空白对照组的培养条件下再分别加入2.5、5和10 μmol/L姜黄素溶液。每组设3个复孔。
(4)TRAP染色并计数。2~3 d换液并于光镜下观察细胞形态,直至见多核巨细胞形成后进行TRAP染色。参照说明书配制底物反应液,置于37℃水浴箱中10 min;随后将细胞固定,加入底物反应液置于培养箱中1 h,随后用苏木精复染2~3 min。染色阳性的体征为细胞胞质呈深红色、胞核呈蓝紫色。将TRAP染色阳性的多核巨细胞(细胞核≥3个)认定为OC。采用双盲法计数阳性细胞,每孔随机取10个视野(×200)计数OC个数,重复计数3次,取均值。
(5)Real-time PCR检测各组细胞RANK基因的表达。细胞培养至14 d,用TRIZOL试剂提取细胞总RNA,将RNA逆转录为cDNA,对cDNA样本进行Real-time PCR分析,检测RANK基因mRNA的表达。反应体系10 μL,cDNA模板(稀释10倍)1 μL,正、反向引物各1 μL,0.1%DEPC水7 μL。Primer 5软件设计引物(见表1),所有引物由南京金斯瑞科技有限公司合成,以甘油醛-3-磷酸脱氢酶(GAPDH)作为内参基因,实验重复5次,目的基因的相对表达值用2-ΔΔCT公式[12]进行标准化。

表1 PCR引物序列
(6)蛋白质印迹法(Western Blot)检测各组细胞RANK蛋白的表达。用RIPA提取细胞总蛋白,并进行蛋白定量(BCA法),煮沸变性5 min,上样后经10%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)分离,转移至聚偏二氟乙烯膜(PVDF膜),5%脱脂奶粉封闭2 h,加入RANK一抗4℃孵育过夜,加入二抗,室温孵育2 h,曝光显影,计算各条带的灰度值,以β-肌动蛋白(β-actin)为内参蛋白,结果以RANK与β-actin吸光度比值来表示。
1.4统计学方法采用SPSS 22.0软件进行统计分析。观测资料主要为计量资料,以±s表示,多组间比较采用单因素方差分析+多重比较LSD-t检验。P<0.05表示差异有统计学意义。
2 结果
2.1姜黄素对细胞存活率的影响CCK-8检测结果显示,培养24 h姜黄素2.5 μmol/L组、姜黄素5 μmol/L组和姜黄素10 μmol/L组细胞存活率(%)分别为(99.28±4.03)、(98.91±2.80)、(99.54±4.50),与空白对照组(100.00±5.31)相比差异无统计学意义(P>0.05);培养48 h姜黄素各浓度组细胞存活率(%)分别为(97.90±1.71)、(96.57±4.01)、(95.50±4.33),与空白对照组(100.00±8.85)相比差异无统计学意义(P>0.05);培养72 h姜黄素各浓度组细胞存活率(%)分别为(93.94±8.10)、(97.61±8.23)、(92.49±8.65),与空白对照组(100.00±2.28)相比差异无统计学意义(P>0.05)。
2.2姜黄素对RA病人OC分化的影响于200×光镜下观察,空白对照组细胞形态均一、分布均匀、轮廓清晰,有3~5个以上细胞核,符合OC的基本特征,见图1A。经不同浓度姜黄素干预后,视野内多核细胞数量明显减少,形态欠规则,大部分为未分化成熟的细胞,见图1B、1C、1D。
姜黄素2.5 μmol/L组、姜黄素5 μmol/L组和姜黄素10 μmol/L组TRAP阳性细胞数(个/10个视野)分别为(103.00±4.36)、(91.00±7.81)和(67.33±4.16),与空白对照组(166.00±11.53)相比均明显减少(P<0.05),说明姜黄素对RA病人OC分化具有抑制作用。见图2。

图2 姜黄素对类风湿关节炎病人破骨细胞分化的影响
2.3姜黄素对各组细胞RANK基因表达的影响采用Real-time PCR法对各组细胞中RANK mRNA水平进行检测。姜黄素2.5 μmol/L组、姜黄素5 μmol/L组和姜黄素10 μmol/L组细胞中RANK mRNA的相对表达量分别为(1.03±0.12)、(0.48±0.10)和(0.26±0.04),与空白对照组(1.44±0.16)相比均明显降低,差异有统计学意义(P<0.05),说明姜黄素能抑制RA病人OC中RANK mRNA的表达水平。见图3。

图3 姜黄素对各组细胞核因子κB受体活化因子(RANK)基因表达的影响
2.4姜黄素对各组细胞RANK蛋白表达的影响蛋白质印迹法结果显示,与空白对照组相比,姜黄素2.5 μmol/L 组、姜黄素 5 μmol/L组和姜黄素 10 μmol/L组细胞中RANK蛋白表达水平明显降低,差异有统计学意义(P<0.05)。可见姜黄素具有抑制RA病人OC中RANK蛋白表达水平的作用。见表2,图4。
表2 各组细胞RANK蛋白表达水平/±s

表2 各组细胞RANK蛋白表达水平/±s
注:与空白对照组比较,aP<0.05
组别空白对照组姜黄素2.5 μmol/L组姜黄素5 μmol/L组姜黄素10 μmol/L组F值P值次数5 5 5 5 RANK/β-actin 0.68±0.11 0.46±0.09a 0.36±0.08a 0.25±0.07a 21.278 0.000
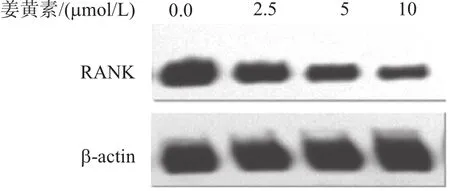
图4 姜黄素给药与否的各组细胞核因子κB受体活化因子(RANK)蛋白电泳图
3 讨论
姜黄素是从中药姜黄中获得的四萜类化合物。《本草纲目》记载姜黄“治风痹臂痛”,《医林纂要》记载姜黄“治四肢风寒湿痹”。RA是慢性炎症性疾病,可造成关节损伤和骨质破坏,属中医“痹证”范畴。历代诸多医家将姜黄用于风寒湿痹,其中的代表方剂是五痹汤,以姜黄为君药,与羌活、白术、防己、甘草同用,通痹止痛。现代药理研究显示,姜黄素具有抗炎、抗氧化和抗癌活性[7]。本课题组前期研究表明,姜黄素能调节RANKL/OPG比值,提高佐剂性关节炎大鼠骨密度水平[9]。本研究进一步探索姜黄素在治疗RA骨破坏中的作用及其可能机制。
OC是主要的骨吸收细胞,来源于骨髓造血干细胞分化而来的单核-巨噬细胞系统,进入外周血后循环在单核细胞层。在多种因素的作用下,这些细胞特定向骨吸收区移动,黏附于骨表面由OPC融合成OC发挥骨吸收功能。OC的异常增生与活化在RA骨破坏中发挥重要作用[2]。OC是终末分化细胞,不能传代且存活时间短,难以分离获得[13]。外周血单核细胞诱导培养法由Fujikawa等[14]首次提出并实验成功,是常用的OC培养方法之一,适用于人体OC研究,可获得大量OC。本研究采用密度梯度离心法分离获得RA病人PBMC,贴壁培养后获得单核细胞,经RANKL和M-CSF诱导分化为OC。CCK-8检测姜黄素的细胞毒性,发现姜黄素2.5、5和10 μmol/L的浓度对细胞存活率无明显影响,故设定为本实验姜黄素干预浓度。TRAP是OC分化和骨吸收功能的特异性酶,是OC分化的标志物,与骨吸收功能密切相关。获得的细胞进行TRAP染色,通过TRAP染色阳性细胞计数来评估OC分化情况。结果显示,经2.5、5和10 μmol/L 姜黄素干预后,OC的数量较对照组明显减少,提示姜黄素能有效地抑制RA病人OC分化。
在OPC向OC分化的过程中,RANKL-RANKOPG系统发挥关键作用[15-16]。RANK是位于OPC及OC表面的I型跨膜受体蛋白,是RANKL信号的唯一靶向受体,在细胞表面与RANKL结合调节OC的分化与功能,促使OC相关基因如TRAP、组织蛋白酶K、基质金属蛋白酶-9等的表达[17-18]。本研究分别从基因和蛋白层面表明姜黄素抑制RA病人OC分化过程中关键信号分子RANK mRNA和蛋白的表达,说明姜黄素可能是通过降低OPC表面RANK的表达,使其与RANKL结合减少,从而减弱RANKL信号传导及下游转录因子的活化,抑制OC的分化成熟及功能。
综上所述,姜黄素对RA病人OC分化和成熟具有抑制作用,其机制可能与下调RANK基因和相关蛋白的表达有关。本研究初步探索了姜黄素抑制RA病人OC分化的可能机制,为开发姜黄素相关药物应用于RA骨破坏的治疗提供了实验依据。(本文图1见插图10-1)
