奥美沙坦酯片的处方筛选与工艺制备
2019-09-25柏丹丹
柏丹丹
(南京海融医药科技股份有限公司,江苏 南京 211100)
奥美沙坦酯片于1995年奥美沙坦酯由日本第一三共株式会社研制成功,随后2002年5月以商品名Benicar 在美国上市,上市规格有:5 mg、20 mg、40 mg。用于治疗高血压,国内已经有多家仿制药上市。用于血管紧张素受体阻断剂一类的降压药。
奥美沙坦酯片在血管紧张素转化酶作用下,由血管紧张素I转化成血管紧张素II。血管紧张素II是肾素-血管紧张素系统的主要升压因子,其作用包括收缩血管、促进醛固酮的合成和释放、刺激心脏以及促进肾脏对钠的重吸收。在许多组织中也发现了AT2受体,但这种受体与心血管稳态无关。奥美沙坦酯片对其有超过12,500倍的亲和力。 AT1受体比AT2受体。
用ACE抑制剂阻断肾素 - 血管紧张素系统,其抑制血管紧张素II的生物合成,适用于抗高血压的常用药物之一。 ACE抑制剂也抑制缓激肽的降解,这一过程也是由血管紧张素转化酶的催化。这种差异是否具有临床相关性尚不清楚。
本次研究主要探讨奥美沙坦酯片的处方筛选通过正交试验L9(34)正交设计成三因素四水平的正交试验,筛选出最优处方;工艺制备中优化通过pH值6.8磷酸盐介质中的体外溶出考察来确定工艺的可行性。通过上述处方筛选与工艺制备的优化最终制剂成品各项指标符合《中国药典》2015版的质量要求。
1 仪器与试剂
1.1 试剂
奥美沙坦酯原料药(外购),一水乳糖(厂家:德国Meggle pharma 公司)、低取代羟丙基纤维素(厂家:日本信越药用辅料公司)、羟丙基纤维素(日本曹达)、微晶纤维素(深圳市优惠普药品股份有限公司)、硬脂酸镁(深圳市优惠普药品股份有限公司)
1.2 仪器
单冲旋转压片机(型号:DP30A型单冲压片机,上海天凡制药机械厂)、智能崩解测试仪(型号:ZB-1E智能崩解仪,天津市天大天发科技有限公司)、溶出仪(型号:ZRS-8GD溶出试验仪,天津市天大天发科技有限公司)、可见紫外分光光度计(型号:TU-1810紫外可见分光光度计,北京普析通用仪器有限公司)、脆碎度测定仪(型号:FT-2000AE,天津市天大天发科技股份有限公司)、湿法混合制粒机(G6,深圳市信宜特科技有限公司)水分测定仪(型号:MA35,Sartotius赛多利斯科学仪器有限公司)。
2 研究方法
查询 FDA、PMDA 上市国家的相关文献发现,奥美沙坦酯为原料药,非活性成分为一水乳糖、低取代羟丙基纤维素、羟丙基纤维素、微晶纤维素、硬脂酸镁等辅料的组成。辅料的比例及组成对该片剂的影响较大,因此本次实验设计将一水乳糖、低取代羟丙基纤维素、羟丙基纤维素、微晶纤维素的用量作为变量,将崩解时限作为观察指标,采用正交试验L9(34)正交设计成三因素四水平的正交试验,根据崩解时间优化处方,具体设计见表1所示。

表1 正交试验设计表
2.1 奥美沙坦酯片的制备
称取奥美沙坦酯和处方量的其他辅料,等量递降顺序混合后过80目筛网后加入湿法制粒机中,以水为粘合剂制软材,搅拌+剪切转速参数分别为10 r/min,时间均为3 min,在40℃烘箱中干燥约1 h,水分控制在≤3%,整粒,加入硬脂酸镁混合均匀,压片,即得。
2.2 崩解时限考察
按照选定制备的普通片3批,每批取6片,置于崩解仪中,按照《中国药典2015》版附录0921崩解时限检查法,37℃纯化水中上下往复振摇,同时进行计时,30 min内应全部崩解。
2.3 溶出度试验
分别取自制奥美沙坦酯素片,按照《中国药典》2015年版的规定,采用第二法对其进行溶出度试验,溶出介质为超声脱气纯化水,转速为50 r/min,分别在5、10、15、30、45、60 min时取出溶出液,0.45 μm水系滤头过滤,使用紫外风光光度法在257 nm下进行含量测定。
2.4 处方验证
按照优选的处方工艺制备奥美沙坦酯片3批,每批取6片,考察崩解时限。
3 结果
3.1 正交试验结果
结果如表2。
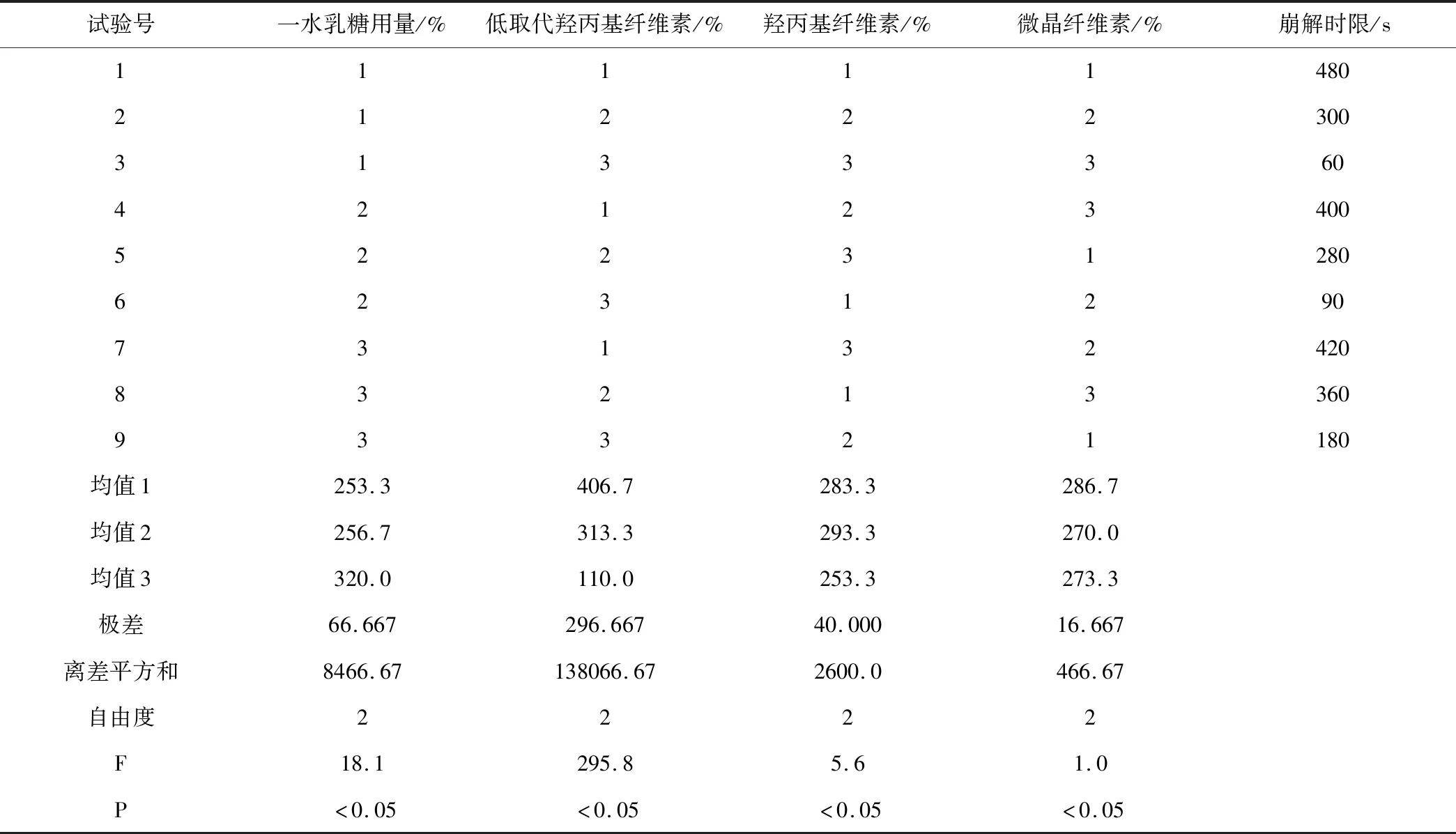
表2 正交试验结果
结果分析:试验时的崩解时限以时间低者为最好,由上述实验结果得出,一水乳糖、低取代羟丙基纤维素、羟丙基纤维素、微晶纤维素的用量对崩解时限影响由大到小依次分别为低取代羟丙基纤维素>一水乳糖>羟丙基纤维素>微晶纤维素。既低取代羟丙基纤维素用量对崩解时限的影响最大,其次是一水乳糖,微晶纤维素对崩解时限的影响最小低。并且四种辅料对奥美沙坦酯片的崩解具有显著影响,根据表2可以知道最佳的处方为A1B3C3D2,即当一水乳糖的用量为70%,低取代羟丙基纤维素用量为8%,羟丙基纤维素用量为10%,微晶纤维素用量为20%时奥美沙坦酯片崩解时限等于3 min,效果较好。
3.2 自研片与参比制剂溶出对比

图1 奥美沙坦酯片自研与参比制剂pH值6.8中的的溶出曲线对比
按照优选的处方工艺,实验室条件下采用湿法工艺制备自制3批样品,分别于5、10、15、30、45、60 min时取溶出液进行HPLC测定,考察在pH值6.8的条件下溶出曲线进行紫外测定,并与参比制剂比较相似性。根据结果如图1所示。
4 讨论
奥美沙坦酯片在血管紧张素转化酶作用下,由血管紧张素I转化成血管紧张素II。
奥美沙坦酯片在从胃肠道吸收时通过酯水解成奥美沙坦而快速且完全地生物活化。绝对生物利用度约为26%。口服给药吸收后,在1~2 h后达到奥美沙坦酯片的血浆浓度峰值。
在体内吸收过程中奥美沙坦酯片进入胃肠道后会水解转化为奥美沙坦,奥美沙坦不会有进一步的代谢吸收。 奥美沙坦酯的总血浆清除率为1.3 L/h,肾清除率为0.6 L/h。 在尿液中回收大约35%至50%的吸收剂量,而其余的通过胆汁排泄。进食后奥美沙坦的生物利用度不会有影响。
奥美沙坦酯片以双相方式消除方式,终末消除半衰期约为13 h。 奥美沙坦酯片在单次口服剂量高达320 mg和多次口服剂量高达80 mg后显示线性药代动力学。 奥美沙坦酯片的稳态水平在3~5天内达到,并且每日一次给药不会发生血浆积聚。
本次研究内容主要是通过研究奥美沙坦酯片的处方筛选及制备工艺的考察,通过研究发现,处方中一水乳糖、低取代羟丙基纤维素、羟丙基纤维素、微晶纤维素的辅料用量对不同处方的奥美沙坦酯片崩解影响较大,因此,本次研究通过正交试验的方法对处方中的一水乳糖、低取代羟丙基纤维素、羟丙基纤维素、微晶纤维素的用量进行优化设计。通过结果分析可知,当一水乳糖的辅料用量为70%,低取代羟丙基纤维素用量为8%,羟丙基纤维素用量为10%,微晶纤维素用量为20%时奥美沙坦酯片崩解时限等于3 min,效果较好。并且在pH值6.8中的溶出曲线也与参比制剂的溶出相似。由此可见,本次研究对奥美沙坦酯片的处方进行优化,各项指标基本达到了《中国药典》2015年版规定质量要求。
