碱性离子液体催化合成查尔酮
2019-09-25马绍红毛银平周慧敏夏慧慧王亚军
马绍红,毛银平,周慧敏,夏慧慧,杨 洋,王亚军
(湖州师范学院 生命科学学院,浙江 湖州 313000)
查尔酮是一种类黄酮化合物,也是一种重要的天然化合物,查尔酮具有很多的药理活性,例如查尔酮具有肝保护的作用[1],查尔酮对肾癌、胰腺癌、宫颈癌、神经细胞癌的增殖都起到治疗作用,可以作为抗癌药物[2]发展。抗疟、抗蛲虫、抗过敏、抗艾滋[3]等药理活性,奥·欧·赫洛威兹研究了一种具有高甜度的查尔酮类化合物可以作为一种低热量的甜味剂[4]。因为查尔酮的共轭效应和它不对称的结构,使其在电子方面的应用非常好,所以是优质的有机非线性光学材料[5],可以作为光计算 、光储存 、激光波长转换材料[6]。在电子领域也可作屏保和液晶显示材料[7]关于查尔酮的用途有更多新的发现,随着各种合成查尔酮的催化剂的不断探索,合成查尔酮的方法也越来越多。
1 实验部分
1.1 仪器和试剂
磁力搅拌器78-1,熔点测定仪WRS-1B,红外光谱仪Nicolet6700,烘箱101A-2,智能恒温磁力搅拌器85-2B及常规合成仪器。
苯乙酮,苯甲醛,95%乙醇,[C4OHMIM]PhCOO,[C4OHMIM]2OAc,[C4OHMIM]2CO3均为市售化学纯试剂。
1.2 实验方法
1.2.1 实验原理

图1 催化原理方程式
苯乙酮和苯甲醛的反应原理是在碱的作用下进行羟醛缩合的反应。本实验是以[C4OHMIM]2CO3为催化剂,探究不同条件对反应的影响。催化原理方程式如图1。
1.2.2 实验步骤
用移液管依次移取1 mmol苯甲醛和1 mmol苯乙酮,加入到100 mL单口烧瓶中充分摇匀混合,然后加入0.25 mmol碱性离子液体催化剂。将冷凝回流装置打开,将温度设置为45℃,将磁力搅拌器放入锅中搅拌并用油浴锅中加热,观察直至反应结束后,加入蒸馏水,再加入10 mL×3乙酸乙酯进行萃取,得到粗产品,取下层水相旋蒸去水,再将碱性离子液体干燥回收,将得到的粗产品用95%的乙醇重结晶,完全析出晶体后再次抽滤,得到查尔酮产物,最后将产物放入烘箱进行干燥,称其重量,计算收率。用熔点测定仪测量熔点。
1.2.3 实验结果与讨论
1.2.3.1 不同离子液体对反应产物收率的影响
用移液管依次移取物质的量比(1∶1.1)1 mmol苯甲醛和1 mmol苯乙酮,加入到100 mL单口烧瓶中,搅拌均勻后,最后加入不同的离子液体([C4OHMIM]2CO3、[C4OHMIM]2OAc、[C4OHMIM]PhCOO),(编号为1,2,3)。之后方法步骤同上。实验结果见表1。

表1 碱性离子液体对产物收率的影响
由表1可以看出,3个不同的碱性离子液体催化剂,在催化合成查尔酮,由于氢氧根本身存在孤对电子,使得离子液体的碱性增强,当反应溶液中碱性离子液体的氢离子一样时,氢氧根离子碱性强弱将会直接影响碱性离子液体的催化活性,碱性越强催化活性越高。综上所述,[C4OHMIM]2CO3可作为本实验最适宜的碱性离子液体催化剂。
1.2.3.2 不同用量对反应产物收率的影响
用移液管依次移取物质的量比(1∶1.1)1 mmol苯甲醛和1 mmol苯乙酮,加入到100 mL单口烧瓶中,搅拌均勻后,最后加入不同用量的离子液体[C4OHMIM]2CO3分别(0.2,0.25,0.3)mmol,(编号为1,2,3)。之后方法步骤同上。实验结果见表2。

表2 离子液体[C4OHMIM]2CO3的用量对产物收率的影响
由表2可知,让其他条件保持不变,只增加[C4OHMIM]2CO3的用量,收率是提高的,剂量增加使活性分子增多,反应物之间的接触面积增大,使反应加快,催化剂用量在0.25是产物收率最高,继续增加催化剂用量时,收率在逐渐降低,可能是剂量增加,稀释了反应中其他反应组分的用量。因此,综上所述,我们选择了0.25 mmol为本次实验的最适用量。
1.2.3.3 离子液体在不同温度下对于反应产物收率的影响
用移液管依次移取物质的量比(1∶1.1)1 mmol苯甲醛和1 mmol苯乙酮,加入到100 mL单口烧瓶中,搅拌均勻后,最后加入离子液体[C4OHMIM]2CO3,(反应温度分别为45℃,50℃,55℃),(编号为1,2,3)。之后方法步骤同上。实验结果见表3。

表3 [C4OHMIM]2CO3的温度对产物收率的影响
由表3可知,其他条件固定时,提高反应温度,收率逐渐增加,苯乙酮和苯甲醛为羟醛缩合反应,在反应过程中催化需要吸收热量,当温度逐渐升高时,反应会正向进行,所以收率提高。当温度过高时,引起了反应的副反应,可能发生了相互间的Clasisen-Schmidt 反应,从而副产物增多,不利于分离。考虑成本选择反应温度为50℃。
1.2.3.4 验证实验
根据单因素实验,最终会得出在每个单因素实验中,有一个最适条件,根据最适条件进行实验,重复多次。实验结果见表4。

表4 验证实验结果收率
本实验查尔酮合成的最佳条件为:选择苯甲醛和苯乙酮物质的量比为(1∶1.1)碱性离子液体0.25 mmol[C4OHMIM]2CO3作为本次实验的催化剂,反应时间为45 min。在这些条件下,反应物得到很高的利用率,得到的产物多,收率高,为查尔酮的绿色合成找到了更优的条件,极大的提高了产率和纯度。
2 产物鉴定
2.1 产物物理性状鉴定
本实验产物为查尔酮,外观呈橙黄色晶体。物理性质观察与文献[8]说明相同。
2.2 产物熔点测定结果
将进行单因素实验得来的结果进行优化实验,对其优化实验结果进行熔点测定,来帮助判断该产物是否为查尔酮。所测熔点与文献[8]所报道的查尔酮熔点57~58℃基本一致,初步判断该产物为查尔酮,测得产物的熔点如表5所示。

表5 产物的熔点
2.3 产物的红外吸收光谱
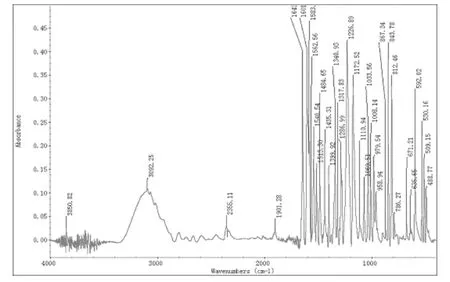
图2 产物的红外光谱图
将制备得来的产物进行红外分析,根据分析结果来判断该产物是否为查尔酮。产物的红外光谱图如图2。
根据图2产物的红外光谱图(IR)分析可知,1650 cm-1为查尔酮结构中碳碳双键的振动峰,1602 cm-1为查尔酮结构中的碳碳单键,1484 cm-1,1435 cm-1吸收峰为苯环上的碳氢的振动峰。综上,该红外吸收光谱数据基本可确定产物的各官能团,与文献报道[9-10]一致,说明该产物为查尔酮。
3 结论
本文通过单因素实验和验证实验优化了查尔酮的合成工艺条件。考察了不同的碱性离子液体、不同用量、不同反应时间和不同的温度等因素对反应收率的影响。本实验的最佳工艺条件为:[C4OHMIM]2CO3碱性离子液体作为实验催化剂,碱性离子液体用量为0.25 mmol,反应温度为50℃,反应时间为45 min。该条件下,收率高,纯度也高。
