便秘通对癌症患者阿片类药物相关便秘的疗效及安全性研究
2019-09-20陈泽刚赵春妮张林松
陈泽刚,赵春妮,张林松
有33%~64%的癌症患者会出现疼痛,并且需要应用阿片类药物治疗[1]。阿片类药物的止痛疗效确切[2],但是,在使用阿片类镇痛药的癌症患者中有60%~90%会出现阿片类药物引起的便秘(OIC)[3-5]。OIC的出现会引起癌症患者对阿片类镇痛药的依从性下降,从而影响阿片类药物对患者癌痛的有效治疗[6-7]。OIC的发生机制主要是由于外源性阿片类药物与位于胃肠道黏膜下的神经元和肌间神经丛中的外周μ-阿片受体结合[8],改变了肠道神经系统的传出功能,减慢肠道蠕动,减少肠腔内液体的分泌,促进胃肠道液体的吸收,从而出现便秘[9]。临床上常常通过增加运动、摄入高纤维食物、服用泻药等方法来缓解便秘的症状[10-11]。但是,这些基于症状的治疗,效果不是很令人满意[12],许多患者寻求中医,特别是中草药的帮助。根据中医理论,便秘以潜在的病因为依据大致分为实证和虚证。实证的特点是热积或气滞,虚证主要与阴血亏虚、阳气不足引起大便干结、肠道推动无力有关[13]。中医内科学将便秘分为实秘和虚秘,实秘是肠胃积热、气机郁滞证,虚秘为气虚便秘、血虚便秘、阴虚便秘证[14],应根据不同证型选择不同的治疗方法和方药。针对癌症患者使用阿片类药物引起的便秘,因为这些患者的体质与仅患便秘的一般患者不同,故其辨证和治法也不相同。便秘通是本课题组在中医经典古方“枳术丸”基础之上,结合癌症患者OIC表现出来的中医证型,经过临证加减炼制而成,为方便患者服用制备而成的丸剂,在治疗癌症患者OIC的过程中发现其疗效确切。但对于本药疗效及安全性缺乏循证医学证据,故本研究通过临床随机试验与安慰剂对照,观察2周,以评估便秘通治疗癌症患者OIC的疗效和安全性,并通过12周的延伸研究进一步评估安全性结果,以期进一步指导临床实践。
1 对象与方法
1.1 研究对象 以2017年1月—2018年2月西南医科大学附属中医医院肿瘤科129例OIC患者为研究对象。纳入标准:(1)年龄>18岁;(2)服用稳定剂量的阿片类药物2周以上;(3)符合癌症患者OIC的诊断标准:前2周内出现5次或更少的自主排便(不是由挽救性泻药引起的排便)和/或在所有排便次数中超过25%经历过排便费力、大便干结和/或硬便的临床表现[15-16];(4)不直接引起便秘和/或腹泻的癌症类型;(5)预期在研究期间(98 d内)保持病情稳定。排除标准:(1)连续7 d没有排便(为了确保入组患者具有一些功能性排便并且没有增加肠穿孔的风险);(2)从未服用过泻药来治疗OIC;(3)在第1剂研究药物之前和之后24 h之内使用过其他泻药;(4)接受可能影响胃肠功能化疗:在筛选前14 d开始新的化疗方案或在研究期间调整化疗方案;(5)有其他潜在影响肠道转运的因素。脱落标准:(1)进入试验后,未坚持按规定时间、剂量服药;(2)治疗过程中,因病情需要使用挽救性泻药;(3)治疗过程中,自行退出或拒绝治疗。本研究经西南医科大学附属中医医院医学伦理审查委员会审批通过,患者均已签署书面知情同意书。
1.2 研究制剂 便秘通处方根据《中国药典》2015年版所规定的标准选择药材,由西南医科大学附属中医医院制剂室按生大黄6 g、枳实15 g、茯苓15 g、生白术15 g、广木香15 g、砂仁9 g组成1剂,通过工艺提炼制成水丸,以10 g为1小袋进行分装,以方便患者使用。安慰剂以淀粉为原料,外观、大小、颜色、剂型、重量、味道、气味等尽可能与便秘通相同。
1.3 研究方法 在随机对照试验中初期选取138例患者,其样本量是根据样本量计算公式计算得出,即每组需要69例患者,组间主要检测终点的差异为20.0%,把握度为90%,假设全分析集(FAS)的排除比例为1%。但因为受病例资料要求限制,最终挑选合格者129例进入研究。使用中央随机化系统和最小化随机算法,将患者分为便秘通组65例和安慰剂组64例。所有研究者和患者对治疗药物的分配不知情,研究药物在外观、标签、包装上难以区分。负责随机分配和治疗分配的人将随机编码放在密闭信封里,只有在病例报告表格的所有数据都被锁定后才会被公开。患者按分组接受便秘通或安慰剂治疗,用法:每日9:00随机给予口服1次便秘通10 g或安慰剂10 g治疗。随机对照研究采用随机、双盲、平行组、安慰剂对照,以评估OIC癌症患者使用便秘通2周后的有效性和安全性。因为考虑到在癌症患者进行长期、安慰剂对照、双盲研究存在道德和技术因素影响,所以还进行了一个开放标签、单臂、为期12周的延伸研究,主要目的用于进一步评估OIC癌症患者服用便秘通的安全性。随机对照试验完成的患者自愿选择进入为期12周的延伸研究,接受便秘通治疗12周,没有继续治疗的患者均随后观察4周。在延伸研究阶段,如果出现不良反应降低了患者的生活质量,则允许口服便秘通剂量减少至5 g或暂时终止治疗,共有89例患者加入延伸研究。2017-01-01至2018-01-31完成随机对照研究,2017-01-15至2018-04-30完成延伸研究。
1.4 疗效评估 有效性的主要研究终点是2周治疗期间出现自发排粪(SBM)反应者的比例。1例SBM反应者是指1周达到3次及以上SBM次数的患者,或者是与基线水平对比每周增加1次及以上SBM[17]。基线水平是指在随机分配前2周内平均每周的SBM次数。随机对照试验的次要研究终点包括每周SBM频率、完全自发排便(CSBM)及不费力SBM。
1.5 安全性评估 两项研究中的安全性评估包括治疗出现的不良反应(TEAEs)、阿片类戒断量表(COWS)评分及评估疼痛强度的11点数字评定量表(NRS)评分。应用标准的国际医学用语词典MedDRA(版本16.1)对TEAEs进行分类[18-19]。采用COWS评分法对阿片类药物戒断症状或体征进行评估。COWS评估阿片类药物戒断的11种常见体征或症状,得分较低表示严重程度较轻的症状。COWS总分≥5分考虑有临床意义,COWS评分与严重程度对应情况:5~12分为轻度戒断不良反应,13~24分为中度戒断不良反应,25~36分为中重度戒断不良反应,>36分为严重戒断不良反应[20]。在随机对照研究中,COWS评分分别在基线时(在第1 d给药前)、第1次给药后1、8、15 d。在延伸研究中,COWS评分在第1 d前(随机对照研究治疗的最后1 d)、给药后第1、15、29、57、85 d进行。在随机对照研究中每天采用NRS评估患者疼痛的严重程度。疼痛评分与疼痛强度对应情况:0分为无痛,1~3分为轻度疼痛,4~6分为中度疼痛,7~9分为重度疼痛,10分为剧烈疼痛[21]。
1.6 统计学方法 采用SPSS 21.0统计软件进行数据分析。呈正态分布的计量资料以(±s)表示,两组间比较采用t检验,多组间比较采用方差分析;呈非正态分布的计量资料以中位数(四分位数间距)〔M(QR)〕表示,多组间比较采用Kruskal-Wallis H检验;计数资料以相对数表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 便秘通组、安慰剂组、延伸研究组患者人口统计学和基线资料比较 便秘通组、安慰剂组、延伸研究组患者的人口统计学和基线资料比较,差异无统计学意义(P>0.05,见表1)。

表1 便秘通组、安慰剂组、延伸研究组患者人口统计学和基线资料比较Table 1 Comparison of demographic information and baseline data between patients in the Bianmitong group,placebo group,and extended group
2.2 疗效
2.2.1 主要研究终点 便秘通组与安慰剂组出现SBM反应者的比例分别为72.3%(47/65)和34.4%(22/64),两组出现SBM反应者的比例比较,差异有统计学意义(χ2=18.651,P<0.001)。
2.2.2 次要研究终点 便秘通组和安慰剂组基线SBMs比较,差异无统计学意义(P>0.05);便秘通组SBMs、CSBMs、不费力SBMs高于安慰剂组,差异有统计学意义(P<0.05,见表2)。
2.3 安全性
2.3.1 临床随机对照研究和延伸研究TEAEs发生情况 安慰剂组与便秘通组TEAEs和退出研究发生情况比较,差异无统计学意义(P>0.05);便秘通组腹泻发生率高于安慰剂组,差异有统计学意义(P<0.05,见表3)。延伸组TEAEs、退出研究、腹泻发生率分别为28.0%(25/89)、9.0%(8/89)、15.7%(14/89)。
2.3.2 对阿片类药物作用的影响 便秘通组和安慰剂组基线、第1次给药后1、8、15 d COWS评分比较,差异无统计学意义(P>0.05,见表4)。基线、给药前1 d、给药后1、8、29、57、85 d延伸组COWS评分分别为(1.51±0.57)(1.67±0.74)(1.58±0.56)(1.58±0.67)(1.58±0.58)(1.63±0.55)(1.60±0.52)分。便秘通组和安慰剂组基线、给药后1~14 d NRS评分比较,差异均无统计学意义(P>0.05,见表5)。
表2 安慰剂组和便秘通组次要研究终点比较(±s,次/周)Table 2 Comparison of study endpoint between the placebo group and Bianmitong group

表2 安慰剂组和便秘通组次要研究终点比较(±s,次/周)Table 2 Comparison of study endpoint between the placebo group and Bianmitong group
注:CSBM=完全自发排便
组别 例数 基线SBMs SBMs CSBMs 不费力SBMs安慰剂组 64 1.09±0.841.40±0.980.77±0.71 1.10±0.83便秘通组 65 0.95±0.744.55±2.592.75±2.18 2.69±2.45 t值 -1.005 9.140 6.946 7.868 P值 0.317 <0.001 <0.001 0.001
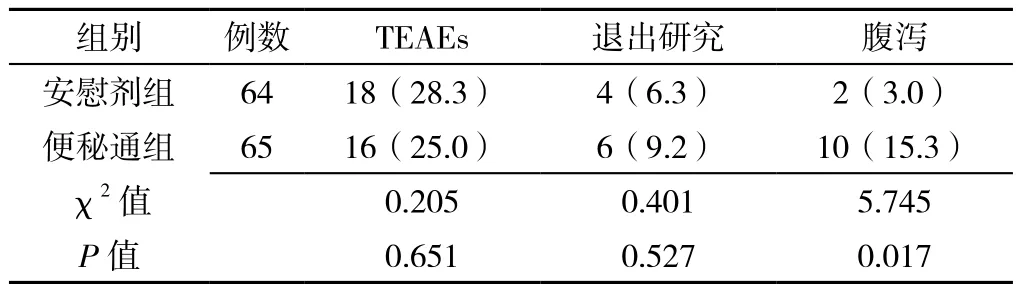
表3 安慰剂组和便秘通组TEAEs发生情况比较〔n(%)〕Table 3 Comparison of TEAEs in the placebo group and Bianmitong group
表4 随机对照研究中阿片类戒断量表(COWS)评分(±s,分)Table 4 Clinical Opiate Withdrawal Scale(COWS) scores in the randomized controlled trial

表4 随机对照研究中阿片类戒断量表(COWS)评分(±s,分)Table 4 Clinical Opiate Withdrawal Scale(COWS) scores in the randomized controlled trial
组别 例数 基线 给药后1 d 给药后8 d给药后15 d安慰剂组 64 1.56±0.53 1.56±0.56 1.58±0.53 1.58±0.56便秘通组 65 1.55±0.56 1.55±0.53 1.58±0.56 1.58±0.53 t值 0.104 0.104 <0.001 <0.001 P值 0.917 0.917 0.999 0.999
表5 随机对照研究中每日评估疼痛评分量表(NRS)的评分(±s,分)Table 5 Daily assessment of Numeric Rating Scale(NRS) scores in the randomized controlled trial

表5 随机对照研究中每日评估疼痛评分量表(NRS)的评分(±s,分)Table 5 Daily assessment of Numeric Rating Scale(NRS) scores in the randomized controlled trial
组别 例数 基线 给药后1 d 给药后2 d 给药后3 d 给药后4 d 给药后5 d 给药后6 d安慰剂组 64 3.67±0.91 3.58±0.60 3.42±0.91 3.67±0.86 3.58±0.92 3.61±1.02 3.53±0.99便秘通组 65 3.44±1.05 3.50±0.96 3.48±0.87 3.42±0.91 3.41±0.97 3.27±0.99 3.39±0.95 t值 1.329 0.567 0.383 1.603 1.021 1.921 0.820 P值 0.186 0.572 0.703 0.111 0.309 0.059 0.414组别 给药后7 d 给药后8 d 给药后9 d 给药后10 d 给药后11 d 给药后12 d 给药后13 d 给药后14 d安慰剂组 3.33±0.75 3.72±0.88 3.59±0.90 3.61±0.92 3.48±0.96 3.55±0.89 3.66±0.98 3.63±0.88便秘通组 3.30±0.99 3.39±1.05 3.42±1.07 3.50±1.01 3.42±1.07 3.45±0.96 3.48±1.02 3.34±1.03 t值 0.194 1.933 0.976 0.646 0.335 0.613 1.022 1.718 P值 0.847 0.055 0.331 0.519 0.738 0.541 0.309 0.088
3 讨论
本研究包括随机、双盲、平行组、安慰剂对照的随机对照研究和单臂、开放标签、延长12周的延伸研究,研究结果显示,随机对照研究中便秘通组SBM反应发生率较安慰剂组高,便秘通组每周SBM频率、CSBMs、不费力SBMs发生率高于安慰剂组。因此,癌痛患者出现OIC后应用便秘通,疗效确切。
在随机对照研究中,安慰剂组与便秘通组TEAEs发生率均较低,分别为28.3%和25.0%,无明显差别,便秘通组与延伸组TEAEs发生率分别为25.0%和28.0%。通过观察癌痛患者出现OIC后接受便秘通治疗,即使治疗持续时间(2周和14周)不同,其TEAEs发生率亦无明显差异,这一点可用来解释便秘通治疗癌症患者OIC的耐受性及安全性,即不会因为应用便秘通的时间延长而产生更多不良反应。此外,便秘通并没有妨碍阿片类药物的镇痛作用和促进阿片类戒断综合征。
根据中医病因病机分析,临床上使用阿片类药物患者,多属癌症中晚期,大部分患者经过手术、放化疗、分子靶向及免疫治疗,机体正气不足。故以虚为本,病程中可伴有气滞、气虚、郁热、燥结、津亏、血虚、阴虚、阳虚等因素。因此,OIC的治疗主要从虚证和实证辨证论治[13-14]。便秘通组方中生白术长于健脾通便,久病必虚,气虚则大便推动无力,故用生白术;方中枳实破气消积、化痰消痞,为行气通便的主药,临床中行气作用强,故为行气通便之良药;与生白术配伍补中有行,使脾气健运,腑气调通,二者共为君药;生大黄泻下攻积、清热泻火、凉血解毒、逐瘀通经,方中配伍少量生大黄,一则泻下通便,二则解毒化瘀,三则不伤正,故为臣药;木香行气止痛、健脾消食,砂仁化湿行气、温中止呕,两药合用增强行气化滞、理气和胃之功效,与白术、茯苓配伍尤适用于脾胃气虚;茯苓利水渗湿,补利兼优;综合全方,益气健脾,行气攻下,攻补兼施。中医通便,有“补气”“理气”“攻下”“润下”等治法,而本方兼具。通过随机对照研究发现,便秘通与安慰剂对比,其发生TEAEs的病例少2例,且TEAEs的类别以胃肠道反应居多,可能与便秘通在治疗癌症患者OIC的同时,显示出调理胃肠功能、缓解胃肠症状方面的作用有关。另外,便秘通为丸剂,使患者治疗方便,易于接受。
本研究存在一些局限性:(1)主要是基于临床观察发现便秘通对癌症患者OIC的疗效确切,未从机制方面对其进行深入研究和阐述;(2)在研究设计方面包括缺乏多中心大样本病例,癌症类型相对较少,安慰剂对照的双盲治疗期相对较短;(3)评价功效的排便频率仅在2周盲法治疗期间收集,而不是在延伸研究的12周开放标签治疗期间进行等。
作者贡献:陈泽刚、赵春妮负责文章的构思与设计、试验的实施、统计分析、撰写论文,对文章整体负责,监督管理;张林松进行研究的实施与可行性分析、数据收集。
本文无利益冲突。
