2-己基-4-乙酰氧基四氢噻吩顺反立体异构体制备及香气特性
2019-09-16郭安齐
郭安齐
(河南医学高等专科学校,郑州 450003)
呋喃类化合物是一类非常重要的杂环香料,数目繁多,在各种香精配方中具有不可替代的重要作用,如肉香味的代表性化合物2-甲基-3-呋喃硫醇、焦香味的代表性化合物糠硫醇、4-羟基-2,5-二甲基-3(2H)-呋喃酮、2-甲基四氢呋喃-3-酮等[1]。相比之下,噻吩类化合物在香料中的地位则要逊色很多,噻吩类香料的数目和应用都非常有限。结构相似的呋喃类香料和噻吩类香料往往具有完全不同的香气特征,如2-戊基呋喃具有水果香,而2-戊基噻吩则具有煎炸的香味;4-羟基-2,5-二甲基-3(2H)-呋喃酮具有甜香、焦糖香、水果香,而4-羟基-2,5-二甲基-3(2H)-噻吩酮则具有似煎肉的香味[2]。
2-己基-4-乙酰氧基四氢呋喃是一个具有甜香、花香和水果香的香料化合物,是美国FEMA(Flavour and Extract Manufacturers' Association)组织在1965年公布的第1批可以安全食用的香料化合物之一,其FEMA号为2566[3]。但是1970年该化合物因为可能存在安全问题,在FEMA组织公布的食用香料的第4批安全列表中被去除[4]。在重新经过安全评价后,2-己基-4-乙酰氧基四氢呋喃在2011年又回到了FEMA组织公布的食用香料的第25批安全列表中[5]。
文献报道了以1-庚烯-4-醇为原料,通过双键环氧化、羟基甲磺酰化以及与硫代醋酸的亲核取代反应,可以制备2-丙基-4-乙酰氧基四氢噻吩。显然如以1-癸烯-4-醇为原料,通过该方法即可以得到2-己基-4-乙酰氧基四氢噻吩,其结构与2-己基-4-乙酰氧基四氢呋喃非常类似,该噻吩结构的香气特征还没有文献报道。本文按上述文献方法制备了2-己基-4-乙酰氧基四氢噻吩(见图1),并通过GC/O对其香气特征和香气阈值进行了评价和测定。
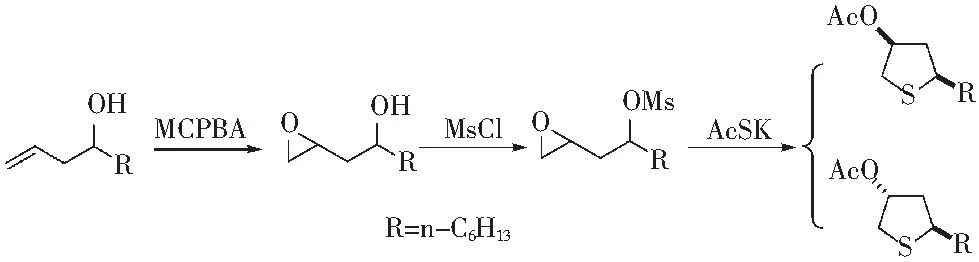
图1 2-己基-4-乙酰氧基四氢噻吩顺反异构体的制备Fig.1 Preparation of cis-trans isomers of 2-hexyl-4-acetoxy-tetrahydro-thiophene
1 实验
1.1 仪器和试剂
Bruker AV300或AV600核磁共振仪、SolariX高分辨质谱仪 瑞士布鲁克公司。所有试剂均购自北京化学试剂公司,均为AR级。
产物顺反立体异构体的香气特性通过GC/O进行评价和测定。GC分析条件:Agilent GC 7890 A,HP-5毛细管柱(30.0 m×250 μm×0.25 μm),氢火焰离子检测器。进样口温度250 ℃,检测器温度250 ℃。载气为氮气,恒流模式0.8 mL/min。采用不分流模式,样品经过色谱柱后,通过一个Y型的三通以1∶1的比例分别进入FID检测器和闻香器。色谱柱至闻香器的加热传输线温度为250 ℃,加湿空气流速为16 mL/min。香气阈值的测定根据Ullrich和Grosch报道的方法,内标采用2-壬酮,其香气阈值为1.7 μg/L。
1.2 1-癸烯-4-醇的制备
在氮气保护作用下,向装有回流冷凝管的四口烧瓶中,加入镁屑(0.16 mol,3.8 g)、无水乙醚40 mL和一小粒碘,加入烯丙基氯(1.0 mL),用电吹风轻微加热引发反应,然后滴加烯丙基氯(0.1 mol,7.7 g)的无水乙醚(40 mL)溶液,控制滴加速度保持回流。滴加完毕后,加入无水乙醚(40 mL),继续搅拌并加热回流0.5 h。待反应液降到室温,将庚醛(0.1 mol,11.4 g)的无水乙醚(30 mL)溶液滴加到制备好的格氏试剂中,控制滴加速度保持轻微的回流。加料完毕后,继续搅拌并加热回流1 h,然后将反应物冷却至室温。用饱和氯化铵溶液淬灭反应,分出乙醚层,水相用乙醚萃取,合并有机相,用饱和食盐水洗涤,无水硫酸镁干燥。过滤旋蒸除去溶剂,然后减压蒸馏,收集79~81 ℃/0.133 kPa的馏分,得到无色透明液体1-癸烯-4-醇13.6 g,产率87%。1H NMR (300 MHz, CDCl3): δ = 0.89 (t, J = 6.9 Hz, 3 H, Me), 1.16~1.53 (m, 10 H, HC5~HC9), 1.62 (d, J = 7.5 Hz,1 H,-OH), 2.14 (m, 1 H, HC3), 2.31 (m, 1 H, HC3), 3.65 (m, 1 H, HC4), 5.12 (m, 2 H, HC1), 5.81 (m, 1 H, HC2)。13C NMR (75 MHz, CDCl3): δ = 14.0 (Me), 22.6 (C9), 25.6 (C6), 29.3 (C7), 31.8 (C8), 36.8 (C5), 41.9 (C3), 70.7 (C4), 117.8 (C1), 135.0 (C2)。产物核磁谱图数据与文献报道数据一致。
1.3 1,2-环氧-4-癸醇的制备
向250 mL的单口烧瓶中加入二氯甲烷(100 mL)和1-癸烯-4-醇(7.8 g, 0.05 mol),在低温浴槽中冷却至-25 ℃,搅拌,分批加入间氯过氧苯甲酸(1.38 g, 0.06 mol)。加入完毕后,在-25 ℃反应10 h。反应结束后加入饱和的10%氢氧化钠溶液,并搅拌30 min,淬灭反应。用二氯甲烷萃取(80 mL×3),饱和食盐水洗涤,无水硫酸镁干燥。过滤除去干燥剂后旋蒸浓缩得粗产物约7.2 g,产率93%。1H NMR (300 MHz,CDCl3): δ = 0.86 (t, J = 6.9 Hz, 3 H, Me), 1.21~1.37 (m, 8 H, HC6~HC9), 1.41~1.64 (m, 3 H, HC5 and HC3), 1.75~1.90 (m, 1 H, H′C3), 2.06 (br. S, 1 H,-OH), 2.50 (dd, J = 4.8, 2.7 Hz,0.55 H, HC1), 2.63 (dd, J = 4.8, 2.7 Hz, 0.45 H, HC1), 2.77 (t, J = 4.8 Hz, 0.55 H, H′C1), 2.85 (t, J = 4.8 Hz, 0.45 H, H′C1), 3.02~3.15 (m, 1 H, HC2), 3.95~4.18 (m, 1 H, HC4)。13C NMR(75 MHz, CDCl3): δ = 13.8 (Me), 22.3 (C9),25.2 and 25.3(C6),29.0(C7),31.5(C8),37.1 and 37.4(C5),39.3 and 39.5(C3),46.4 and 46.9(C1),45.0 and 50.2(C2),68.8 and 69.7(C4)。产物核磁谱图数据与文献报道数据一致。粗产物未经进一步分离提纯直接用于下一步反应。
1.4 1,2-环氧-4-癸基甲磺酸酯的制备
向装有温度计、搅拌器、恒压滴液漏斗的四口烧瓶内加入1,2-环氧-4-癸醇(2.6 g, 0.02 mol)、二氯甲烷40 mL、三乙胺(5.6 mL, 0.04 mol),开动搅拌,0 ℃下滴加甲磺酰氯(1.9 mL, 0.024 mol),控制滴加速度,使体系温度维持在0~5 ℃内,约1 h滴加完毕,升温至25 ℃,反应12 h。反应结束后冷却,加20 mL水。用二氯甲烷萃取(30 mL×3),合并有机相,用20%的硫酸溶液洗涤(30 mL),再用饱和碳酸氢钠溶液洗涤(40 mL),最后用饱和食盐水洗涤(50 mL),无水硫酸镁干燥。过滤,旋蒸除去二氯甲烷,将剩余物柱层析分离提纯,得到产物1,2-环氧-4-癸基甲磺酸酯4.0 g,产率78%。1H NMR (300 MHz, CDCl3):δ=0.89 (t,J=6.9 Hz,3 H,Me),1.33~1.52(m,8 H, HC6~HC9),1.66~1.89(m,3 H,HC3 and HC5),1.97~2.16(m,1 H,H′C3),2.51(dd,J=4.5,2.7 Hz,0.55 H,HC1),2.54(dd,J=4.8,2.4 Hz,0.45 H,HC1),2.81(t,J=4.5 Hz,0.55 H,H′C1),2.85(t,J=4.8 Hz,0.45 H,H′C1)3.03 and 3.06(s,3 H,Me(mesyl),3.06(m,1 H,HC2,与甲磺酰基甲基部分重叠),4.87(m,1 H,HC4)。13C NMR(75 MHz,CDCl3):δ=13.7(Me),22.2(C9),24.5 and 24.8(C6),28.6 and 28.6(C7),31.3(C8),34.3 and 34.8(C5),37.4 and 37.5(C3),38.1 and 38.3(Me(mesyl)),45.9 and 47.1(C1),48.2 and 48.3(C2),80.9 and 81.0(C4)。HRMS(ESI):m/z[M+Na+]calcd for C11H22NaO4S,273.1131;found:273.1130。
1.5 2-己基-4-乙酰氧基四氢噻吩的制备
在氮气保护下,向装有温度计、搅拌器、恒压滴液漏斗的四口烧瓶内加入无水乙腈100 mL、无水碳酸钾(6 g,40 mmol)、硫代醋酸(2 mL,28 mmol)、18-冠醚(0.2 g,0.7 mmol),室温搅拌15 min。然后向溶液中加入1,2-环氧-4-癸基甲磺酸酯(5.0 g, 20 mmol),室温下搅拌。滴加完毕,升温至回流反应。反应12 h结束。冷却,过滤,滤液用100 mL 5%的稀盐酸洗涤,再用饱和碳酸氢钠溶液洗涤(50 mL×3),用饱和食盐水洗涤(60 mL),无水硫酸镁干燥。过滤,旋蒸除去乙腈,将剩余产品柱层析分离提纯,得到产物cis-2-己基-4-乙酰氧基四氢噻吩1.8 g,产率约为39%;产物trans-2-己基-4-乙酰氧基四氢噻吩2.0 g,产率约为43%。cis-2-己基-4-乙酰氧基四氢噻吩:1H NMR(600 MHz,CDCl3):δ=0.88(t,J=7.2 Hz,3 H,Me(hexyl)),1.22~1.43(m,8 H,HC2′~HC5′(hexyl)),1.62(m,1 H,HC1′(hexyl)),1.67 (m,1 H,H′C1′(hexyl)),1.79(dt,J=15.0,7.2 Hz,1 H,HC3),2.06(s,3 H,Me(acetyl)),2.37(m,1 H,H′C3),2.88(dd,J=11.4,6.0 Hz,1 H,HC5),3.13(dd,J=11.4,6.6 Hz,1 H,H′C5),3.36(m,1 H,HC2),5.29(m,1 H,HC4)。13C NMR (150 MHz, CDCl3):δ=14.0 (Me(hexyl)),21.1(Me(acetyl)),22.6(C5′(hexyl)),28.7(C3′(hexyl)),29.0(C2′(hexyl)),31.7(C4′(hexyl)),35.3(C5),37.9(C1′(hexyl)),41.0(C3),45.1(C2),76.5(C4),170.4(C=O)。HRMS(ESI):m/z[M+Na+]calcd for C12H22NaO2S, 253.1232;found:253.1230。trans-2-己基-4-乙酰氧基四氢噻吩:1H NMR(600 MHz,CDCl3):δ=0.85(t,J=6.6 Hz,3 H,Me(hexyl)),1.21-1.33(m,8 H, HC2′~HC5′(hexyl)),1.55(m,1 H,HC1′(hexyl)),1.62(m,1 H,HC3),1.67(m,1 H,H′C1′(hexyl)),2.02(s,3 H,Me(acetyl)),2.25(d,J=13.8 Hz,1 H,H′C3),2.86(d,J=12.0 Hz,1 H,HC5),3.17(dd,J=12.0,4.8 Hz,1 H,H′C5),3.47(m,1 H,HC2),5.45(m,1 H,HC4)。13C NMR(150 MHz,CDCl3):δ=14.0(Me(hexyl)),21.2 (Me(acetyl)),22.5(C5′(hexyl)),29.1(C3′(hexyl)),29.2(C2′(hexyl)),31.6(C4′(hexyl)),36.6(C1′(hexyl)),37.0(C5),42.5(C3),46.9(C2),77.1(C4),170.4(C=O)。HRMS(ESI):m/z[M+Na+]calcd for C12H22NaO2S,253.1232;found:253.1231。
2 结果与讨论
2.1 2-己基-4-乙酰氧基四氢噻吩顺反立体异构体的制备及构型确认
本文根据文献中的方法,首先以正庚醛为原料,与烯丙基氯化镁通过格氏反应得到1-癸烯-4-醇,产率为87%。1-癸烯-4-醇在间氯过氧苯甲酸的作用下,双键氧化得到1,2-环氧-4-癸醇,产率为93%。所得环氧化物为一对非对映体混合物,从核磁氢谱可以看出,两者比例为55∶45。这一结果与文献中1-庚烯-4-醇环氧化产物的异构体比例非常接近。1-癸烯-4-醇和环氧化产物均为已知的化合物,核磁谱图数据与文献报道一致。2-环氧-4-癸醇与甲磺酰氯作用,将羟基转换为甲磺酸酯,产率为78%。该产物结构经过核磁共振谱图和高分辨质谱进行了确认。所得的1,2-环氧-4-癸基甲磺酸酯和硫代醋酸在碱性条件下反应,粗产物经过柱层析分离得到两个异构体产物。根据核磁谱图数据和高分辨质谱结果推测,两个异构体产物应该为顺反立体异构体,产率分别为39%和43%。为了确认两个立体异构体的相对构型,两个异构体产物分别测定了相应的NOE谱图,见图2和图3。
图2和图3中均有3张图,其中:(a)为产物的核磁氢谱,(b)为照射4号氢得到的NOE差谱,(c)为照射2号氢得到的NOE差谱。在图2(b)中照射4号氢,2号氢信号有明显增强;在图2(c)中照射2号氢同样也观察到了4号氢信号有明显增强。可见2号氢和4号氢之间存在明显的NOE效应,由此可以推测该产物为cis构型。相比之下,在图3(b)中照射4号氢,2号氢信号无明显增强;同样在图3(c)中照射2号氢,4号氢信号也无明显增强。可见该产物中2号氢和4号氢之间不存在NOE效应,由此可以推测该产物为trans构型。和文献报道的2-丙基-4-乙酰氧基四氢噻吩顺反异构体的核磁数据相比,特征峰的化学位移和峰形非常相似。
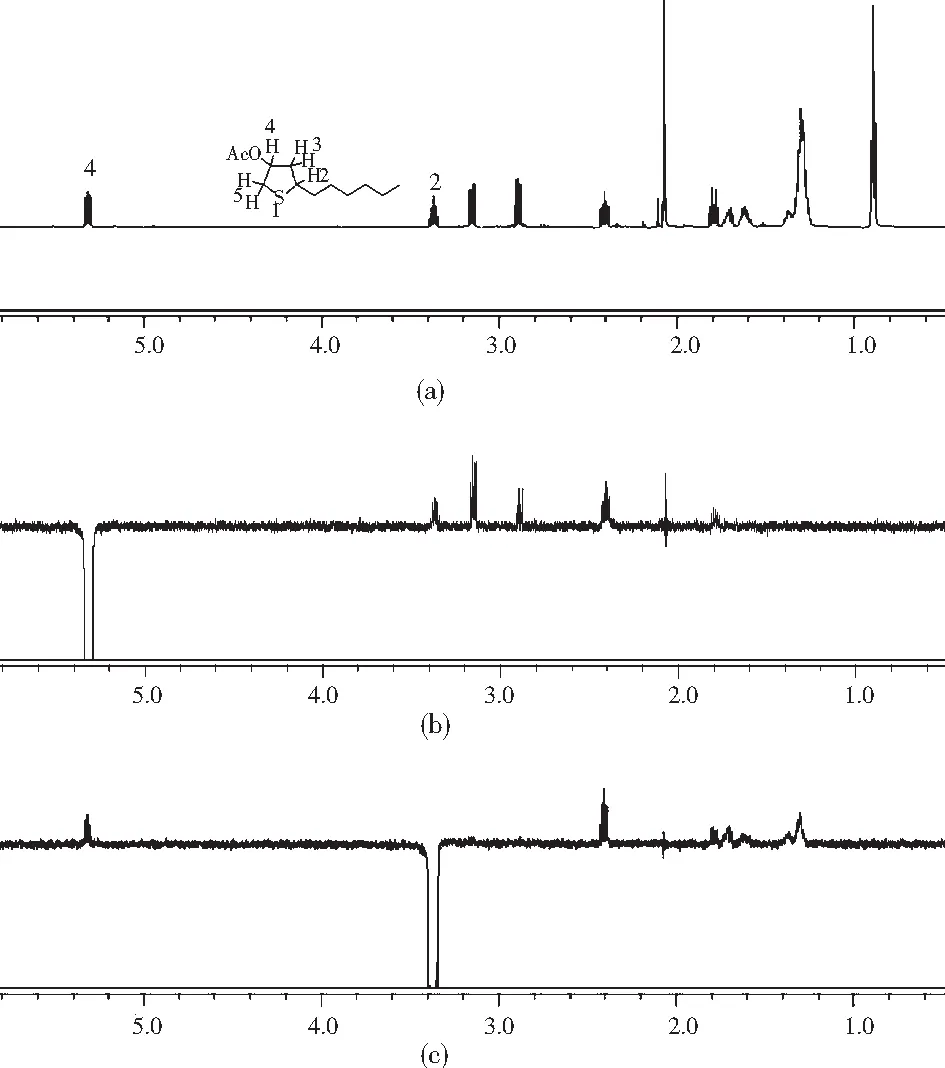
图2 cis-2-己基-4-乙酰氧基四氢噻吩NOE谱图Fig.2 NOE spectrogram of cis-2-hexyl-4-acetoxy-tetrahydro-thiophene
2.2 2-己基-4-乙酰氧基四氢噻吩顺反立体异构体的香气特性
本文对所得到的2-己基-4-乙酰氧基四氢噻吩的两个顺反立体异构体的香气特征和香气阈值通过GC/O进行了评价和测定,结果见表1。评香结果表明,cis构型带有香菇味、油脂味、塑料味和汽油味;trans构型表现出了青香、甜香、清凉味。以2-壬酮为内标,根据Ullrich和Grosch报道的方法,采用逐步稀释的方法,测得cis和trans两个异构体在空气中的香气阈值分别为60 μg/L和4.2 μg/L。trans构型阈值更低,表明其香气强度更强于cis构型。相应的2-己基-4-乙酰氧基四氢呋喃是具有甜香、花香和水果香的香料化合物,其中cis构型具有水果香、甜香、焦香,带有熟蒜的味道,而trans构型具有弱的奶香、甜香、青香,带有洋葱的味道。cis构型的香气强度要比trans构型更强[6]。

表1 2-己基-4-乙酰氧基四氢噻吩顺反立体异构体的香气特征和香气阈值Table 1 Aroma characteristics and aroma thresholds of cis-transstereoisomers of 2-hexyl-4-acetoxy-tetrahydro-thiophene
由此可见,尽管2-己基-4-乙酰氧基四氢噻吩和2-己基-4-乙酰氧基四氢呋喃除去杂环结构,其他取代基团相同,但评香结果表明两者的香气特征表现出明显不同,两个顺反异构体相对强度也相反。这一结果也与其他呋喃类和噻吩类香料间表现出的香气区别一致。说明在其他官能团完全相同的情况下,呋喃环和噻吩环的杂环结构会对香气产生显著的影响。
3 结论
本文以正庚醛为原料,通过格氏反应制备1-癸烯-4-醇,然后通过环氧化、甲磺酸酯化和亲核取代三步反应,得到了2-己基-4-乙酰氧基四氢噻吩的两个异构体。异构体产物的顺反相对构型经过核磁谱共振氢谱、碳谱和NOE谱图进行了确认。评香结果表明,两者的香气特征存在明显差别,trans异构体香气强度强于cis异构体。该噻吩产物与呋喃结构类似物2-己基-4-乙酰氧基四氢呋喃香气特征具有显著区别。本文研究结果对于噻吩类香料的研究和开发具有一定的参考价值。
