CaMoO4:Eu3+纳米荧光粉的尺寸调控及光学性能研究
2019-09-11杨流赛孟晓燕孙宇杰熊玉环王运健
杨流赛,孟晓燕,罗 伟,孙宇杰,熊玉环,王运健
(1.上饶师范学院化学与环境科学学院,江西上饶334000;2.淮北师范大学化学与材料科学学院,安徽淮北235000)
稀土离子掺杂钼酸盐是一种重要的发光材料,在紫外区具有宽而强的电荷迁移带吸收,因其具有优越的发光性能和良好的显色、变色效应而被广泛应用于制备光学纤维、温度传感器、发光材料、催化材料等各方面[1-5].目前主要是采用传统的高温固相法来制备发光材料[6].例如Li等人采用高温固相法制备了SrMoO4:Eu3+红色发光粉,为了进一步提高其发光强度,补偿Eu3+取代Sr2+格位时引起的价态不匹配,特别引入Na+作为电荷补偿剂对所制备的SrMoO4:Eu3+进行性能改善[7].高温固相法合成荧光粉虽然比较成熟,合成的晶体结构清晰,发光强度高,但合成温度高,能耗高,样品颗粒大且形貌不规则.因此,目前很多研究者采用反应温度低的湿化学方法,通过控制合成条件来合成不同形貌和粒径的稀土掺杂钨/钼酸盐发光材料,并对其发光性能进行了研究.在荧光粉体制备中,最为常见湿化学方法为共沉淀法[8-9]、溶胶 - 凝胶法[10-11]和水热合成法[12-14].其中,水热法在材料形貌和尺寸的可控合成方面具有优势,而且可以严格地控制掺杂量,由于水热反应在液相快速对流中进行,所以产物结晶度高、纯度高、颗粒分散性好,避免了因高温煅烧或球磨等后处理程序引进不必要的杂质和结构上的缺陷.根据文献报道[15-17],纳米材料晶粒尺寸的变化会引起其结构和物理化学性质相应的改变,此外,掺杂效应可改变晶格内部结构,从而改变材料的性质,因此研究纳米材料的尺寸效应及掺杂效应具有重要的科学意义.
在各种钼酸盐材料中白钨矿结构的CaMoO4具有制备工艺简单、合成成本低等优点,是一种优良的荧光粉基质材料,所以Eu3+掺杂CaMoO4荧光粉发光性质的研究十分活跃[18-19],但多数研究集中在如何提高材料的发光强度和效率方面,然而有关尺寸效应和掺杂效应对其晶格结构和光学性能的研究却鲜有报道.因此,本工作主要通过调节水热反应温度、反应时间和掺杂量来制备CaMoO4:Eu3+纳米荧光粉,并利用X-射线粉末衍射、扫描电镜、红外光谱、紫外-可见光漫反射光谱和荧光光谱测试,进一步研究CaMoO4:Eu3+纳米晶的尺寸变化以及掺杂浓度对所得样品的相结构、形貌、表面状态、光学吸收以及发光性能的影响.
1 实验
1.1 主要试剂
二水合钼酸钠(国药集团,AR),氯化钙(国药集团,AR),三氯化铕(国药集团,纯度为99.99%),盐酸(国药集团,AR),蒸馏水(自制).
1.2 样品制备
Ca1-xEuxMoO4(x=0.01,0.02,0.04,0.06,0.08)纳米晶的合成:先以Eu3+掺杂质量百分比浓度为2%样品为例.在100 mL烧杯中,分别加入9.8 mL 1mol/L 的 CaCl2溶液和 4 mL 0.05 mol/L的EuCl3溶液,再将10 mL 1mol/L的Na2MoO4溶液逐渐滴加到上述溶液中,产生白色沉淀,用盐酸调节溶液的pH值至9,混合后溶液的总体积为70 mL,充分搅拌30 min,然后将反应混合物转移至100 mL反应釜中.水热条件下160℃反应8 h,待反应体系自然降温后,将反应釜中上层清液弃去,得到的白色沉淀用蒸馏水离心,洗涤3次,在烘箱中80℃温度下烘干后得到样品,研磨后进行表征.其他不同掺杂浓度的Ca1-xEuxMoO4样品按照相应的化学计量比合成,制备方法同上.
同理,在保持Eu3+掺杂摩尔浓度为2%前提下,一方面,设定水热反应时间为2 h,改变反应温度(120,140,160,180 和 200 ℃),其它合成条件不变,可获得不同水热温度下的 Ca0.98Eu0.02MoO4荧光粉;另一方面,设定水热温度为160℃,改变反应时间(1,2,4,8和16 h),其它合成条件不变,可获得不同水热时间下的 Ca0.98Eu0.02MoO4荧光粉.
1.3 材料表征
粉末样品的物相结构通过日本Rigaku Mini-Flex II粉末衍射仪测试,纳米晶的颗粒大小采用Scherrer公式 D=0.9λ/(βcosθ)计算得到,其中λ为所用的X射线波长(0.15418 nm),θ是晶面的衍射角,β为去除仪器误差的半峰宽.采用美国PerkinElmer公司生产的 Frontier FT-IR型傅立叶变换红外光谱仪测试样品的红外光谱.样品的紫外-可见漫反射光谱采用BaSO4做背底,在Varian Cary 5000紫外-可见光谱仪进行测试.采用Phenom ProX型飞纳台式扫描电镜观察样品的形貌.采用JEM2010透射电镜观察产物颗粒形貌及尺寸.通过日立F-7000荧光分光光度计表征样品的荧光性能.
2 结果与分析
2.1 结构表征
图1给出了水热反应2 h在不同温度下合成Eu3+掺杂质量分数为2%样品的XRD谱图.从图1可以看出,合成样品的衍射峰均与 CaMoO4(JCPDS,No.29-0351)标准卡片一致,没有出现其他衍射峰.依据(112)最强衍射峰,由Scherrer公式计算得到CaMoO4:Eu3+样品的颗粒尺寸.当反应温度从200℃下降至120℃,CaMoO4:Eu3+纳米晶的平均粒径依次为 40.2、38.9、36.8、21.7和21.1 nm.同时,通过改变水热反应时间也是调控晶体粒度的一种方法.图2是反应温度为160 ℃在不同反应时间合成 Ca0.98Eu0.02MoO4样品的XRD谱图,得到的样品均为纯相的四方白钨矿型CaMoO4晶体.当反应时间从16 h缩短至1 h,纳米颗粒的平均粒径分别为 43.2、40.5、38.0、36.8和31.5 nm.因此,随着水热反应温度的降低,CaMoO4:Eu3+纳米晶都表现出尺寸减小的趋势,这与图1衍射峰(112)渐渐地变宽相一致.同理,缩短水热反应时间,也在图2中观察到了类似的现象.
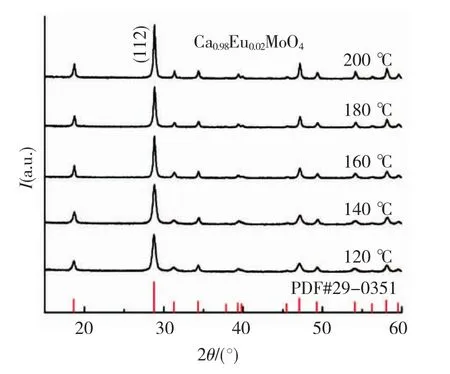
图1 不同水热温度下反应2 h合成Ca0.98Eu0.02MoO4样品的 XRD谱图,底部竖线为标准 PDF卡片CaMoO4的衍射峰Fig.1 XRD patterns of the Ca0.98Eu0.02MoO4samples prepared under various hydrothermal temperature for 2 h,vertical bars at the bottom denote the standard data for CaMoO4
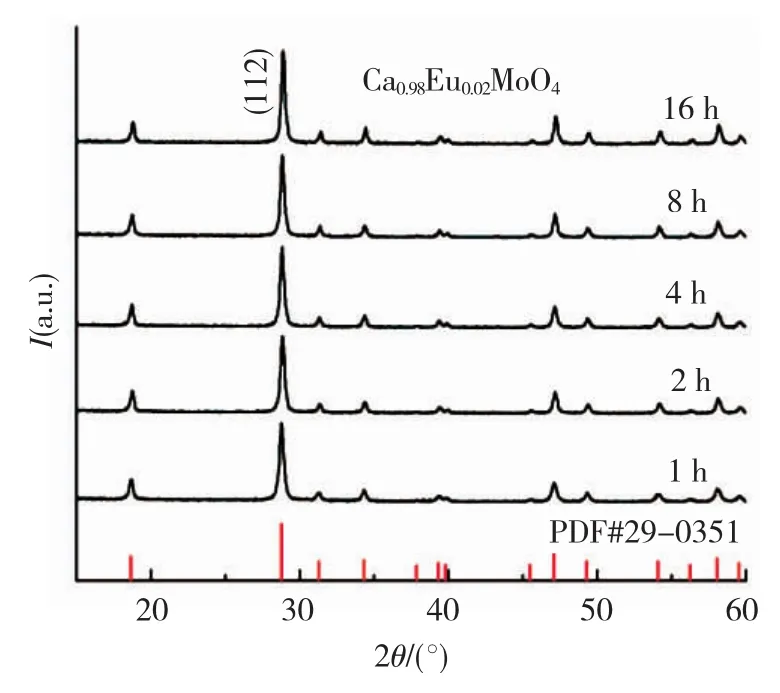
图2 在160℃水热反应不同时间合成Ca0.98Eu0.02MoO4样品的XRD谱图Fig.2 XRD patterns of the Ca0.98Eu0.02MoO4samples prepared under 160℃at different hydrothermal time
图3 是改变Eu3+掺杂量制备 Ca1-xEuxMoO4纳米晶的XRD谱图,可以发现,掺杂后样品相结构没有改变,均为纯相CaMoO4结构,说明在较低的质量分数范围内,Eu3+很容易掺杂到CaMoO4晶格中[13];但随着Eu3+掺杂量的增加,样品的衍射峰略有宽化,意味着晶粒尺寸逐渐减小[20],通过Scherrer公式计算(112)主峰,得到不同Eu3+掺杂量样品的平均晶粒分别为 48.9、40.5、35.3、32.7和31.1 nm.由此可见,随着掺杂 Eu3+离子浓度增加,CaMoO4纳米晶的平均粒径由48.9 nm减小到31.1 nm,这是由于异价离子Eu3+进入CaMoO4晶格中引起了晶格畸变,从而抑制晶粒长大.根据文献报道[8],Eu3+的离子半径(0.109 nm)与Mo6+(0.041 nm)相差较大,而与Ca2+离子半径(0.099 nm)相近.所以,Eu3+占据 Mo6+格点会使晶格畸变过大,这在能量上不利的,而Eu3+更容易取代Ca2+的位置进入晶格.根据电荷平衡原理,在 CaMoO4基质晶格中掺入Eu3+后,那么就产生一个Ca2+离子空位,可以采用下述方程来表示:
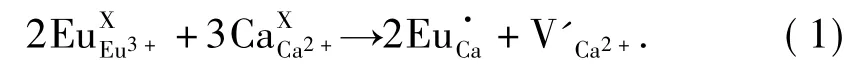
由于Eu3+进入格位取代Ca2+为不等价取代,使晶体产生了空位缺陷,因此需要进行电荷补偿.根据固体材料的缺陷理论和电中性原理,在原料中掺入等电量的碱金属Na+离子可以中和电荷从而防止这种空位缺陷的形成.电荷平衡可以用下面的方程表示:
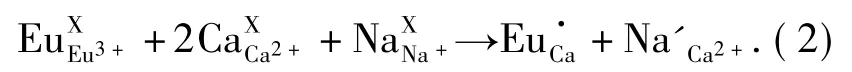
因此,原料中二水合钼酸钠可以提供Na+离子作为电荷补偿剂,而且Na+离子半径较小,很容易取代 Ca2+离子格位,从而达到电荷平衡[18].
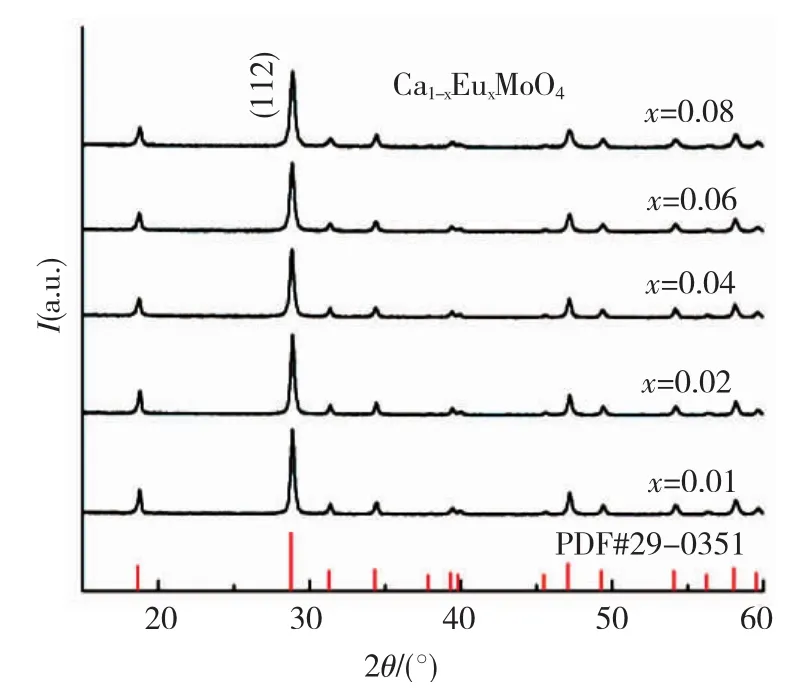
图3 在160℃水热反应8 h合成Ca1-xEuxMoO4样品的XRD谱图Fig.3 XRD patterns of the Ca1-xEuxMoO4samples hydrothermal prepared under 160℃for 8 h
2.2 紫外-可见漫反射光谱分析
图4 (a)和(b)分别给出了不同水热温度和反应时间合成 Ca0.98Eu0.02MoO4样品的紫外 - 可见漫反射光谱,可以看到,所有样品在紫外光区都出现了一个强烈的宽带吸收峰,同时紫外-可见漫反射图陡峭的变化说明吸收并不是由于杂质能级的跃迁而是由带隙转移引起的[21],这与样品在外观上呈现白色相符.值得注意的是,随着反应温度的降低或反应时间的缩短,这两批样品的光吸收边都发生了蓝移,这与水热合成的样品粒度减小以及结晶度变差有关.Tong等人报道了[15],随着CdWO4颗粒尺寸从21 nm减小到11 nm,纳米颗粒光吸收边发生蓝移,这与本实验中观察的现象类似.说明导带与价带之间的能隙增加,这与纳米颗粒的表面结构有关;根据之前的XRD结果分析,随着反应温度的降低或反应时间的缩短,Ca0.98Eu0.02MoO4纳米晶的尺寸都表现出逐渐减小的趋势,由于纳米晶尺寸减小会引起表层原子无序度增加和结晶度变差,导致电子跃迁难度增加,进一步引起带隙的增大,从而发生蓝移.
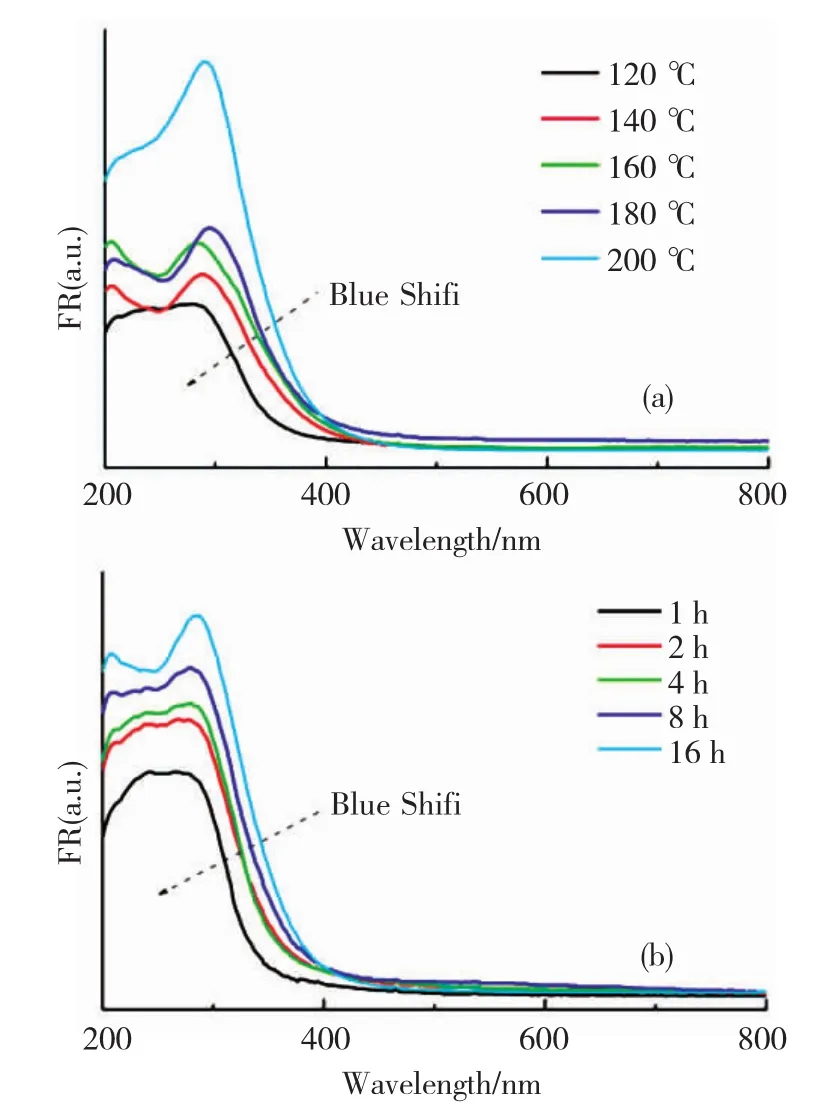
图4 (a)不同水热温度下反应2 h和(b)在160℃水热反应不同时间合成 Ca0.98Eu0.02MoO4 样品的紫外-可见漫反射谱图Fig.4 Diffuse reflectance spectra of the Ca0.98Eu0.02MoO4 samples prepared(a)under various hydrothermal temperature for 2 h and(b)for 160℃at different reaction time
图5 (a)给出了不同Eu3+掺杂浓度样品的紫外-可见漫反射光谱,可以看出所有样品在紫外光区(200~380 nm)都出现了一个强烈的宽带吸收峰,属于基质与Eu3+离子之间相互作用产生吸收的电荷迁移带[22].从图5可以看出,随着掺杂质量分数的增加,样品的吸收带边逐渐发生红移,对于Eu3+掺杂质量分数为8%的样品,在可见光区出现了明显的吸收,这是由于达到Eu3+掺杂极限之后,样品中存在微量的氧化铕造成的.根据文献报道[21],CaMoO4是直接带隙半导体,掺杂Eu3+样品的能带由 Tauc公式计算[23],图 5(b)是由(αhν)2~hν线性部分外推至(αhν)2=0 得到样品的禁带宽度.从图中可以看出,Eu3+掺杂质量分数为1%时,Eg约为3.85 eV,随着掺杂质量分数的增加,样品的禁带宽度逐渐减小,当掺杂量为8%时,Eg约为3.49 eV.因为这批样品除了Eu3+掺杂质量分数不同外,其他反应条件保持一致,所以在纳米尺度内Eu3+离子的引入是影响CaMoO4纳米晶带隙的关键因素.样品在紫外光区产生的宽带吸收峰,属于CaMoO4基质与 Eu3+离子之间相互作用产生吸收的电荷迁移带,导致Mo-O及 Eu-O迁移带存在部分重叠.随着Eu3+掺杂质量分数的增加,导致这两个迁移带的相互作用增强,使得CaMoO4:Eu3+纳米晶的紫外-可见漫反射吸收带边产生了红移.因此,Eu3+离子的引入是导致CaMoO4纳米晶的带隙下降的主要原因.
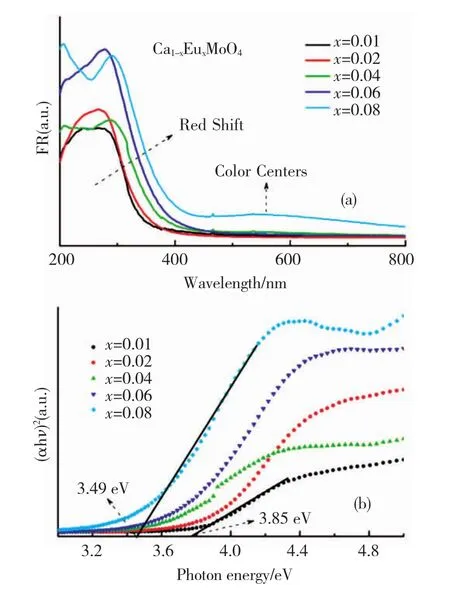
图5 在160℃水热反应8 h下合成Ca1-xEuxMoO4样品的(a)紫外 -可见漫反射谱图和(b)能量与(αhν)2关系曲线Fig.5 (a)Diffuse reflectance spectra and(b)the energy dependence of(αhν)2of Ca1-xEuxMoO4samples hydrothermally prepared under 160℃for 8 h
2.3 红外光谱分析
图6 展示了在相同水热反应条件下合成样品Ca1-xEuxMoO4的红外谱图.根据XRD表征可知,CaMoO4属四方晶系,不同Eu3+掺杂样品观察到了CaMoO4晶格振动吸收峰[24],位于 430 cm-1的弱峰,对应于MoO4四面体中O-Mo-O键的反对称弯曲振动;位于837 cm-1的最强峰归属于Mo-O键的反对称伸缩振动[25].值得注意的是,对于Eu3+掺杂的样品,在747 cm-1和700 cm-1出现了新的峰,而且这两个峰都随着Eu3+掺杂的增加逐渐增强,这与Eu3+掺杂后引起的MoO4体晶格畸变有关.
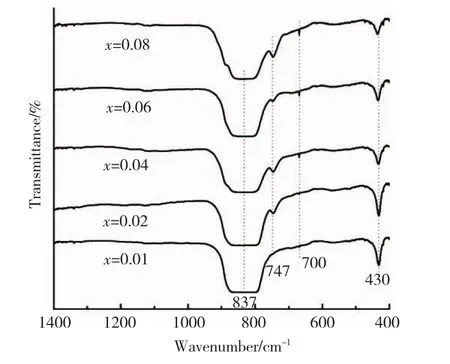
图6 在160℃水热反应8 h合成Ca1-xEuxMoO4样品的红外吸收光谱Fig.6 FT - IR spectra of Ca1-xEuxMoO4samples hydrothermally prepared under 160℃for 8 h
2.4 形貌分析
Eu3+掺杂对样品形貌的影响通过扫描电镜观察.如图7(a)所示,未掺杂CaMoO4样品为具有规则形貌的椭球状结构,该结构是由纳米粒子组装而成的微米级结构,其尺寸大小比较均匀.由图7(b)变化到7(f)可以看出,随着Eu3+掺杂量的增加,样品的组装结构逐渐解离,分解为尺寸均匀的颗粒状纳米形貌;同时纳米颗粒尺寸随着Eu3+掺杂量的增加而减小,这与XRD计算的平均粒径变化结果一致.由于 Eu3+掺杂会影响CaMoO4纳米晶的表面电荷分布以及晶体在溶液中的生长和自组装性质,从而导致规则形貌的椭球状结构发生解离以及纳米颗粒尺寸的减小.同时,为了更好地观察CaMoO4:Eu3+样品的颗粒形貌,补充了 Ca0.98Eu0.02MoO4纳米荧光粉的TEM 形貌图,如插图 7(c) 所示,Ca0.98Eu0.02MoO4纳米荧光粉的乙醇溶液经过超声后,观察到分散度比较好、尺寸分布较均匀的纳米颗粒形貌,这与XRD计算得到的平均粒径 (40.5 nm)比较接近.

图7 在160℃水热反应8 h合成Ca1-xEuxMoO4样品的 SEM 照片:(a)x=0,(b)x=0.01,(c)x=0.02,(d)x=0.04,(e)x=0.06,(f)x=0.08,插图为 Ca0.98Eu0.02MoO4纳米荧光粉的 TEM 形貌图Fig.7 SEM images of Ca1-xEuxMoO4samples hydrothermally prepared under 160℃ for 8 h:(a)x=0,(b)x=0.01,(c)x=0.02,(d)x=0.04,(e)x=0.06,(f)x=0.08(inset shows a TEM image of the Ca0.98Eu0.02MoO4nanocrystals)
2.5 荧光性能分析
监测614 nm,测得 CaMoO4:Eu3+样品的激发光谱如图8左所示.由图可以看出,在200~350 nm有一个宽的激发带,最大激发峰位于275 nm处,这是由于Mo-O及Eu-O迁移带引起的,而且两个迁移带有部分重叠;同时,在350~420 nm的一系列窄带光谱,来源于Eu3+的4f电子跃迁吸收,其中位于363,383和395 nm,分别归属于7F0→5D4,7F0→5L7以及7F0→5L6电子跃迁[24].在激发谱图中,选择275 nm作为有效的激发波长具有更高的能量传递效率,得到Eu3+离子的跃迁能级5D0→7FJ(J=1-4)特征发射,具体电子跃迁能级在图8右中标出,且以5D0→7F2(614 nm)电偶极跃迁发射为主,说明Eu3+在CaMoO4基质中主要占据非反演对称中心的格位,观察到纯红色的光[24].除了荧光强度有所不同外,制备的其他CaMoO4:Eu3+荧光粉也观察到类似的发射光谱.
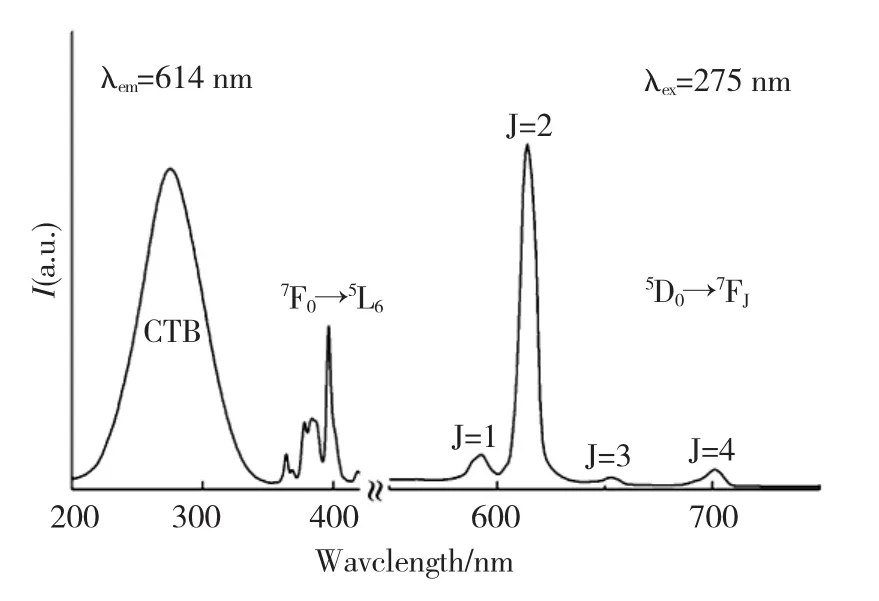
图8 样品 Ca0.98Eu0.02MoO4 的荧光激发(λem=614 nm)和发射(λex=275 nm)谱图Fig.8 Photoluminescence excitation(λem=614 nm)and emission spectra( λex=275 nm) of Ca0.98Eu0.02 MoO4nanocrystals
在 275 nm 紫外光激发下,Ca0.98Eu0.02MoO4样品的发射峰强度随水热反应温度以及反应时间的变化关系如图9所示,且以 Eu3+的5D0→7F2(614 nm)电偶极跃迁发射强度进行对比.从图中可以看出,随着水热反应温度的降低或者反应时间的缩短,荧光强度逐渐减弱.对于这些样品,Eu3+掺杂质量分数为2%、反应pH值、原料的初始浓度都保持一致.因此,反应温度和反应时间是影响纳米颗粒尺寸以及结晶性的关键因素.由于CaMoO4:Eu3+纳米晶的尺寸较小,比表面积比较大,所以表面原子的分布占整个纳米颗粒的比例较大,不可以忽视.一方面,表层原子无序度增加,使得纳米颗粒的结晶性随着尺寸的减小而变差;另一方面,表面分布的Eu3+离子很容易以弱的化学键与表面吸附的杂质、溶剂相结合,使处于表面态的原子、电子与处于小颗粒内部的原子、电子的行为有很大的差别,这些吸附物在掺杂稀土离子周围产生很高的振动能,而且缺少有效地保护层,导致荧光很容易发生猝灭.这也说明,随着水热反应温度的降低或者反应时间的缩短,样品的晶粒尺寸逐渐减小以及纳米晶的结晶度降低,从而导致样品的发光强度逐渐减弱.
荧光粉的发光强度除了受纳米晶的尺寸和结晶性影响外,还取决于稀土离子的掺杂浓度,即基质中发光中心的多少.为了研究 Eu3+含量对Ca1-xEuxMoO4荧光粉发光强度的影响,对掺杂不同浓度的Ca1-xEuxMoO4系列样品进行了荧光强度分析,如图10所示.从图中可以看出,样品的发光强度随着Eu3+浓度的增加而增加,但掺杂质量分数达到6%之后,继续提高掺杂浓度,发光强度反而降低.其中,主要原因是由于Eu3+离子之间的平均距离减小,增强了Eu3+离子间的电子交叉弛豫振动,通过无辐射跃迁消耗激发态能量,产生了浓度淬灭效应导致发光强度下降[13].另一方面,随着Eu3+离子浓度的增加,一些 Eu3+未能进入CaMoO4基质晶格而以微量的氧化铕形式存在,影响了发光强度.
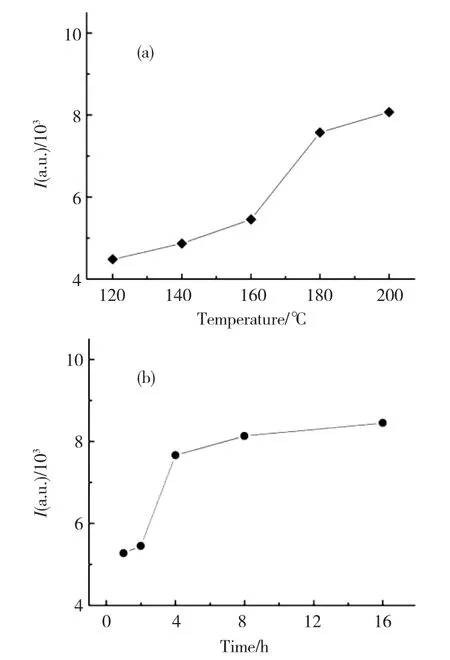
图9 Ca0.98Eu0.02MoO4 样品的 614 nm 发射峰强度(a)随水热反应温度的变化关系和(b)随水热反应时间的变化关系Fig.9 Emission intensity at 614 nm of Ca0.98Eu0.02MoO4as a function of the hydrothermal(a)reaction temperature and(b)reaction time
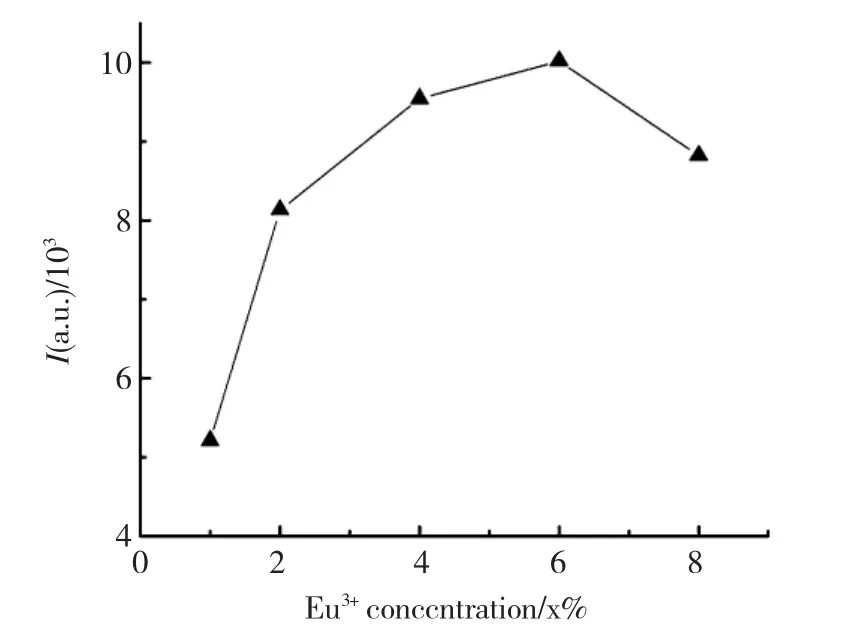
图10 Ca1-xEuxMoO4样品的614 nm发射峰强度随Eu3+掺杂质量百分比的变化关系Fig.10 Emission intensity at 614 nm of the Ca1-xEuxMoO4 samples as a function of Eu3+doping concentration
3 结论
通过水热法合成了CaMoO4:Eu3+纳米荧光粉,由于Eu3+进入格位取代Ca2+为不等价取代,所以原料中二水合钼酸钠可以提供Na+作为电荷补偿剂,从而达到平衡电荷的效果.所合成样品均为四方晶系白钨矿结构的CaMoO4纳米晶.研究结果表明,一方面,随着水热反应温度的降低或者反应时间的缩短,都会使得样品的晶粒尺寸逐渐减小以及纳米晶的结晶度下降,不仅导致样品的发光强度逐渐减弱,而且引起了样品的紫外可见光吸收带边发生蓝移;另一方面,随着Eu3+掺杂浓度的增加,由于异价离子Eu3+进入CaMoO4晶格中引起晶格畸变,从而抑制晶粒长大,导致其颗粒尺寸逐渐减小.此外,由于Mo-O及Eu-O迁移带有部分重叠,发生相互作用使得CaMoO4:Eu3+纳米晶的紫外可见光吸收带边产生了红移,并发现其荧光猝灭时质量分数为6%.
