基于巴戟天配方颗粒的标准汤剂特征图谱
2019-09-10李军山李雪利高杰高晗张肖建孙福仁牛丽颖
李军山 李雪利 高杰 高晗 张肖建 孙福仁 牛丽颖

摘 要:为了使巴戟天配方颗粒的质量标准更加科学规范,通过对15批产自不同地区的巴戟天饮片进行标准汤剂的制备,以及对标准汤剂干膏粉进行研究,确定了巴戟天标准汤剂的出膏率范围;采用高效液相色谱法对主含成分耐斯糖进行了含量测定,研究了巴戟天配方颗粒的PLC特征图谱分析方法,并对特征谱图中的水晶兰苷进行了指认。结果表明,在以流动相作为提取溶剂、甲醇-水(二者体积比为3∶97)为流动相的条件下,耐斯糖含量的转移率范围为73.21%~94.49%,标准汤剂出膏率范围为49.05%~55.87%。基于巴戟天配方颗粒的标准汤剂特征图谱研究方法严谨、可行,更加科学地阐明了配方颗粒与标准汤剂研究的一致性。
关键词:中药化学;巴戟天;标准汤剂;转移率;出膏率;特征图谱
中图分类号:R284.1 文献标志码:A
Abstract: In order to make the quality standard of Morinda officinalis ow prescription granules more scientific and standardized, 15 batches of Morinda officinalis ow decoction pieces produced in different regions are prepared with standard decoction, and the dry extract powder of standard decoction is studied to determine the range of extraction rate of Morinda officinalis standard decoction. The content of the main component Nystose is determined by high performance liquid chromatography. The PLC characteristic chromatogram analysis method of Morinda officinalis ow prescription granules is researched, and the crystal glycoside in the characteristic chromatogram is identified. The results show that under the flow phase as extraction solvent, methanol-water(3∶97) as mobile phase, the transfer rate of nesaccharide content is in the range of 73.21%~94.49% , and the extraction rate of standard decoction is in the range of 49.05%~55.87%. The quality standard established by the standard decoctio
n characteristic map research institute based on Morinda officinalis ow prescription granules is rigorous and feasible, which more scientifically illustrates the consistency between the prescription granules and the standard decoction research.
Keywords:chemistry of Chinese material medica; Morinda officinalis ow; standard decoction; transfer rate; extraction rate; characteristic chromatograms[T][ST][2*2]
巴戟天為茜草科植物巴戟天[WTBX]Morinda officinalis ow的干燥根[1],是中国著名的“四大南药”之一[2],始载于《神农本草经》[3],味甘辛,性微温,具有补肾阳、强筋骨、祛风湿之功效,用于治疗阳痿遗精、宫冷不孕、月经不调、风湿痹痛、筋骨痿软等[4]。巴戟天药材中主要含有蒽醌类、环烯醚萜苷类、多糖类等成分[5-7]。其中,蒽醌类化合物主要有2-羟基-1-甲氧基蒽醌、rubiasin A和rubiasin B等,均具有抗菌、降压、降脂、抗癌、抗病毒、凝血等活性[8]。环烯醚萜苷类化合物主要包括水晶兰苷[9]、四乙酰车叶草苷[10]等,具有较强的抗炎镇痛作用。目前,从巴戟天中分离得到的糖类主要有水溶性多糖(MOP-1)、甘露糖、巴戟甲素(原称巴戟素)、耐斯糖等多种低聚糖,研究表明其具有显著的抗抑郁作用。
饮片标准汤剂是以中医理论为指导、临床应用为基础,参考现代提取方法,经标准化工艺制备而成的单味中药饮片水煎剂,其规范了工艺参数和质量标准的建立原则[11]。配方颗粒的各项指标及生产过程必须与标准汤剂确定的质量标准相吻合。本研究按照标准汤剂制备方法,以采自15个不同产地的巴戟天饮片为原料制备标准汤剂,测定15批巴戟天标准汤剂的干膏量,确定出膏率范围,并对耐斯糖进行含量测定,确定含量及转移率范围。经过方法摸索,得出巴戟天标准汤剂的PLC特征图谱,以期使巴戟天配方颗粒的质量标准更加科学和规范。
1 主要仪器与试药
Shimadzu Corporation LC-20AT高效液相色谱仪,Sartouius CPA225D分析天平,水循环真空泵,SENCO Technology Co.Ltd.提供;M-A5002电子天平,浙江余姚市纪铭称重校验设备有限公司提供;DG-9140A干燥箱,江苏太仓精宏仪器设备有限公司提供;超声波清洗器,江苏昆山禾创超声仪器有限公司提供。
耐斯糖对照品,批号为111891-201403;水晶兰苷对照品,批号为111870-201303;乙腈,批号为20161014;甲醇,色谱纯,批号为20161020;水,纯化水;磷酸,分析纯。
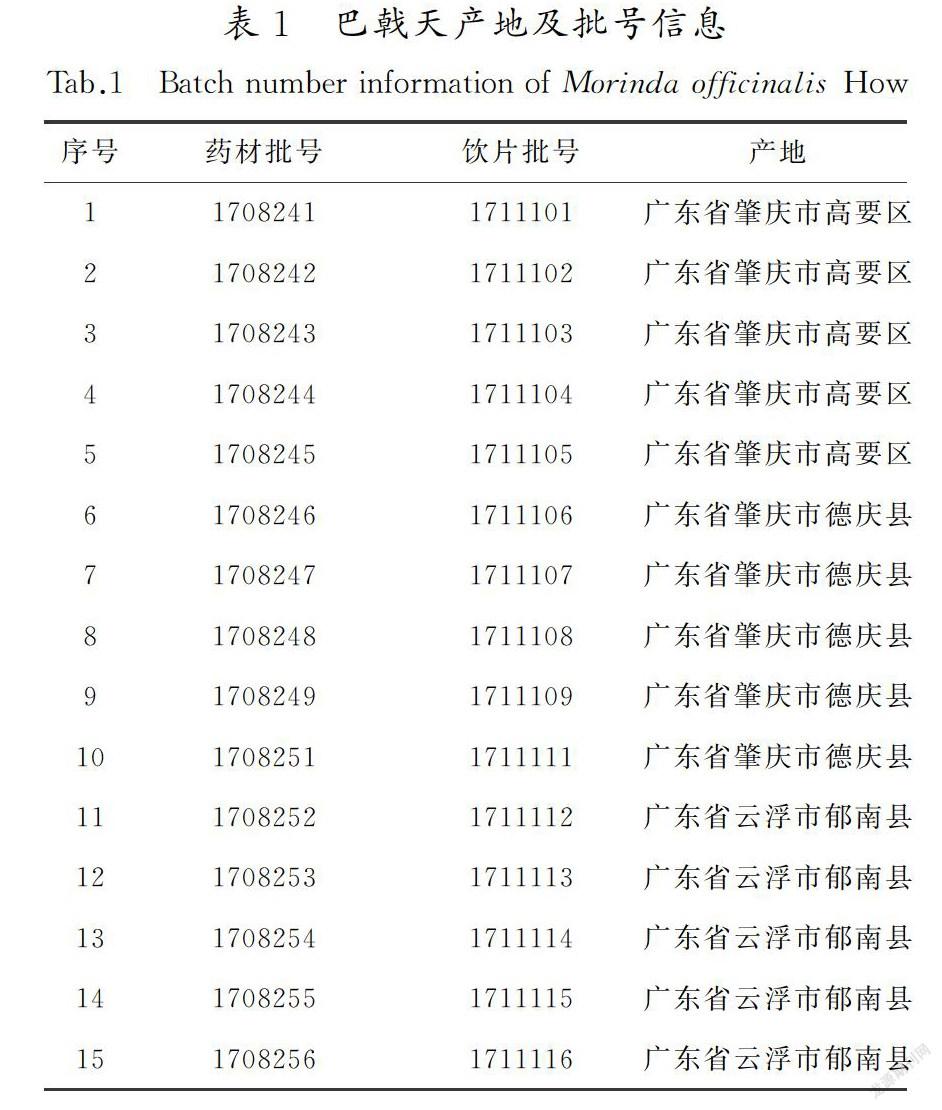
巴戟天药材共计15批,经河北省药品检验研究院孙宝惠老师鉴定为正品,样品来源信息见表1。
2 方法与结果
2.1 标准汤剂样品制备
取巴戟天饮片100 g,放入2 L圆底烧瓶中,加水提取2次。第一煎加水900 mL,先泡30 min,然后开启加热,煮沸后计时60 min;第二煎加水700 mL,煮沸后计时40 min。合并2次煎液,使用孔径为0.048 mm的过滤材质,在药液热时进行过滤。将滤液用旋转蒸发器于低温(55 ℃,-0.095 MPa)浓缩,浓缩至相对密度为1.03~1.06(55 ℃)的流浸膏,放置在不锈钢盘中冷冻干燥,制成标准汤剂干燥粉末[12-18]。
2.2 标准汤剂中耐斯糖含量的测定
2.2.1 色谱条件
以十八烷基硅烷键合硅胶为填充剂,流动相组成水与甲醇体积比为97∶3,采用蒸发光散射检测器检测,理论塔板数按耐斯糖峰计算应不低于3 000。
2.2.2 对照品溶液的制备
取耐斯糖标准品适量,精密称定,置于50 mL容量瓶中,加入流动相,制成每1 mL含200 μg的溶液。
2.2.3 供试品溶液的制备
取巴戟天标准汤剂0.2 g,精密称定,置于150 mL具塞锥形瓶中,精密加入流动相50 mL,称重,于沸水浴中加热30 min,放冷,再次称重,用流动相补足减失的质量,摇匀,过滤,即得[19]。
2.2.4 测定方法
精密吸取对照品溶液10 μL、对照品溶液30 μL、供试品溶液10 μL,注入液相色谱仪,测定,采用外标两点法对数方程计算。
2.2.5 线性关系考察
精密吸取对照品溶液50,100,200,300,400 μL,按“221”所述条件进样分析,纵坐标为耐斯糖峰面积的对数值,横坐标为耐斯糖进样量的对数值,制作标准曲线。结果表明,耐斯糖进样量在1041 9~8334 9 mg范围内,回归方程为Y=1582 9X+5533×10-1,r=0999 7,表明线性关系良好。
2.2.6 精密度实验
取巴戟天标准汤剂样品(标3,下同),按“2.2.3”所述方法制备供试品溶液,连续进样6针,测定峰面积(耐斯糖)的RSD值为0.87%,结果表明精密度良好。
2.2.7 稳定性实验
取巴戟天标准汤剂样品,按“2.2.3”所述方法制备供试品溶液,在1,3,6,10,14,18 h进样测定耐斯糖含量。经计算,各样品中耐斯糖峰面积的RSD值为1.56%,说明18 h内此样品溶液稳定。
2.2.8 重复性实验
取巴戟天标准汤剂样品供试品6份,每份0.2 g,精密称定。按“2.2.3”所述方法处理标准汤剂样品,按“2.2.1”所述条件进样测定,计算供试品中耐斯糖含量。6份供试品中耐斯糖含量的RSD值为1.05%,表明该方法重复性良好。
2.2.9 加標回收实验
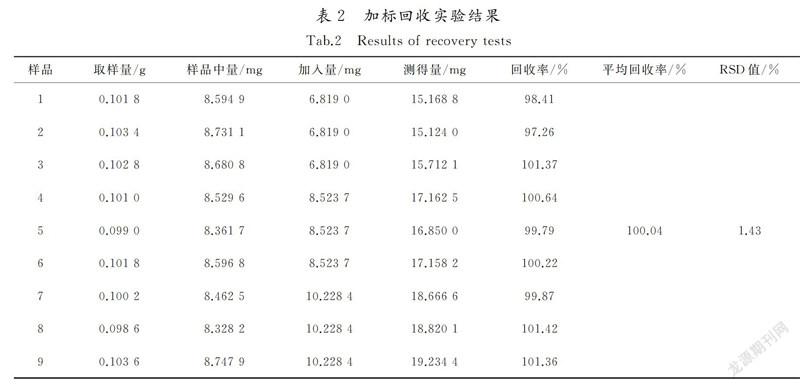
精密称取巴戟天标准汤剂样品,共计9份,每份约0.1 g,每3份为一组。于每组中精密加入耐斯糖对照品相当于巴戟天标准汤剂所含耐斯糖量的80%,100%,120%,置于具塞锥形瓶中,按“2.2.1”所述条件进样10 μL进行测定,耐斯糖平均加标回收率为10080%,加标回收率RSD值为1.51%。表明本方法的准确度良好,结果见表2。
2.3 15批标准汤剂出膏率及含量测定
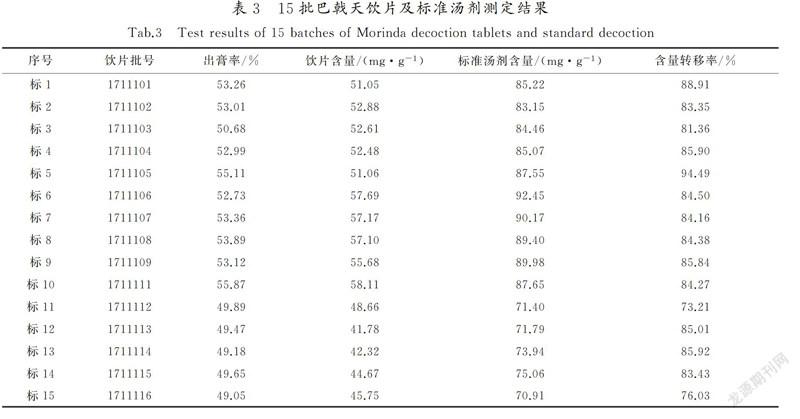
按“2.1”所述方法制备15批标准汤剂,标准汤剂出膏率的计算取标准汤剂干燥粉末质量([WTBX]m2)与巴戟天饮片质量(m1)之比值。按“2.2”所述方法测定巴戟天饮片、巴戟天标准汤剂的含量,得到含量转移率。15批巴戟天饮片及标准汤剂测定结果详见表3。
出膏率=m2/m1,含量转移率=[SX(]标准汤剂含量×出膏率饮片含量[SX)]×100% 。
从表3可以看出,15批巴戟天标准汤剂出膏率为49.05%~55.87%,出膏率平均值为52.08%,SD值为2.24;标准汤剂中耐斯糖含量范围为70.91~92.45 mg/g,平均值为82.55 mg/g,SD值为7.71;耐斯糖含量转移率范围为73.21%~94.49%,均值为84.05%,SD值为4.88。
3 巴戟天标准汤剂特征图谱的建立
3.1 色谱条件
色谱柱:Agilent公司ZORBAX Eclipse Plus C18柱(4.6 mm×250 mm,5 μm);流动相:乙腈-0.03%磷酸溶液,按表4比例进行梯度洗脱;检测波长:235 nm;流速:1 mL/min;柱温:30 ℃;进样量:10 μL。
3.2 对照品溶液的制备
精密称取水晶兰苷对照品12.5 mg,置于50 mL量瓶中,加入25%(体积分数,下同)甲醇定容,制成每1 mL含水晶兰苷0.25 mg的对照品溶液,即得。水晶兰苷对照图谱见图1。
3.3 供试品溶液的制备
取本品0.3 g,精密称定,置于磨口三角瓶中。精密量取25%甲醇25 mL,加入三角瓶中,称重,密塞,超声处理30 min,放至室温后再次称定质量,用25%甲醇补足减失的质量,摇匀,用0.45 μm微孔滤膜过滤,即得[20-21]。巴戟天标准汤剂特征图谱见图2。
3.4 方法学考察
3.4.1 精密度
取巴戟天标准汤剂样品(标3),按“3.3”所述方法处理样品,重复进样6次,以水晶兰苷为S峰,计算其他主要色谱峰的相对保留时间(RRT)及相对峰面积(RPA)。结果显示,各峰RRT的RSD值<0.8%,RPA的RSD值<21%,表明仪器的精密度良好。
3.4.2 稳定性
取同一批标准汤剂制备的样品溶液,按“3.1”所述条件,分别在0,3,6,9,12,15,18 h进样分析,以水晶兰苷为参照物峰,计算其他色谱峰的RRT及RPA。结果表明,各峰RRT的RSD值<0.7%,RPA的RSD值<2.2%,表明在18 h内样品溶液稳定。
3.4.3 重复性
取巴戟天标准汤剂样品(标3),按“3.3”所述方法制备供试品溶液,制备平行样品6份,按“3.1”所述条件进样分析,以水晶兰苷为参照物峰,计算其他色谱峰的RRT及RPA。结果表明,各峰RRT的RSD值<1.4%,RPA的RSD值<2.9%,表明该方法具有良好的重复性。
3.5 样品测定
取按“2.1”所述方法制得的样品,按照“3.3”所述方法制备样品溶液,分别进样,按“3.1”色谱条件测定PLC图谱。测定完成后,把15批PLC图谱导入相似度评价系统软件中进行分析,见图3。15批巴戟天标准汤剂共呈现7个共有特征峰,以2号峰水晶兰苷为参照峰,计算7个共有色谱峰的RRT及RPA,结果见表4和表5。
结果表明,15批巴戟天标准汤剂各特征峰的RRT均在规定值±5%范围内:峰1(0.81)、峰2(100)、峰3(1.30)、峰4(3.09)、峰5(3.42)、峰6(376)、峰7(4.25)。
4 讨 论
4.1 提取溶剂
在巴戟天配方标准汤剂特征图谱样品的制备方法中,考察了纯化水、无水乙醇、100%甲醇、70%甲醇、25%甲醇、70%乙醇、20%乙醇共7种提取溶剂,以色谱峰个数、基线稳定性等为考察指标,最终确定用25%甲醇进行样品溶液的制备。
4.2 流动相
在特征图谱条件摸索阶段,对有机相考察了甲醇、乙腈,对水相考察了0.1%磷酸、0.1%冰醋酸、003%磷酸及水对反应的影响情况。通过对比色谱图发现,流动相为乙腈-0.03%磷酸时,色谱图基线平稳,色谱峰分离良好,因此选用乙腈-0.03%磷酸作为流动相。
4.3 色谱柱及柱温
考察了ZORBAX Eclipse Plus C18及InertSustain AQ-C18色谱柱,以及柱温为25,30,35 ℃对反应的影响情况。结果显示,采用ZORBAX Eclipse Plus C18色谱柱、柱温为30 ℃时的效果最优。
4.4 提取用纯化水、饮用水
先后考察了采用符合《中华人民共和国药典》要求的纯化水、饮用水提取时的差异情况。从实验结果可以看出,提取效果受提取用水的影响也较小。
4.5 浸泡时间
先后考察了不浸泡、浸泡30 min、浸泡60 min对反应的影响情况。结果发现,浸泡时间对提取效果的影响也较小。
5 结 语
1) 对15批不同产地的巴戟天饮片进行了标准汤剂的制備,并对标准汤剂干膏粉进行了研究,确定了巴戟天标准汤剂的出膏率范围,为巴戟天配方颗粒量的确定提供了可靠数据。
2) 通过采用高效液相色谱法进行分析,明确了巴戟天标准汤剂中耐斯糖含量的测定及特征图谱分析方法,阐明了配方颗粒与传统标准汤剂的一致性。
3) 本研究对巴戟天配方颗粒水溶性多糖耐斯糖进行了含量及转移率的考察,但在特征图谱部分只对环烯醚萜苷类成分中的水晶兰苷进行了色谱峰指认,后续将对指纹图谱中其他6个特征峰进行研究,以获得更多的信息,更好地监控巴戟天配方颗粒的质量。
参考文献/References:
[1] 国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015.
[2] 陈红,裴占柱,程再兴,等.盐巴戟天与生巴戟天中水晶兰苷含量对比研究.中医学报,2013,28(10):1504-1505.
CEN ong,PEI Zhanzhu,CENG Zaixing, et al. Comparative study on the content of monotropein in Morinda officinalis processed with salt and raw Morinda officinalis .China ournal of Chinese Medicine, 2013,28(10):1504-1505.
[3] 吴凌凤, 曾令杰. 巴戟天化学成分与质量控制研究进展.广东药学院学报,2012, 28(1):98-101.
WU Lingfeng, ZENG Lingjie. Chemical constituents from the roots of Morinda officinalis and the quality control. ournal of Guangdong Pharmaceutical University,2012, 28(1):98-101.
[4] 賴满香,阮志燕,许意平.补肾中药巴戟天药理作用研究进展.亚太传统医药,2017,13(1):63-65.
[5] 吴冬凡,房志坚.巴戟天石油醚部位的化学成分研究.亚太传统医药,2009,5(11):42.
[6] 周法兴,文洁,马燕.巴戟天的化学成分研究.中药通报,1986,11(9):42-43.
[7] 何传波,陈玲,李琳,等.巴戟天水溶性多糖分离纯化的研究.云南农业大学学报,2006,21(3):320-323.
[8] 段淑娥,李敏.中草药中蒽醌化合物的研究进展.西安文理学院学报,2005,8(1):24-28.
DUAN Shu′e,LI Min.Advance in anthraquinone of Chinese erbal medicine .ournal of Xi′an University of Arts & Science,2005,8(1):24-28.
[9] 李竣,张华林,蒋林,等.南药巴戟天化学成分.中南民族大学学报(自然科学版),2010,29(4):53-56.
LI un,ZANG ualin,IANG Lin, et al.Chemical constitution of the roots from Morinda officinalis.ournal of South-Central University for Nationalities(Natural Science Edition),2010,29(4):53-56.
[10]陈士林,刘安,李琦,等.中药饮片标准汤剂研究策略.中国中药杂志,2016,41(8):1367-1375.
CEN Shilin,LIU An,LI Qi, et al.Research strategies in standard decoction of medicinal slices.China ournal of Chinese Materia Medica,2016,41(8):1367-1375.
[11]戎立保.巴戟天多糖提取工艺比较.内蒙古中医药,2009(12):30.
[12]朱广伟,李西文,陈士林.白芍饮片标准汤剂质量标准研究.世界中医药,2016,11(5):753-757.
ZU Guangwei,LI Xiwen,CEN Shilin.Quality standard research on standard decoction of Paeonialactiflora.World Chinese Medicine,2016,11(5):753-757.
[13]林伟雄,乐智勇,车海燕,等.甘草饮片标准汤剂的研究.中国中药杂志,2017,42(3):6-11.
LIN Weixiong,LE Zhiyong,CE aiyan, et al.Research on Glycyrrhizeae Radix standard decoction. China ournal of Chinese Materia Medica,2017,42(3):6-11.
[14]孙宝莹,郭涛,李西文,等.葛根饮片标准汤剂的研究.世界中医药,2016,11(8):1586-1589.
SUN Baoying,GUO Tao,LI Xiwen, et al.Preparation and quality standard study on the Kudzuvine root standard decoction. World Chinese Medicine,2016,11(8):1586-1589.
[15]张鹏,邬兰,李西文,等.人参饮片标准汤剂的评价及应用探讨.中国实验方剂学杂志,2017,23(11):1-10.
ZANG Peng,WU Lan, LI Xiwen, et al. Evaluation and application of standard decoction of Ginseng Radix Et Rhizoma . Chinese ournal of Experimental Traditional Medical Formulae,2017,23(11):1-10.
[16]徐姣,赵嵘,代云桃,等.栀子标准汤剂的质量评价方法考察.中国实验方剂学志,2017,23(7):1-6.
XU iao,ZAO Rong,DAI Yuntao, et al. Quality evaluation of standard decoction of Gardeniae ructus. Chinese ournal of Experimental Traditional Medical Formulae,2017,23(7):1-6.
[17]林超,王希希,黄群,等.巴戟天蒽醌与多糖联合提取工艺优化.粮食科技与经济,2017,42(3):71-76.
LIN Chao,WANG Xixi,UANG Qun, et al. Optimizing the extraction technology of anthraquinone and polysaccharide from Morinda officinalis. Grain Science and Technology and Economy,2017,42(3):71-76.
[18]张晓凤.巴戟天配方颗粒中多糖含量测定.北方药学,2014,11(9):15.
[19]史辑,刘梓晗,王玲,等.PLC测定不同产地巴戟天中5种茜草素型蒽醌的含量.中药材,2015,38(2):245-248.
SI i,LIU Zihan,WANG Ling, et al. Determination of five active components in Morinda officinalis from different habitats by PLC .ournal of Chinese Medicinal Materials,2015,38(2):245-248.
[20]刘瑾,徐吉银,罗进辉,等.不同产地巴戟天中水晶兰苷的含量测定.中成药,2010,32(3):517-519.
LIU in,XU iyin,LUO inhui, et al. Determination of crystal blue glycoside in Morinda officinalis from different origins .Chinese Traditional Patent Medicine,2010,32(3):517-519.
[21]郭念欣,李颖春,蔡佳良,等.不同生长年限的巴戟天化学成分的指纹图谱.中国实验方剂学杂志,2011,17(11):65-67.
GUO Nianxin,LI Yingchun,CAI ialiang, et al. Chromatographic fingerprint of components of Morinda officinalis in different harvest period . Chinese ournal of Experimental Traditional Medical Formulae,2011,17(11):65-67.
