《分散系及其分类》教学设计
2019-09-10朱倩
朱倩
【中图分类号】 G633.8 【文献标识码】 A 【文章编号】 1992-7711(2019)09-168-02
0
前言
《分散系及其分类》是人教版高中化学必修1第二章第1节《物质的分类》中的一课,通常用1个课时完成分散系及其分类、胶体的性质及应用的教学内容。高考对胶体的考察要求并不高,学生也不容易在这个内容上失分。这就导致了在此知识模块的教学过程中,教师往往忽略了对学生学习能力的培养,缺乏足够的思维引导,只是通过简单的问答、分析过程就得出结论,将考点生硬地灌输给学生,以致于学生虽然能够通过死记硬背做对题,却依然对胶体的本质没有深刻的理解认识。
胶体与生活的联系比较密切,很容易引发学生的学习兴趣和欲望,如果能够深度引导学生思考,就可以在学习知识的过程中同时培养学生的化学科学素养,增强学科思维,实验探究能力以及在后续学习中对知识的迁移应用能力。以下为笔者从以上目标出发尝试整理的教学设计。
一、教材、学情分析
本节课的内容是对初中学习过的溶液、浊液知识的拓展,内容难度要求不高,但其中所涉及到的分类观,微粒观,变化观等学科思想,对于后续的离子反应等知识的学习起到一个启示的作用。学生通过初中的学习已经了解分子、原子、离子的概念,但还不会主动从微观的视角去分析物质。学生知道溶液和浊液在外观上的区别,但不会主动去思考本质的差别。本节内容要学习的胶体,更是一个陌生的领域。胶体的性质不是物质本身具有的性质,是因为聚集状态而表现出的特有性质,因而可以在理性分析中引领学生从新的角度去认识物质的本质,从而认识胶体。
二、教学目标及重难点
2.1.教学目标
知识与技能:通过分散系的定义及其分类,能够对常见的混合物进行分类。能够从粒子大小的角度来理解胶体。掌握丁达尔效应,知道用丁达尔效应来鉴别溶液和胶体。了解胶体的介稳性及在生活中的应用。
过程与方法:在学习过程中,学会通过图形,实验探究等方法来获取信息和知识。通过学习物质不同分散状态下的性质,明白从分散质粒子大小的角度对物质进行分类是更为本质的一种思想。
情感态度及价值观:从生活中的丁达尔效应出发,激发学生的学习兴趣,认识到生活中处处是化学之美。
2.2.重难点
能够从分散质粒子大小的角度形成对胶体的概念。
三、教学过程设计
3.1分散系及其分类
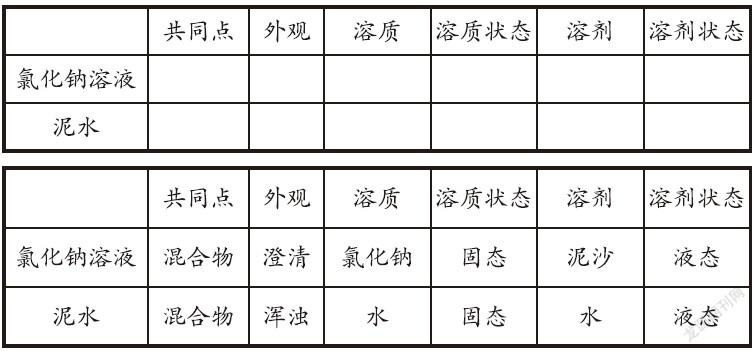
[情境引入]往两只盛有蒸馏水的烧杯中分别加入食盐颗粒和泥沙,搅拌后静置,让学生观察,并从表格中的内容对两份物质进行分析。
提问:如何將泥沙和水分离?为什么可以这样操作?同样的方法能不能分离氯化钠和水?
学生思考:可以通过过滤的方法,因为水能透过滤纸,而泥沙颗粒较大,不能透过滤纸,同样的方法不能分离氯化钠和水,因为溶液中的离子很细小,能够透过滤纸。
[设计意图]衔接初高中,从实验出发,引发学生的兴趣,且引导学生从溶质粒子大小的角度思考两种物质。
[概念延伸]像这样把一种(或多种)物质分散到另一种(或多种)物质中得到的体系,称为分散系。
根据分散质和分散剂各有三种不同聚集状态,可以得到9种不同类型的分散系,让学生通过合作讨论,对每种不同的分散系分别找到生活中对应的实例,加强学生对分散系这个概念的理解。
[设计意图]让学生应用之前学习的交叉分类法进行分散系的分类,形成分类砚。并将生活联系到课程中,加强学习与应用,学习与生活的联系。
3.2胶体的性质及其制备、应用
[情境引入]除了根据分散质和分散剂不同的聚集状态对混合物进行分类外,也有其它的分类方法。像前面的氯化钠溶液和泥水,都是固体分散质分散到液体分散剂中,但是却形成了不同外观的分散系,在初中我们将它们分为溶液和浊液两类。刚刚我们发现过,这两种分散系的区别在于分散质粒子的大小不同,溶液中的分散质能够透过滤纸,而浊液中的分散质不能,那有没有具体的数据根据分散质粒子的大小来区别溶液和浊液呢?
[设疑]在溶液中,分散质粒子是小于1nm的,浊液中分散质粒子大于100nm。根据学习过的知识,溶液和浊液的稳定性有什么区别?如果分散质粒子在1-100nm之间,形成的分散系和溶液,浊液的性质会不会有所不同?
[设计意图]从具体数据上出发,让学生真正从分散质粒子大小的角度来认识溶液和浊液的区别,培养科学的认知方法。溶液比浊液稳定,浊液在静置后会出现分散质沉淀现象,而溶液不会。再过渡到分散质粒子直径介于两者之间的分散系,激发学生的学习欲望。
[实验观察]向学生展示三份分散系:氯化钠溶液,泥水,和另外一份“红褐色液体”,让学生从外观上判断,学生会认为“红褐色液体”为溶液。
[实验1]教师用激光笔照射三份物质,让学生观察现象。
[实验2]将“红褐色液体”进行过滤操作,观察现象。
[学生思考]三份物质中,仅有“红褐色液体”在激光笔照射下出现光亮的通路,而氯化钠溶液中并不有,说明这份物质和溶液有区别。根据光照射到物体时会发生反射或者散射的知识,思考并尝试解释。另外,过滤后“红褐色液体”没有明显变化,说明其分散质粒子能够透过滤纸。
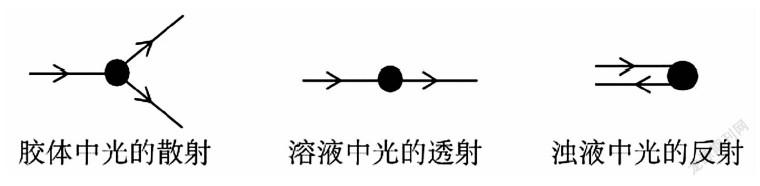
[图文解释]为什么“红褐色液体”能够在激光照射下出现光亮的通路呢?教师可以通过图片结合文字来说明。在光的传播过程中,光线照射到粒子时,如果粒子大于入射光波长很多倍,则发生光的反射,比如泥水;如果粒子小于入射光波长,则发生光的散射,这时观察到的是光波环绕微粒而向其四周放射的光,称为散射光。此时分散质粒子就像是一个个发光体。“红褐色液体”分散质粒子介于溶液中溶质粒子和浊液粒子之间,为1-100nm。小于可见光波长(400nm-700nm),因此,当可见光透过时会产生明显的散射作用。而对于溶液,其分散质粒子一般不超过1nm,虽然分子或离子更小,但因散射光的强度随散射粒子体积的减小而明显减弱,因此,溶液对光的散射作用很微弱。而这种分散质粒子大小在1-100nm之间的分散系,称为“胶体”。光束通过胶体出现光亮通道的现象,叫丁达尔效应。利用丁达尔效应,可以区别溶液和胶体。
[设计意图]通过两组实验,让学生对这份“红褐色液体”的性质有了直观的了解,使学生能够从更加本质,即分散质粒子大小这种微观的角度来理解溶液,胶体,浊液的区别。也能够理解丁达尔效应产生的原理。
[图片展示]生活中一些丁达尔效应的现象,演唱会上的灯光,海面上透过云层的光束,电影放映室中投射到屏幕的光束等等。
[设计意图]使学生认识到生活中丁达尔效应的美学,如果没丁达尔效应,生活中将少了许多美。
[学生实验]“红褐色的液体”是制备好的氢氧化铁胶体,如何能够制备得到呢?提供蒸馏水,NaOH溶液,饱和氯化铁溶液及实验仪器。
[分组实验]各小组组内讨论得出制备方法,并根据自己的需要选择药品自行制备,并对自己的实验结果进行评价分析。
[设计意图]学生从学过的知识中,容易想到用氯化铁和氢氧化钠来制备,但结果是失败的。原因是OH-离子浓度太大,使得氢氧化铁分子以大颗粒的形式聚集,形成沉淀。在此基础上,可以提示学生从降低OH-离子浓度,用水来代替氢氧化钠,或者尝试减小氢氧化铁颗粒的大小上去制备胶体。通过这个实验探究,学生可以认识到分散质粒子大小能够改变分散系聚集状态。
[實验反思]在用氯化铁饱和溶液和沸水制备胶体的过程中,有些小组也会经历失败。抓住机会分析原因,可以得出胶体是一种介稳状态的分散系。再让学生阅读课后的科学视野,从而使学生知道,胶体的介稳性是因为胶体粒子是带电的,同时也在做布朗运动,过度加热煮沸,使用自来水,滴加过量氯化铁都可能使胶体粒子聚沉。
[联系生活]举例胶体在生活中的实例,如豆腐的制作,止血贴,江河入海口三角洲的形成等等。
[设计意图]培养学生的阅读能力,将知识生活化,丰富视野,让学生感觉自己学到的知识能够在生活中得到应用,或者解释生活中的现象,有助于培养兴趣。
[课后拓展]
①布置学生课后网上查阅,调查胶体发展的历史,以及前沿科学中胶体的应用,纳米材料的相关资料,进行小组报告。
②家庭小实验。在自制的豆浆中,分别加入食盐,白糖,搅拌、静置,分别观察,记录现象。
[设计意图]将课堂延伸,让学生在日常的生活中也能应用学科思维,培养学生收集信息的能力,动手能力和科学的探究精神。
四、教学反思
高考对胶体的要求虽然不高,这个知识点却是培养学生兴趣很好的出发点。本节涉及到的学科思维,实验探究思想,在后续的学习中也依然能够起到作用。这个教学设计中,紧密联系生活,教师引导,学生思考的模式,让学生获得知识的同时也收获能力。当然,也还有许多待改进的地方,需要在以后的实践中作进一步的研究。
